文档内容
探究水的电离
重难点 题型 分值
1. 水的电离平衡
重点 2. 影响水的电离平衡的因素
3. 有关水的离子常数的判断问题
选择题 3-5分
1. 影响水的电离平衡的因素
难点
2. 水的离子积常数影响因素
一、水的电离
1. 水的电离
(1)水是一种极弱的电解质,能发生微弱的电离:HO+HO HO++OH-,简
2 2 3
写为HO H++OH-。实验测得25℃时,1L水中有1×10-7molH O发生电离,则室温下,
2 2
第1页纯水中c(H+)=c(OH-)= 1. 0×10-7。
【注意】
HO+HO HO++OH-
2 2 3
在水溶液中,H+和OH-都不是单独存在的。为了书写方便,通常仍写成H+和OH-。
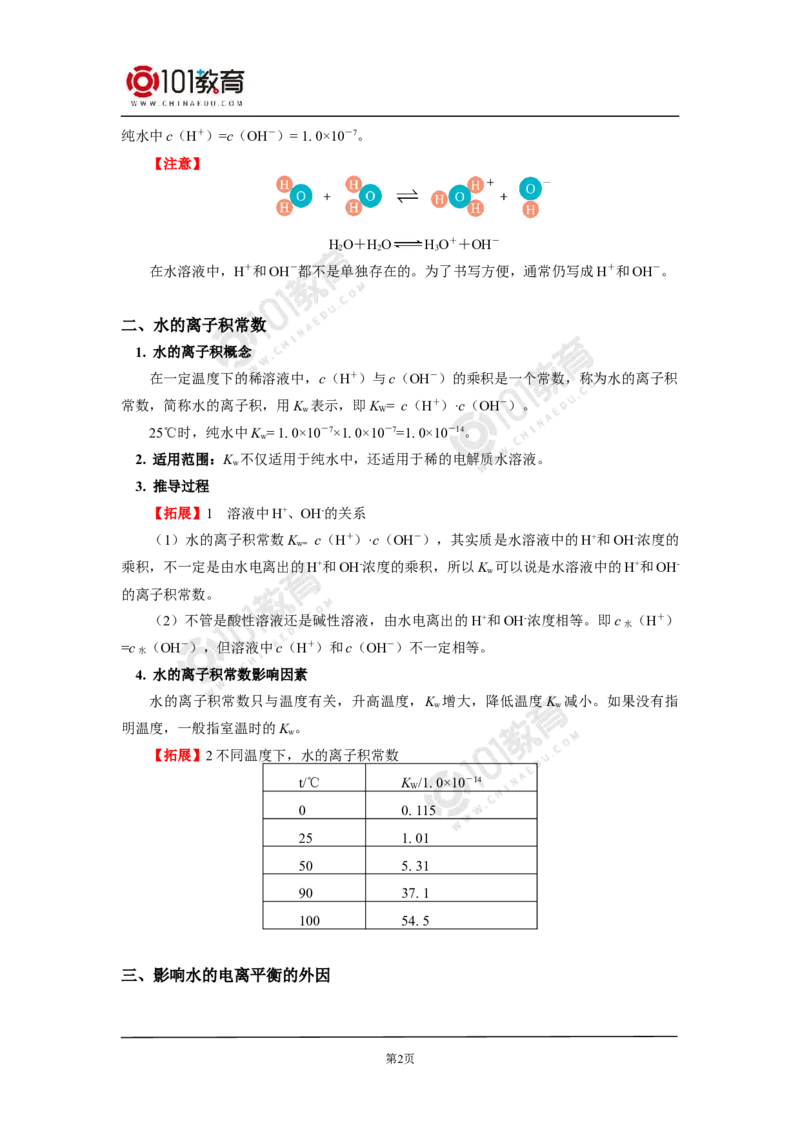
二、水的离子积常数
1. 水的离子积概念
在一定温度下的稀溶液中,c(H+)与c(OH-)的乘积是一个常数,称为水的离子积
常数,简称水的离子积,用K 表示,即K = c(H+)·c(OH-)。
w W
25℃时,纯水中K = 1. 0×10-7×1. 0×10-7=1. 0×10-14。
w
2. 适用范围:K 不仅适用于纯水中,还适用于稀的电解质水溶液。
w
3. 推导过程
【拓展】1 溶液中H+、OH-的关系
(1)水的离子积常数K c(H+)·c(OH-),其实质是水溶液中的H+和OH-浓度的
w=
乘积,不一定是由水电离出的H+和OH-浓度的乘积,所以K 可以说是水溶液中的H+和OH-
w
的离子积常数。
(2)不管是酸性溶液还是碱性溶液,由水电离出的H+和OH-浓度相等。即c (H+)
水
=c (OH-),但溶液中c(H+)和c(OH-)不一定相等。
水
4. 水的离子积常数影响因素
水的离子积常数只与温度有关,升高温度,K 增大,降低温度K 减小。如果没有指
w w
明温度,一般指室温时的K 。
w
【拓展】2不同温度下,水的离子积常数
t/℃ K /1. 0×10-14
W
0 0. 115
25 1. 01
50 5. 31
90 37. 1
100 54. 5
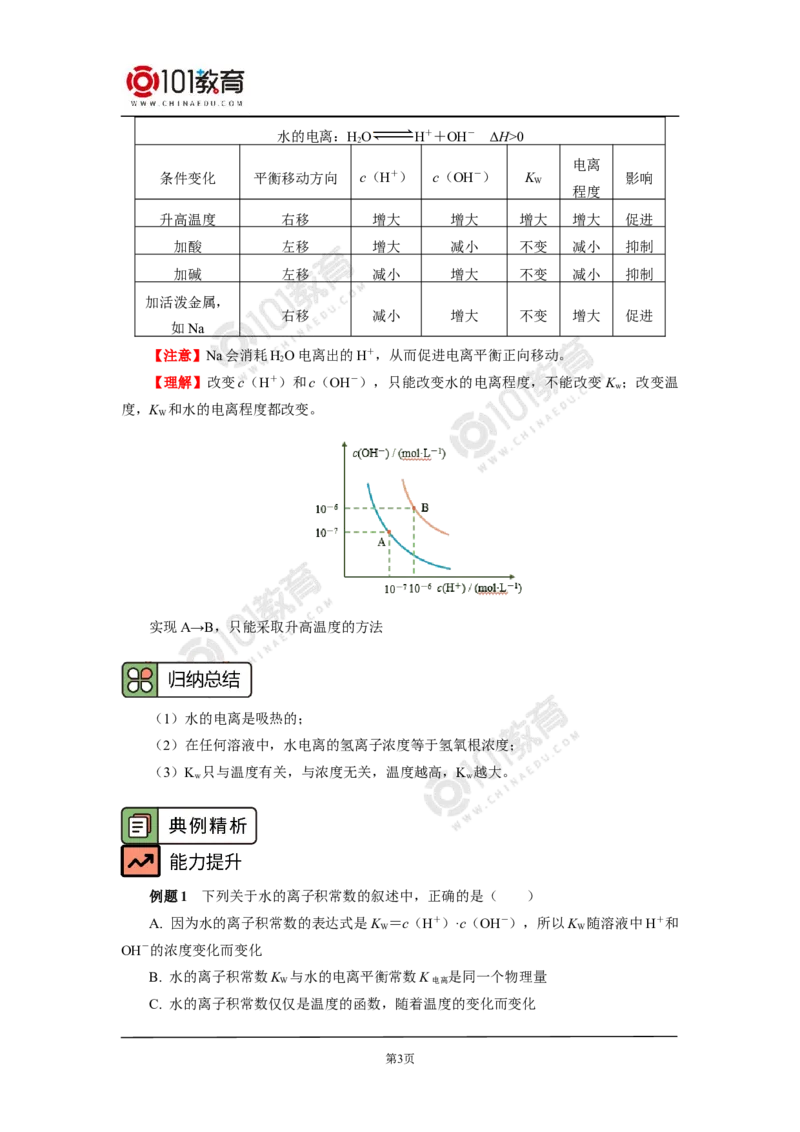
三、影响水的电离平衡的外因
第2页水的电离:HO H++OH- ΔH>0
2
电离
条件变化 平衡移动方向 c(H+) c(OH-) K 影响
W
程度
升高温度 右移 增大 增大 增大 增大 促进
加酸 左移 增大 减小 不变 减小 抑制
加碱 左移 减小 增大 不变 减小 抑制
加活泼金属,
右移 减小 增大 不变 增大 促进
如Na
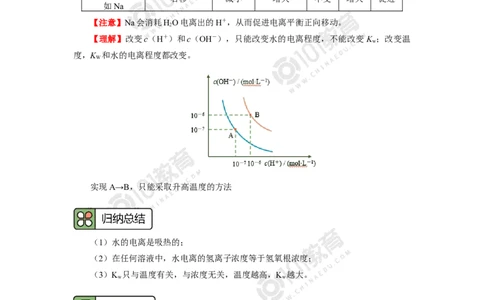
【注意】Na会消耗HO电离出的H+,从而促进电离平衡正向移动。
2
【理解】改变c(H+)和c(OH-),只能改变水的电离程度,不能改变 K ;改变温
w
度,K 和水的电离程度都改变。
W
实现A→B,只能采取升高温度的方法
(1)水的电离是吸热的;
(2)在任何溶液中,水电离的氢离子浓度等于氢氧根浓度;
(3)K 只与温度有关,与浓度无关,温度越高,K 越大。
w w
例题1 下列关于水的离子积常数的叙述中,正确的是( )
A. 因为水的离子积常数的表达式是K =c(H+)·c(OH-),所以K 随溶液中H+和
W W
OH-的浓度变化而变化
B. 水的离子积常数K 与水的电离平衡常数K 是同一个物理量
W 电离
C. 水的离子积常数仅仅是温度的函数,随着温度的变化而变化
第3页D. 水的离子积常数K 与水的电离平衡常数K 是两个没有任何关系的物理量
W 电离
【答案】C
【解析】水的离子积常数K =K ·c(HO),一定温度下K 和c(HO)都是不变
W 电离 2 电离 2
的常数,所以K 仅仅是温度的函数。水的离子积常数的表达式是 K =c(H+)·c(OH
W W
-),但是只要温度一定,K 就是一个不变的常数,溶液中H+的浓度变大,OH-的浓度就
W
变小,反之亦然。
例题2 25 ℃时,水的电离达到平衡:HO H++OH- ΔH>0,下列叙述正确的
2
是( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
w
C. 向水中加入少量CHCOOH,平衡逆向移动,c(H+)降低
3
D. 将水加热,K 增大,c(H+)不变
w
【答案】B
【解析】向水中加入稀氨水,c(OH-)增大,平衡逆向移动,c(H+)减小,A项不
2−
正确;向水中加入少量固体NaHSO :NaHSO===Na++H++SO4 ,相当于加入一元强酸,
4 4
所以向水中加入NaHSO ,导致c(H+)增大,但K 不变,B项正确;向水中加入少量
4 w
CHCOOH后,使水的电离平衡逆向移动,c(OH-)减小,c(H+)增大,C项不正确;
3
将水加热,水的电离平衡正向移动,c(H+)、c(OH-)均增大,K 增大,c(H+)增大,
w
但仍呈中性,D项不正确。
例题3 已知水中存在如下平衡:HO+HO HO++OH-ΔH>0,现欲使平衡向右
2 2 3
移动,且所得溶液呈酸性,选择的方法是( )
A. 加热水至100℃[其中c(H+)= 1×10-6 mol·L-1]
B. 向水中加入NaHSO
4
C. 向水中加入Cu(NO )
3 2
D. 向水中加入NaOH
【答案】C
【解析】水的电离过程是吸热过程,加热至100℃,促进水电离,溶液中c(H+)=c
2−
(OH-),呈中性,A错误;NaHSO 在水中完全电离生成Na+、H+和SO4 ,相当于加入
4
一元强酸,所以向水中加入NaHSO,导致c(H+)增大,水的电离平衡左移,B错误;向
4
水中加入Cu(NO ) , Cu2+和OH-反应生成Cu(OH) 沉淀,消耗OH-,促进水的电离
3 2 2
第4页平衡向右移动,c(H+)增大,溶液呈酸性,C正确;向水中加入NaOH,c(OH-)增大,
抑制水的电离,平衡向左移动,D错误。
(答题时间:40分钟)
一、选择题
1. 由水电离出的c(OH-)=1×10-13 mol·L-1的无色溶液中,一定能大量共存的离子组
是( )
− −
A. Cl-、AlO2 、Na+、K+ B. Fe3+、NO3 、K+、H+
− 2− +
C. NO3 、Ba2+、K+、Cl- D. Al3+、SO4 、NH4、Cl-
*2. 25 ℃时,水的电离达到平衡:HO H++OH-。下列叙述错误的是( )
2
A. 向水中通入氨气,平衡逆向移动,c(OH-)增大
B. 向水中加入少量稀硫酸,c(H+)增大,K 不变
w
C. 将水加热平衡正向移动,K 变大
w
D. 升高温度,平衡正向移动,c(H+)增大,pH不变
*3. 一定温度下,用水稀释0. 1 mol·L-1的一元弱酸HA,随稀释进行,下列数值一定增
大的是(K 表示水的离子积,K 表示HA的电离常数)( )
w a
c(H+)
K
A. K B. a
w
c(HA)
C.
c(A−)
D. c(OH-)
二、非选择题
4. (1)某温度(t ℃)时,水的K =1×10-12,则该温度( )(填“>”“<”或
w
“=”)25 ℃,其理由是__________________。
(2)该温度下,在c(H+)=1×10-7 mol·L-1的NaOH溶液中,由水电离出的c(OH
-)=( )mol·L-1。
5. (1)25 ℃时,10 L 水中含 OH-的物质的量为( )mol,含 H+的个数为
____________个(设阿伏加德罗常数为N ,下同)。
A
(2)25 ℃时,1 g水中含H+的个数为( )个。
*6. 某同学为探究K 的影响因素,做了以下实验:
w
(1)查阅资料,不同温度下水的离子积常数。
t/℃ 0 10 20 25 40 50 90 100
第5页K /10-14 0. 134 0. 292 0. 681 1. 01 2. 92 5. 47 38. 0 55. 0
w
由此推出:随着温度的升高,K 的值( );水的电离程度( );水的电离平
w
衡向( )移动,水的电离过程是( )过程。
(2)取三支烧杯A、B、C,分别加入适量水,再向B、C烧杯中分别加入适量盐酸和
NaOH,分析并填写下表:
纯水 加少量盐酸 加少量NaOH
c(H+) 1. 0×10-7mol·L-1 增大
c(OH-) 1. 0×10-7mol·L-1 增大
c(H+)和c(OH
c(H+)=c(OH c(H+) c(H+)
-)
-) c(OH-) c(OH-)
大小比较
水的电离平
不移动
衡移动方向
K 值 1. 0×10-14
w
综上所述,可得出如下结论:
①温度、______________、______________均能影响水的电离平衡。
②K 只受______________的影响,而与其他因素无关。
w
第6页1.【答案】C
【解析】水电离出的c(OH-)=1×10-13 mol·L-1时,溶液可能呈酸性,也可能呈碱
−
性。A项中AlO2 在酸性条件下不能大量共存;B项中Fe3+和H+在碱性条件下不能大量共
+
存,且Fe3+溶液有颜色;C项在酸性或碱性条件下都能大量共存;D项中Al3+、NH4在碱
性条件下不能大量共存。
2.【答案】D
【解析】向水中通入NH ,c(OH-)增大,平衡左移,A正确;向水中加入少量稀
3
HSO ,c(H+)增大,但温度不变,K 不变,B正确;将水加热,水的电离平衡正向移动,
2 4 w
K 变大,C正确;升高温度,能促进水的电离,c(H+)增大,pH减小,D错误。
w
3.【答案】D
c(H+)c(A−) c(H+)
c(HA) K
【解析】温度不变,K 不变,A不符合题意;根据K= ,推出 a
w a
c(HA) n(HA)
=
c(A−)= n(A−),加水稀释时,HA电离程度增大,n(HA)减小,n(A-)增大,则
n(HA)
n(A−)减小,B、C不符合题意;加水稀释HA电离程度增大,但是c(H+)减小,由K
w
不变,可知c(OH-)增大,D符合题意。
4. 【答案】(1)> 升温促进水电离,K 增大 (2)1×10-7
w
【解析】(1)升高温度,K 增大,现K =1×10-12>1×10-14,因此温度高于25 ℃。
w w
(2)NaOH溶液中由水电离出来的 c(OH-)等于溶液中 c(H+),即为1×10-7
mol·L-1。
5. 【答案】(1)10-6 10-6N (2)10-10N
A A
【解析】(1)常温下,K =1×10-14,c (H+)=c (OH-)=1×10-7 mol·L-1。1
w 水 水
L水中含n(OH-)=1×10-7 mol,n(H+)=1×10-7 mol,故10 L水中含OH-的物质的
量为1×10-6 mol,含H+的个数为10-6N 个。
A
(2)1 L水即1 000 g水中含H+的物质的量为1×10-7 mol,故1 g水中含H+的物质的
量为1×10-10 mol,即含H+的个数为10-10N 个。
A
6. 【答案】(1)增大 增大 右 吸热
(2)减小 减小 > < 向左 向左 1. 0×10-14 1. 0×10-14 ①酸 碱 ②温度
【解析】水的电离是吸热的,在升高温度时,K 增大,在向水中加入酸或碱时,c(H
w
+)或c(OH-)增大,抑制水的电离,但溶液中只要温度不变,K 不变。
w
第7页酸、碱溶液中水的电离
重难点 题型 分值
1. 掌握酸和碱对水电离平衡的影响
重点
2. 掌握酸碱溶液中水电离的计算
选择题 2-4分
1. 掌握酸和碱对水电离平衡的影响
难点
2. 掌握酸碱溶液中水电离的计算
1. 酸、碱溶液中水的电离
(1)由于存在水的电离平衡,则在纯水中和任何酸、碱、盐的水溶液中均存在H+和
OH-。在酸、碱、盐的稀溶液中,c(H+)与c(OH-)的乘积都等于K ,即K =c(H+)
w w
·c(OH-)。
(2)在酸溶液中,酸电离出的H+抑制了水的电离,使水电离出的c(H+)与c(OH
第8页-)减小;在碱性溶液中,碱电离出的OH-抑制了水的电离,也使水电离出的c(H+)与c
(OH-)减小。
【注意】由水的电离平衡HO H++OH-及其移动规律:Kw=c(H+)·c(OH
2
-)中Kw的大小只与温度有关,而与c(H+)、c(OH-)变化无关,在碱性或酸性的稀
溶液中,同样存在Kw=c(H+)·c(OH-),且在25℃时,Kw恒为1×10–14
2. 在酸、碱溶液中水电离出的c(H+)或c(OH-)的计算
在酸、碱溶液中,水的电离出的c (H+)、c (OH-)与c(H+)、c(OH-)存在
水 水
如下关系:
(1)在酸性溶液中K = c (H+)·c (OH-)(忽略水电离出的H+的浓度),即c
w 酸 水
(OH-)= c (H+)= c(OH-)(酸溶液中的OH-都是由水电离出来的)= 。
水 水
(2)碱溶液中K =c (H+)·c (OH-)(忽略水电离出的OH-的浓度),即c (H
w 水 碱 水
+)=c (OH-)=c(H+)(碱溶液中的H+都是由水电离出来的)= 。
水
【注意】
①K =c(H+)·c(OH-)式中的c(H+)和c(OH-)分别是指溶液中H+和OH-的
w
总浓度,一般来说,当溶液中 c(H+)或c(OH-)大于由于水电离出的 c(H+)和c
(OH-)的1000倍时,水的电离可以忽略。
②温度一定,任何稀溶液的电解质水溶液中c(H+)·c(OH-) =K ,这一关系不变,
w
酸性溶液稀释时,c(H+)减小,但c(OH-)增大;碱性溶液稀释时,c(OH-)减小,c
(H+)增大。
例如,25℃时,0. 01mol/L盐酸中,c(H+)=0. 01mol/L,由水电离出的c(H+)、c
(OH-)均为1×10-12 mol/L;25℃时,0. 01mol/LNaOH溶液中,c(OH-)=0. 01mol/L,
由水电离出的c(OH-)、c(H+)均为1×10-12 mol/L。
(1)酸碱溶液中水的电离是受到抑制的
在酸溶液中,水电离出的 c(H+)浓度可以忽略,在碱溶液中,水电离出的c(OH
-) 浓度可以忽略。
(2)酸碱溶液中水的离子常数公式
第9页例题1 25℃时,下列三种溶液中,由水电离出的氢离子的浓度之比是( )
①1 mol/L的盐酸
②0. 1 mol/L的盐酸
③0. 01 mol/L的NaOH溶液
A. 1∶10∶100
B. 1∶10-1∶10-12
C. 14∶13∶12
D. 14∶13∶2
【答案】A
【解析】25℃时,水离子积常数Kw=1. 01×10-14 mol/L。酸溶液中水电离出的c (H
水
+)等于该
例题2 室温下,0. 01 mol/L NaOH溶液中的c(H+)是0. 0005 mol/L Ba(OH) 溶液
2
中c(H+)的( )
A. 10倍 B. 20倍 C. 1/10倍 D. 1/20倍
【答案】C
【解析】根据两溶液的c(OH-),分别求出两溶液中c(H+)
例题3 现有下列物质①100 ℃纯水、②25 ℃ 0. 1 mol/L HCl溶液、③25 ℃ 0. 1
mol/L KOH溶液、④25 ℃ 0. 1 mol/L Ba(OH) 溶液。
2
(1)这些物质与25 ℃纯水相比,能促进水电离的是________(填序号),能抑制水
的电离的是________,水电离的c(OH-)等于溶液中c(OH-)的是________,水电离的
c(H+)等于溶液中c(H+)的是________。
(2)②和③溶液中水的电离度相等,进而可推出的结论是:同一温度下,
________________时,水的电离度相等。
【答案】(1)① ②③④ ①② ①③④
(2)酸溶液中的c(H+)等于碱溶液中的c(OH-)
【解析】水的电离过程吸热,升温,促进水的电离,酸或碱抑制水的电离;强酸溶液
中,由于酸电离出的c(H+)远大于水电离出的c(H+),酸电离的c(H+)可看成溶液
中的c(H+),强碱溶液中,由于碱电离的c(OH-)远大于水电离的c(OH-),碱电离
的c(OH-)可看成溶液中的c(OH-)。
第10页答题时间(40分钟)
一、选择题
1. 下列说法正确的是( )
A. 水的电离方程式:HO===H++OH-
2
B. 升高温度,水的电离程度增大
C. 在NaOH溶液中没有H+
D. 在HCl溶液中没有OH-
2. 向蒸馏水中滴入少量盐酸后,下列说法中错误的是( )
A. c(H+)·c(OH-)不变
B. pH减小了
C. c(OH-)降低了
D. 水电离出的c(H+)增加了
3. 把1 mL 0. 1 mol·L-1的HSO 加水稀释制成2 L溶液,在此溶液中由水电离产生的H
2 4
+,接近于( )
A. 1×10-4 mol·L-1 B. 1×10-8 mol·L-1
C. 1×10-11 mol·L-1 D. 1×10-10 mol·L-1
*4. 25 ℃时,在等体积的①0. 5 mol·L-1的HSO 溶液中 ②0. 05 mol·L-1Ba(OH) 溶
2 4 2
液中 ③1 mol·L-1 NaCl溶液中 ④纯水中,发生电离的水的物质的量之比是( )
A. 1∶10∶107∶107 B. 107∶107∶1∶1
C. 107∶106∶2∶2 D. 107∶106∶(2×107)∶2
5. 下列溶液一定显酸性的是( )
A. 含H+的溶液
B. c(OH-)7,错误;B项,盐酸中c(H+)=1×10-3
mol·L-1,Ba(OH) 溶液中c(OH-)=1×10-3 mol·L-1,两者又是等体积混合,故有n
2
(H+)=n(OH-),混合后溶液的pH=7,错误;C项,因醋酸是弱酸,反应时酸过量,
反应后pH<7,正确;D项,因NH ·H O是弱碱,反应时碱过量,反应后pH>7,错误。
3 2
7.【答案】B
【解析】pH<7的溶液不一定呈酸性,如100 ℃时,pH=6为中性溶液,pH<7可能为
碱性溶液,故A正确;NH ·H O是弱碱,在相同温度下,物质的量浓度相等的氨水、
3 2
NaOH溶液,氢氧化钠溶液中的c(OH-)大于氨水中的c(OH-),故B错误;在相同温
度下,pH相等的盐酸、CHCOOH溶液,c(H+)和c(OH-)分别相等,根据电荷守恒,
3
分别有c(Cl-)+c(OH-)=c(H+),c(CHCOO-)+c(OH-)=c(H+),因此c
3
第13页(Cl-)=c(CHCOO-),故C正确;氨水和盐酸反应后的溶液中存在电荷守恒c(Cl-)
3
+ +
+c(OH-)=c(NH4)+c(H+),若c(Cl-)=c(NH4),则c(OH-)=c(H
+),溶液呈中性,故D正确。
8.【答案】(1)1. 0×10-13 (2)12
【解析】(1)该温度下,水的离子积:K =c(H+)·c(OH-)=10-(a+b)=1. 0×10
W
-13。
0.1L×0.4mol⋅L−1 −0.1L×0.2mol⋅L−1
0.2L
(2)c(OH-)= =0. 1 mol·L-1,
1×10−13mol2 ⋅L−2
c(H+)=K /c(OH-)=
0.1mol⋅L−1
=1×10-12 mol·L-1,pH=12。
W
第14页