文档内容
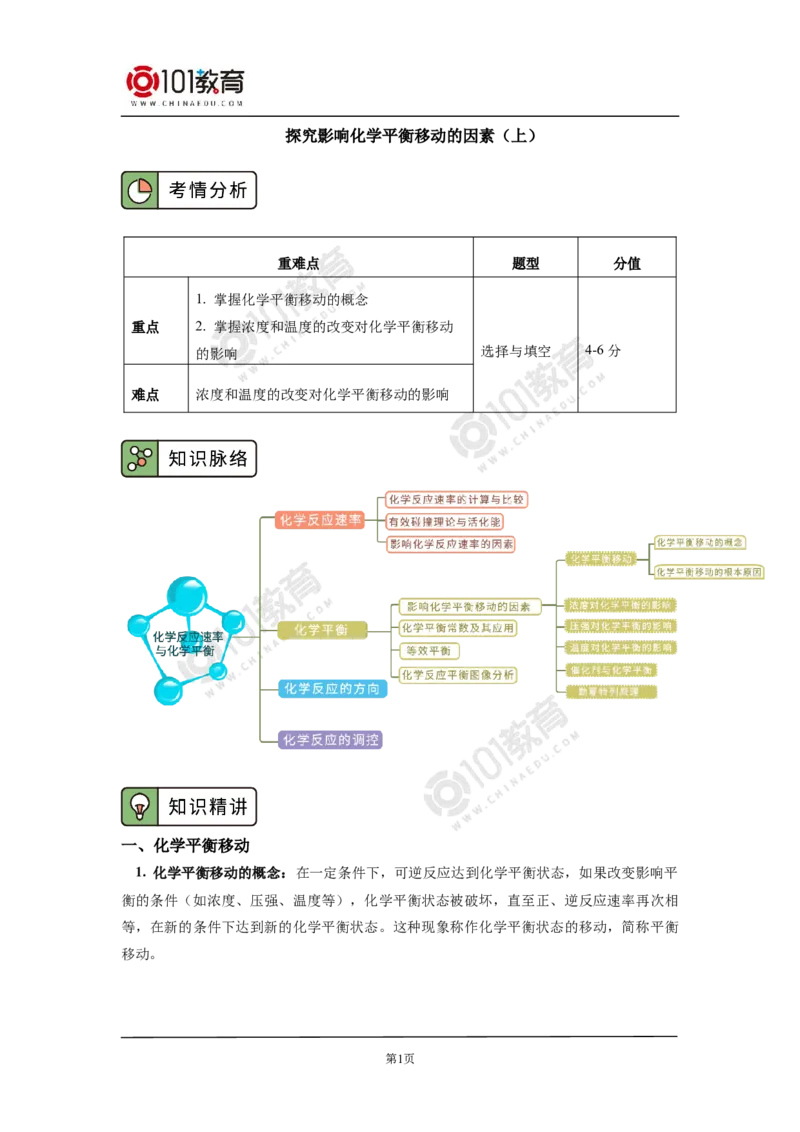
探究影响化学平衡移动的因素(上)
重难点 题型 分值
1. 掌握化学平衡移动的概念
重点 2. 掌握浓度和温度的改变对化学平衡移动
的影响 选择与填空 4-6分
难点 浓度和温度的改变对化学平衡移动的影响
一、化学平衡移动
1. 化学平衡移动的概念:在一定条件下,可逆反应达到化学平衡状态,如果改变影响平
衡的条件(如浓度、压强、温度等),化学平衡状态被破坏,直至正、逆反应速率再次相
等,在新的条件下达到新的化学平衡状态。这种现象称作化学平衡状态的移动,简称平衡
移动。
第1页【注意】化学平衡的移动包括可逆反应旧化学平衡的破坏和新化学平衡的建立过程。
【划重点】化学平衡移动的根本原因
化学平衡移动的根本原因是影响平衡的条件改变导致 v ≠v 。即 v =v
正 逆 正 逆
⃗改变条件v ≠v ⃗改变条件v’ =v’ 。
正 逆 正 逆
2. 化学平衡移动方向的判断
外界条件改变:
若v =v ,平衡不移动;
正 逆
若v >v ,平衡向正反应方向移动;
正 逆
若v p
C. X点时v(正)>v(逆)
D. X点比Y点的正反应速率大
6. 下列叙述中说明某化学平衡一定发生移动的是( )
A. 混合体系中气体密度发生变化 B. 正、逆反应速率改变
C. 混合物中各组分的浓度改变 D. 反应物的转化率改变
二、填空题
*7. 对于反应A(?)+2B(g) nC(g)在一定条件下达到平衡后,改变下列条件,
请回答:
(1)改变A的量,平衡不移动,则A为_____________________ 。
(2)增大压强,平衡不移动,当n=2时,A的状态为_____________________;当
n=3时,A的状态为_____________________。
( 3 ) 若 A 为 固 体 , 压 缩 体 积 增 大 压 强 , C 的 百 分 含 量 减 小 , 则
_____________________。
第7页1.【答案】B
【解析】化学平衡移动的根本原因是速率发生改变后v'(正)≠v'(逆)。
2.【答案】D
【解析】A项,未体现正与逆的关系,故不能说明达到平衡状态;只要反应发生,H
2
和CO的体积比就为1∶1,保持不变,B不能说明达到平衡状态;形成2 mol H-O键,同
时生成1 mol C,都表示的是逆反应,C不能说明达到平衡状态;混合气体密度和平均相对
分子质量都保持不变,说明气体的质量和物质的量不变,D能说明反应达平衡状态。
3.【答案】A
【解析】4v正(O )=5v逆(NO)证明化学反应的正逆反应速率是相等的,达到了
2
化学平衡状态,A正确;单位时间内生成x mol NO,同时消耗x mol NH ,只表示了正反
3
应方向,则不能说明化学反应的正、逆反应速率是相等的,B错误;若增加容器体积即减
小压强,化学反应速率减慢,C错误;反应速率之比等于方程式的化学计量数之比,所以
3v正(NH )=2v正(HO),D错误。
3 2
4.【答案】A
【解析】氮气和氢气的反应是一个反应前后气体体积减小的反应,气体的压强越大,
氮气的转化率越大,随着反应的进行,a容器内气体的压强不变,b容器内气体的压强减小,
a容器中气体的压强大于b容器中气体的压强,所以a容器中氮气的转化率大。
5.【答案】C
【解析】增大压强,平衡逆向移动,说明 nv(逆);X点压强小于Y的压强,所以X点比Y点的正反应速率小。
6.【答案】D
【解析】对于反应前后气体体积相等的反应来说,增大压强,气体的密度增大,平衡
不移动,A错误;对于反应前后气体体积不变的反应,增大压强反应速率增大,但平衡不
发生变化,B错误;对于反应前后气体体积相等的反应来说,增大体系的体积,体系各组
分的物质的量浓度减小,平衡不移动,C错误;反应物的转化率发生变化,说明物质的量
一定在变化,化学平衡一定发生移动。
7.【答案】(1)固态或纯液态 (2)固态或纯液态 气态 (3)n≥3
【解析】(1)改变A的量,平衡不移动,则A为固态或纯液态。
(2)增大压强平衡不移动,当n=2时,A为固态或纯液态,n=3时A为气态。
(3)若A为固体,压缩体积增大压强,C的百分含量减小,说明平衡逆向移动,则
n≥3。
第8页探究影响化学平衡移动的因素(下)
重难点 题型 分值
1. 掌握压强和催化剂对化学平衡移动的影
响
重点
2. 运用勒夏特列原理判断化学平衡移动的
选择与填空 4-6分
方向
1. 压强和催化剂对化学平衡移动的影响
难点
2. 勒夏特列原理
一、压强对化学平衡的影响
(1)以N+3H 2NH 为例探究增大压强对平衡的影响
2 2 3
①加压解释
压缩体积,增大压强,导致反应物浓度增大,故正反应速率增大,生成物浓度增大,
逆反应速率也增大,但是反应物气体分子数多,故正反应速率增大得多,逆反应速率增大
第9页得少,导致v >v ,平衡正向移动,即平衡向气体分子数减小的方向移动。
正 逆
②图像理解
其他条件不变时,压缩体积,增大压强的速率—时间图像和浓度—时间图像
【图像变化规律】对于反应前后气体体积改变的可逆反应,改变压强,影响平衡,速
率—时间图像和浓度—时间图像都突变。
③总结规律:其他条件不变时,增大压强,平衡向气体体积缩小的方向移动。
【理解】1 对于反应物与生成物中都有气体的可逆反应,改变压强,气体分子数多的
一方速率改变得多。压缩体积,增大压强,气体分子数多的一方速率增加得多,气体分子
数少的一方速率增加的少;增大体积,减小压强,气体分子数多的一方速率减少得多,气
体分子数少的一方速率减少得少。
(2)以N+3H 2NH 为例探究减小压强对平衡的影响
2 2 3
①减压解释
增大体积,减小压强,导致反应物浓度减小,故正反应速率减小,生成物浓度减小,
逆反应速率减小,但是反应物气体分子数增多,故正反应速率减小得多,逆反应速率减小
得少,导致v <v ,平衡逆向移动,即平衡向气体分子数增大的方向移动。
正 逆
②图像理解
其他条件不变时,增大体积,减小压强的速率—时间图像和浓度—时间图像
③总结规律:其他条件不变时,减小压强,平衡向气体体积增大的方向移动。
(3)以H (g)+I (g) 2HI(g)为例探究改变压强对反应前后气体体积分数
2 2
相同的反应的影响
①相关解释
对于反应前后气体分子数相同的可逆反应,改变压强,正、逆反应速率同等程度改变,
若增大压强,正逆反应速率同等程度增大,若减小压强,正逆反应速率同等程度减小,故
第10页平衡不移动。
②图像理解(以H(g)+I(g) 2HI(g)为例)
2 2
【理解】2 对于反应前后气体分子数相同的可逆反应,改变压强,正、逆反应速率
会同等程度改变,但是平衡不移动,对应的反应物的转化率、生成物的产率都不改变。
③规律总结:其他条件不变时,对于反应前后气体分子数相同的可逆反应,改变压强,
平衡不移动。
【注意】探究压强对化学平衡的影响时一般是探究有气体参与的化学反应,对于无气
体参与的化学反应,改变压强,对化学平衡的移动无影响。
二、催化剂与化学平衡
加入催化剂(默认正催化剂)可以同等程度地降低正逆反应的活化能,可以同等程度
地加快正、逆反应速率,故不影响化学平衡,但能改变反应达到平衡所需的时间。
【举例】某放热反应加入催化剂(b为加入催化剂)前后反应体系能量变化图:
1. 图像理解
以N+3H 2NH 为例探究加入催化剂对平衡的影响
2 2 3
【图像变化规律】加入催化剂,速率—时间图像突变,浓度—时间图像不变。
第11页【举例】对于反应N+3H 2NH ,NH 的体积分数随时间变化情况如图所示:
2 2 3 3
其中m表示使用催化剂时的情况,n表示未使用催化剂时的情况。
2. 规律总结:加入催化剂可同等程度地改变正、逆反应速率,不影响化学平衡。
三、勒夏特列原理
1. 勒夏特列原理内容
如果改变影响平衡的一个条件(参加反应的物质的浓度、温度、气体反应的压强等),
则平衡将向着能够减弱这种改变的方向移动。
【理解】3
①浓度:增大反应物浓度,平衡正向移动,使反应物浓度减小一些。
②压强(化学反应前后气体分子数不等的反应):增大压强,平衡向气体分子数减小
的方向移动,使压强减小一些。
③温度:升高温度,平衡向吸热反应方向移动,使温度降低一些。
2. 解读
(1)勒夏特列原理仅适用于已达到平衡的反应体系,不可逆过程或未达到平衡的可逆
过程均不能使用该原理。此外,勒夏特列原理对所有的动态平衡(如溶解平衡、电离平衡
和水解平衡等)都适用。
(2) 勒夏特列原理 只适用于判断改变影响平衡的一个因素时平衡移动的方向。 若同时
改变影响平衡移动的几个因素,则不能简单地根据勒夏特列原理来判断平衡移动的方向,
只有在改变的条件对平衡移动的方向影响一致时,才能根据勒夏特列原理进行判断。
(3) 勒夏特列原理中的“减弱”不等于“消除”,更不是“扭转” , 即平衡移动不能
将外界影响完全消除,而只能减弱。如平衡体系的压强为p,若其他条件不变,将体系的
压强增大到2p,平衡将向气体分子数减小的方向移动,达到新平衡时体系的压强介于 p-2p
之间。
【易错】应用勒夏特列原理时应弄清是否真的改变了影响化学平衡的条件。如改变平
衡体系中固体或纯液体的量,或对于有气体存在的化学平衡体系,在恒温恒容条件下充入
“惰性气体”,均未改变影响化学平衡的因素。
【小结】
1. 浓度对平衡移动与速率之间关系的影响
第12页化学平衡 以可逆反应mA(g)+nB(g) pC(g)+qD(g)为例
体系浓度 减小生成物浓
增大反应物浓度 增大生成物浓度 减小反应物浓度
变化 度
平衡移动
正向移动 逆向移动 逆向移动 正向移动
方向
v(逆)瞬间减
v ( 正 ) 瞬 间 增 v ( 逆 ) 瞬 间 增 v ( 正 ) 瞬 间 减
小,v(正)缓
大,v(逆)缓慢 大,v(正)缓慢 小,v(逆)缓慢
速率变化 慢减小,且 v
增大,且v´(正) 增大,且v´(逆) 减小,且v´(逆)
´ ( 正 ) > v
>v´(逆) >v´(正) >v´(正)
´(逆)
图像
【图像变化规律】通过改变浓度影响化学平衡时,速率—时间图像和浓度—时间图像
中主动改变的一方突变,因平衡移动改变的一方渐变。
2. 温度对平衡移动与速率之间关系的影响
以可逆反应mA(g)+nB(g) pC(g)+qD(g)为例。
温度变化 ΔH>0 ΔH<0 ΔH<0 ΔH>0
温度变化 升温 升温 降温 降温
平衡移动
正向移动 逆向移动 正向移动 逆向移动
方向
v(正)v(逆) v(正)v(逆)
v(正)v(逆)同 v(正)v(逆)同
同时增大,且v 同时减小,且 v
速率变化 时 增 大 , 且 v 时 减 小 , 且 v
´ ( 正 ) > v ´ ( 正 ) > v
´(逆)>v´(正) ´(逆)>v´(正)
´(逆) ´(逆)
图像
【图像变化规律】改变温度,速率—时间图像都是突变,浓度—时间图像都是渐变。
3. 压强对平衡移动与速率之间关系的影响
第13页m、n、p、q
m+n>p+q ΔH<0 ΔH<0 ΔH>0
间的关系
体系压强变
加压 加压 减压 减压
化
平衡移动方
正向移动 逆向移动 正向移动 逆向移动
向
v(正)v(逆) v(正)v(逆) v(正)v(逆) v(正)v(逆)
同时增大,且 v 同时增大,且 v 同时减小,且v 同时减小,且 v
速率变化
´ ( 正 ) > v ´ ( 逆 ) > v ´ ( 正 ) > v ´ ( 逆 ) > v
´(逆) ´(正) ´(逆) ´(正)
图像
【图像变化规律】对于反应前后气体体积改变的可逆反应,改变压强,影响平衡,速
率—时间图像和浓度—时间图像都突变。
4. 催化剂对化学平衡的影响
对速率的影响
条件改变 平衡移动方向 说明
v v 结果
正 逆
正催化剂 增大 增大 v = v 不移动 可缩短达到平衡时所需时间
正 逆
负催化剂 减小 减小 v = v 不移动 可延长达到平衡时所需时间
正 逆
例题1 下列变化过程能用勒夏特列原理解释的是( )
A. 工业合成氨中选择高温条件下进行
B. 棕红色NO 加压后颜色先变深后变浅
2
C. SO 催化氧化成SO 的反应,往往需要使用催化剂
2 3
D. H 、I、HI平衡混合气加压后颜色变深
2 2
【答案】B
【解析】选择高温,平衡逆向移动,不利于合成氨,A项错误;使用催化剂只能加快
第14页反应速率,对化学平衡移动无影响,C项错误;H 、I 、HI混合气体加压平衡不移动,但
2 2
颜色加深,D项错误;只有B项能用勒夏特列原理解释。
例题2 某密闭容器中发生如下反应:X(g) + 3Y(g) 2Z(g) ΔH<0,
如图表示该反应的速率(v)随时间(t)变化的关系,t、t、t 时刻外界条件有所改变,但
2 3 5
都没有改变各物质的初始加入量。下列说法中正确的是( )
A. t 时升高了温度
2
B. t 时降低了温度
3
C. t 时增大了压强
5
D. t 时反应物转化率最低
6
【答案】D
【解析】由图可知,t 时正、逆反应速率同等程度增大;t 时正、逆反应速率均减小,
2 3
但正反应速率减小得更多,平衡逆向移动;t 时正、逆反应速率均增大,逆反应速率增大
5
得更多,平衡逆向移动,结合可逆反应的特点及平衡移动来解答。正反应为放热反应,若
t 时升高温度,则平衡逆向移动,与图像不符,图像中t 时正、逆反应速率同等程度增大,
2 2
应为使用催化剂,故A错误。该反应反应前后气体分子数减小,若t 时减小压强,正、逆
3
反应速率均减小,但正反应速率减小得更多,平衡逆向移动,与图像相符;正反应放热,
若t3时降低温度,平衡正向移动,与图像不符,则应为减小压强,故 B错误。该反应为放
热反应,且反应前后气体分子数减小,t 时正、逆反应速率均增大,且平衡逆向移动,则
5
应为升高温度,故C错误。由图可知,t 时改变条件平衡未移动,t 时改变条件平衡逆向移
2 3
动,t 时改变条件平衡继续逆向移动,则t 时反应物的转化率最低,故D正确。
5 6
【点拨】化学平衡的图像需看清楚横、纵坐标表示的意义,对于速率一时间图像,确
定条件改变后平衡移动的方向,再判断图像是否正确。
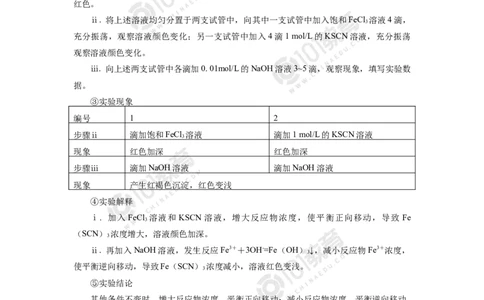
第15页例题3 下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,
其中图像和实验结论表述均正确的是( )
A. ①是其他条件一定,反应速率随温度变化的图像,正反应ΔH>0
B. ②是在平衡体系的溶液中溶入少量KCl晶体后化学反应速率随时间变化的图像
C. ③是在有无催化剂存在下建立的平衡图像,b是使用催化剂时的曲线
D. ④是一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p>p
1 2
【答案】A
【解析】由图可知,反应达到平衡时,升高温度正反应速率大于是逆反应速率,平衡
正向移动,则正反应ΔH>0,A正确;该反应实质为Fe3++3SCN- Fe(SCN) ,故KCl
3
对FeCl +3KSCN Fe(SCN) +3KCl 的平衡移动无影响,反应速率不变,与图像不符,
3 3
B错误;使用催化剂加快反应速率,但不影响平衡移动,则 a是使用催化剂时的曲线,C
错误;加入B,可促进A的转化,但压强对该反应的平衡移动无影响,压强与转化率的关
系与图像不符,D错误。
【点拨】速率一温度图像中,升高温度,吸热方向的反应速率随温度升高增大得较多,
反映在图像中为斜率较大,曲线较陡。
(答题时间:40分钟)
一、选择题
1. 在一定的温度和压强下,合成氨反应 3H(g)+N(g) 2NH (g)达到平衡时,
2 2 3
下列操作平衡不发生移动的是( )
A. 恒温恒容充入氨气 B. 恒温恒容充入氮气
C. 恒温恒容充入氦气 D. 恒温恒压充入氦气
2. 在CuCl 水溶液中存在如下平衡:[Cu(HO) ]2+(蓝)+4Cl- [CuCl ]2-
2 2 4 4
(绿)+4HO能使黄绿色CuCl 溶液向蓝色转化的操作是( )
2 2
A. 加入少量食盐晶体
B. 加入少量CuCl 固体
2
C. 加入少量CuSO 固体
4
第16页D. 加入少量AgNO 固体
3
3. 对处于平衡状态的反应:2A(g)+B(g) 2C(g) ΔH<0,下列叙述正确的
是( )
A. 增大压强,v(正)增大,v(逆)减小
B. 升高温度,v(正)减小,v(逆)增大
C. 增大A浓度的瞬间,v(正)增大,v(逆)不变
D. 增大A浓度的瞬间,v(正)增大,v(逆)减小
4. 在常温下,下列可逆反应达平衡后,压缩容器容积增大压强,平衡发生移动的是(
)
A. Cl +HO H++Cl-+HClO
2 2
B. 2NO (g) 2NO(g)+O(g)
2 2
C. 2HI(g) H(g)+I (g)
2 2
D. FeCl +3KSCN Fe(SCN)+3KCl
3 3
*5. 已知反应A(g)+2B (g) 2AB (g) ΔH<0,下列说法正确的是( )
2 2 2
A. 升高温度,正反应速率增加,逆反应速率减小
B. 升高温度有利于反应速率的增加,从而缩短达到平衡所需的时间
C. 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D. 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
二、填空题
*6. 反应:mA+nB pC在某温度下达到平衡时:
(1)若A、B、C都是气体,减压后,正反应速率小于逆反应速率,则m、n、p的关
系为________。
(2)若只有C为气体,且m+n=p,在加压时,化学平衡发生移动,则平衡必定是向
________方向发生移动。
(3)如果在体系中增加或减少 B 的量,平衡均不移动,则 B 是________态或
________态。
(4)若升高温度,A的转化率减小,则此反应的逆反应是________反应。
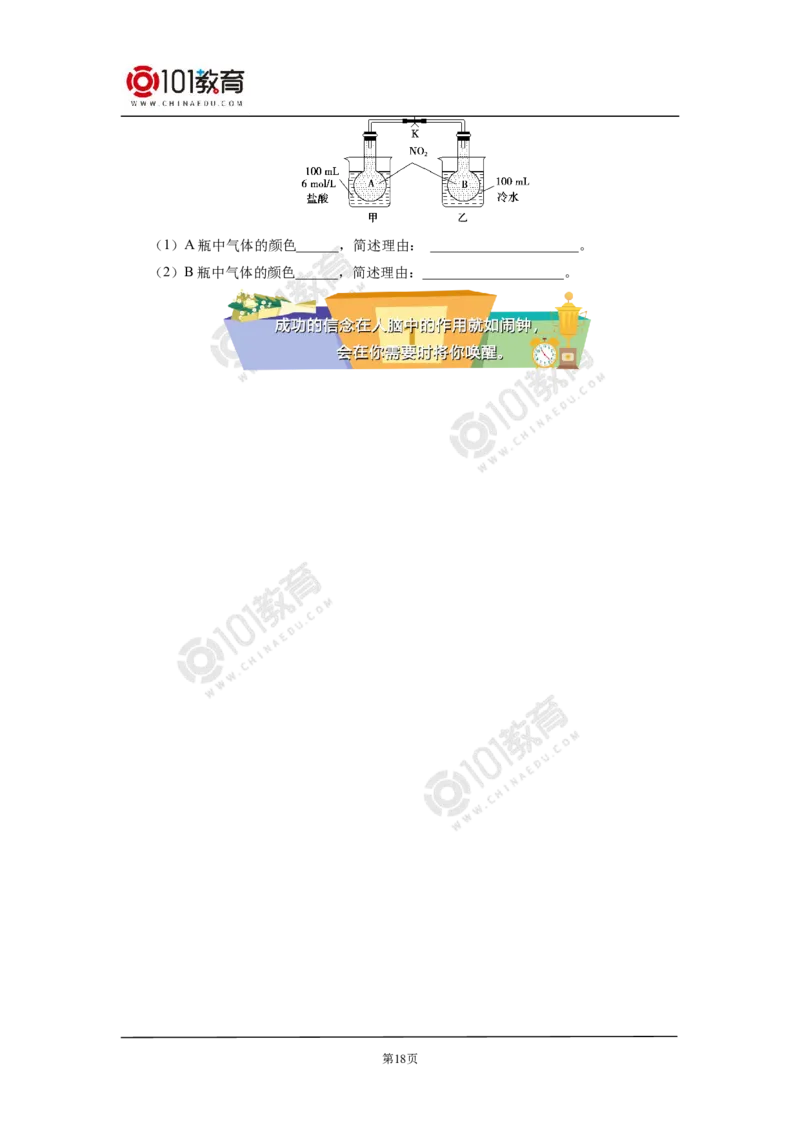
7. 如图所示,烧杯甲中盛放100 mL 6 mol·L-1 HCl溶液,烧杯乙中盛放100 mL冷水,
现向烧杯甲的溶液中放入25 g NaOH固体,同时向烧杯乙中放入25 g NH NO 固体,搅拌
4 3
使之溶解。
第17页(1)A瓶中气体的颜色______,简述理由: _____________________。
(2)B瓶中气体的颜色______,简述理由:____________________。
第18页1.【答案】C
【解析】A项增大了c(NH ),平衡逆向移动;B项增大了c(N ),平衡正向移动;
3 2
C项对各组分的浓度无影响,平衡不移动;D项容器容积增大,相当于减压,平衡逆向移
动。
2.【答案】D
【解析】加入食盐晶体或CuCl 固体,溶液中Cl-浓度增大,平衡右移,A、B错误;
2
加入CuSO 固体,对平衡无影响,C错误;加入AgNO 固体,与Cl-反应,使c(Cl-)降
4 3
低,平衡逆向移动,溶液变为蓝色,D正确。
3.【答案】C
【解析】增大压强,正、逆反应速率都增大,A错误;升高温度,正、逆反应速率都
增大,B错误;增大A浓度的瞬间,v(正)增大,v(逆)不变,C正确,D错误。
4.【答案】B
【解析】A、D项,是在溶液中进行的反应,压强对平衡无影响;B项,增大压强化学
平衡逆向移动;C项,属于气体体积不变的反应,增大压强平衡不移动。
5.【答案】(1)m+n>p (2)逆反应 (3)液 固 (4)吸热
【解析】(1)若A、B、C都是气体,减压后,正反应速率小于逆反应速率,则平衡
逆向移动,故m+n>p。(2)若只有C为气体,m+n=p,则加压时,平衡向气体化学计
量数小的方向移动,即逆向移动。(3)若增加或减少B的量,平衡均不移动,则B为固
态或液态。(4)升高温度,A的转化率减小,则平衡逆向移动,此反应的逆反应为吸热反
应。
6.【答案】B
【解析】A (g)+2B (g) 2AB (g)是放热反应,且是气体体积减小的反应。
2 2 2
所以升高温度,平衡向逆反应方向移动;增大压强,平衡向正反应方向移动,C、D均错
误。升高温度,正、逆反应速率均加快,达到平衡需要的时间减少,A错误;正确答案为
B。
7.【答案】(1)变深 NaOH溶解放热,中和HCl也放热,甲中溶液及A中气体温度升
高,2NO (g) NO(g) ΔH<0,平衡逆向移动,NO 浓度增大,颜色加深
2 2 4 2
(2)变浅 NH NO 溶解吸热,乙中溶液及 B 中气体温度降低,2NO NO
4 3 2 2 4
ΔH<0,平衡正向移动,NO 浓度减小,颜色变浅
2
【解析】甲中氢氧化钠溶解及盐酸与氢氧化钠发生中和反应均放出热量;乙中
NH NO 固体溶解要吸收热量。2NO (g) NO (g) ΔH<0,温度升高,平衡向逆
4 3 2 2 4
反应方向移动,颜色加深;温度降低,平衡向正反应方向移动,颜色变浅。
第19页第20页