文档内容
第一章 原子结构与性质
第二节 原子结构与元素的性质
1.2.2 元素周期律
一.选择题
1. 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Y、Z的族序数之和为
12;X与Y的电子层数相同;向过量的ZWY溶液中滴入少量硫酸铜溶液,观察到既有黑色沉
淀生成又有臭鸡蛋气味的气体放出。下列说法正确的是
A. 原子半径由大到小的顺序为:
B. 酸性:
C. ZWY是离子化合物,其水溶液中只存在电离平衡
D. 单质熔点:
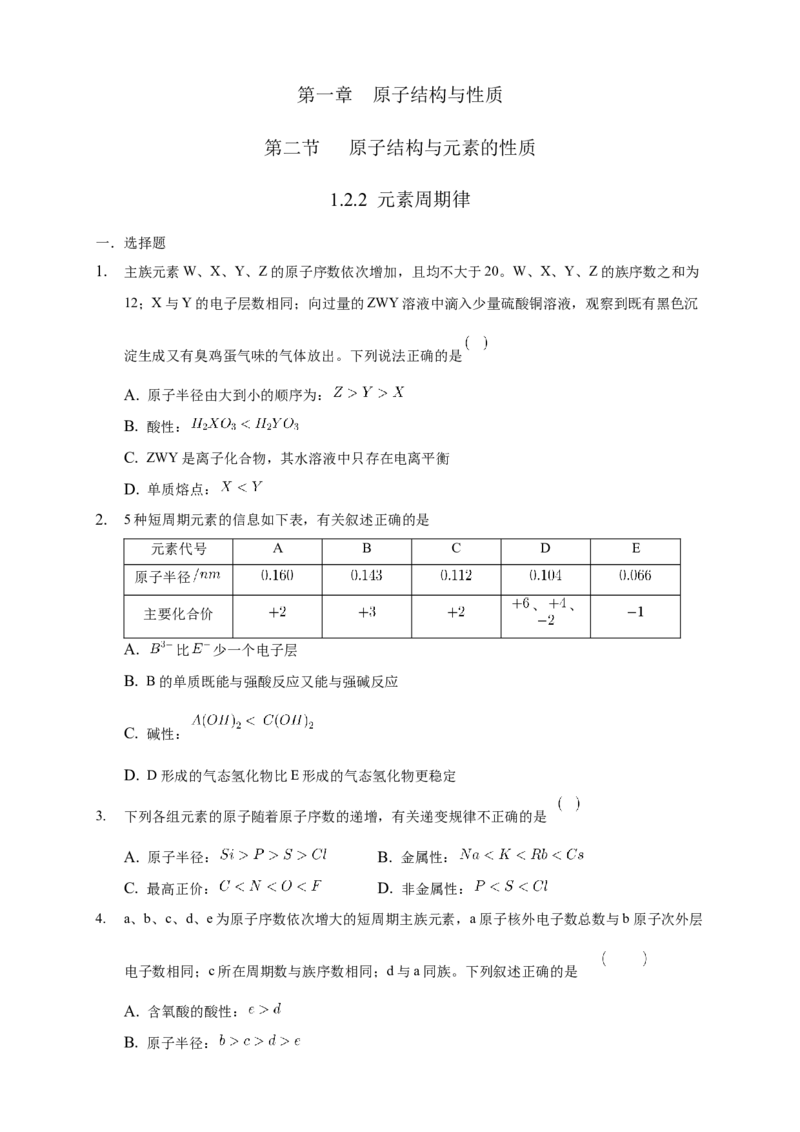
2. 5种短周期元素的信息如下表,有关叙述正确的是
元素代号 A B C D E
原子半径
、 、
主要化合价
A. 比 少一个电子层
B. B的单质既能与强酸反应又能与强碱反应
C. 碱性:
D. D形成的气态氢化物比E形成的气态氢化物更稳定
3. 下列各组元素的原子随着原子序数的递增,有关递变规律不正确的是
A. 原子半径: B. 金属性:
C. 最高正价: D. 非金属性:
4. a、b、c、d、e为原子序数依次增大的短周期主族元素,a原子核外电子数总数与b原子次外层
电子数相同;c所在周期数与族序数相同;d与a同族。下列叙述正确的是
A. 含氧酸的酸性:
B. 原子半径:C. 由a和b两种元素形成的化合物不可能含共价键
D. b、c元素对应最高价氧化物的水化物之间不可能发生反应
5. 下列关于元素周期表和元素周期律的说法不正确的是
A. 第ⅦA族从氟到碘,简单氢化物的稳定性逐渐减弱
B. 因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强
C. 第三周期从钠到氯,最高价氧化物对应水化物的碱性逐渐减弱,酸性逐渐增强
D. 氧与硫为同主族元素,氧比硫的原子半径小、非金属性强
6. 下列各组性质比较中,正确的有 个
沸点: ; 离子还原性: ;
酸性: ; 金属性: ;
气态氢化物稳定性: ; 半径: 。
A. 5 B. 4 C. 3 D. 2
7. 元素W、X、Y和Z在周期表中的相对位置如图所示,其中元素Z位于
第四周期,W、X、Y原子的最外层电子数之和为18,下列说法正确的
是
A. 氢化物沸点:
B. 原子半径的大小:
C. 氧化物的水化物的酸性:
D. 推测Z是半导体材料,Z与Y可形成化合物
8. 元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其
原子半径及主要化合价列表如下,其中 用于呼吸面具或潜水艇中作为氧气来源。
元素代号 M R Q T X Y Z
原子半径
主要化合价 、 、
下列说法正确的是
A. T、Z的最高价氧化物对应水化物的酸性
B. R、X、Y的单质失去电子能力最强的是X
C. M与Q两种元素形成的是离子化合物
D. M、Q、Z都在第2周期9. 几种短周期元素的原子半径和主要化合价见下表,下列有关说法中,正确的是
元素代号 X Y Z L M Q
原子半径
主要化合价 、 、
A. 与稀盐酸反应的剧烈程度:M单质 单质
B. Y与Q形成的化合物一定不能与氢氧化钠溶液反应
C. 简单氢化物稳定性:
D. 等物质的量的X、Y的单质与足量盐酸反应,生成 一样多
10. 运用元素周期律分析下面的推断,其中错误的是
A. 已知Ra是第七周期第ⅡA族元素,故 的碱性比 的碱性强
B. 已知As是第四周期第ⅤA族元素,故A 的稳定性比 的稳定性弱
C. 已知Cs是第六周期第ⅠA族元素,原子半径比Na的原子半径大,Cs与水反应比Na与水
反应更剧烈
D. 已知Cl的非金属性比S强,故HClO的酸性比 的强
11. X、Y、Z、W均为短周期元素,它们在元素周期表的位置如图所示。若Y原子的最外层电子
数是次外层电子的3倍,下列说法中正确的是 。
A. 原子半径: X
B. 4种元素的氢化物中,Y元素的氢化物最不稳定
C. 最高价氧化物对应水化物的酸性:
D. X的最高价氧化物对应的水化物能与其气态氢化物发生反应
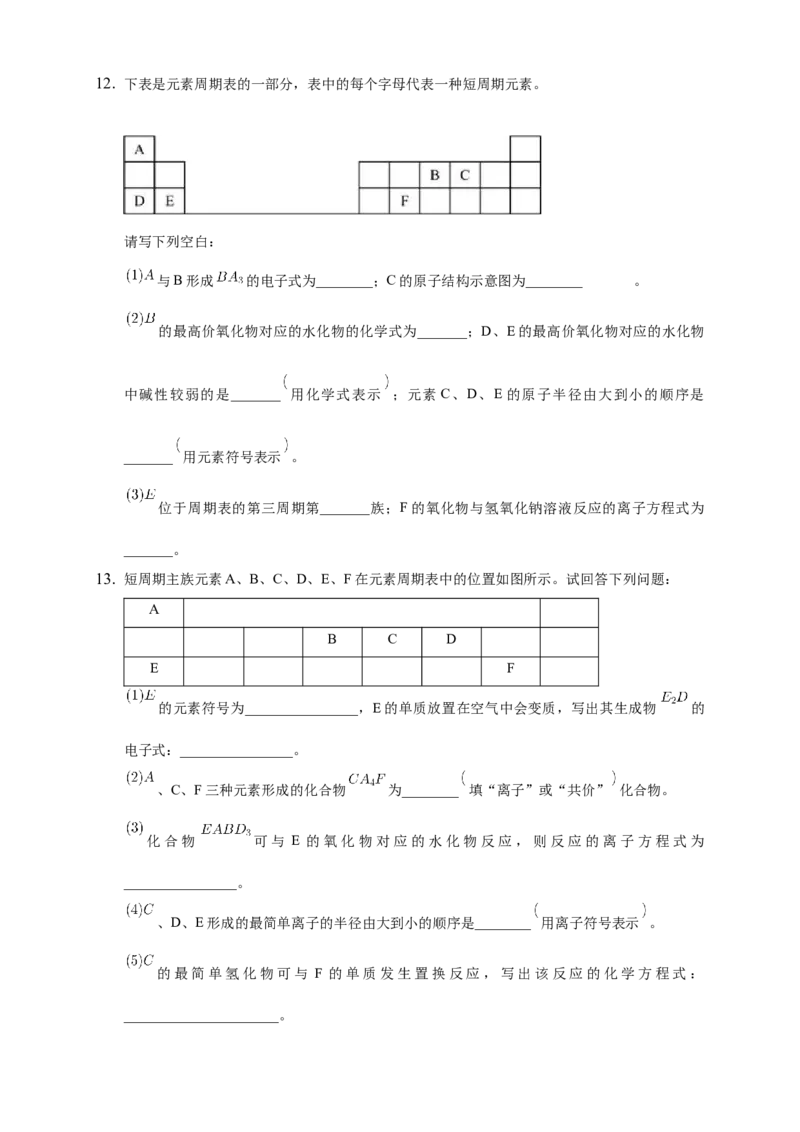
二、填空题12. 下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
请写下列空白:
与B形成 的电子式为________;C的原子结构示意图为________ 。
的最高价氧化物对应的水化物的化学式为_______;D、E的最高价氧化物对应的水化物
中碱性较弱的是_______ 用化学式表示 ;元素 C、D、E的原子半径由大到小的顺序是
_______ 用元素符号表示 。
位于周期表的第三周期第_______族;F的氧化物与氢氧化钠溶液反应的离子方程式为
_______。
13. 短周期主族元素A、B、C、D、E、F在元素周期表中的位置如图所示。试回答下列问题:
A
B C D
E F
的元素符号为________________,E的单质放置在空气中会变质,写出其生成物 的
电子式:________________。
、C、F三种元素形成的化合物 为________ 填“离子”或“共价” 化合物。
化合物 可与 E 的氧化物对应的水化物反应,则反应的离子方程式为
________________。
、D、E形成的最简单离子的半径由大到小的顺序是________ 用离子符号表示 。
的最简单氢化物可与 F 的单质发生置换反应,写出该反应的化学方程式:
______________________。元素B、C、D均能与A形成化合物,分别为 、 、 。这三种物质中沸点最高
的是________ 填化学式,下同 ,稳定性由强至弱的顺序依次为________。
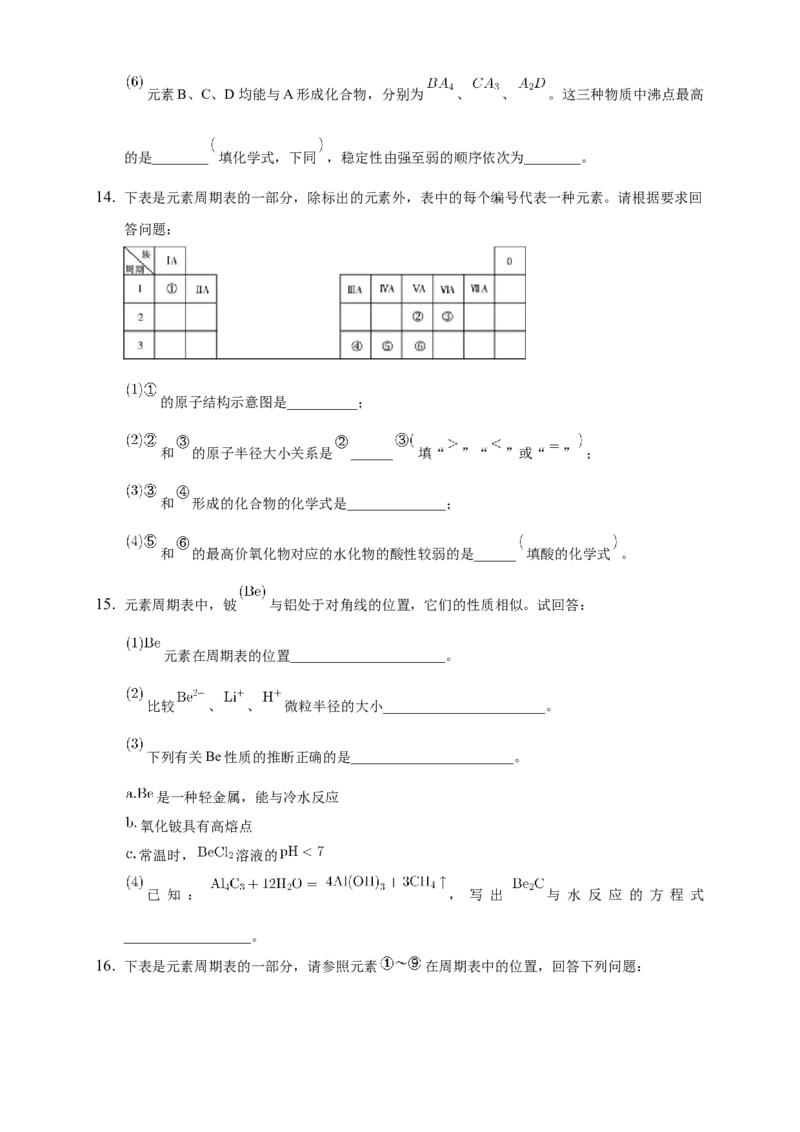
14. 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回
答问题:
的原子结构示意图是__________;
和 的原子半径大小关系是 ______ 填“ ”“ ”或“ ” ;
和 形成的化合物的化学式是______________;
和 的最高价氧化物对应的水化物的酸性较弱的是______ 填酸的化学式 。
15. 元素周期表中,铍 与铝处于对角线的位置,它们的性质相似。试回答:
元素在周期表的位置______________________。
比较 、 、 微粒半径的大小_______________________。
下列有关Be性质的推断正确的是_______________________。
是一种轻金属,能与冷水反应
氧化铍具有高熔点
常温时, 溶液的
已 知 : , 写 出 与 水 反 应 的 方 程 式
__________________。
16. 下表是元素周期表的一部分,请参照元素 在周期表中的位置,回答下列问题:族
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
周期
1
2
3
表中化学性质最不活泼的元素,其原子结构示意图为________________。
分别与 、 、 形成的简单化合物中,最稳定的是________ 填化学式 。
、 、 的原子半径由小到大的顺序为___________________ 填元素符号 。
、 、 的最高价氧化物对应水化物酸性由强到弱的顺序为________________ 填化学
式 。
两元素形成的淡黄色固体物质的电子式为_____________________,该物质含有的化学键
类型是_____________________。
表中最高价氧化物对应水化物具有两性的元素是________________ 填序号 ,写出该元素
的 单 质 与 元 素 的 最 高 价 氧 化 物 对 应 水 化 物 的 水 溶 液 反 应 的 离 子 方 程 式
________________________。