文档内容
《分子结构与物质的性质》第一课时 教学设计
课题 《分子结构与物质 单元 2 学科 化学 年级 高二
的性质》
本章内容比较系统地介绍了分子的结构与性质,内容比较丰富。首先,在第一章有关
电子云和原子轨道等概念的基础上,介绍了共价键的主要类型δ键和π键,以及键参数
——键能、键长、键角;接着,在共价键概念的基础上,介绍了分子的立体结构,并根据价层
电子对互斥理论和杂化轨道理论对简单共价分子结构的多样性和复杂性进行了解释;最
后,介绍了极性分子和非极性分子、分子间作用力、氢键等概念,以及它们对物质性质的影
响,并从分子结构的角度说明了“相似相溶“规则、无机含氧酸分子的酸性等。本节教学内
教材
容是人教版高中化学选择性必修第二册第二章《分子结构与性质》第三节《分子结构与物质
分析 的性质》第一课时。这一课时的教学内容主要是共价键的极性。
本节安排了“共价键的极性、分子的极性以及键的极性对物质性质的影响”这部分内
容。学生通过学习这部分知识,认识杂共价键的分类,知道共价键的极性与非极性的判断方
法,能从键的极性角度去理解分子的极性。掌握分析极性的判断方法,建立分子极性判断的
思维模型。学生能够在分子水平上,从分子结构的视角认识物质的性质,进一步形成有关物
质结构的基本观念;学生的学习兴趣能得到有效保持,学生的科学素养能得到进一步提高。
宏观辨识与微观探析:通过对共价键的极性的学习,能从微观角度理解极性共价键与
教学目 非极性共价键。
标与核
心素养 证据推理与模型认知:通过对分子极性的学习,掌握分子极性的判断方法,建立分子极
性与键极性的关联思维模型。
重点 共价键的极性、分子的极性
难点教学过程
教学环节 教师活动 学 生 活 设计意图
动
导入新课 【旧知回顾】共价键根据不同分类标准可以有多种分类。 思 考 回 通过回顾,
顾 引发学生
兴趣,提高
学生学习
积极性。
讲授新课 第三节 分子结构与物质的性质
第一课时 共价键的极性
一、键的极性
1.共价键的分类
极性共价键:由不同原子形成的共价键,电子对会发生偏移。 通过回顾
非极性共价键:由相同原子形成的共价键,电子对不发生偏 共价键的
移。 类型,认识
2.键的极性 共价键的
极性与非
极性,能从
组成元素、
共用电子
对的偏移、
电负性差
注:(1)电负性差值越大的两原子形成的共价键的极性越强
值角度理
(2)共用电子对偏移程度越大,键的极性越强
解共价键
3.键的极性判断方法
的极性。
(1)根据组成元素:
同种元素:A-A型为非极性键
不同种元素:A-B型为极性键
(2)根据共用电子对是否偏移:
共用电子对有偏移:极性键
共用电子对没有偏移:非极性键
(3)根据元素的电负性:
成键原子电负性相同:非极性键
成键原子电负性不同:极性键 了解极性
注意:键的极性只取决于成键原子的元素种类或电负性的差 可以用极
异,与其他因素无关。 性向量来
同种非金属元素原子间形成的共价键是非极性键 认 真 思 表示,从而
不同种非金属元素原子间形成的共价键是极性键 考 形象的理
根据共用电子对是否偏移,共价键有极性键、非极性键之分。 解极性的以共价键结合的分子是否也有极性分子、非极性分子之分呢? 概念。
分子的极性又是根据什么来判定呢?
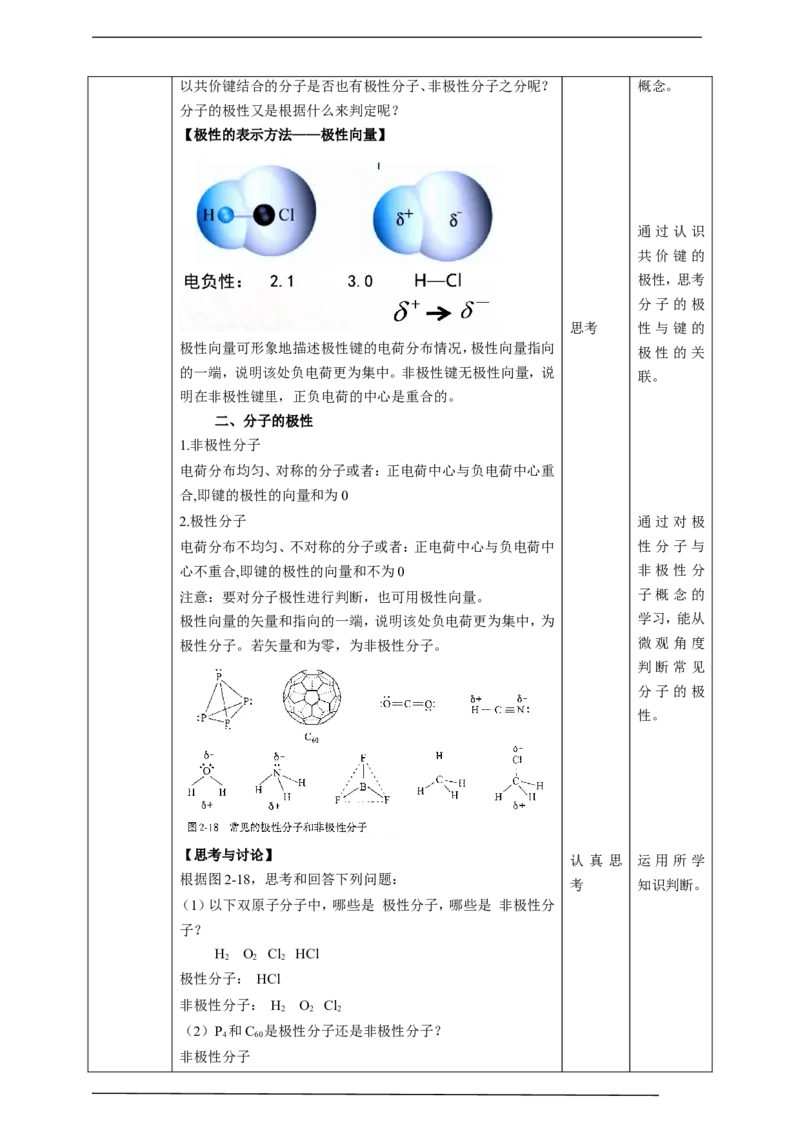
【极性的表示方法——极性向量】
通过认识
共价键的
极性,思考
分子的极
思考 性与键的
极性向量可形象地描述极性键的电荷分布情况,极性向量指向
极性的关
的一端,说明该处负电荷更为集中。非极性键无极性向量,说
联。
明在非极性键里,正负电荷的中心是重合的。
二、分子的极性
1.非极性分子
电荷分布均匀、对称的分子或者:正电荷中心与负电荷中心重
合,即键的极性的向量和为0
2.极性分子 通过对极
电荷分布不均匀、不对称的分子或者:正电荷中心与负电荷中 性分子与
心不重合,即键的极性的向量和不为0 非极性分
注意:要对分子极性进行判断,也可用极性向量。 子概念的
极性向量的矢量和指向的一端,说明该处负电荷更为集中,为 学习,能从
极性分子。若矢量和为零,为非极性分子。 微观角度
判断常见
分子的极
性。
【思考与讨论】
认 真 思 运用所学
根据图2-18,思考和回答下列问题:
考 知识判断。
(1)以下双原子分子中,哪些是 极性分子,哪些是 非极性分
子?
H O Cl HCl
2 2 2
极性分子: HCl
非极性分子: H O Cl
2 2 2
(2)P 和C 是极性分子还是非极性分子?
4 60
非极性分子(3)以下化合物分子中,哪些是极性分子,哪些是非极性分 归纳总结
子?
CO HCN H O NH BF CH CHCl
2 2 3 3 4 3
极性分子: HCN HO NH CHCl
2 3 3
非极性分子: CO BF CH
2 3 4
【总结】
判断分子的极性可依据分子中化学键的极性的向量和。
只含非极性键的分子一定是非极性分子;含极性键的分子有没
有极性,必修依据分子中极性键的极性的向量和是否等于零而
定。当分子中各个键的极性的向量和等于零时,是非极性分
子,否则是极性分子。或者,我们可根据分子的正电中心和负
电中心是否重合来判断它是否是极性分子。
3.分子的极性的判断方法
注意:取决于原子间的共价键是否有极性。
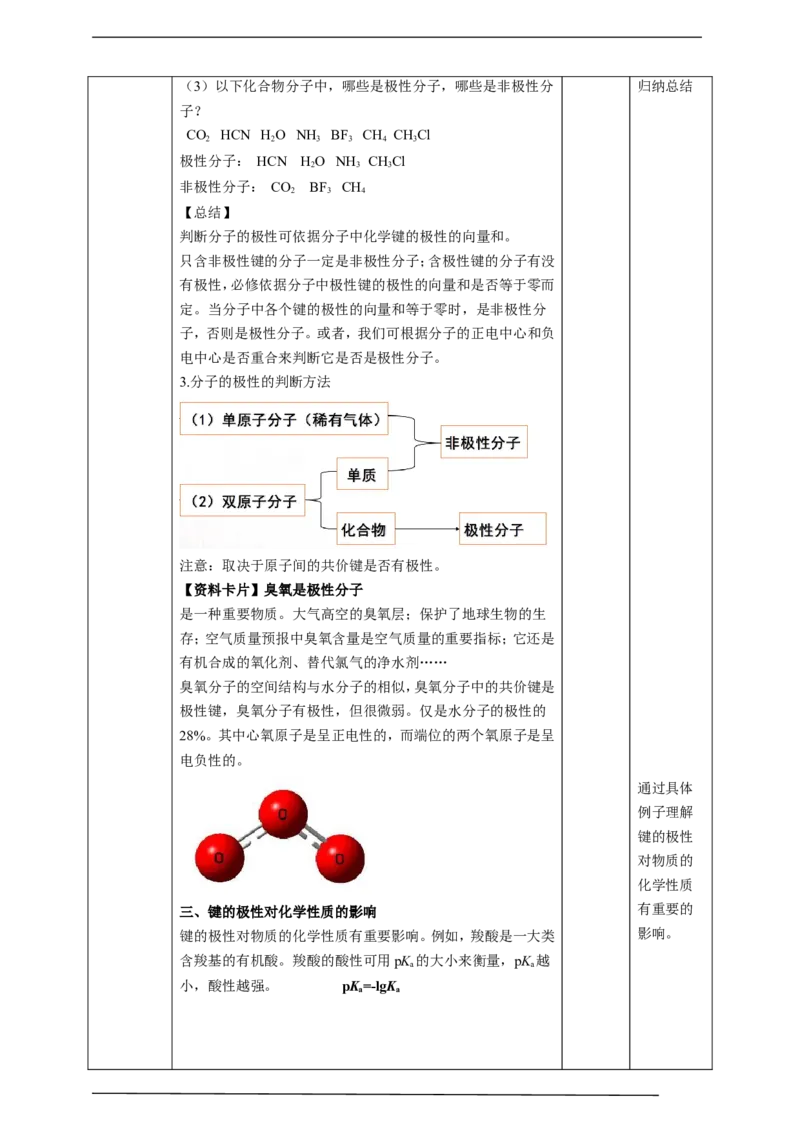
【资料卡片】臭氧是极性分子
是一种重要物质。大气高空的臭氧层;保护了地球生物的生
存;空气质量预报中臭氧含量是空气质量的重要指标;它还是
有机合成的氧化剂、替代氯气的净水剂……
臭氧分子的空间结构与水分子的相似,臭氧分子中的共价键是
极性键,臭氧分子有极性,但很微弱。仅是水分子的极性的
28%。其中心氧原子是呈正电性的,而端位的两个氧原子是呈
电负性的。
通过具体
例子理解
键的极性
对物质的
化学性质
三、键的极性对化学性质的影响 有重要的
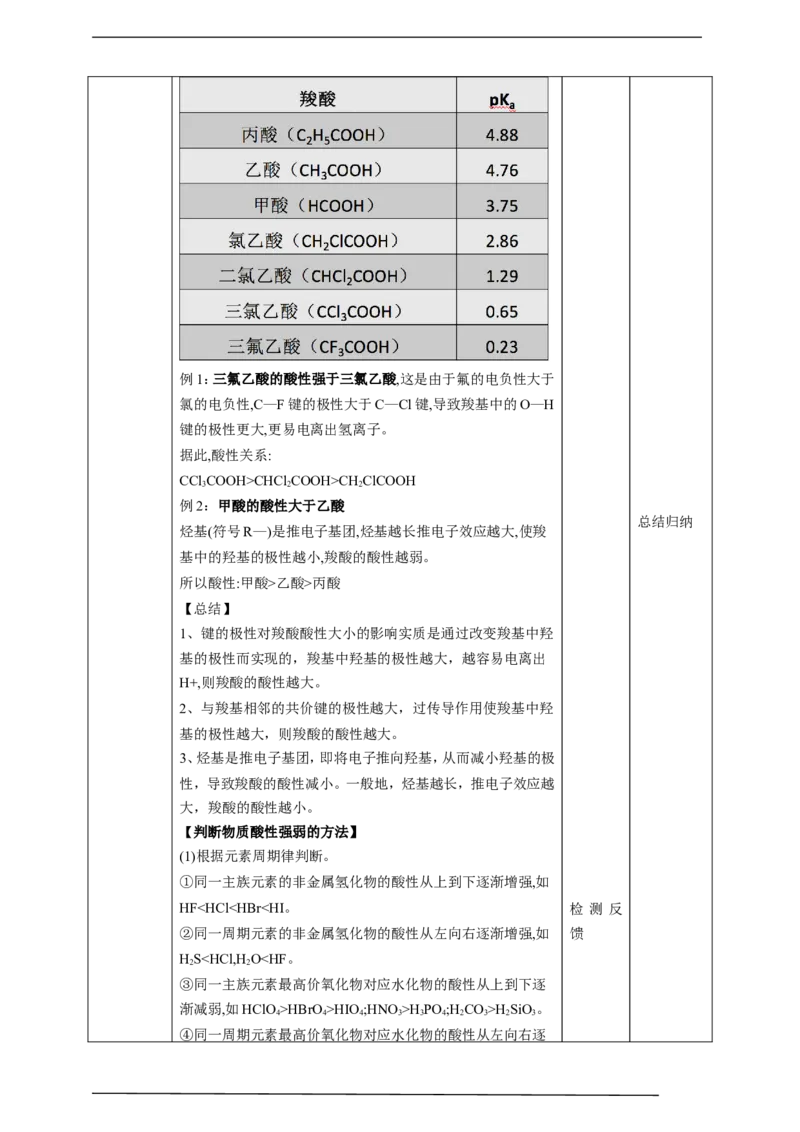
键的极性对物质的化学性质有重要影响。例如,羧酸是一大类 影响。
含羧基的有机酸。羧酸的酸性可用pK 的大小来衡量,pK 越
a a
小,酸性越强。 pK =-lgK
a a例1:三氟乙酸的酸性强于三氯乙酸,这是由于氟的电负性大于
氯的电负性,C—F键的极性大于C—Cl键,导致羧基中的O—H
键的极性更大,更易电离出氢离子。
据此,酸性关系:
CCl COOH>CHCl COOH>CH ClCOOH
3 2 2
例2:甲酸的酸性大于乙酸
总结归纳
烃基(符号R—)是推电子基团,烃基越长推电子效应越大,使羧
基中的羟基的极性越小,羧酸的酸性越弱。
所以酸性:甲酸>乙酸>丙酸
【总结】
1、键的极性对羧酸酸性大小的影响实质是通过改变羧基中羟
基的极性而实现的,羧基中羟基的极性越大,越容易电离出
H+,则羧酸的酸性越大。
2、与羧基相邻的共价键的极性越大,过传导作用使羧基中羟
基的极性越大,则羧酸的酸性越大。
3、烃基是推电子基团,即将电子推向羟基,从而减小羟基的极
性,导致羧酸的酸性减小。一般地,烃基越长,推电子效应越
大,羧酸的酸性越小。
【判断物质酸性强弱的方法】
(1)根据元素周期律判断。
①同一主族元素的非金属氢化物的酸性从上到下逐渐增强,如
HFHBrO>HIO;HNO >H PO ;H CO>H SiO。
4 4 4 3 3 4 2 3 2 3
④同一周期元素最高价氧化物对应水化物的酸性从左向右逐渐增强,如HPO