文档内容
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
1. 了解晶体与非晶体的区别,了解获得晶体的一般途径。
2. 知道物质的聚集状态会影响物质的性质,通过改变物质的聚集状态能获得特殊的材料。
3. 认识简单的晶胞,类推其他晶胞的分析方法。
4. 知道晶体X射线衍射实验是测定物质结构的基本方法和实验手段。
5. 学会晶胞中微粒数的计算方法(均摊法),能根据晶胞的结构确定晶体的化学式。
重点:晶体与非晶体的区别;晶体的自范性、各向异性,结晶的方法、对晶胞的认识
难点:晶体与非晶体的区别、对晶胞的认识
一、物质聚集状态
1.物质聚集状态
除了三态,还有更多的物质聚集状态,如 、离子液体、晶态、非晶态,以及介乎晶态
和非晶态之间的塑晶态、 等。
2.等离子体
(1)概念:气态物质在 或者在 激发下,分子发生分解,产生 等。这种
由电子、阳离子和电中性粒子组成的整体上呈 的物质 称为等离子体。
(2)特点
等离子体具有良好的 和 。
(3)应用
运用等离子体显示技术可以制造等离子体显示器;
利用等高子体可以进行化学合成;
核聚变也是在等离子态下发生的等。
3.液晶
(1)概念:物质加热到达到熔点后,先呈浑浊态,再加热达到一定温度时,浑浊态变透明清亮态,将熔点至澄清点温度范围内的物质状态称为液晶。
(2)特征:
液晶是介于 和 之间的物质状态,既具有液体的流动性、黏度、性变形等,
又具有晶体的某些物理性质,如导热性、光学性质等。
(3)应用
液晶已有广泛的应用。例如,手机、电脑和电视的液晶显示器,由于施加电场可使液晶的长轴取向
发生不同程度的改变,从而显示数字、文字或图像。再如,合成高强度液晶纤维已广泛应用于飞
机、火箭、坦克、舰船、防弹衣、防弹头盔等。
二、晶体和非晶体
1.晶体和非晶体的概念
(1)晶体
概念:内部微粒(原子、离子或分子)在三维空间里呈 排列而构成的具有
的固体。
分类:根据组成晶体的微粒和微粒间的相互作用,可分为 、 、 和金属晶
体。
(2)非晶体
概念:内部微粒(原子、离子或分子)在三维空间里呈 排列而构成的 规则几何外形的
固体。
(3)晶体和非晶体的本质差异
自范性 微观结构
晶体
非晶体
[学生活动]
具有规则几何外形的固体一定是晶体吗?
2.晶体的特点
(1)自范性
概念:晶体能 多面体外形的性质。
晶体呈现自范性的条件之一: 。如熔融物质冷却凝固速率过快时,常常只得到看不到多面体外形的粉末或没有规则的外形的块状物。
晶体的自范性是晶体中粒子在微观空间里呈现周期性的有序排列的 。
(2)各向异性
同一晶体中,在不同方向上质点排列一般是不一样的,因此,晶体的许多物理性质,如
、 、导电性、光学性质等,常常随方向的不同而有所差异。
(3)熔点
晶体有 的熔点,而非晶体没有固定熔点。
(4)晶体能使X-射线产生的衍射
晶体物质能使X-射线产生 ,非晶体只有散射效应。这是测定晶体结构的重要实验方法。
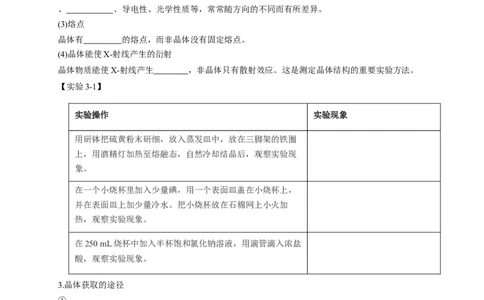
【实验3-1】
实验操作 实验现象
用研钵把硫黄粉末研细,放入蒸发皿中,放在三脚架的铁圈
上,用酒精灯加热至熔融态,自然冷却结晶后,观察实验现
象。
在一个小烧杯里加入少量碘,用一个表面皿盖在小烧杯上,
并在表面皿上加少量冷水。把小烧杯放在石棉网上小火加
热,观察实验现象。
在250 mL烧杯中加入半杯饱和氯化钠溶液,用滴管滴入浓盐
酸,观察实验现象。
3.晶体获取的途径
① 。
② 。
③ 。
【思考与讨论】
(1) 图3-7是某同学找到的一张玻璃结构的示意图,根据这张图判断玻璃是不是晶
体?为什么?
(2) 根据晶体物理性质的各向异性的特点,能鉴别用玻璃仿造的假宝石。请你列举一些可能有效的方法鉴别假宝石。
【总结】
固体 外观 微观结构 自范性 各向异性 熔点
晶体
非晶体
本质区别
三、晶胞
1.晶胞的概念
描述晶体结构的 叫做晶胞。晶胞是晶体中最小的 。
2、晶体和晶胞的关系:整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。
(1)“无隙”是相邻晶胞之间 。
(2)“并置”是所有晶胞都是 排列的,取向 。
(3)所有晶胞的 及其内部的原子 、 及几何排列是完全相同的。
(4)一般来说,晶胞都是 。
3、平行六面体晶胞中粒子个数的计算。
(1)晶胞的顶角原子是 个晶胞共用的,晶胞棱上的原子是 个晶胞共用的,晶胞面上的原
子是 个晶胞共用的。
(2)晶胞中微粒数目的确定。
“均摊法”是计算每个晶胞平均拥有的粒子数目的常用方法。其基本理念是每个粒子被 n个晶
胞所共用,则该粒子有1/n属于这个晶胞。
(3) 晶胞中微粒数目的确定
[例1]金属铜晶胞中原子个数的计算。铜晶胞
金属铜的一个晶胞中,位于晶胞 的铜原子有 个,位于 的铜原有
个,金属铜晶胞中所含的铜原子数为 。
[例2]氯化钠晶胞中所含的Na+、Cl-数。
3.晶胞中粒子数目的计算(以金属铜为例):
氯化钠晶胞如图所示,其中体积较小的为 离子(填“Na+”或“Cl-”
下同),体 在 积较 铜 大 的 的 晶 为 胞 结 构 中 离,铜 子 原 ,则 子 晶 不 胞 全 中 属 含 于 该 晶 胞 ,个 按 N 均 a+ 摊 (提 原 示 则 :晶,金 胞 属 中心 铜 还 的 有 一 一 个 个Na+)和
晶胞的原子数=8× +6× =4。
个Cl-。
结合下图,钠、1锌、1碘、金刚石晶胞中含有原子的数目分别为2、2、8、
[例3]8 试。计 算钠、锌、碘、8金刚2石晶胞中含有原子的数目
钠、锌、碘、金刚石晶胞示意图
钠、锌、碘、金刚石晶胞示意图
金属钠的一个晶胞的原子数=
金属锌的一个晶胞的原子数=
碘的一个晶胞的原子数=
金刚石的一个晶胞的原子数=
四.晶体结构的测定
1.X射线衍射原理
单一波长的X射线通过晶体时,X射线和晶体中的 相互作用,会在记录仪上产生分立的
或明锐的衍射峰。
2.X射线衍射实验获得晶胞信息
晶体的X射线衍射实验图经过计算,可以获得包括晶胞 和大小、分子或原子在观空间有
序排列呈现的 、原子在晶胞里的 和位置等,以及结合晶体化学组成的信息推出原子之间的相互关系。
3.X射线衍射实验获得分子信息
通过晶体X射线衍射实验,可以测定晶胞中各个原子的 ,根据原子坐标,可以计算原
子间的 ,判断哪些原子之间存在化学键,确定 和键角,得出分子的 。
一、物质聚集状态
1.物质聚集状态
等离子体 液晶态
2.等离子体
高温 在外加电场 电子和阳离子 电中性 聚集体
导电性 流动性
3.液晶
液态 晶态
二、晶体和非晶体
1.晶体和非晶体的概念
(1)周期性 离子晶体 分子晶体 原子晶体
(2)相对无序 不具有
(3)
自范性 微观结构
晶体 有(能自发呈现多面体外形) 原子在三维空间里呈周期性有序排列
非晶体 没有(不能自发呈现多面体外形) 原子排列相对无序
[学生活动]
不一定,因为非晶体也能加工成规则的几何外形,如玻璃饰品。
2.晶体的特点
(1)自范性
自发地呈现多面体外形的性质 晶体生长的速率适当 宏观表象
(2)各向异性
硬度 导热性
(3) 熔点
固定
(4)衍射
【实验3-1】
硫加热融化,自然冷却结晶后,得到黄色晶体
固体直接变成紫色蒸气,蒸气遇冷又重新凝聚成紫黑色的固体
有白色细小晶体析出3.晶体获取的途径
熔融态物质凝固析出晶体
气态物质冷却不经液态直接凝固(凝华)
溶质从溶液中析出
【思考与讨论】
1. 晶体与非晶体的根本区别在于构成固体中的粒子在微观空间里是否呈现周期性的有序排列。观
察教科书中的图3-7玻璃的结构示意图,构成玻璃的粒子无周期性的排列,是无序的,所以玻璃是非
晶体。
2. 利用晶体与非晶体的性质差异来鉴别玻璃和宝石。宝石是晶体,具有固定的熔点和各向异性,
可用硬度、熔点、折光率等性质来鉴别宝石。
(1)可观察宝石的形状,具有多面体的外形;实验它的硬度,可在玻璃上划出痕迹,初步确定它是晶
体;
(2)可利用宝石的折光率鉴别;
(3)可利用X-射线衍射仪鉴别。
【总结】
固体 外观 微观结构 自范性 各向异性 熔点
具有自发形成的 原子在三维空间呈
晶体 有 有 固定
规则的几何外形 周期性有序排列
不能自发形成规
非晶体 原子排列相对无序 没有 没有 不固定
则的几何外形
本质区别 微观原子在三维空间里是否呈现周期性有序排列
三、晶胞
1.晶胞的概念
基本单元 重复单元
2、晶体和晶胞的关系
没有任何间隙 平行 相同
形状 种类 个数 平行六面体
3、平行六面体晶胞中粒子个数的计算。
(1)8 4 2
(3)晶胞中微粒数目的确定
[例1]面心 6 顶点 8 4
[例2]Na+ Cl- 4 4
[例3]四.晶体结构的测定
1.X射线衍射原理
电子
2.X射线衍射实验获得晶胞信息
形状 对称类型 数目
3.X射线衍射实验获得分子信息
位置(坐标) 距离 键长 空间结构
1. 下列关于晶体与非晶体的说法正确的是
A. 晶体与非晶体的本质区别在于是否有固定的熔、沸点
B. 晶体有自范性的原因是粒子在微观空间呈周期性有序排列
C. 固体食盐、水晶、塑料、胆矾、玻璃均属于晶体
D. 区分晶体与非晶体的最科学可靠的方法是检测其是否具有各向异性
【答案】B
【解析】
A.晶体与非晶体的根本区别在于其内部粒子在空间上是否按一定规律做周期性重复排列,故A错
误;
B.晶体有自范性的原因是粒子在微观空间呈周期性有序排列,故B正确;
C.塑料、玻璃没有固定的熔沸点,不属于晶体,故C错误;
D. 射线衍射法是区分晶体和非晶体的最科学的方法,故D错误。
2. 下列有关晶胞的说法正确的是
A. 晶胞是晶体中最小的结构单元
B. 晶胞中所有的粒子都为几个晶胞共用
C. 晶胞均为长方体
D. 不同晶体的晶胞不一定相同
【答案】D
【解析】
A.晶胞是晶体的最小重复单元,但不一定是最小结构单元,故A错误;
B.晶胞中有些粒子为晶胞独自拥有,故B错误;
C.晶胞多数为平行六面体,不一定为长方体,故C错误;D.不同晶体的晶胞可能相同,也可能不相同,故D正确。
3. 元素X的某价态离子 中所有电子正好充满K、L、M三个电子层,它
与 形成的晶胞结构如图所示.下列说法中错误的是
A. 的核外电子数为18
B. 该晶体中阳离子与阴离子的个数比为
C.
D. 晶体中每个 周围有2个等距离且最近的
【答案】A
【解析】
A.由中 所有电子正好充满K、L、M三个电子层,可知 为 ,其核外电子数为28,故
A错误;
B.利用均摊法可知该晶胞中 的个数为 , 的个数为 ,该晶体中阳离子
与阴离子的个数比为 ,故B正确;
C.该晶体中阳离子与阴离子的个数比为 ,晶体的化学式为 ,根据化合物中各元素正、负化
合价代数和为0可以确定 ,故C正确;
D.由图可知,晶体中与 等距离且最近的 有2个,故D正确。
4. 射线金相学 中记载关于铜与金可形成两种有序的金属互化物,其结构如图所示。下列
有关说法正确的是
A. 图Ⅰ、Ⅱ中物质的化学式相同
B. 图Ⅱ中物质的化学式为
C. 图Ⅱ中与每个铜原子紧邻的铜原子有3个
D. 设图Ⅰ中晶胞的边长为 ,则图Ⅰ中合金的密度为
【答案】B
【解析】A.根据均摊法可知,图Ⅰ中含有铜原子数为 ,金原子数为 ,图Ⅱ中含
有铜原子数为 ,金原子数为 ,图Ⅰ中物质的化学式AuCu,图Ⅱ中物质的化学式
,故A错误;
B.根据A中计算可知图Ⅱ中物质的化学式为 ,故B正确;
C.根据图Ⅱ的结构图可知,以顶点铜原子为例,与每个铜原子紧邻的铜原子分布在经过该顶点的晶
胞的棱边上,共有6个,故C错误;
D.根据A的计算可知图Ⅰ中晶胞中含有铜原子数为2,金原子数为2,所以晶体的密度为
,故D错误。
故选B。
5. 已知NaH的晶胞如图,晶胞边长为a。下列说法中错误的是
A. 钠离子的配位数是6
B. 该结构单元中氢离子数目为4
C. 氢离子之间的最短距离为
D. 基态钠离子的价电子排布式为
【答案】C
【解析】
A.钠离子周围最近的氢离子有6个,则配位数是6,故A正确;
B.理由均摊法计算,该结构单元中氢离子数目为 ,故B正确;
C.氢离子之间的最短距离为面对角线的一半,即 ,故C错误;D.基态钠离子核外电子为10个,价电子排布式为 ,故D正确。
6. 几种晶体晶胞结构如图所示,其中干冰的晶胞为立方体, 分子取向分别与晶胞体对角线
方向平行。下列说法错误的是
A. 晶胞的平移性特征包括“化学上相同”和“几何上相同”,以上晶胞都是面心晶胞
B. 以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐
标。铜晶胞中有4种原子坐标,有4个原子
C. 干冰晶胞中有4种不同取向的 分子,一个分子周围有12个紧邻的分子
D. 碘分子排列有2种不同取向,2种取向不同的碘分子以4配位数交替配位形成层状结构
【答案】A
【解析】
A.晶胞的平移性特征包括“化学上相同 原子或分子相同 ”和“几何上相同 原子的排列和取向相
同 ”,铜晶胞为面心晶胞,干冰中的二氧化碳分子取向不同,因此不是面心晶胞,而是简单立方
晶胞,故A错误;
B.以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。铜晶
胞中有4种原子坐标,均摊法确定每个晶胞中有4个原子,故B正确;
C.干冰晶胞中有4种不同取向的 分子,位于顶点分子取向相同,三对面心各不相同,一个分子
周围有12个平面,则有12个紧邻的分子,故C正确;
D.碘分子的排列有2种不同的取向,在顶点和面心不同,2种取向不同的碘分子以4配位数交替配
位形成层状结构,故D正确。