文档内容
第二节 分子晶体和共价晶体
一、分子晶体
1.概念:只含分子的晶体。
2.粒子间的作用
分子晶体中相邻的分子间以分子间作用力相互吸引。
3.常见分子晶体及物质类别
物质种类 实例
所有非金属氢化物 H O、NH 、CH 等
2 3 4
部分非金属单质 卤素(X )、O 、N 、白磷(P )、硫(S )等
2 2 2 4 8
部分非金属氧化物 CO 、P O 、SO 、SO 等
2 4 10 2 3
几乎所有的酸 HNO 、H SO 、H PO 、H SiO 等
3 2 4 3 4 2 3
绝大多数有机物 苯、乙醇、乙酸、乙酸乙酯等
【注】稀有气体为的分子为单原子分子,因此,有稀有气体单质形成的晶体也
是分子晶体。
4.物理特性
(1)分子晶体的熔、沸点较低,密度较小,硬度较小,较易熔化和挥发,部
分分子晶体易升华,(如干冰、碘、红磷等)。
(2)一般是绝缘体。分子晶体在固态和熔融状态下均不存在自由移动的离子
或自由电子,因而分子晶体在固态和熔融状态下都不能导电。有些分子晶体的
水溶液能导电,如HI、乙酸等。
1(3)溶解性符合“相似相溶规律”。
【注】分子晶体熔、沸点高低的比较规律
①分子晶体中分子间作用力越大,物质熔、沸点越高,反之越低。
②具有氢键的分子晶体,熔、沸点反常高。
5.分子晶体的常见堆积方式
分子间作用力 堆积方式 实例
分子采用密堆积,
范德华力 如C 、干冰、I 、O
每个分子周围有12 个紧邻的分 60 2 2
子
分子不采用密堆积,
范德华力、氢
如HF、NH 、冰
每个分子周围紧邻的分子少于 3
键
12个
6.常见分子晶体的结构分析
(1)冰
①水分子之间的主要作用力是氢键,当然也存在范德华力。
② 氢键 有方向性,它的存在迫使在四面体中心的每个水分子与四面体顶角
2方向的4 个相邻水分子互相吸引。
(2)干冰
①干冰中的CO 分子间只存在范德华力,不存在氢键。
2
②每个晶胞中有4 个CO 分子,12 个原子。
2
每个CO 分子周围等距离紧邻的CO 分子数为12 个。
2 2
【注】冰晶体中,每个水分子与其他 4个水分子形成氢键,每个水分子平均
形成2个氢键(每个氢键由2个水分子均摊,故4× =2)
二、共价晶体
1.定义:所有原子都以共价键相互结合形成共价键三维骨架结构的晶体叫
共价晶体。
2.构成微粒及微粒间的作用力
共价晶体
【注】①共价晶体中不存在单个分子,因此,共价晶体的化学式不代表
其实际组成,只表示其组成的原子个数比。
②共价晶体融化时被破坏的作用力是共价键。
3③共价晶体中只有共价键,但含有共价键的晶体不一定是共价晶体。
如CO 、H O等分子晶体中也含有共价键。
2 2
3.常见的共价晶体
物质种类 实例
某些非金属单质 晶体硼、晶体硅、晶体锗、金刚石等
某些非金属化合物 碳化硅(SiC)、氮化硅(Si N )、氮化硼(BN)等
3 4
某些氧化物 二氧化硅(SiO )等
2
4.共价晶体的物理性质
(1)熔点很高。共价晶体中,原子间以较强的共价键结合,融化时破坏共
价键,需要很高的能量。
(2)硬度很大。共价键三维骨架结构决定了共价晶体的硬度,如金刚石
是天然存在的最硬的物质。
(3)一般不导电,但晶体硅、锗是半导体。
(4)难溶于一般的溶剂。
【注】结构相似的共价晶体,其原子半径越小,键长越短,键能越大,键越稳
定,共价晶体的熔点越高,硬度越大。
5.典型的共价晶体
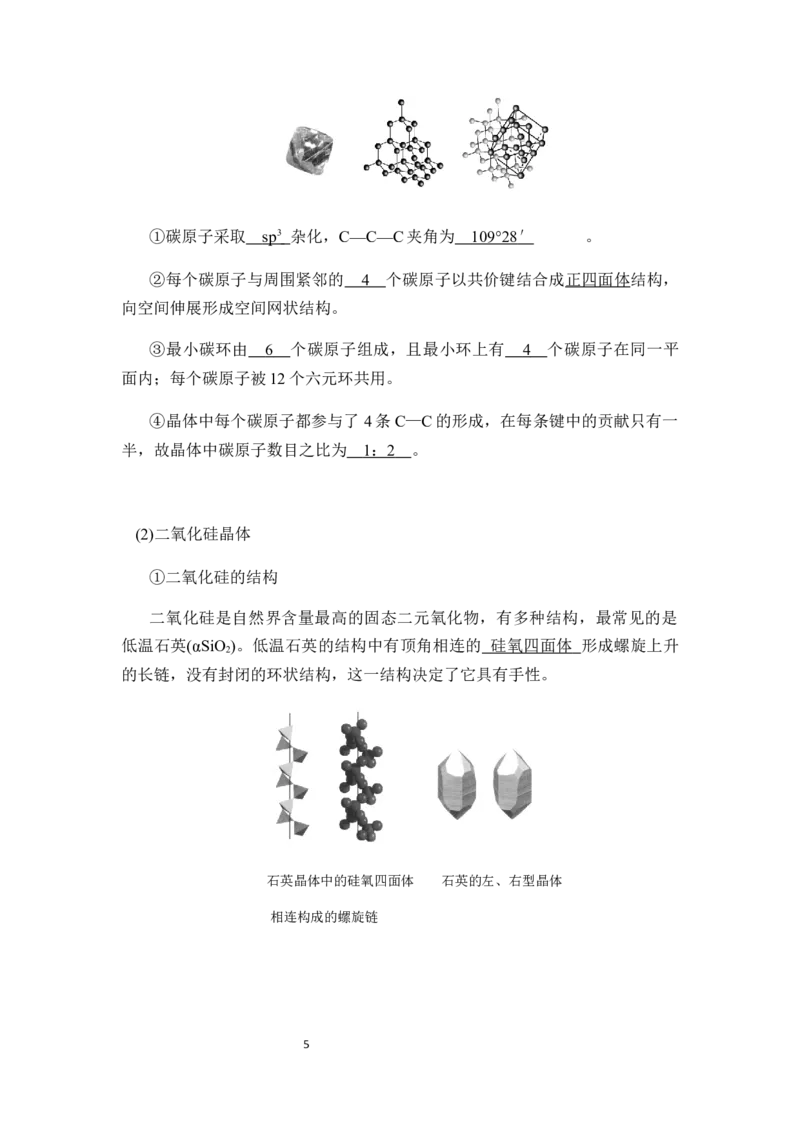
(1)金刚石
4①碳原子采取 s p 3 杂化,C—C—C夹角为 109°2 8 ′ 。
②每个碳原子与周围紧邻的 4 个碳原子以共价键结合成正四面体结构,
向空间伸展形成空间网状结构。
③最小碳环由 6 个碳原子组成,且最小环上有 4 个碳原子在同一平
面内;每个碳原子被12个六元环共用。
④晶体中每个碳原子都参与了 4条C—C的形成,在每条键中的贡献只有一
半,故晶体中碳原子数目之比为 1 : 2 。
(2)二氧化硅晶体
①二氧化硅的结构
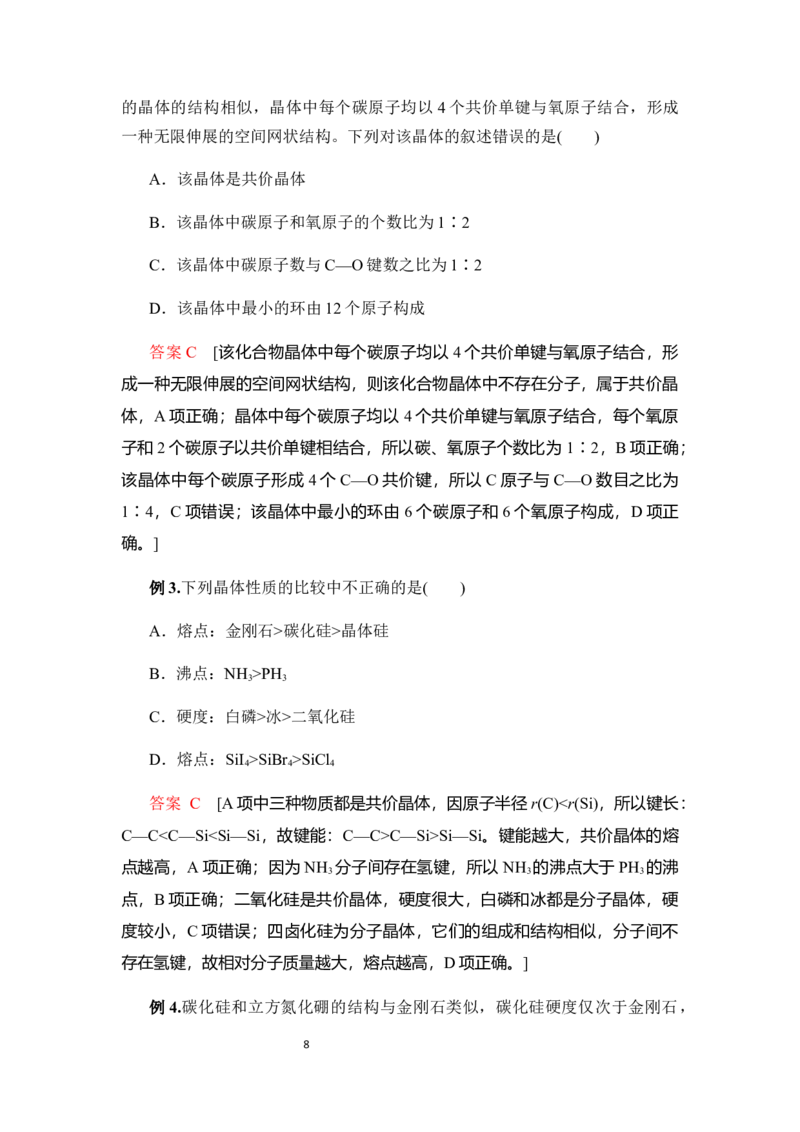
二氧化硅是自然界含量最高的固态二元氧化物,有多种结构,最常见的是
低温石英(αSiO )。低温石英的结构中有顶角相连的 硅氧四面体 形成螺旋上升
2
的长链,没有封闭的环状结构,这一结构决定了它具有手性。
石英晶体中的硅氧四面体 石英的左、右型晶体
相连构成的螺旋链
5①Si原子采取 s p 3 杂化,正四面体内O—Si—O键角为 109°2 8 ′ 。
②每个Si原子与 4 个O原子形成 4 个共价键, S i 原子位于正四面体的
中心, O 原子位于正四面体的顶点,同时每个 O原子被 2 个硅氧正四面体共
用;每个O原子和 2 个Si原子形成 2 个共价键,晶体中Si原子与O原子个数
比为 1 ∶ 2 。
③最小环上有 1 2 个原子,包括 6 个O原子和 6 个Si原子。
(2)二氧化硅的用途
二氧化硅是制造水泥、玻璃、人造红宝石、单晶硅、硅电电池、芯片和光
导纤维的原料。
【注】二氧化硅为共价晶体,晶体中不存在单个分子,其化学式为 SiO ,
2
不存在分子式。
【拓展】共价晶体与分子晶体熔、沸点高低的比较
(1)晶体类型不同:共价晶体>分子晶体
理由:共价晶体的熔、沸点与共价键有关,分子晶体的熔、沸点与分子间
作用力有关。共价键的作用力远大于分子间作用力。
(2)晶体类型相同
①共价晶体
一般来说,对结构相似的共价晶体来说,键长越短,键能越大,晶体的熔、
沸点越高。例如:金刚石>二氧化硅>碳化硅>晶体硅。
6②分子晶体
a.若分子间有氢键,则分子间作用力比结构相似的同类晶体大,故熔、沸
点较高。如HF>HI;NH >PH ;H O>H Te。
3 3 2 2
b.组成和结构相似的分子晶体,一般相对分子质量越大,范德华力越大,
熔、沸点越高。如I >Br >Cl >F ;SnH >GeH >SiH >CH 。
2 2 2 2 4 4 4 4
c.组成和结构不相似的物质(相对分子质量接近),分子的极性越大,范德
华力越大,熔、沸点越高。如CO>N 。
2
d.同类别的同分异构体,支链越多,熔、沸点越低。如正戊烷>异戊烷>
新戊烷。
例1. 我们可以将SiO 的晶体结构想象为:在晶体硅的Si—Si键之间插入O
2
原子。根据SiO 晶体结构图,下列说法不正确的是( )
2
A.石英晶体中每个Si原子通过Si—O极性键与4个O原子作用
B.每个O原子也通过Si—O极性键与2个Si原子作用
C.石英晶体中 Si原子与O原子的原子个数比为 1∶2,可用“SiO ”来表
2
示石英的组成
D.在晶体中存在石英分子,故能叫分子式
答案 D [晶体硅的结构是五个硅原子形成正四面体结构,其中有一个位于
正四面体的中心,另外四个位于四面体的顶点,故 SiO 的结构为每个硅原子周
2
围有四个氧原子,而每个氧原子周围有两个硅原子,在晶体中 Si原子与O原子
的原子个数比为1∶2,“SiO ”仅表示石英的组成,故没有单个的SiO 分子。]
2 2
例2.最近科学家成功研制成了一种新型的碳氧化物,该化合物晶体与 SiO
2
7的晶体的结构相似,晶体中每个碳原子均以4个共价单键与氧原子结合,形成
一种无限伸展的空间网状结构。下列对该晶体的叙述错误的是( )
A.该晶体是共价晶体
B.该晶体中碳原子和氧原子的个数比为1∶2
C.该晶体中碳原子数与C—O键数之比为1∶2
D.该晶体中最小的环由12个原子构成
答案C [该化合物晶体中每个碳原子均以 4个共价单键与氧原子结合,形
成一种无限伸展的空间网状结构,则该化合物晶体中不存在分子,属于共价晶
体,A项正确;晶体中每个碳原子均以 4个共价单键与氧原子结合,每个氧原
子和2个碳原子以共价单键相结合,所以碳、氧原子个数比为 1∶2,B项正确;
该晶体中每个碳原子形成 4个C—O共价键,所以 C原子与C—O数目之比为
1∶4,C项错误;该晶体中最小的环由 6个碳原子和6个氧原子构成,D项正
确。]
例3.下列晶体性质的比较中不正确的是( )
A.熔点:金刚石>碳化硅>晶体硅
B.沸点:NH >PH
3 3
C.硬度:白磷>冰>二氧化硅
D.熔点:SiI >SiBr >SiCl
4 4 4
答案 C [A项中三种物质都是共价晶体,因原子半径r(C)C—Si>Si—Si。键能越大,共价晶体的熔
点越高,A项正确;因为NH 分子间存在氢键,所以 NH 的沸点大于PH 的沸
3 3 3
点,B项正确;二氧化硅是共价晶体,硬度很大,白磷和冰都是分子晶体,硬
度较小,C项错误;四卤化硅为分子晶体,它们的组成和结构相似,分子间不
存在氢键,故相对分子质量越大,熔点越高,D项正确。]
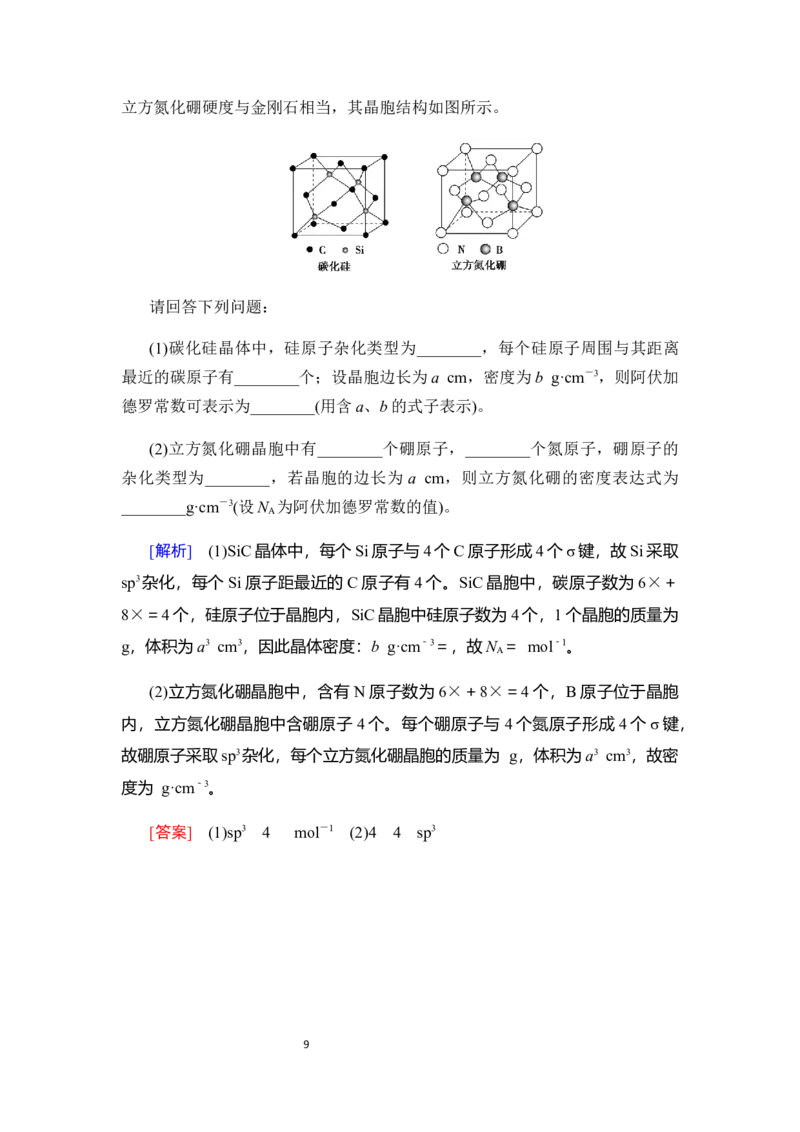
例4.碳化硅和立方氮化硼的结构与金刚石类似,碳化硅硬度仅次于金刚石,
8立方氮化硼硬度与金刚石相当,其晶胞结构如图所示。
请回答下列问题:
(1)碳化硅晶体中,硅原子杂化类型为________,每个硅原子周围与其距离
最近的碳原子有________个;设晶胞边长为a cm,密度为b g·cm-3,则阿伏加
德罗常数可表示为________(用含a、b的式子表示)。
(2)立方氮化硼晶胞中有________个硼原子,________个氮原子,硼原子的
杂化类型为________,若晶胞的边长为 a cm,则立方氮化硼的密度表达式为
________g·cm-3(设N 为阿伏加德罗常数的值)。
A
[解析] (1)SiC晶体中,每个Si原子与4个C原子形成4个σ键,故Si采取
sp3杂化,每个Si原子距最近的C原子有4个。SiC晶胞中,碳原子数为6×+
8×=4个,硅原子位于晶胞内,SiC晶胞中硅原子数为4个,1个晶胞的质量为
g,体积为a3 cm3,因此晶体密度:b g·cm-3=,故N = mol-1。
A
(2)立方氮化硼晶胞中,含有 N原子数为6×+8×=4个,B原子位于晶胞
内,立方氮化硼晶胞中含硼原子 4个。每个硼原子与 4个氮原子形成 4个σ键,
故硼原子采取sp3杂化,每个立方氮化硼晶胞的质量为 g,体积为a3 cm3,故密
度为 g·cm-3。
[答案] (1)sp3 4 mol-1 (2)4 4 sp3
9