文档内容
8.1 自然资源的开发利用(精讲)
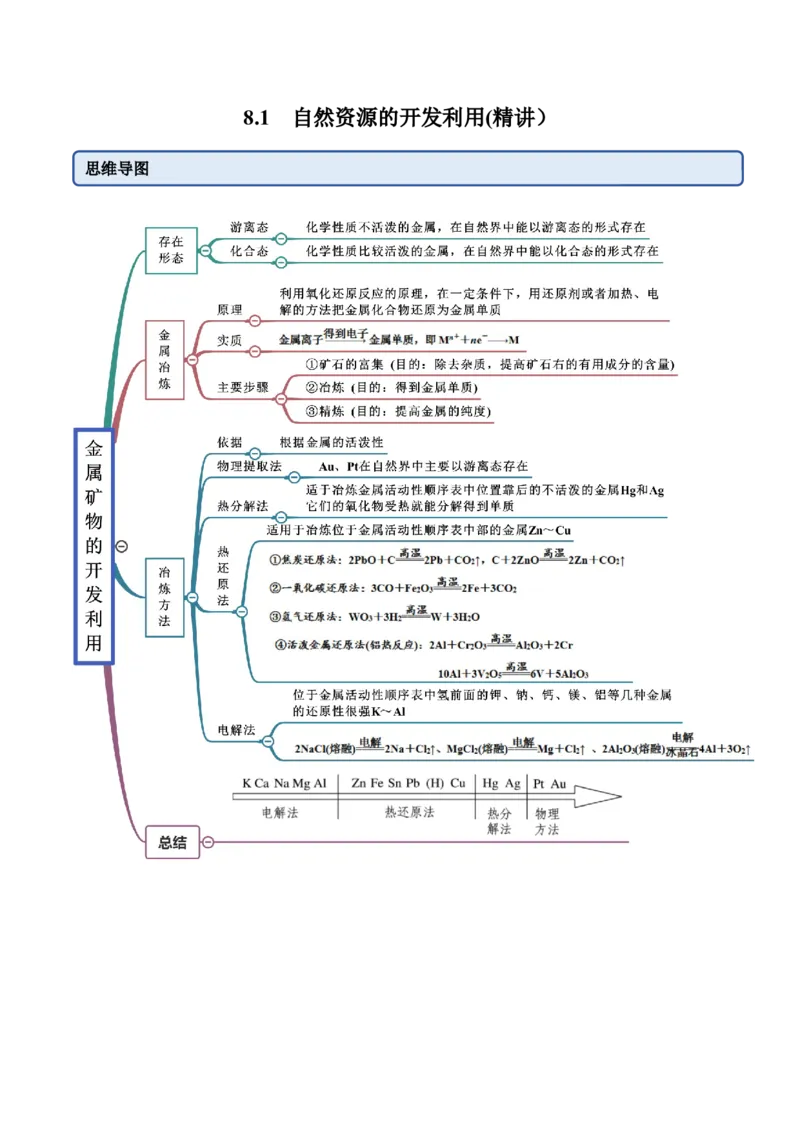
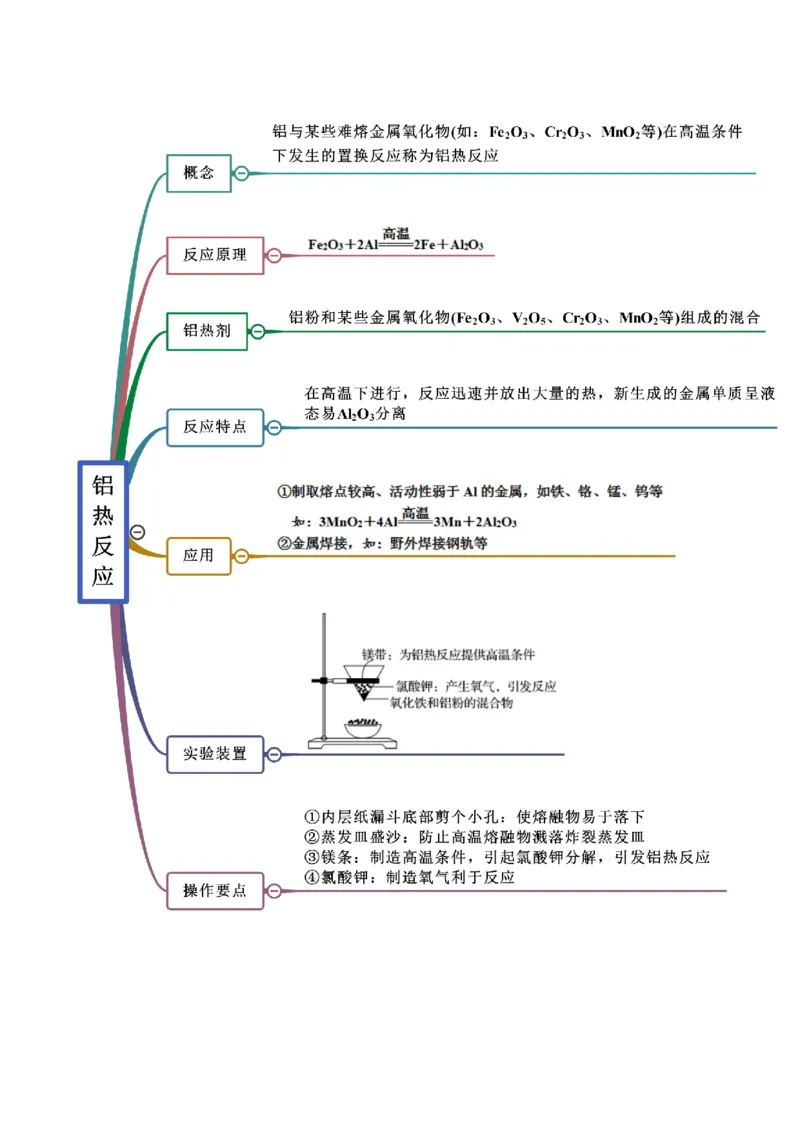
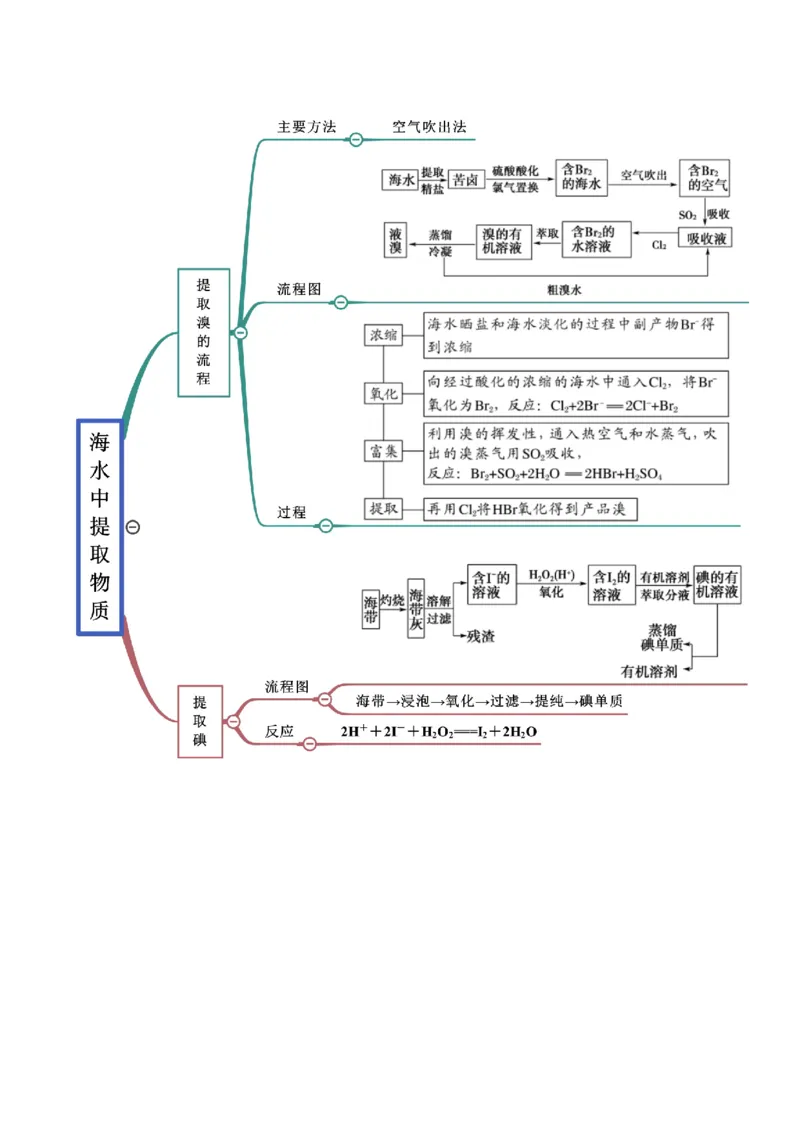
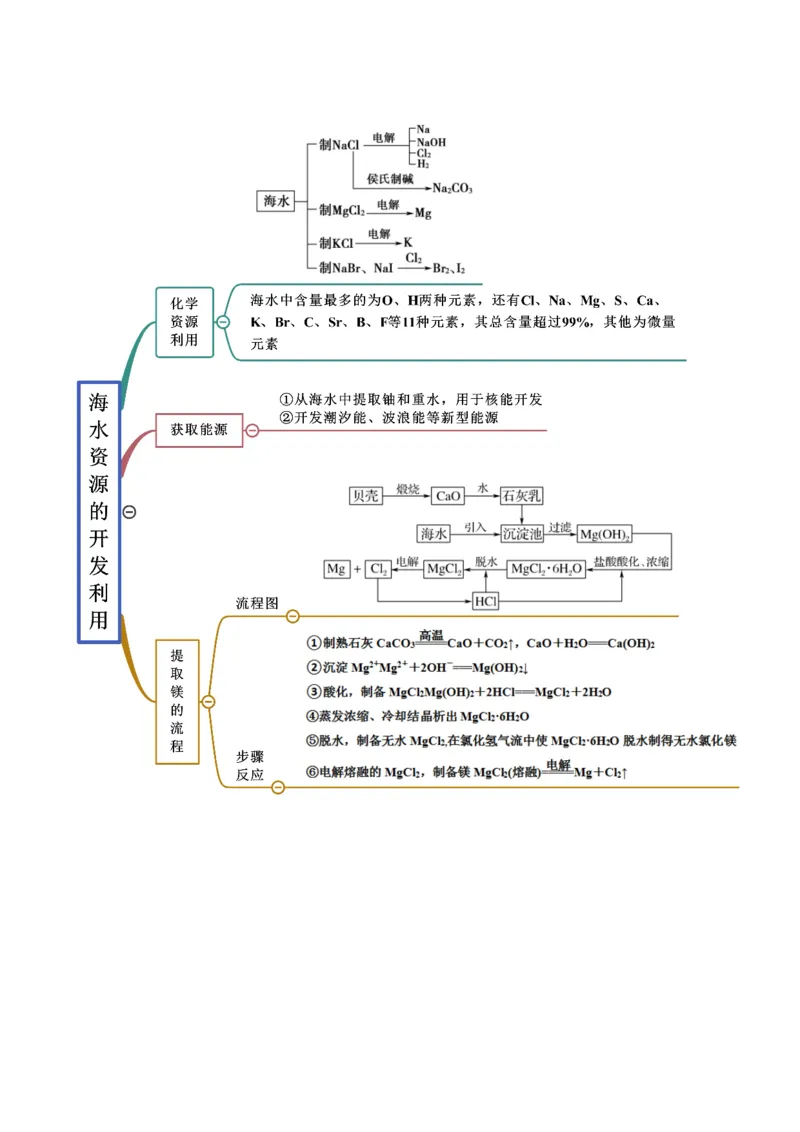
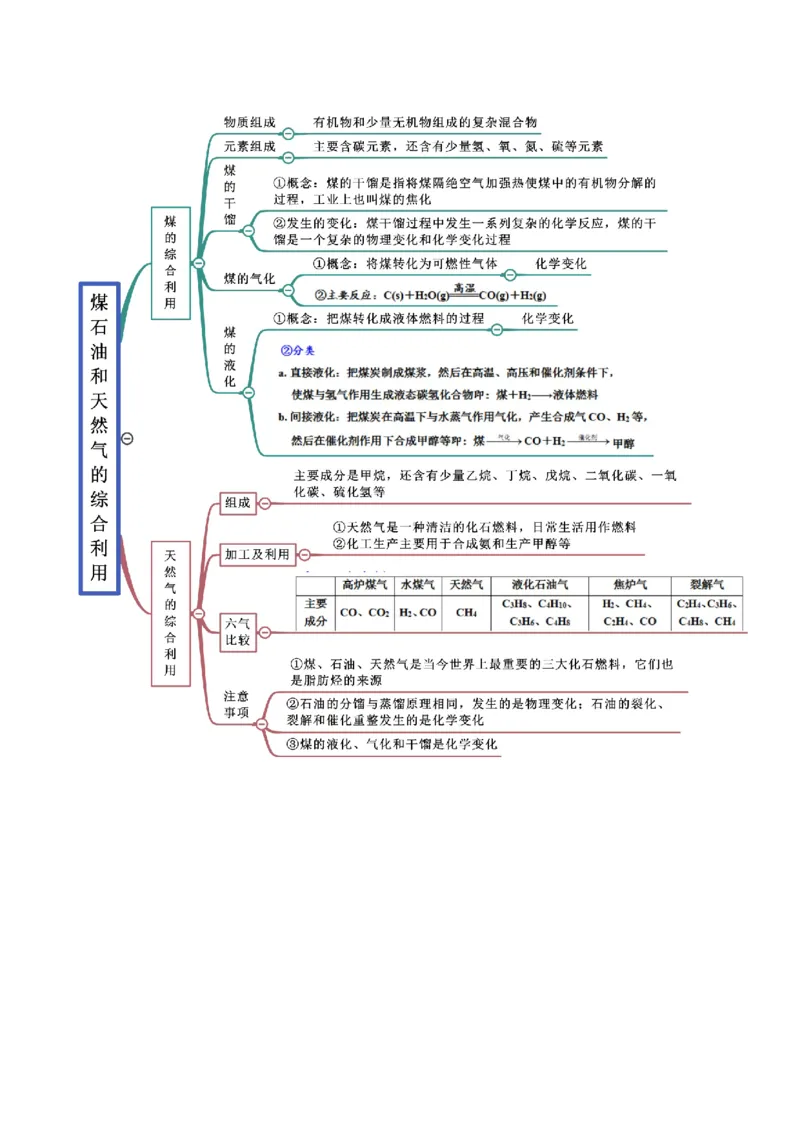
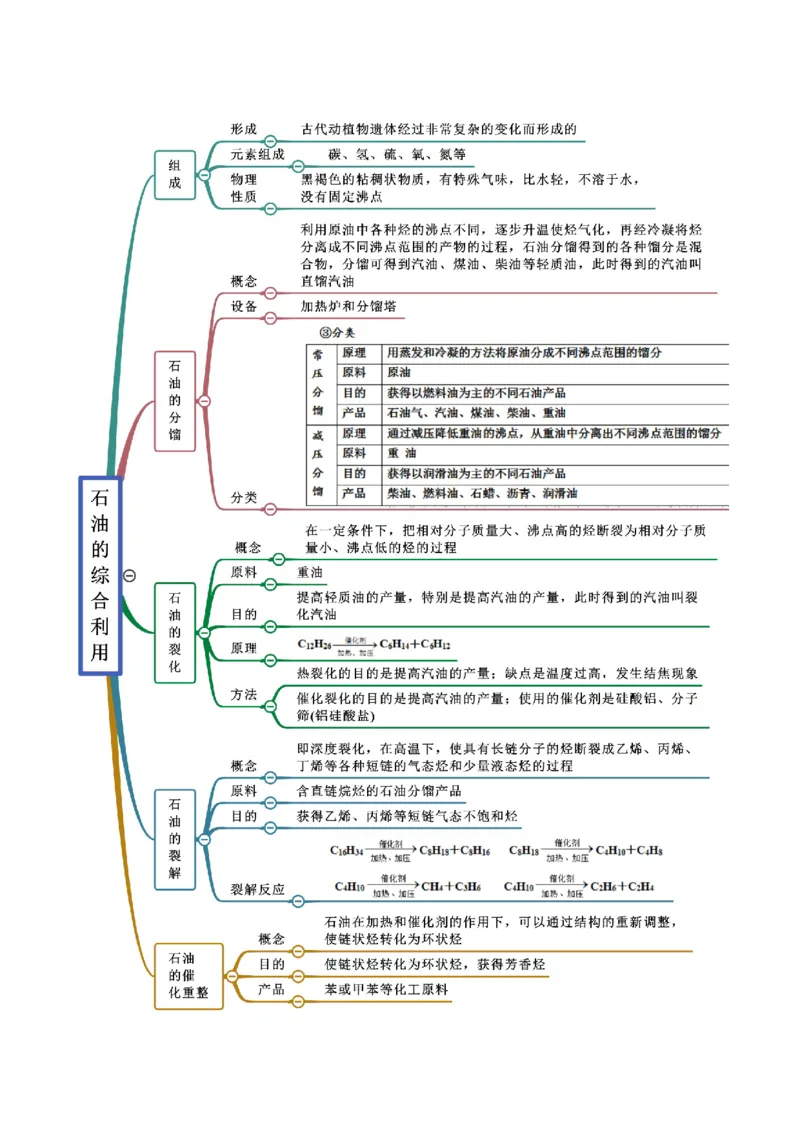
思维导图常见考点
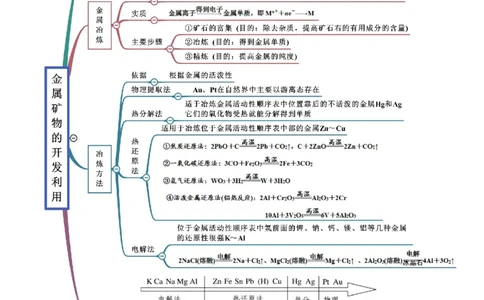
考点一 金属矿物的开发利用
【例1-1】(2021·云南·玉溪市江川区第二中学高一期末)表中金属的冶炼原理与方法不完全正确的是
选项 冶炼原理 方法
A 2HgO 2Hg+O↑ 热分解法
2
B 2Al O(熔融) 4Al+3O ↑ 电解法
2 3 2
C 2CuO 2Cu+O ↑ 热分解法
2
D 3CO+Fe O 2Fe+3CO 热还原法
2 3 2
【答案】C
A.Hg是不活泼的金属,冶炼时采用热分解方法,故金属的冶炼原理与方法均合理,A正确;
B.Al是活泼金属,采用电解熔融Al O 的方法冶炼,为降低其熔化温度,要加入助溶剂冰晶石,冶炼方
2 3
法及反应原理均合理,B正确;
C.Cu是比较活泼的金属,采用热还原方法冶炼,金属的冶炼反应原理和方法均不合理,C错误;
D.Fe是比较活泼的金属,采用热还原方法冶炼,金属的冶炼反应原理和方法均合理,D正确;
故合理选项是C。
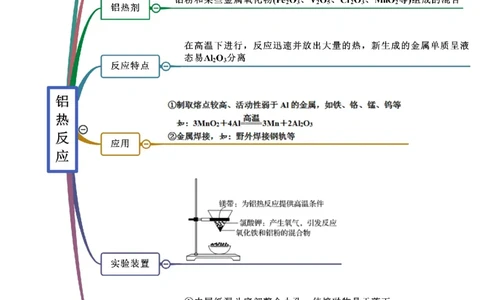
【例1-2】(2021·安徽·蒙城第一中学高一期末)铝热反应常用于焊接钢轨,其焊接速度快,设备简易,适
用于野外作业。实验室采用如图装置进行铝热反应,下列说法错误的是A.该反应的实质是金属的置换反应
B.该反应是放热反应,Fe O 和铝粉的混合物被称为铝热剂
2 3
C.铝单质很活泼,通常表面附着层致密的氧化铝薄膜
D.铝热反应只能用于冶炼铁、锰、铬、镁等熔点较高的金属
【答案】D
【解析】A.该反应为2Al+Fe O Al O+2Fe,反应特点是单质与化合物反应产生新的单质和新的化合
2 3 2 3
物,故实质上是金属的置换反应,A正确;
B.作为铝热剂重要组成的金属氧化物,铝热剂应为Al和过渡元素的氧化物所形成的混合物,B正确;
C.铝单质很活泼,容易被空气中的氧气氧化为氧化铝,氧化铝非常致密,对内层金属起保护作用,因此
在金属铝表面通常附着一层致密的氧化铝薄膜,C正确;
D.铝热反应是金属铝和金属氧化物之间的置换反应,反应放出大量的热,使产生的金属以液态形式存在。
利用铝热反应可以冶炼还原性比Al弱,但是熔点较高的金属,如金属铁、锰、铬等金属,但镁还原性比铝
强,不能用铝热反应制取,D错误;
故合理选项是D。
【例1-3】(2021·四川·东辰国际学校高一阶段练习)工业上用铝土矿(主要成分为Al O,还有少量的
2 3
Fe O 等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
2 3
(1)I和II步骤中分离溶液和沉淀的操作,所用到的玻璃仪器是:_________;
(2)沉淀M中除含有泥沙外,一定还含有_______,固体N是________;
(3)滤液X中,含铝元素的溶质的化学式为_______,它属于_____(填“酸”、“碱”或“盐”)类物质;(4)实验室里常往AlCl 溶液中加入___________(填“氨水”或“NaOH溶液”)来制取Al(OH) ;
3 3
(5)将铝粉和氧化铁的混合物点燃,反应放出大量的热量,生成的液态的铁用来焊接铁轨。
请写出反应的化学方程式:______________________。
【答案】(1)漏斗 玻璃棒 烧杯
(2)Fe O Al O
2 3 2 3
(3)NaAlO 盐
2
(4)氨水
(5)2Al+ Fe O Al O+2Fe
2 3 2 3
【解析】铝土矿中加入浓NaOH溶液,Fe O 和氢氧化钠不反应,氧化铝与NaOH反应生成NaAlO ,步骤I
2 3 2
利用过滤除去Fe O,沉淀M为氧化铁等不溶物,滤液X含有偏铝酸钠;步骤II通入二氧化碳将AlO 转
2 3
化为氢氧化铝沉淀,过滤得氢氧化铝,加热分解氢氧化铝得到氧化铝。
(1)I和II步骤分离固体与溶液的方法为过滤,所用的玻璃仪器为:烧杯、漏斗、玻璃棒;
(2)根据分析可知,沉淀M中还含有不溶于NaOH溶液的Fe O;氢氧化铝受热分解生成的固体N为
2 3
Al O;
2 3
(3)根据分析可知,滤液X中,含铝元素的溶质的化学式为NaAlO ;NaAlO 由酸根阴离子和金属阳离子
2 2
构成,属于盐;
(4)氢氧化铝溶于强碱,实验室通常用弱碱氨水与铝盐反应制备氢氧化铝沉淀;
(5)铝和氧化铁反应生成铁和氧化铝的方程式为:2Al+ Fe O Al O+2Fe。
2 3 2 3
【一隅三反】
1.(2021·全国·高一课时练习)氧化还原反应广泛应用于金属的冶炼,下列有关金属冶炼的说法错误的是
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.热分解法、热还原法、电解法冶炼金属中,金属元素都由化合态转变为游离态
C.铝热反应中铝作为还原剂将铁从其氧化物中置换出来
D.用磁铁矿炼铁的反应中,1molFe O 被CO还原成Fe,转移9mol电子
3 4
【答案】D
【解析】A.电解熔融氯化钠生成钠和氯气,故A正确;
B.冶炼金属是金属元素都由化合态转变为游离态,故B正确;C.铝还原金属氧化物生成金属单质和氧化铝为铝热反应,故C正确;
D.用磁铁矿炼铁的反应为 ,当有1 被 还原成 时,转移8
电子,D项错误。
故选D。
2.(2021·甘肃·舟曲县第一中学高一期末)下列关于钙、钠、铁的冶炼方法正确的是
A.电解法、热分解法、热还原法 B.电解法、电解法、热分解法
C.热还原法、热分解法、热还原法 D.电解法、电解法、热还原法
【答案】D
【解析】金属Ca和Na是活泼金属,用电解法冶炼,CaCl Ca+Cl ↑,2NaCl 2Na +Cl ↑,Fe的金属
2 2 2
活动性排在中间位置,可用热还原法冶炼,3CO+Fe O 2Fe+3CO ,因此冶炼方法分别为电解法、电解
2 3 2
法、热还原法,故选D。
3.(2021·全国·高一课时练习)下列关于铝热剂的叙述中正确的是
A.利用铝热剂的反应,常用于冶炼高熔点的金属
B.铝热剂就是指铝和氧化铁混合后的物质
C.铝热剂发生的铝热反应需要镁带和氯酸钾引燃,所以铝热反应时一个吸热反应
D.工业上常用铝热反应来大量冶炼金属铁
【答案】A
【解析】A.铝的还原性强,且铝热反应放出大量的热,则可以通过铝热反应冶炼某些高熔点金属,A正
确;
B.铝热剂是铝粉和难熔金属氧化物的混合物,并不只是指铝和氧化铁混合后的物质,B错误;
C.铝热反应中放出大量的热,所以铝热反应为放热反应,C错误;
D.铝热反应可以用来冶炼出高熔点金属,如金属铁,但工业上是通过CO还原法冶炼大量的铁,D错误;
故选A。
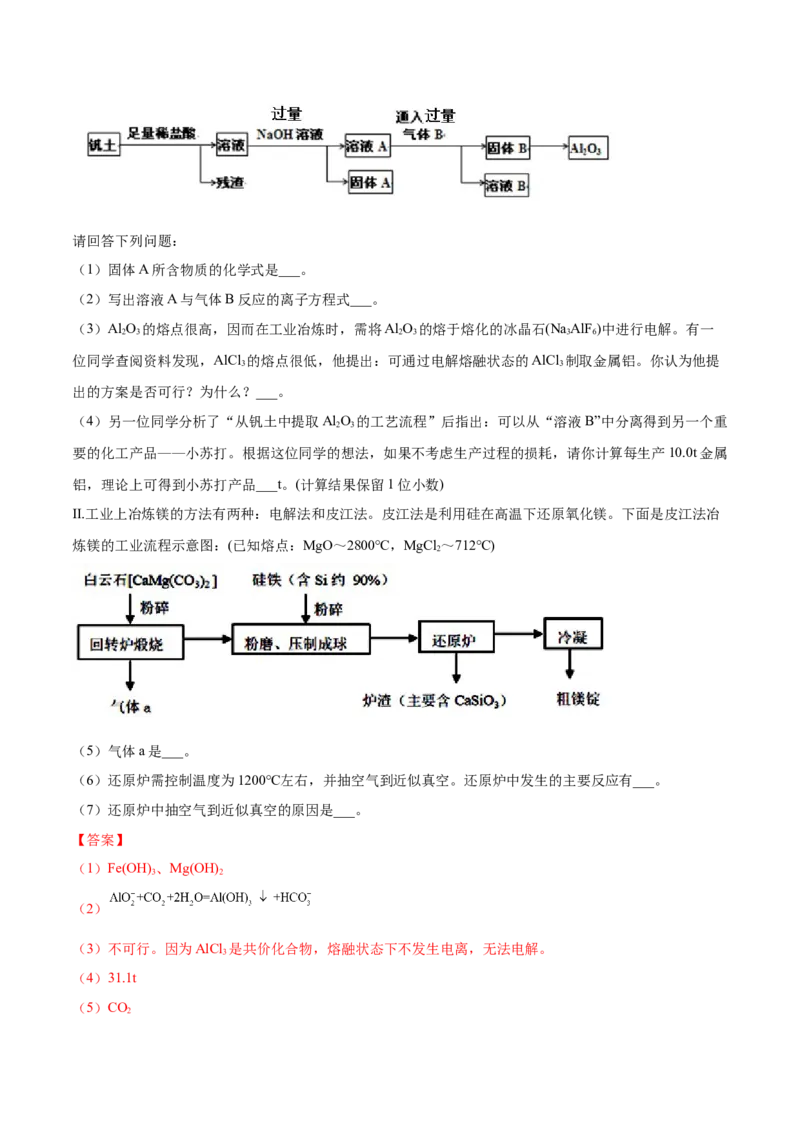
4.(2021·福建·泉州五中高一期中)Ⅰ.工业上冶炼金属铝的原料来源于自然界中重要的矿物质钒土(主要
成分:Al O;还有SiO、Fe O、FeCO、MgCO 等杂质)。从钒土中提取得到Al O 的工艺流程如图所示:
2 3 2 2 3 3 3 2 3请回答下列问题:
(1)固体A所含物质的化学式是___。
(2)写出溶液A与气体B反应的离子方程式___。
(3)Al O 的熔点很高,因而在工业冶炼时,需将Al O 的熔于熔化的冰晶石(Na AlF)中进行电解。有一
2 3 2 3 3 6
位同学查阅资料发现,AlCl 的熔点很低,他提出:可通过电解熔融状态的AlCl 制取金属铝。你认为他提
3 3
出的方案是否可行?为什么?___。
(4)另一位同学分析了“从钒土中提取Al O 的工艺流程”后指出:可以从“溶液B”中分离得到另一个重
2 3
要的化工产品——小苏打。根据这位同学的想法,如果不考虑生产过程的损耗,请你计算每生产10.0t金属
铝,理论上可得到小苏打产品___t。(计算结果保留1位小数)
Ⅱ.工业上冶炼镁的方法有两种:电解法和皮江法。皮江法是利用硅在高温下还原氧化镁。下面是皮江法冶
炼镁的工业流程示意图:(已知熔点:MgO~2800℃,MgCl ~712℃)
2
(5)气体a是___。
(6)还原炉需控制温度为1200℃左右,并抽空气到近似真空。还原炉中发生的主要反应有___。
(7)还原炉中抽空气到近似真空的原因是___。
【答案】
(1)Fe(OH) 、Mg(OH)
3 2
(2)
(3)不可行。因为AlCl 是共价化合物,熔融状态下不发生电离,无法电解。
3
(4)31.1t
(5)CO
2(6) 、
(7)防止高温下的镁单质再被空气中的氧气氮气等气体氧化
【解析】(1)矾土经过量盐酸浸泡后,除SiO 不反应,其余金属元素均生成氯化物溶于水中,那么向溶
2
液中加入过量NaOH溶于后,Al元素生成NaAlO 溶于水中,Fe元素最终形成Fe(OH) ,Mg元素最终形成
2 3
Mg(OH) ,过滤后即为固体A的主要成分,所以本问应填“Fe(OH) 、Mg(OH) ”;
2 3 2
(2)溶液A中Al元素以 的形式存在,要获得Al(OH) ,须向溶液中通入足量CO,故本问离子方程
3 2
式应填“ ”;
(3)电解熔融态离子化合物是获取某些活泼金属的工业手段,但AlCl 是共价化合物,熔融态以分子形式
3
存在,不能电离成离子,故无法电解,所以本问应填“不可行。因为AlCl 是共价化合物,熔融状态下不
3
发生电离,无法电解”;
(4)按照关系式法,根据反应方程式的系数比例关系,设理论上可得x t小苏打
,解之,得x=31.1,所以本问应填“31.1t”;
(5)白云石是钙镁碳酸盐,高温煅烧会形成氧化钙氧化镁及二氧化碳,故本问应填“CO”;
2
(6)根据题目所给信息,1200℃高温下MgO与Si发生置换反应,生成SiO 和蒸汽状态的Mg,生成的
2
SiO 又在高温下与CaO生成硅酸钙(题目提示:炉渣主含CaSiO ),所以本问应填“ 、
2 3
”;
(7)金属镁是一种活泼的金属单质,一定条件下能与空气中的氧气、氮气、二氧化碳均发生化学反应,
故在制备金属镁时要避免金属镁与空气接触,所以本问应填“防止高温下的镁单质再被空气中的氧气氮气
等气体氧化”;
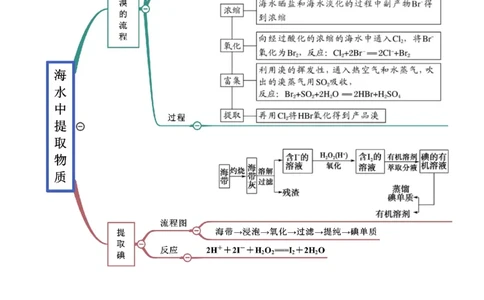
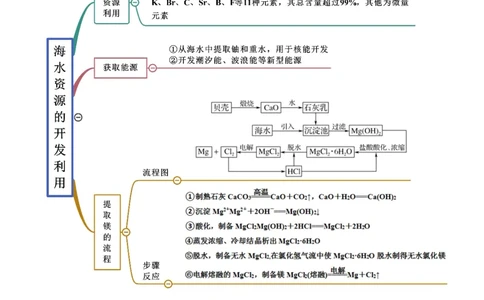
考点二 海水资源的开发利用
【例2】(2021·江苏省响水中学高一期中)碘( Godine)是人体必需的微量元素,是维持人体甲状腺正常功能
所必需的元素, 人体缺碘时就会患甲状腺肿大,人们主要从饮水、粮食、蔬菜和周围环境中获取碘。多食海
带,海鱼等含碘丰富的食品,对于防治甲状腺肿大很有效。某化学课外活动小组在实验室以海带为原料获得少量碘水,并以四氯化碳(沸点76.8℃)为溶剂将碘从碘水中提取出来,甲同学设计实验流程如图所示。请
回答下列问题:
(1)上述流程中灼烧时必须用到最主要的实验仪器有酒精灯、泥三角和___________(填名称)。
(2)操作①的名称为___________;
(3)操作②中发生反应的离子方程式为______________________,乙同学对操作②进行了改进,用绿色
氧化剂HO 代替氯气并加适量稀盐酸,则所发生的离子反应方程式是
2 2
____________________________________。
(4)操作③的实验名称为___________,最主要的实验仪器的名称为___________;
(5)丙同学补充增加了一步操作:从碘的CCl 溶液中经过___________提取了碘单质并回收CCl (填该操
4 4
作名称)
(6)目前,我国推行全民食用的加碘盐是在食盐中加入___________这一物质(填写化学式)。
【答案】(1)坩埚(2)过滤(3) Cl +2 I-=2Cl- +I H O +2 I-+2H+=I +2H O
2 2 2 2 2 2
(4)萃取分液 分液漏斗 (5)蒸馏(6)KIO
3
【解析】海带在坩埚中灼烧成粉末,加水溶解后过滤得到含碘化钾的水溶液,通入氯气,反应生成碘单质,
再加入四氯化碳进行萃取分离。据此解答。
(1)灼烧时使用到的主要仪器有:坩埚、泥三角和酒精灯;
(2)操作①分离固体和液体的操作,即为过滤操作。
(3)作②中发生氯气和碘离子的置换反应,反应的离子方程式为Cl +2 I-=2Cl- +I ,乙同学对操作②进行
2 2
了改进,用绿色氧化剂HO 代替氯气并加适量稀盐酸,则所发生的离子反应方程式是HO +2 I-
2 2 2 2
+2H+=I +2H O;
2 2
(4)根据分析,操作③的实验名称为萃取分液,最主要的实验仪器的名称为分液漏斗。
(5)碘单质易升华,从碘的四氯化碳溶液中分离碘单质,用蒸馏的方法分离。
(6)碘盐中的成分为碘酸钾,化学式为:KIO 。
3【一隅三反】
1.(2021·江苏省苏州实验中学高一阶段练习)海洋是一个资源宝库,海水资源的开发和利用是现代和未
来永恒的主题。下面是海水利用的流程图:
下列有关说法不正确的是
A.反应②加热MgCl •6H O应在HCl气流保护下制备无水MgCl
2 2 2
B.氯碱工业在阳极产生了使湿润淀粉碘化钾试纸变蓝的气体
C.过程中制得NaHCO 是先往精盐溶液中通入CO,再通入NH
3 2 3
D.反应⑤中,用NaCO 水溶液吸收Br 后,用70~80%硫酸富集Br
2 3 2 2
【答案】C
【解析】A.MgCl 是强酸弱碱盐,若将其晶体加热,MgCl 会溶解在结晶水中并发生反应产生Mg(OH) 、
2 2 2
HCl,HCl会随水挥发逸出,不能得到无水MgCl ,若将MgCl •6H O在HCl气流中进行加热,反应产生的
2 2 2
Mg(OH) 会与HCl发生反应产生MgCl ,HO挥发逸出,就可得到无水MgCl ,A正确;
2 2 2 2
B.氯碱工业电解饱和NaCl溶液,在阳极上Cl-失去电子变为Cl 逸出,Cl 具有强氧化性,会将湿润的试纸
2 2
上的KI氧化为I,I 遇淀粉溶液变为蓝色,可见阳极产生了使湿润淀粉碘化钾试纸变蓝的气体,B正确;
2 2
C.在反应过程中为增大CO 在溶液中的溶解度,应该先往精盐溶液中通入NH ,使溶液显碱性,然后再
2 3
通入CO,就可以制得NaHCO ,C错误;
2 3
D.碳酸钠溶液显碱性,在反应⑤中,用NaCO 水溶液吸收Br 后,反应达到NaBr、NaBrO,再用70~
2 3 2
80%的浓硫酸反应就可以重新生成Br ,达到富集Br 的目的,D正确;
2 2
故合理选项是C。
2.(2021·全国·高一专题练习)从海水中提取镁的工艺流程可表示如图:下列说法不正确的是
A.用此法提取镁的优点之一是原料来源丰富
B.直接电解MgCl 溶液也可以得到镁单质
2
C.步骤④用到的实验仪器有蒸发皿、酒精灯、玻璃棒、三脚架等
D.上述工艺流程中涉及化合、分解和复分解反应
【答案】B
【解析】A.海水中镁元素含量高,从海水中提取镁的优点之一是原料来源丰富,A正确;
B.电解熔融MgCl 可得到金属镁和氯气,直接电解MgCl 溶液得到氢氧化镁和氯气,B错误;
2 2
C.步骤④加盐酸后要浓缩结晶,需要用到的实验仪器有蒸发皿、酒精灯、玻璃棒、三脚架等,C正确;
D.题述工艺流程中涉及碳酸钙分解生成氧化钙和二氧化碳的反应,该反应为分解反应,涉及氧化钙与水
生成氢氧化钙的反应,该反应为化合反应,氢氧化镁与盐酸的反应为复分解反应,D正确;
答案选B。
3.(2021·上海市南洋模范中学高一期中)海水是巨大的资源宝库,人类可以从海水中提取各种化工产品。
下图是某工厂对海水综合利用的示意图:
(1)写出电解饱和食盐水的化学方程式______,检验氯气生成的方法是_______。
(2)液氯储存在钢瓶中,钢瓶上应贴的标签为___________(选填字母编号)。
A.自燃品 B.爆炸品 C.有毒品 D.易燃品
(3) 加入盐酸充分反应后,操作③是从 溶液中获得 晶体,此处需要进行的
实验操作依次为:___________、冷却结晶、___________、洗涤、干燥。
(4)操作⑤是向溶液中鼓入热空气,即可将溴单质从溶液中分离出来,此方法的成功应用是基于溴单质
有___________性。(5)粗溴的精制过程是先将粗溴用 水溶液吸收,将其转变成 ,再通 ,最后蒸馏得到高纯溴。
用 水溶液吸收 的吸收率可达95%,有关反应的离子方程式为 ___________
(将上述离子反应方程式补充完整),由此反应可知,除环境保护外,在工业生产中应解决的
主要问题是___________。
【答案】
(1) 用湿润的淀粉KI试纸,如果试纸变蓝,说明有氯气生成
(2)C
(3)加热浓缩 过滤
(4)挥发
(5)H+ 强酸对设备的严重腐蚀问题
【解析】海水晒盐后过滤分离出滤液和粗盐,①为过滤,粗盐经精制得到较为纯净的氯化钠,电解饱和食
盐水可用于制备氢氧化钠、氯气和氢气,滤液加入石灰乳沉淀镁离子后操作②为过滤,在滤液中通入Cl
2
是将滤液中的Br-氧化为Br ,再利用热的空气将Br 吹出,操作⑤中利用SO 吸收发生SO +Br +2H O=4H+
2 2 2 2 2 2
+2Br-+SO2-;再通入Cl 将Br-氧化为Br ,两次Br-→Br 转化的目的是对溴元素进行富集;氢氧化镁加入盐
4 2 2 2
酸溶解得到氯化镁溶液,氯化镁溶液中得到氯化镁晶体,操作③是加热蒸发、冷却结晶得到无水氯化镁,
操作④为电解熔融氯化镁得到金属镁,以此解答该题。
(1)电解饱和食盐水的化学方程式为 ,检验氯气生成的方法是用湿
润的淀粉KI试纸,如果试纸变蓝,说明有氯气生成,故答案为: ;用
湿润的淀粉KI试纸,如果试纸变蓝,说明有氯气生成;
(2)液氯有毒,储存在钢瓶中,钢瓶上应贴的标签为c,故答案为:c;
(3)Mg(OH) 加入盐酸充分反应后,操作③是从MgCl 溶液中获得MgCl •6H O晶体,此处需要进行的实
2 2 2 2
验操作依次为加热浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:加热浓缩、过滤;
(4)操作⑤是向溶液中鼓入热空气或水蒸气,即可将溴单质从溶液中分离出来,此方法的成功应用是基
于溴单质有挥发性,故答案为:挥发;
(5)粗溴的精制过程是先将粗溴用SO 水溶液吸收,将其转变成Br-,再通Cl,最后蒸馏得到高纯溴,用
2 2
SO 水溶液吸收Br 的吸收率可达95%,有关反应的离子方程式为SO +Br +2H O=4H++2Br-+SO2-,由此反
2 2 2 2 2 4应可知,除环境保护外,在工业生产中应解决的主要问题是强酸对设备的严重腐蚀问题,故答案为:H+;
强酸对设备的严重腐蚀问题。
考点三 煤、石油和天然气的综合利用
【例3-1】(2021·吉林长春·高一期末)下列说法不正确的是
A.煤的干馏是化学变化
B.煤液化后可以得到甲醇等液体燃料
C.煤经气化和液化两个物理变化过程,可变为清洁能源
D.根据煤的干馏产品,可推知煤中含有C、H、O、N等元素
【答案】C
【解析】A.煤的干馏是将煤隔绝空气加强热使其分解的过程,有新物质生成,属于化学变化,故A正确;
B.煤的液化是用煤制取甲醇、液态烃等液体燃料的过程,属于化学变化,故B正确;
C.煤的气化是指将煤在高温下与水接触转变为水煤气(一氧化碳和氢气)的过程,煤的液化是指把煤转化成
甲醇等液体燃料的过程,二者均属于化学变化,故C错误;
D.煤的干馏是将煤隔绝空气加强热使其分解的过程,煤的干馏产品有焦炉气(H 、CH、C H、CO)、煤焦
2 4 2 4
油(苯、甲苯、酚等)、粗氨水、粗苯和焦炭,则可推知煤中含有C、H、O、N等元素,故D正确;
答案为C。
【例3-2】(2021·全国·高一专题练习)煤是一种常用燃料。由于煤燃烧产生的废气中含有SO 、CO、NO
2 2
和NO等多种有害气体和烟尘,会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再
排放。
(1)煤的气化和液化能提高煤的利用率,又能减少有害气体的排放。写出煤气化的主要反应的化学方程式:
___________;煤液化是___________(填“物理”或“化学”)变化。
(2)煤的干馏是煤综合利用的重要途径。煤干馏时得到的固体产品是___________,其用途是___________。
(3)将煤直接进行燃烧,造成环境污染的主要方面之一是形成硝酸型酸雨。写出有关物质转化为硝酸的化学
方程式:___________。
(4)向煤中添加生石灰是燃煤脱硫的一种方法,而且能变废为宝,用化学方程式表示反应原理:
___________。
【答案】(1)C+HO(g) CO+H 化学
2 2
(2)焦炭 可作燃料及工业原料
(3)2NO+O=2NO,3NO +HO=2HNO +NO
2 2 2 2 3
(4) CaO+SO =CaSO ,2CaSO+O=2CaSO
2 3 3 2 4【解析】(1)水煤气是由碳与水蒸气高温下反应生成的一氧化碳和氢气的混合物,则其反应为:C+HO(g)
2
CO+H;煤的液化是指从煤中产生液体燃料的一系列方法的统称。最初的液化方法是先利用煤产生
2
氢和一氧化碳的混合气体,然后使这种气体在催化作用下成为液态碳氢化合物燃料 ,属于化学变化,故
答案为:C+HO(g) CO+H;化学;
2 2
(2) 煤在隔绝空气条件下加热、分解,生成焦炭(或半焦)、煤焦油、粗苯、煤气等产物的过程,煤的干
馏是属于化学变化,其中焦炭可用作燃料及工业原料的固体物质,故答案为:焦炭;可作燃料及工业原料;
(3) 由于煤燃烧产生的废气中含有SO 、CO、NO 和NO多种有害气体,其中NO 和NO时形成硝酸型酸雨
2 2 2
的主要成分,则NO和NO 转化硝酸型酸雨的反应方程式为:2NO+O=2NO,3NO +HO=2HNO +
2 2 2 2 2 3
NO,故答案为:2NO+O=2NO,3NO +HO=2HNO +NO;
2 2 2 2 3
(4)氧化钙为碱性氧化物,煤燃烧的废气中含有酸性气体二氧化硫,则氧化钙与二氧化硫反应生成亚硫酸钙;
亚硫酸钙再被氧气氧化为硫酸钙,则其反应分别为:CaO+SO =CaSO ,2CaSO+O=2CaSO ,故答案为:
2 3 3 2 4
CaO+SO =CaSO ,2CaSO+O=2CaSO 。
2 3 3 2 4
【一隅三反】
1.(2021·甘肃·兰州市第二十七中学高一期末)下列说法正确的是
A.石油分馏获得的汽油是纯净物
B.石油的裂化是物理变化
C.煤干馏后可以得到粗苯
D.石油的裂解可以得到氯乙烯
【答案】C
【解析】A.石油分馏得到的汽油是混合物,A错误;
B.石油的催裂化是在一定的条件下,将相对分子质量较大、沸点较高的经断裂为相对分子质量较小、沸
点较低的经的过程,属于化学变化,B错误;
C.煤干馏是将煤隔绝空气加强热使煤分解的过程,可得到焦炭、煤焦油、焦炉煤气、粗氨水、粗苯等,C
正确;
D.石油是由多种烷经和环烷经构成的,故由元素C、H、S等构成,无氯元素,故裂解不能得到氯乙烯,
D错误;故选C。
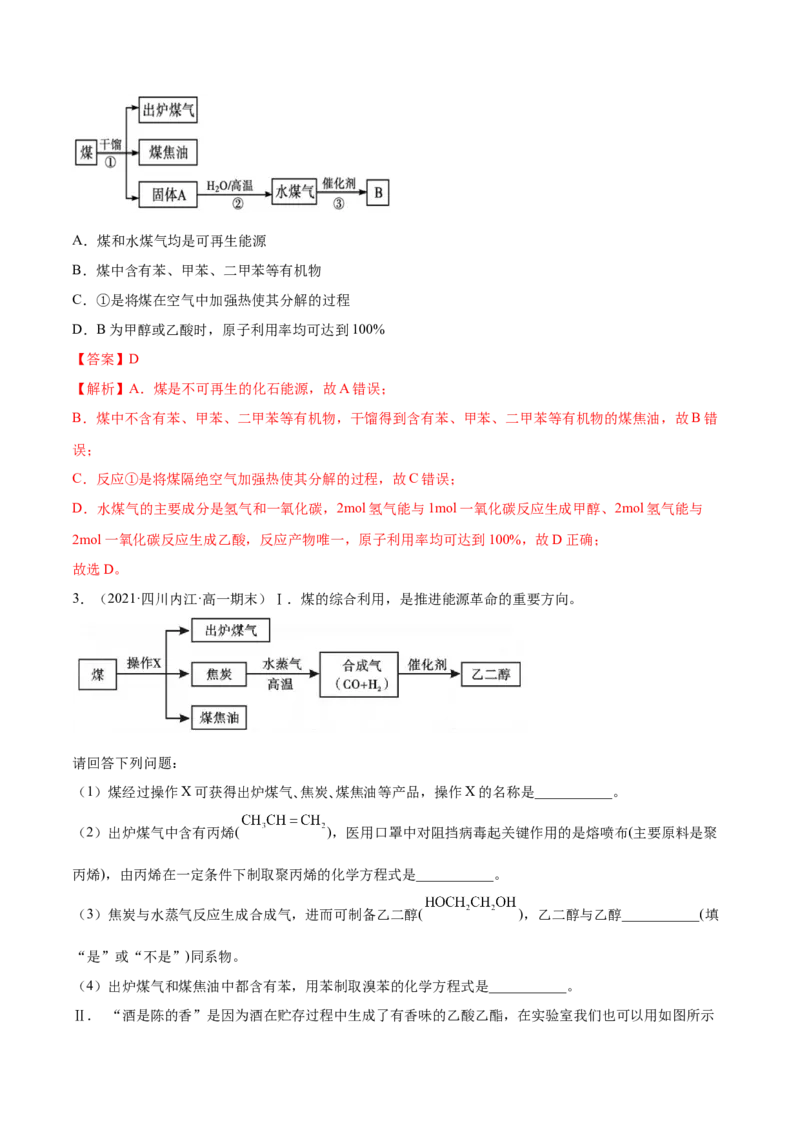
2.(2021·辽宁丹东·高一期末)有关煤的综合利用如图所示,下列说法正确的是A.煤和水煤气均是可再生能源
B.煤中含有苯、甲苯、二甲苯等有机物
C.①是将煤在空气中加强热使其分解的过程
D.B为甲醇或乙酸时,原子利用率均可达到100%
【答案】D
【解析】A.煤是不可再生的化石能源,故A错误;
B.煤中不含有苯、甲苯、二甲苯等有机物,干馏得到含有苯、甲苯、二甲苯等有机物的煤焦油,故B错
误;
C.反应①是将煤隔绝空气加强热使其分解的过程,故C错误;
D.水煤气的主要成分是氢气和一氧化碳,2mol氢气能与1mol一氧化碳反应生成甲醇、2mol氢气能与
2mol一氧化碳反应生成乙酸,反应产物唯一,原子利用率均可达到100%,故D正确;
故选D。
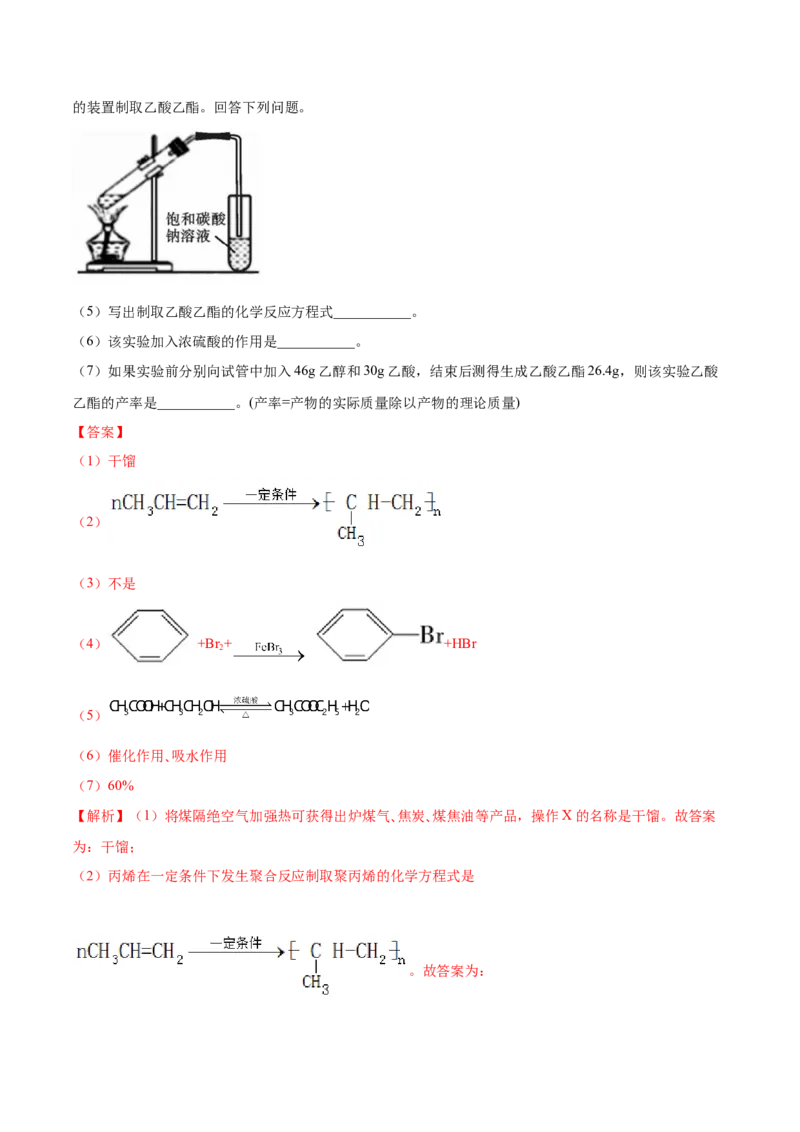
3.(2021·四川内江·高一期末)Ⅰ.煤的综合利用,是推进能源革命的重要方向。
请回答下列问题:
(1)煤经过操作X可获得出炉煤气、焦炭、煤焦油等产品,操作X的名称是___________。
(2)出炉煤气中含有丙烯( ),医用口罩中对阻挡病毒起关键作用的是熔喷布(主要原料是聚
丙烯),由丙烯在一定条件下制取聚丙烯的化学方程式是___________。
(3)焦炭与水蒸气反应生成合成气,进而可制备乙二醇( ),乙二醇与乙醇___________(填
“是”或“不是”)同系物。
(4)出炉煤气和煤焦油中都含有苯,用苯制取溴苯的化学方程式是___________。
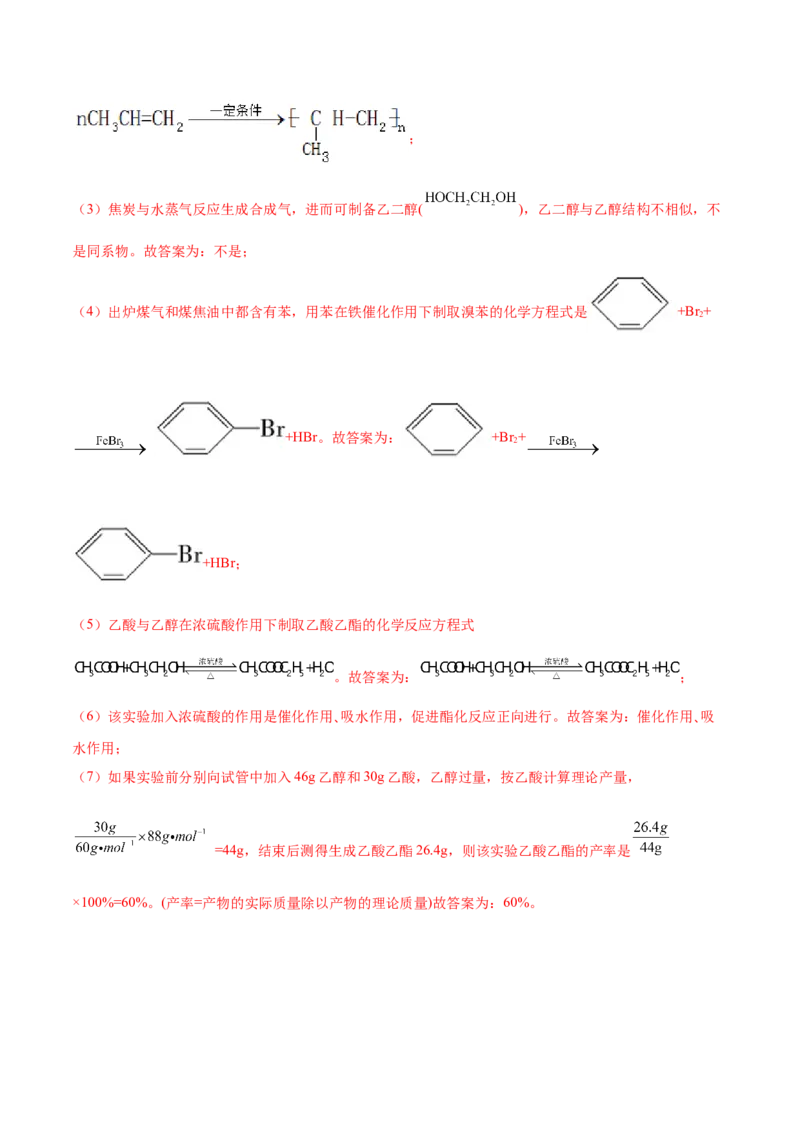
Ⅱ. “酒是陈的香”是因为酒在贮存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题。
(5)写出制取乙酸乙酯的化学反应方程式___________。
(6)该实验加入浓硫酸的作用是___________。
(7)如果实验前分别向试管中加入46g乙醇和30g乙酸,结束后测得生成乙酸乙酯26.4g,则该实验乙酸
乙酯的产率是___________。(产率=产物的实际质量除以产物的理论质量)
【答案】
(1)干馏
(2)
(3)不是
(4) +Br + +HBr
2
(5)
(6)催化作用、吸水作用
(7)60%
【解析】(1)将煤隔绝空气加强热可获得出炉煤气、焦炭、煤焦油等产品,操作X的名称是干馏。故答案
为:干馏;
(2)丙烯在一定条件下发生聚合反应制取聚丙烯的化学方程式是
。故答案为:;
(3)焦炭与水蒸气反应生成合成气,进而可制备乙二醇( ),乙二醇与乙醇结构不相似,不
是同系物。故答案为:不是;
(4)出炉煤气和煤焦油中都含有苯,用苯在铁催化作用下制取溴苯的化学方程式是 +Br +
2
+HBr。故答案为: +Br +
2
+HBr;
(5)乙酸与乙醇在浓硫酸作用下制取乙酸乙酯的化学反应方程式
。故答案为: ;
(6)该实验加入浓硫酸的作用是催化作用、吸水作用,促进酯化反应正向进行。故答案为:催化作用、吸
水作用;
(7)如果实验前分别向试管中加入46g乙醇和30g乙酸,乙醇过量,按乙酸计算理论产量,
=44g,结束后测得生成乙酸乙酯26.4g,则该实验乙酸乙酯的产率是
×100%=60%。(产率=产物的实际质量除以产物的理论质量)故答案为:60%。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育