文档内容
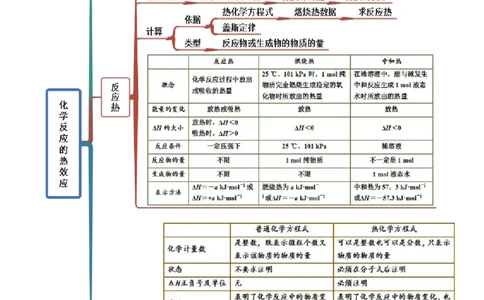
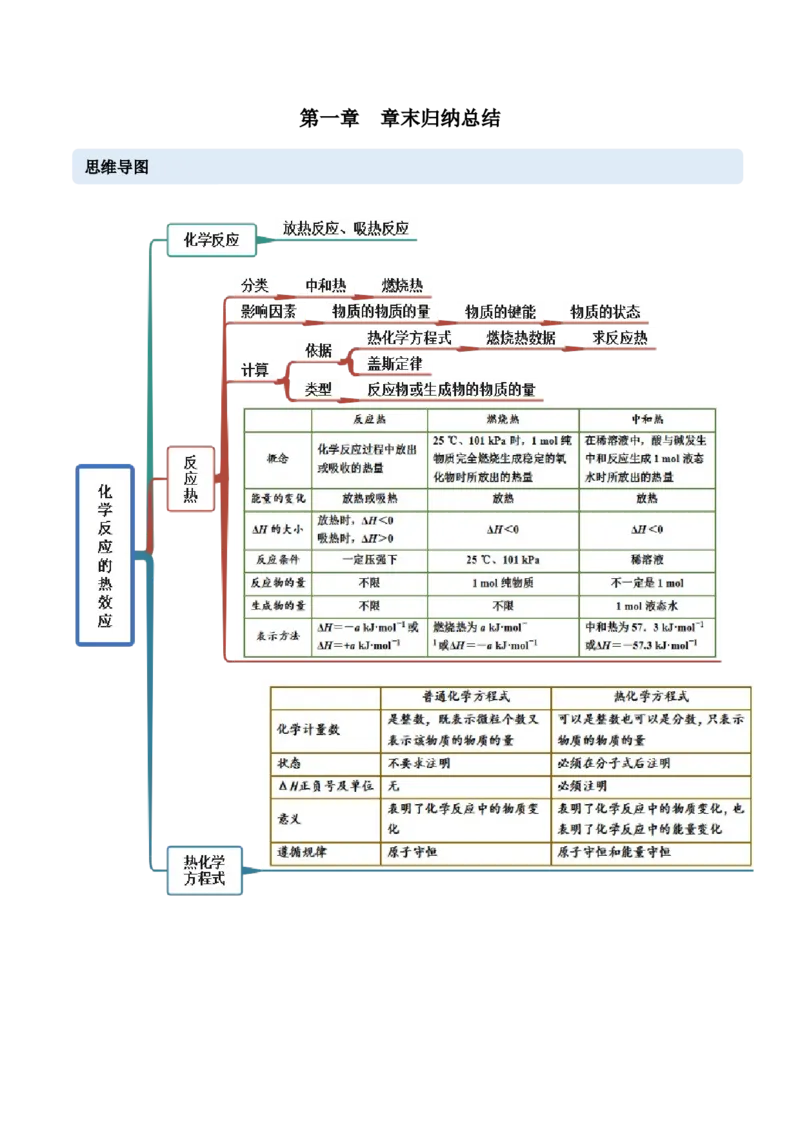
第一章 章末归纳总结
思维导图常见考向
考向一 吸热、放热反应
【例1】下列变化中属于吸热反应的是 ( )
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④KClO 分解制取O
3 2
⑤生石灰与水反应生成熟石灰 ⑥CaCO 高温分解 ⑦CO+C 2CO
3 2
⑧Ba(OH)•8H O与固体NH Cl混合 ⑨C+H O(g) CO+H ⑩Al与盐酸反应
2 2 4 2 2
A.②④⑥⑦⑧⑨ B.①②④⑥⑦⑧⑨
C.①③④⑤⑥⑧⑩ D.①②④⑧⑨
【一隅三反】
1.(2022·上海市川沙中学高一期末)有关反应热效应的说法正确的是
A.铝热反应是放热反应 B.氧化还原反应都属于放热反应
C.需要加热的反应都是吸热反应 D.有化学键断裂的反应是吸热反应
2.(2022·四川甘孜·高二期末)下列各组物质之间的相互反应,说法错误的是
A. 是吸热反应 B. 与 是放热反应
C. 燃烧是放热反应 D. 与 是吸热反应
3.某化学反应过程的能量变化如图所示,下列叙述正确的是
A.该反应为吸热反应 B.该反应为放热反应
C.反应物的总能量等于生成物的总能量 D.反应物的总能量低于生成物的总能量
考向二 热化学方程式
【例2】写出下列反应的热化学方程式:(1)1 mol C与1 mol水蒸气反应生成1 mol CO和1 mol H ,吸热131.5kJ:
2
(2)用CO(g)还原1 mol Fe O(s),放热24.8 kJ。
2 3
(3)1 mol HgO(s)分解生成液态汞和氧气时,吸热90.7 kJ
(4)1 mol N (g)与适量H(g)起反应,生成NH (g),放出92.2 kJ热量。
2 2 3
(5)1 mol N (g)与适量O(g)起反应,生成NO (g),吸收68 kJ热量。
2 2 2
(6)1 mol Cu(s)与适量O(g)起反应,生成CuO(s),放出157 kJ热量。
2
【一隅三反】
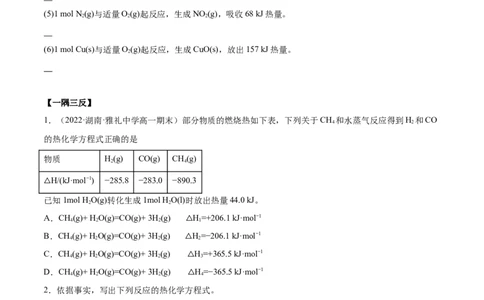
1.(2022·湖南·雅礼中学高一期末)部分物质的燃烧热如下表,下列关于CH 和水蒸气反应得到H 和CO
4 2
的热化学方程式正确的是
物质 H(g) CO(g) CH(g)
2 4
H/(kJ·mol−1) −285.8 −283.0 −890.3
△已知1mol HO(g)转化生成1mol HO(l)时放出热量44.0 kJ。
2 2
A.CH(g)+ H O(g)=CO(g)+ 3H (g) H=+206.1 kJ·mol−1
4 2 2 1
B.CH
4
(g)+ H
2
O(g)=CO(g)+ 3H
2
(g) △H
2
=−206.1 kJ·mol−1
C.CH 4 (g)+ H 2 O(g)=CO(g)+ 3H 2 (g) △ H 3 =+365.5 kJ·mol−1
D.CH
4
(g)+ H
2
O(g)=CO(g)+ 3H
2
(g) △H
4
=−365.5 kJ·mol−1
2.依据事实,写出下列反应的热化学方△程式。
(1)1molCu(s)与适量 (g)反应生成CuO(s),放出157.3kJ的热量
(2)1mol (g)与适量 (g)反应生成 (g)和 (l),放出1411.0kJ的热量
(3)1molC(s)与适量 (g)反应生成CO(g)和 (g),吸收131.5kJ的热量。(4)11.2L(标准状况)H 在足量Cl 中燃烧生成HCl气体,放出91.5kJ热量。
2 2
(5) 已知1molC(石墨,s)与适量HO(g)反应生成CO(g)和H(g),吸收131.3kJ热量。
2 2
(6)1.7gNH(g)发生催化氧化反应生成气态产物,放出22.67kJ的热量。
3
(7)已知:N(g)+3H(g) 2NH (g) ΔH=-92kJ·mol−1,请写出1molNH 分解对应的热化学方程式
2 2 3 3
。若1molN (g)和3mol⇌H (g)在一定条件下发生反应,放出的热量___________92kJ(填“大于”“小于”或
2 2
“等于”),理由是________ ___。
考向三 中和热
【例4】分别取40 mL的0.50 mol·L-1盐酸与40 mL的0.55 mol·L-1NaOH溶液进行中和反应。通过测定反
应过程中放出的热量可计算中和热。回答下列问题:
(1)理论上稀强酸、稀强碱反应生成1 mol 水时放出57.3 kJ的热量,写出表示稀硫酸和稀NaOH溶液反应
的中和热的热化学方程式____________________________________________。
(2)从实验装置上看,可知下图装置中缺少的仪器是___________。
(3)某学生实验记录数据如下:
①近似认为0.55mol·L-1的NaOH溶液和0.50 mol·L-1的盐酸的密度都是1 g·cm-3,中和后生成溶液的比热
容c=4.18 J·g-1·℃-1。则中和热△H=__________(取小数点后一位)。②上述实验数值结果与理论值有偏差,产生偏差的原因可能是________(填字母)。
a.实验装置保温、隔热效果差
b.实验量取盐酸时误取了浓硫酸
c.用温度计测定NaOH溶液起始温度后直接测定盐酸溶液的温度
(4)实验中改用50mL0.50mol·L-1的盐酸跟40mL0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所求
中和热_________(填“相等”或“不相等”),所放出的热量________(填“相等”或“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会______(填“偏大”、
“偏小”或“无影响”).
【一隅三反】
1.关于中和热测定的叙述中错误的是
A.碱液稍过量的目的是确保盐酸被完全中和
B.该实验可以直接在烧杯中进行
C.该实验需要重复2~3次,实验数据可取平均值代入计算
D.不可以用铜丝代替玻璃搅拌器
2.中和反应是放热反应,下列关于中和反应热测定的说法错误的是
A.等温条件下,试管中进行的中和反应,反应体系向空气中释放的热量就是反应的热效应
B.测定中和反应热时,需要快速的将两种溶液混合
C.测定中和反应热时,最重要的是要保证实验装置的隔热效果
D.不同的酸碱反应生成1mol水释放的热量可能不相同
3.50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应
过程中所放出的热量可计算中和反应的反应热。请回答下列问题:
(1)从实验装置上看,图中缺少的一种玻璃仪器是_______。
(2)实验中改用6.94mL 15mol/L硫酸溶液与60mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所求得
的生成1mol HO(l)时放出的热量_______(填“相等”或“不相等”),简述理由:_______。
2
(3)若三次平行操作测得数据中,起始时盐酸与NaOH溶液平均温度相同,而终止温度与起始温度差(t -t )分
2 1
别为①3.3℃、②3.5℃、③4.5℃,则最终代入计算式的温度差的平均值为_______℃。4.利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L-1
NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合
液最高温度。回答下列问题:
(1)为什么所用NaOH溶液要稍过量?_______。
(2)倒入NaOH溶液的正确操作是_______(填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是_______(填序号)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,
其反应热分别为ΔH、ΔH、ΔH,则ΔH、ΔH、ΔH 的大小关系为_______。
1 2 3 1 2 3
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1.为了
计算中和热,某学生实验记录数据如下:
起始温度t/℃ 终止温度t/℃
1 2
盐酸 氢氧化钠溶液 混合溶液
1 20.0 20.1 23.2
2 20.2 20.4 23.4
3 20.5 20.6 23.6
依据该学生的实验数据计算,该实验测得的中和热ΔH=_______(结果保留一位小数)。
(6)_______(填“能”或“不能”)用Ba(OH) 溶液和硫酸代替氢氧化钠溶液和盐酸,理由是_______。
2
考向四 盖斯定律
【例4】室温下,将1mol的CuSO •5H O(s)溶于水会使溶液温度降低,热效应为ΔH;将1mol的CuSO (s)
4 2 1 4溶于水会使溶液温度升高,热效应为ΔH,CuSO •5H O受热分解的化学方程式为:CuSO •5H O(s)
2 4 2 4 2
CuSO (s)+5HO(l),热效应为ΔH。则下列判断正确的是( )
4 2 3
A.ΔH>ΔH B.ΔH>ΔH
2 3 3 1
C.ΔH+ΔH=ΔH D.ΔH+ΔH>ΔH
1 3 2 1 2 3
【一隅三反】
1.下列各组热化学方程式中,化学反应的 前者小于后者的有( )
①
②
③
④
⑤
⑥
A.2项 B.3项 C.4项 D.5项2.(2022·湖北十堰·高一期末)工业上高炉炼铁时常以赤铁矿和焦炭为原料,而将赤铁矿中的 转化
为铁的过程中实际起作用的是CO。反应过程中 发生的一系列变化:
则反应 的 为
A. B.
C. D.
考向五 综合运用
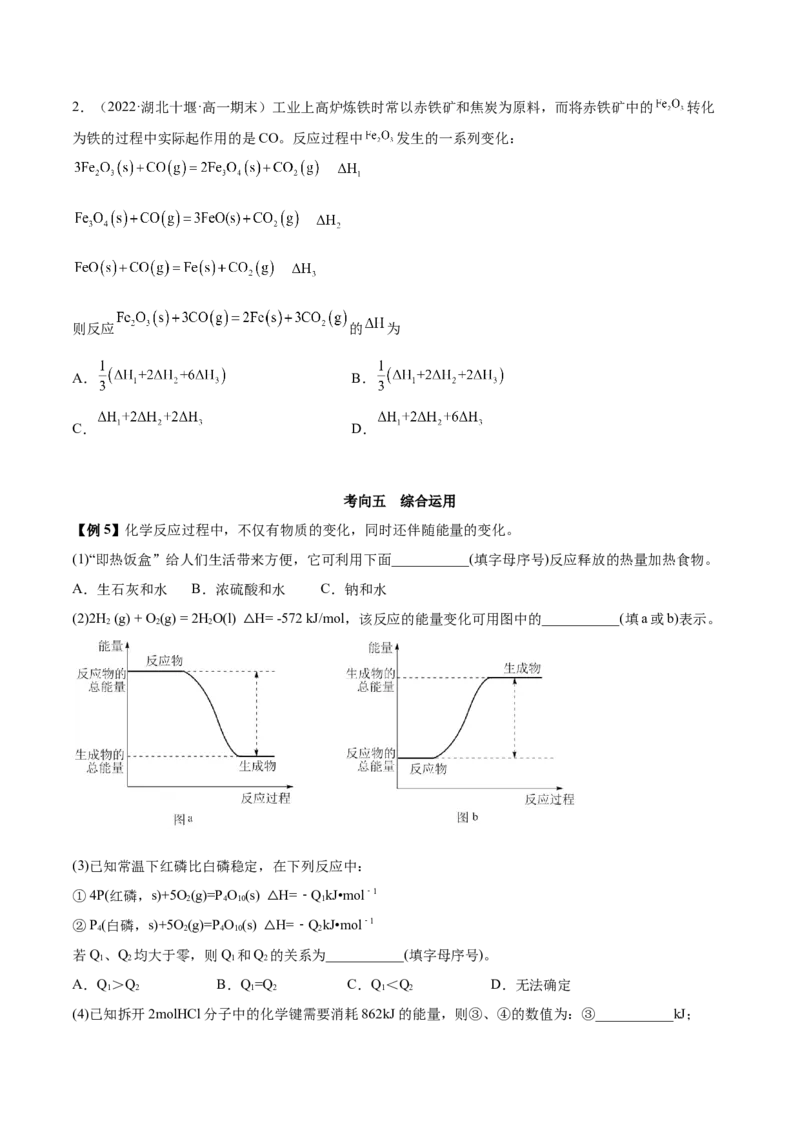
【例5】化学反应过程中,不仅有物质的变化,同时还伴随能量的变化。
(1)“即热饭盒”给人们生活带来方便,它可利用下面___________(填字母序号)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水 C.钠和水
(2)2H (g) + O(g) = 2HO(l) H= -572 kJ/mol,该反应的能量变化可用图中的___________(填a或b)表示。
2 2 2
△
(3)已知常温下红磷比白磷稳定,在下列反应中:
①4P(红磷,s)+5O(g)=P O (s) H=﹣QkJ•mol﹣1
2 4 10 1
②P
4
(白磷,s)+5O
2
(g)=P
4
O
10
(s) △H=﹣Q
2
kJ•mol﹣1
若Q
1
、Q
2
均大于零,则Q
1
和Q 2△的关系为___________(填字母序号)。
A.Q>Q B.Q=Q C.Q<Q D.无法确定
1 2 1 2 1 2
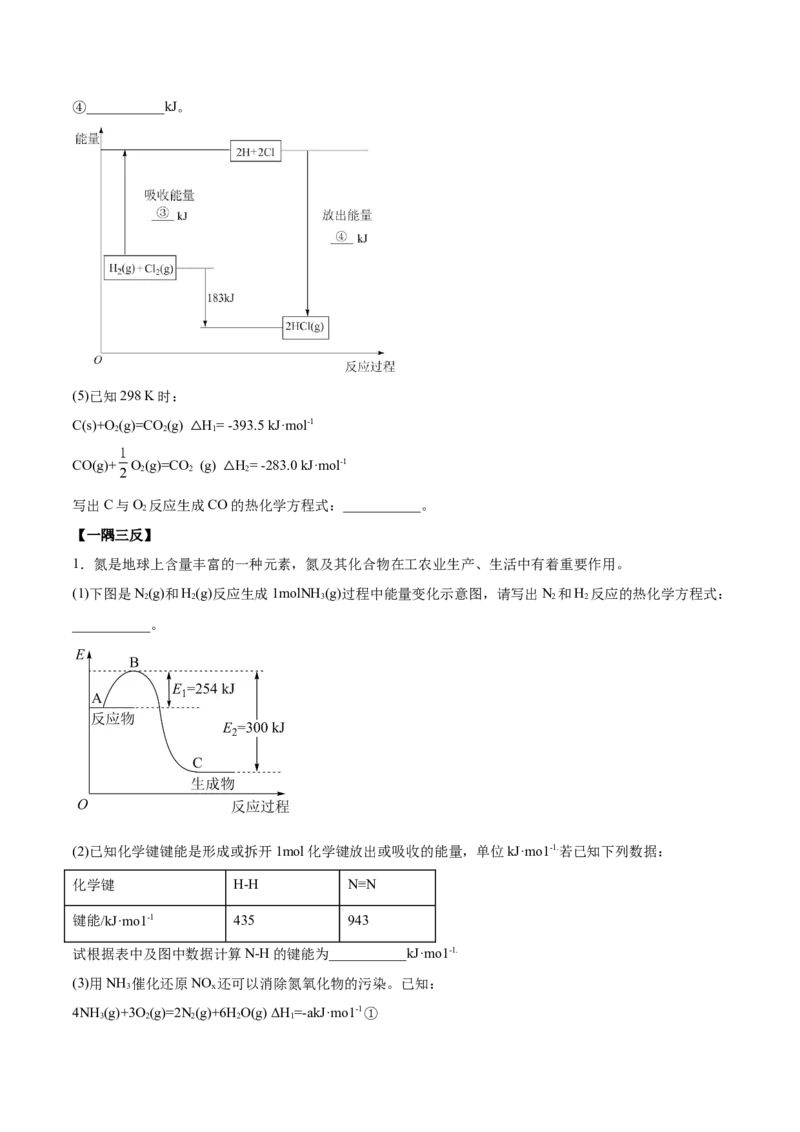
(4)已知拆开2molHCl分子中的化学键需要消耗862kJ的能量,则③、④的数值为:③___________kJ;④___________kJ。
(5)已知298 K时:
C(s)+O(g)=CO (g) H= -393.5 kJ·mol-1
2 2 1
△
CO(g)+ O(g)=CO (g) H= -283.0 kJ·mol-1
2 2 2
△
写出C与O 反应生成CO的热化学方程式:___________。
2
【一隅三反】
1.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)下图是N(g)和H(g)反应生成1molNH (g)过程中能量变化示意图,请写出N 和H 反应的热化学方程式:
2 2 3 2 2
___________。
(2)已知化学键键能是形成或拆开1mol化学键放出或吸收的能量,单位kJ·mo1-1.若已知下列数据:
化学键 H-H N≡N
键能/kJ·mo1-1 435 943
试根据表中及图中数据计算N-H的键能为___________kJ·mo1-1.
(3)用NH 催化还原NO 还可以消除氮氧化物的污染。已知:
3 x
4NH (g)+3O(g)=2N(g)+6HO(g) ΔH=-akJ·mo1-1①
3 2 2 2 1N(g)+O(g)=2NO(g) ΔH=-bkJ·mo1-1②
2 2 2
若1molNH 还原NO至N,则该反应过程中的反应热ΔH=___________kJ·mo1-1(用含a、b的式子表示)。
3 2 3
2.根据信息书写热化学方程式:
(1)化合物AX 和单质X 在一定条件下反应可生成化合物AX 回答下列问题:已知AX 的熔点和沸点分别
3 2 5. 3
为-93.6 ℃和76 ℃,AX 的熔点为167 ℃。室温时AX 与气体X 反应生成1 mol AX ,放出热量123.8 kJ。
5 3 2 5
该反应的热化学方程式为___________。
(2)在25 ℃、101 kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO 用过量饱和石
2
灰水吸收可得100 g CaCO 沉淀,则乙醇燃烧的热化学方程式为___________。
3
(3)在一定条件下,将1 mol N 和3 mol H 充入一密闭容器中发生反应生成氨气,达到平衡时N 的转化率为
2 2 2
25%,放出Q kJ的热量,写出N 与H 反应的热化学方程式为___________。
2 2
(4)化学反应N+3H 2NH 的能量变化如图所示
2 2 3
试写出N(g)和H(g)反应生成NH (l)的热化学方程式:___________。
2 2 3
(5)NaBH (s)与HO(l)反应生成NaBO (s)和氢气,在25 ℃、101 kPa下,已知每消耗3.8 g NaBH (s)放热21.6
4 2 2 4
kJ,该反应的热化学方程式是___________。
3.回答下列问题
(1)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢
转化为氯气的技术成为科学研究的热点。回答下列问题:
Deacon直接氧化法可按下列催化过程进行:
CuCl (s)=CuCl(s)+ Cl(g) H=+83 kJ·mol-1
2 2 1
△
CuCl (s)+ O(g)= CuO(s)+ Cl(g) H=-20 kJ·mol-1
2 2 2
△
CuO(s) + 2HCl(g)= CuCl (s)+HO(g) H=-121 kJ·mol-1
2 2 3
则4HCl(g)+O
2
(g)=2Cl
2
(g)+2H
2
O(g)的 △H=_______kJ·mol-1
(2)甲烷CH
4
是一种高效清洁的新能源,△0.25mol甲烷完全燃烧生成液态水放出热量222.5kJ,则甲烷燃烧的热化学方程式为_______。
(3)已知常温下红磷比白磷稳定,在下列反应中
①4P (红磷,s) +5O (g)=P O (s) H =-Q kJ/mol
2 4 10 1
②P
4
(白磷,s)+5O
2
(g)= P
4
O
10
(s) △H =-Q
2
kJ/mol
若Q
1
、 Q
2
均大于零,则Q
1
和Q
2
的△关系为_______(填字母序号)。
A.Q>Q B.Q=Q C.Q