文档内容
专题二 物质的化学变化
专题提升演练
1.下列有关化学变化的说法正确的是( )
A.从海水中获得物质都需经过化学变化
B.用石灰浆粉刷墙壁,干燥后墙面变硬发生了化学变化
C.石油分馏得到汽油、煤油、柴油等属于化学变化
D.潮湿的衣服被晾干了是化学变化
解析:海水晒盐是利用了蒸发结晶的原理,此过程中没有新物质形成,是物理变化;石灰浆的成
分是氢氧化钙,吸收空气中的二氧化碳生成了碳酸钙固体和水,发生了化学变化;石油中各组
分的沸点不同,石油分馏利用各物质沸点的不同,将它们分离出来,没有生成新物质,属于物理
变化;湿衣服晾干是水由液态变为气态,属于物理变化。
答案:B
2.科学研究表明,氨气在常压下就可液化为液氨,液氨可作汽车的清洁燃料,其燃烧时的主要反
应为4NH +3O 2X+6HO。下列说法中不正确的是( )
3 2 2
A.氨气在常压下液化是物理变化
B.X的化学式为N
2
C.液氨具有可燃性属于化学性质
D.液氨属于混合物
解析:液氨是氨气的液态,属于单质,是纯净物。
答案:D
[来源:学&科&网Z&X&X&K]
3.如图表示两种气体发生的化学反应,其中相同的球代表同种原子。根据图示信息,下列说法
正确的是( )
A.该反应生成两种物质
B.该反应是复分解反应
C.化学反应前后原子的种类不变
D.分子在化学变化中是不可分的
解析:由反应的图示可知,反应后生成的分子种类只有一种,所以生成物是一种物质,故A错误;
该反应的反应物是两种,生成物是一种,所以该反应是化合反应,故B错误;反应的前后都含有
两种原子,且原子的种类没有改变,故C正确;该反应前后分子的种类发生了改变,所以化学反
应中分子可以再分,故D错误。
答案:C
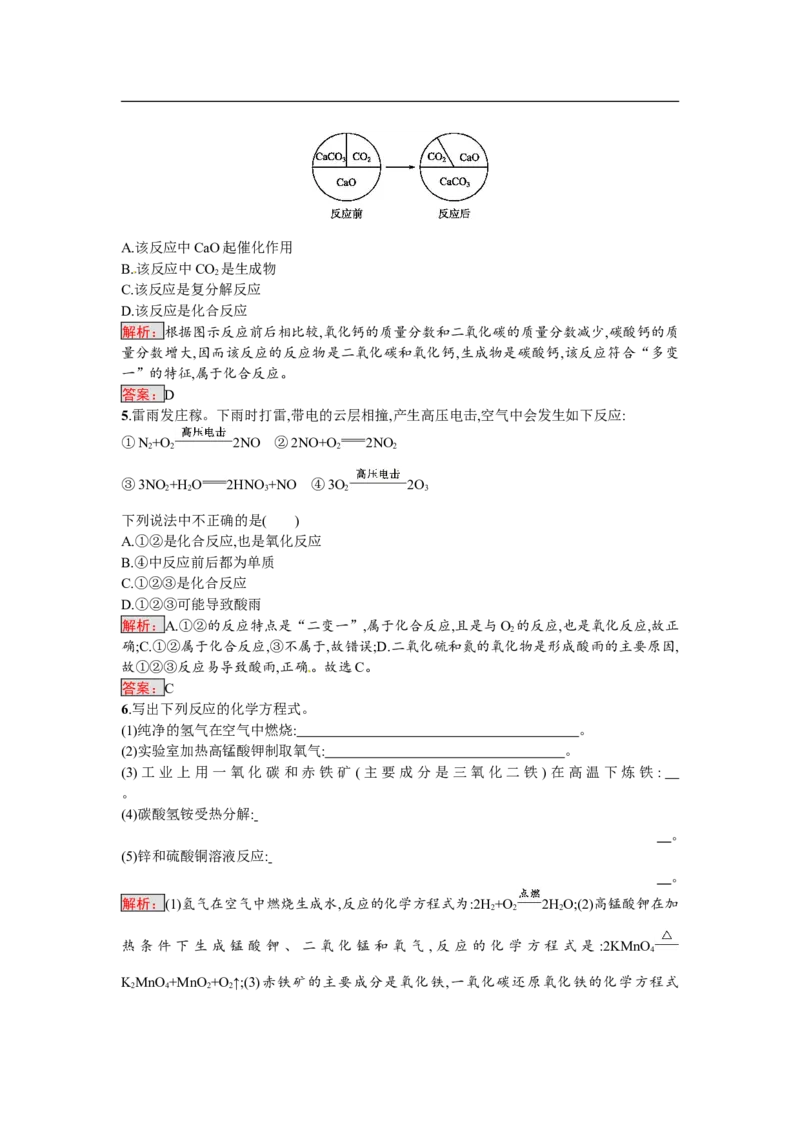
4.如图表示三种物质在密闭容器中反应前后质量比例的变化。下列说法正确的是( )A.该反应中CaO起催化作用
B.该反应中CO 是生成物
2
C.该反应是复分解反应
D.该反应是化合反应
解析:根据图示反应前后相比较,氧化钙的质量分数和二氧化碳的质量分数减少,碳酸钙的质
量分数增大,因而该反应的反应物是二氧化碳和氧化钙,生成物是碳酸钙,该反应符合“多变
一”的特征,属于化合反应。
答案:D
5.雷雨发庄稼。下雨时打雷,带电的云层相撞,产生高压电击,空气中会发生如下反应:
①N+O 2NO ②2NO+O 2NO
2 2 2 2
③3NO +H O 2HNO+NO ④3O 2O
2 2 3 2 3
下列说法中不正确的是( )
A.①②是化合反应,也是氧化反应
B.④中反应前后都为单质
C.①②③是化合反应
D.①②③可能导致酸雨
解析:A.①②的反应特点是“二变一”,属于化合反应,且是与O 的反应,也是氧化反应,故正
2
确;C.①②属于化合反应,③不属于,故错误;D.二氧化硫和氮的氧化物是形成酸雨的主要原因,
故①②③反应易导致酸雨,正确。故选C。
答案:C
6.写出下列反应的化学方程式。
(1)纯净的氢气在空气中燃烧: 。
(2)实验室加热高锰酸钾制取氧气: 。
(3)工业上用一氧化碳和赤铁矿 (主要成分是三氧化二铁 )在高温下炼铁:
。
(4)碳酸氢铵受热分解:
。
(5)锌和硫酸铜溶液反应:
。
解析:(1)氢气在空气中燃烧生成水,反应的化学方程式为:2H +O 2HO;(2)高锰酸钾在加
2 2 2
热条件下生成锰酸钾、二氧化锰和氧气 ,反应的化学方程式是 :2KMnO
4
KMnO +MnO+O ↑;(3)赤铁矿的主要成分是氧化铁,一氧化碳还原氧化铁的化学方程式
2 4 2 2是:3CO+Fe O 2Fe+3CO ;(4)碳酸氢铵分解产生氨气、二氧化碳和水,反应的化学方程式为:
2 3 2
NH HCO NH ↑+CO ↑+H O;(5)锌的金属活动性比铜强,与硫酸铜溶液反应生成硫酸锌和
4 3 3 2 2
铜,反应的化学方程式为:Zn+CuSO ZnSO+Cu。
4 4
答案:(1)2H +O 2HO
2 2 2
(2)2KMnO KMnO +MnO+O ↑
4 2 4 2 2
(3)3CO+Fe O 2Fe+3CO
2 3 2
(4)NH HCO NH ↑+CO ↑+H O
4 3 3 2 2
(5)Zn+CuSO ZnSO+Cu
4 4
7.甲、乙、丙、丁四种物质在一定条件下能发生如下反应:
甲+乙 丙+丁
(1)若甲、丙为化合物,乙、丁为单质,则上述反应的基本反应类型是 ,写出
一个符合该反应类型的化学方程式: 。
(2)若甲、乙、丙、丁均为化合物,且甲溶液呈蓝色,乙为烧碱,则乙的化学式为 ,发
生反应时观察到的现象是 。
(3)若甲、乙、丙、丁均为化合物,且丙为水,丁为盐,则该反应 (填“一定”或“不一
定”)是中和反应,理由是 。
(4)若甲、乙、丙为化合物,丁为单质,且乙、丙是组成元素相同的气体,该反应在工业上的用途
可能是 。
解析:(1)一种单质和一种化合物反应生成另一种单质和另一种化合物的反应属于置换反应。
(2)甲溶液为蓝色,应为可溶性的铜盐,乙为烧碱,化学式为NaOH,则二者反应后生成氢氧化铜
蓝色沉淀。(3)若甲、乙、丙、丁均为化合物,且丙为水,丁为盐,则该反应不一定是中和反应,因为
中和反应的反应物必须为酸和碱,而甲和乙不一定是酸和碱,可能是金属氧化物和酸或者非金
属氧化物和碱的反应。(4)若甲、乙、丙为化合物,丁为单质,且乙、丙是组成元素相同的气体,该
反应为一氧化碳还原金属氧化物的反应,例如CO+CuO Cu+CO ,这类反应在工业上用于
2
冶炼金属。
答案:(1)置换反应 Zn+H SO ZnSO+H ↑(化学方程式合理即可)
2 4 4 2
(2)NaOH 有蓝色沉淀从溶液中析出
(3)不一定 某些金属氧化物与酸反应可以生成盐和水或某些非金属氧化物与碱反应也
可以生成盐和水
(4)冶炼金属(或炼铁)
8.将CO 通入NaOH溶液中无明显现象。某学习小组的同学为了观察到CO 与NaOH溶液反
2 2
应的明显外观现象,并同时利用这一反应来验证质量守恒定律,设计了下列实验。请根据实验
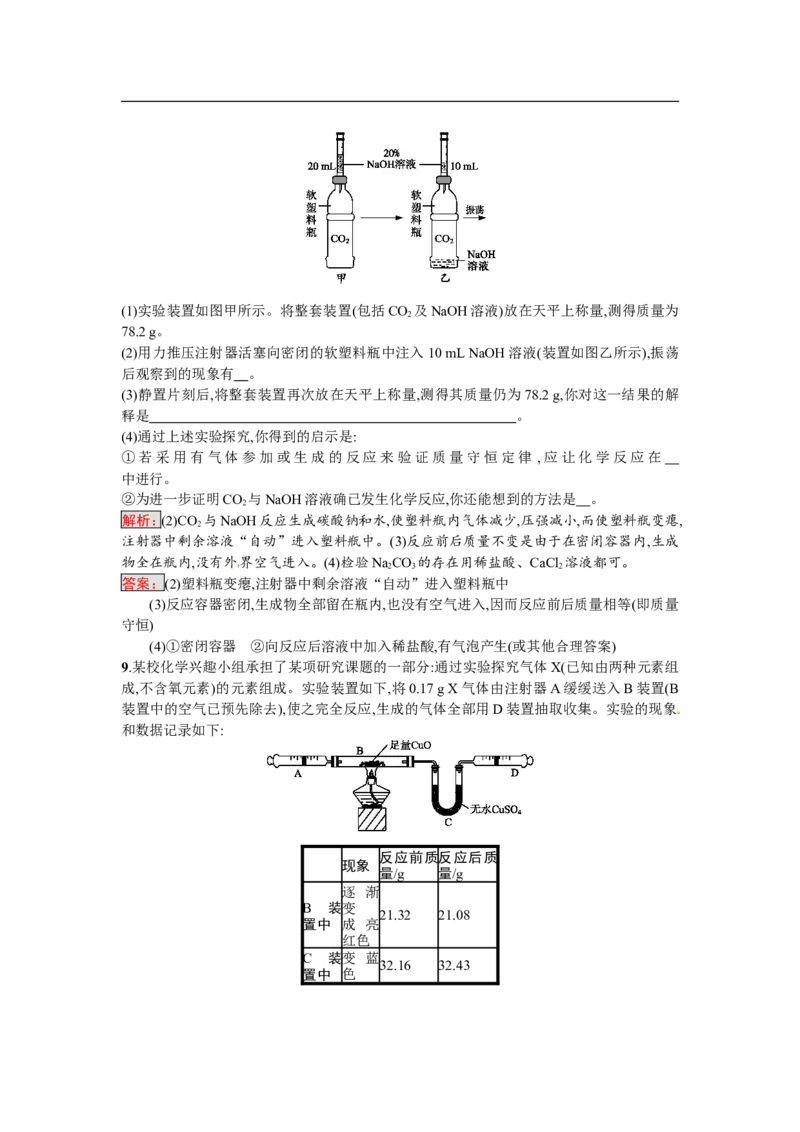
过程及内容,思考并回答相关问题。(1)实验装置如图甲所示。将整套装置(包括CO 及NaOH溶液)放在天平上称量,测得质量为
2
78.2 g。
(2)用力推压注射器活塞向密闭的软塑料瓶中注入10 mL NaOH溶液(装置如图乙所示),振荡
后观察到的现象有 。
(3)静置片刻后,将整套装置再次放在天平上称量,测得其质量仍为78.2 g,你对这一结果的解
释是 。
(4)通过上述实验探究,你得到的启示是:
①若采用有气体参加或生成的反应来验证质量守恒定律 ,应让化学反应在
中进行。
②为进一步证明CO 与NaOH溶液确已发生化学反应,你还能想到的方法是 。
2
解析:(2)CO 与NaOH反应生成碳酸钠和水,使塑料瓶内气体减少,压强减小,而使塑料瓶变瘪,
2
注射器中剩余溶液“自动”进入塑料瓶中。(3)反应前后质量不变是由于在密闭容器内,生成
物全在瓶内,没有外界空气进入。(4)检验NaCO 的存在用稀盐酸、CaCl 溶液都可。
2 3 2
答案:(2)塑料瓶变瘪,注射器中剩余溶液“自动”进入塑料瓶中
(3)反应容器密闭,生成物全部留在瓶内,也没有空气进入,因而反应前后质量相等(即质量
守恒)
(4)①密闭容器 ②向反应后溶液中加入稀盐酸,有气泡产生(或其他合理答案)
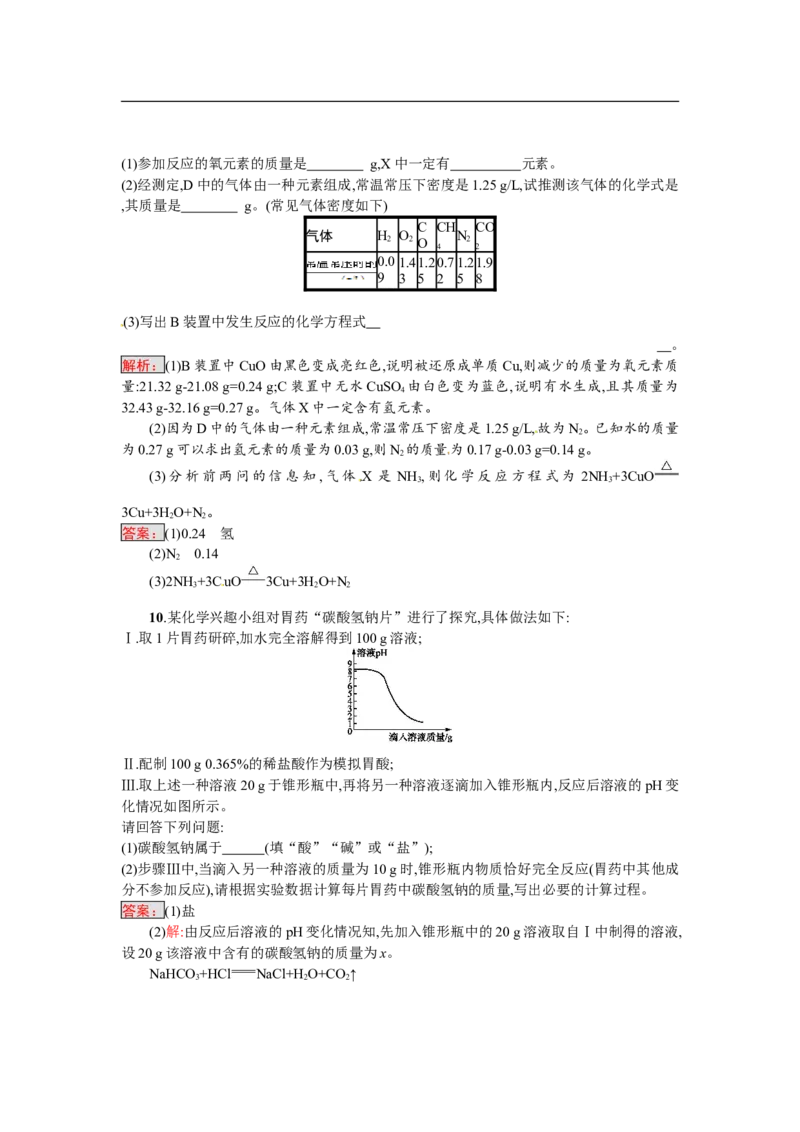
9.某校化学兴趣小组承担了某项研究课题的一部分:通过实验探究气体X(已知由两种元素组
成,不含氧元素)的元素组成。实验装置如下,将0.17 g X气体由注射器A缓缓送入B装置(B
装置中的空气已预先除去),使之完全反应,生成的气体全部用D装置抽取收集。实验的现象
和数据记录如下:
反应前质反应后质
现象
量/g 量/g
逐 渐
B 装变
21.32 21.08
置中 成 亮
红色
C 装变 蓝
32.16 32.43
置中 色(1)参加反应的氧元素的质量是 g,X中一定有 元素。
(2)经测定,D中的气体由一种元素组成,常温常压下密度是1.25 g/L,试推测该气体的化学式是
,其质量是 g。(常见气体密度如下)
C CH CO
气体 H O N
2 2 O 2
4[来源:Zxxk.Com] 2
0.01.41.20.71.21.9
9 3 5 2 5 8
[ 来
源:Z*xx*k.Com]
(3)写出B装置中发生反应的化学方程式
。
解析:(1)B装置中CuO由黑色变成亮红色,说明被还原成单质Cu,则减少的质量为氧元素质
量:21.32 g-21.08 g=0.24 g;C装置中无水CuSO 由白色变为蓝色,说明有水生成,且其质量为
4
32.43 g-32.16 g=0.27 g。气体X中一定含有氢元素。
(2)因为D中的气体由一种元素组成,常温常压下密度是1.25 g/L,故为N。已知水的质量
2
为0.27 g可以求出氢元素的质量为0.03 g,则N 的质量为0.17 g-0.03 g=0.14 g。
2
(3)分析前两问的信息知,气体 X 是 NH ,则化学反应方程式为 2NH +3CuO
3 3
3Cu+3H O+N。
2 2
答案:(1)0.24 氢
(2)N 0.14
2
(3)2NH +3CuO 3Cu+3H O+N
3 2 2
10.某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下:
Ⅰ.取1片胃药研碎,加水完全溶解得到100 g溶液;
Ⅱ.配制100 g 0.365%的稀盐酸作为模拟胃酸;
[来源:学*科*网]
Ⅲ.取上述一种溶液20 g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变
化情况如图所示。
请回答下列问题:
(1)碳酸氢钠属于 (填“酸”“碱”或“盐”);
(2)步骤Ⅲ中,当滴入另一种溶液的质量为10 g时,锥形瓶内物质恰好完全反应(胃药中其他成
分不参加反应),请根据实验数据计算每片胃药中碳酸氢钠的质量,写出必要的计算过程。
答案:(1)盐
(2)解:由反应后溶液的pH变化情况知,先加入锥形瓶中的20 g溶液取自Ⅰ中制得的溶液,
设20 g该溶液中含有的碳酸氢钠的质量为x。
NaHCO +HCl NaCl+H O+CO↑
3 2 284 36.5
x 10 g×0.365%
解得:x=0.084 g
每片胃药中碳酸氢钠的质量是0.084 g× =0.42 g
答:每片胃药中碳酸氢钠的质量是0.42 g。