文档内容
专题五 物质的检验、提纯和推断
专题提升演练
1.某气体由氢气、一氧化碳、甲烷中的一种或几种组成,点燃该气体后,依次通过下图所示的装
置,测得两装置的质量均增加,则下列对气体组成的推断不正确的是( )
A.可能只有甲烷
B.可能只有氢气
C.可能是甲烷和一氧化碳
D.可能三种气体都存在
解析:氢气燃烧生成水,只有盛浓硫酸的装置质量增加,与题意不符。
答案:B
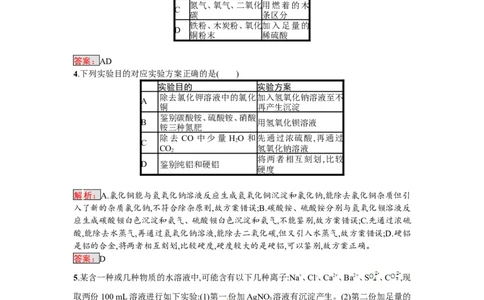
2.银铜合金广泛用于航空工业,从切割废料中回收银并制备铜化工产品的工艺流程如图所示:
[已知Al(OH) 和Cu(OH) 开始分解的温度分别为450 ℃和80 ℃]
3 2
下列关于该流程的说法不正确的是( )
A.操作Ⅰ和操作Ⅱ都是过滤
B.溶液C的主要成分是NaSO
2 4
C.固体B的主要成分是Al(OH) 和Cu(OH)
3 2
D.该生产流程所得的主要产品是Ag和CuAlO
2
解析:由题意可知,银铜合金废料在空气中熔炼时,铜与氧气反应生成了氧化铜,氧化铜与硫酸
反应生成了硫酸铜,硫酸铜、硫酸铝与加入的氢氧化钠反应分别生成了氢氧化铜、氢氧化铝沉
淀和硫酸钠,在煮沸时,氢氧化铜分解生成了氧化铜和水,所以过滤时得到的溶液C的主要成
分是硫酸钠,固体B的主要成分是Al(OH) 和CuO,固体B在惰性气体中煅烧得到了CuAlO。
3 2
所以:A.由工艺流程图可知,操作Ⅰ和操作Ⅱ都是固液分离的过程,操作名称是过滤,故正确;B.
由上述分析可知,溶液C的主要成分是NaSO ,故正确;C.由上述分析可知,固体B的主要成分
2 4
是 Al(OH) 和 CuO,故错误;D.由工艺流程图可知,该生产流程所得的主要产品是 Ag 和
3
CuAlO,故正确。
2
答案:C
3.(双选)下表中各组物质的鉴别方法正确的是( )
选
需要鉴别的物质 鉴别方法
项稀盐酸、氯化钠
滴加石蕊
A 溶液、
溶液
氢氧化钠溶液
硫酸钾、硫酸钡、加入足量
B
碳酸钙 的水
续表
选
需要鉴别的物质 鉴别方法
项
氮气、氧气、二氧化用燃着的木
C
碳 条区分
铁粉、木炭粉、氧化加入足量的
D
铜粉末 稀硫酸
答案:AD
4.下列实验目的对应实验方案正确的是( )
实验目的 实验方案
除去氯化钾溶液中的氯化加入氢氧化钠溶液至不
A
[来源:学科网铜 再产生沉淀
ZXXK]
鉴别碳酸铵、硫酸铵、硝酸
B 用氢氧化钡溶液
铵三种氮肥
除去 CO 中少量 HO 和先通过浓硫酸,再通过
C 2
CO 氢氧化钠溶液
2
将两者相互刻划,比较
D 鉴别纯铝和硬铝
硬度
解析:A.氯化铜能与氢氧化钠溶液反应生成氢氧化铜沉淀和氯化钠,能除去氯化铜杂质但引
入了新的杂质氯化钠,不符合除杂原则,故方案错误;B.碳酸铵、硫酸铵分别与氢氧化钡溶液反
应生成碳酸钡白色沉淀和氨气、硫酸钡白色沉淀和氨气,不能鉴别,故方案错误;C.先通过浓硫
酸,能除去水蒸气,再通过氢氧化钠溶液,能除去二氧化碳,但又引入水蒸气,故方案错误;D.硬铝
是铝的合金,将两者相互刻划,比较硬度,硬度较大的是硬铝,可以鉴别,故方案正确。
答案:D
5.某含一种或几种物质的水溶液中,可能含有以下几种离子:Na+、Cl-、Ca2+、Ba2+、S 、C ,现
取两份100 mL溶液进行如下实验:(1)第一份加AgNO 溶液有沉淀产生。(2)第二份加足量的
3
Ba(NO ) 溶液,有白色沉淀产生,再加入过量的稀硝酸沉淀部分溶解。根据上述实验,以下推测
3 2
正确的是( )
A.一定存在Cl-
B.一定存在C ,可能存在Ba2+
C.一定存在Na+
D.一定存在S ,可能存在Ca2+解析:(1)加入AgNO 溶液有沉淀产生,说明溶液中可能存在 Cl-、C 、S ;(2)加足量
3
Ba(NO ) 溶液后,有沉淀产生,再加入过量的稀硝酸沉淀部分溶解,说明溶液中一定有C 和S
3 2
;Ba2+与S 不共存,Ca2+和C 不共存,所以没有Ba2+和Ca2+;又根据电荷守恒,溶液中一定
有阳离子,因此一定有Na+,综上可知溶液中一定有Na+、C 和S ,可能有Cl-,一定没有Ca2+、
Ba2+。
答案:C
6.请回答下列与物质提纯有关的问题。
(1)下列两个方案都可以除去铜粉中少量的CuO,从环境保护和操作简便等方面考虑,较好的
方案是 (填“a”或“b”)。
a.用稀盐酸除去CuO
b.用CO还原CuO
(2)要除去KSO 溶液中的少量KOH,不能选用稀盐酸,原因是会生成 (填名称或化学
2 4
式)而引入新的杂质。
(3)要将NaCl溶液中少量的NaSO 转化为沉淀而除去,可选用适量的 (填名称或化学
2 4
式)溶液。
解析:(1)CO还原CuO方案不好,由于CO有毒,排入空气中会造成环境污染。(2)用盐酸除
KOH,会 生成 KCl 而引入新杂质。(3)除去 NaCl 溶液中少量的 NaSO ,需加入
2 4
BaCl ,Na SO +BaCl BaSO↓+2NaCl,不能加入Ba(NO )、Ba(OH) ,因为加入这两种物质,在
2 2 4 2 4 3 2 2
除去杂质的同时还生成了NaNO 、NaOH,引入新的杂质。
3
答案:(1)a
(2)氯化钾(或KCl)
(3)BaCl (或氯化钡)
2
7.现有三瓶失去标签的无色溶液:盐酸、氯化钠溶液和澄清石灰水。已知指示剂加入中性溶液
中不变色。
(1) 往 三 种 无 色 溶 液 中 加 入 某 种 指 示 剂 即 可 区 别 它 们 , 该 指 示 剂 可 选 用
。
(2)装澄清石灰水的试剂瓶口常出现白膜,白膜主要成分的化学式是 。
(3)上述溶液中,属于盐溶液的是 。
解析:(1)紫色石蕊在酸、碱、盐中可以显示不同的颜色,取样品,滴入石蕊,显红色的是盐酸,显
紫色的是氯化钠溶液,显蓝色的是澄清石灰水;(2)氢氧化钙与二氧化碳反应会生成白色的碳
酸钙沉淀,所以装澄清石灰水的试剂瓶口常出现白膜,白膜主要成分的化学式是CaCO ;(3)氯
3
化钠是由金属离子和酸根离子组成的化合物,所以氯化钠溶液属于盐溶液。
答案:(1)紫色石蕊溶液
(2)CaCO
3
(3)氯化钠溶液
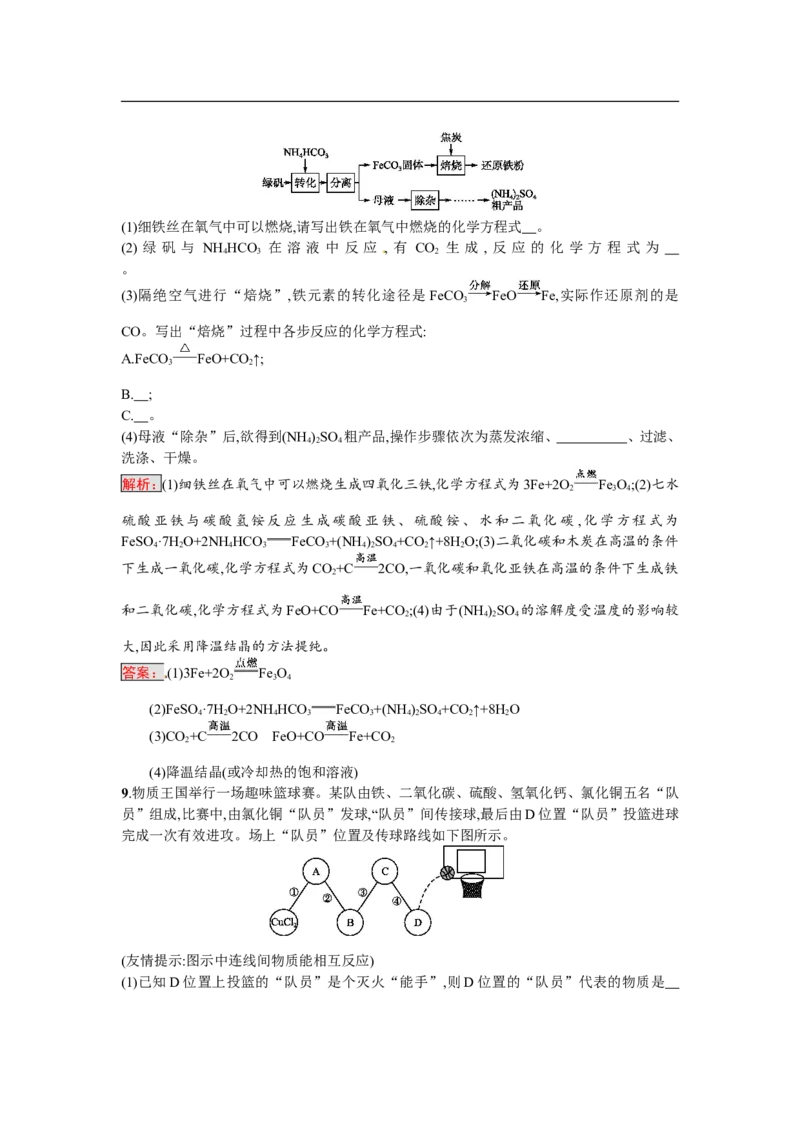
8.绿矾又名七水硫酸亚铁,其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂
等。绿矾(FeSO ·7HO)的一种综合利用工艺如下:
4 2(1)细铁丝在氧气中可以燃烧,请写出铁在氧气中燃烧的化学方程式 。
(2) 绿 矾 与 NH HCO 在 溶 液 中 反 应 , 有 CO 生 成 , 反 应 的 化 学 方 程 式 为
4 3 2
。
(3)隔绝空气进行“焙烧”,铁元素的转化途径是 FeCO FeO Fe,实际作还原剂的是
3
CO。写出“焙烧”过程中各步反应的化学方程式:
A.FeCO FeO+CO↑;
3 2 [来源:学.科.网Z.X.X.K]
B. ;
C. 。
(4)母液“除杂”后,欲得到(NH )SO 粗产品,操作步骤依次为蒸发浓缩、 、过滤、
4 2 4
洗涤、干燥。
解析:(1)细铁丝在氧气中可以燃烧生成四氧化三铁,化学方程式为3Fe+2O Fe O;(2)七水
2 3 4
硫酸亚铁与碳酸氢铵反应生成碳酸亚铁、硫酸铵、水和二氧化碳 ,化学方程式为
FeSO ·7HO+2NH HCO FeCO+(NH)SO +CO ↑+8H O;(3)二氧化碳和木炭在高温的条件
4 2 4 3 3 4 2 4 2 2
下生成一氧化碳,化学方程式为CO+C 2CO,一氧化碳和氧化亚铁在高温的条件下生成铁
2
和二氧化碳,化学方程式为FeO+CO Fe+CO ;(4)由于(NH )SO 的溶解度受温度的影响较
2 4 2 4
大,因此采用降温结晶的方法提纯。
答案:(1)3Fe+2O Fe O
2 3 4
(2)FeSO ·7HO+2NH HCO FeCO+(NH)SO +CO ↑+8H O
4 2 4 3 3 4 2 4 2 2
(3)CO +C 2CO FeO+CO Fe+CO
2 2
(4)降温结晶(或冷却热的饱和溶液)
9.物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队
员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球
完成一次有效进攻。场上“队员”位置及传球路线如下图所示。
[来源:学.科.网Z.X.X.K]
(友情提示:图示中连线间物质能相互反应)
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置的“队员”代表的物质是。
(2)B位置“队员”所代表的物质的一种用途是 。
(3)写出连线④代表的物质间发生反应的化学方程式 。
连线①代表的物质间发生化学反应的基本类型是 反应。
解析:D是个灭火“能手”,证明是二氧化碳;五种物质中能与二氧化碳反应的只有氢氧化钙,
故C是氢氧化钙;氢氧化钙除了能与二氧化碳反应还能与硫酸反应,故B是硫酸;则A是铁,与
硫酸铜反应的化学方程式为Fe+CuSO FeSO +Cu,故属于置换反应。
4 4 [来源:学.科.网Z.X.X.K]
答案:(1)CO
2
(2)金属除锈等
(3)Ca(OH) +CO CaCO ↓+H O 置换
2 2 3 2
10.A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素。其中A为无色气体
单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分。它们之间的部分转化关系如图
所示(图中反应条件及部分反应物、生成物已省略)。
[来源:学|科|网]
回答下列问题:
(1)写出下列物质的化学式:A ;D 。
(2)写出由物质C转化为物质B的化学方程式: 。
(3)写出物质 C 与过氧化钠(NaO)反应生成碳酸钠和物质 A 的化学方程式:
2 2
。
解析:(1)A、B、C、D是初中化学常见的物质,D是大理石的主要成分,所以D是碳酸钙,B、C为
氧化物,且B为有毒气体,所以B是一氧化碳,一氧化碳和C可以相互转化,碳酸钙和C也可以
相互转化,所以C是二氧化碳,A为无色气体单质,会转化成一氧化碳和二氧化碳,所以A是氧
气;(2)物质C转化为物质B的反应是二氧化碳与碳高温生成一氧化碳,化学方程式为CO+C
2
2CO;(3)二氧化碳和过氧化钠(Na O)反应生成碳酸钠和氧气,化学方程式为2CO+2Na O
2 2 2 2 2
2NaCO+O 。
2 3 2
答案:(1)O CaCO
2 3
(2)CO +C 2CO
2
(3)2CO +2Na O 2NaCO+O
2 2 2 2 3 2