文档内容
第五单元 化学方程式
知能优化训练
中考回顾
1.(2017四川内江中考)下列反应属于复分解反应的是( )
A.CO+H O HCO
2 2 2 3
B.2HCl+Ca(OH) CaCl +2H O
2 2 2
C.2KMnO KMnO +MnO+O ↑
4 2 4 2 2
D.2Na+2HO 2NaOH+H ↑
2 2
答案:B
2.(2017天津中考)已知A+3B 2C+3D中,已知2.3 g A跟4.8 g B恰好完全反应生成4.4 g C
。又知D的相对分子质量为18,则A的相对分子质量为( )
A.23 B.46 C.92 D.96
答案:B
3.(2017湖南邵阳中考)下列化学方程式及其反应类型都正确的是( )
反
选 应
化学方程式
项 类
型
化
合
A Mg+O MgO
2 2 反
应
分
解
B HO HO+O↑
2 2 2 2 反
应
置
换
C Fe+H SO FeSO +H ↑
2 4 4 2 反
应
复
分
2KNO+Ba(OH) Ba(NO )+2K
D 3 2 3 2 解
OH
反
应
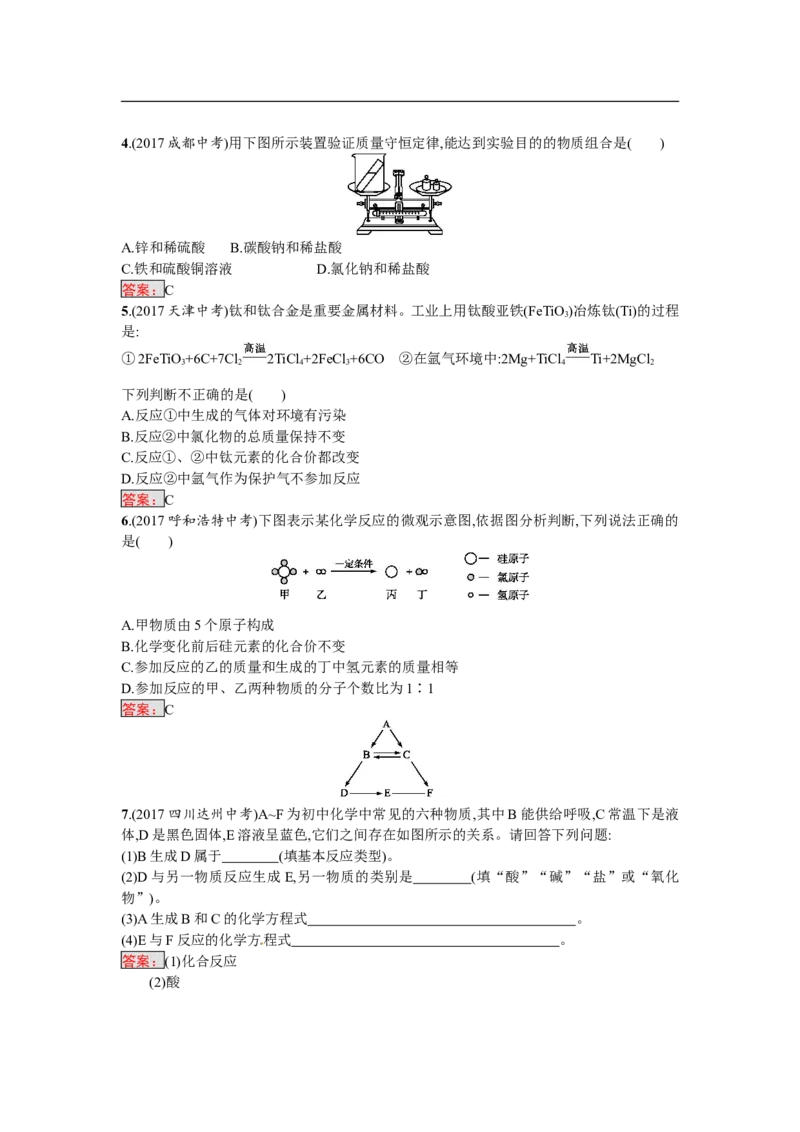
答案:C4.(2017成都中考)用下图所示装置验证质量守恒定律,能达到实验目的的物质组合是( )
A.锌和稀硫酸 B.碳酸钠和稀盐酸
C.铁和硫酸铜溶液 D.氯化钠和稀盐酸
答案:C
5.(2017天津中考)钛和钛合金是重要金属材料。工业上用钛酸亚铁(FeTiO)冶炼钛(Ti)的过程
3
是:
①2FeTiO+6C+7Cl 2TiCl +2FeCl +6CO ②在氩气环境中:2Mg+TiCl Ti+2MgCl
3 2 4 3 4 2
下列判断不正确的是( )
A.反应①中生成的气体对环境有污染
B.反应②中氯化物的总质量保持不变
C.反应①、②中钛元素的化合价都改变
D.反应②中氩气作为保护气不参加反应
答案:C
6.(2017呼和浩特中考)下图表示某化学反应的微观示意图,依据图分析判断,下列说法正确的
是( )
A.甲物质由5个原子构成
B.化学变化前后硅元素的化合价不变
C.参加反应的乙的质量和生成的丁中氢元素的质量相等
D.参加反应的甲、乙两种物质的分子个数比为1∶1
答案:C
[来源:学.科.网Z.X.X.K]
7.(2017四川达州中考)A~F为初中化学中常见的六种物质,其中B能供给呼吸,C常温下是液
体,D是黑色固体,E溶液呈蓝色,它们之间存在如图所示的关系。请回答下列问题:
(1)B生成D属于 (填基本反应类型)。
(2)D与另一物质反应生成E,另一物质的类别是 (填“酸”“碱”“盐”或“氧化
物”)。
(3)A生成B和C的化学方程式 。
(4)E与F反应的化学方程式 。
答案:(1)化合反应
(2)酸(3)2H O 2HO+O↑
2 2 2 2
(4)CuCl +Ca(OH) Cu(OH) ↓+CaCl (答案合理即可)
2 2 2 2
8.(2017四川绵阳中考)已知:Al(OH) 沉淀可溶于NaOH溶液,其反应的化学方程式为
3
Al(OH) +NaOH NaAlO +2H O
3 2 2
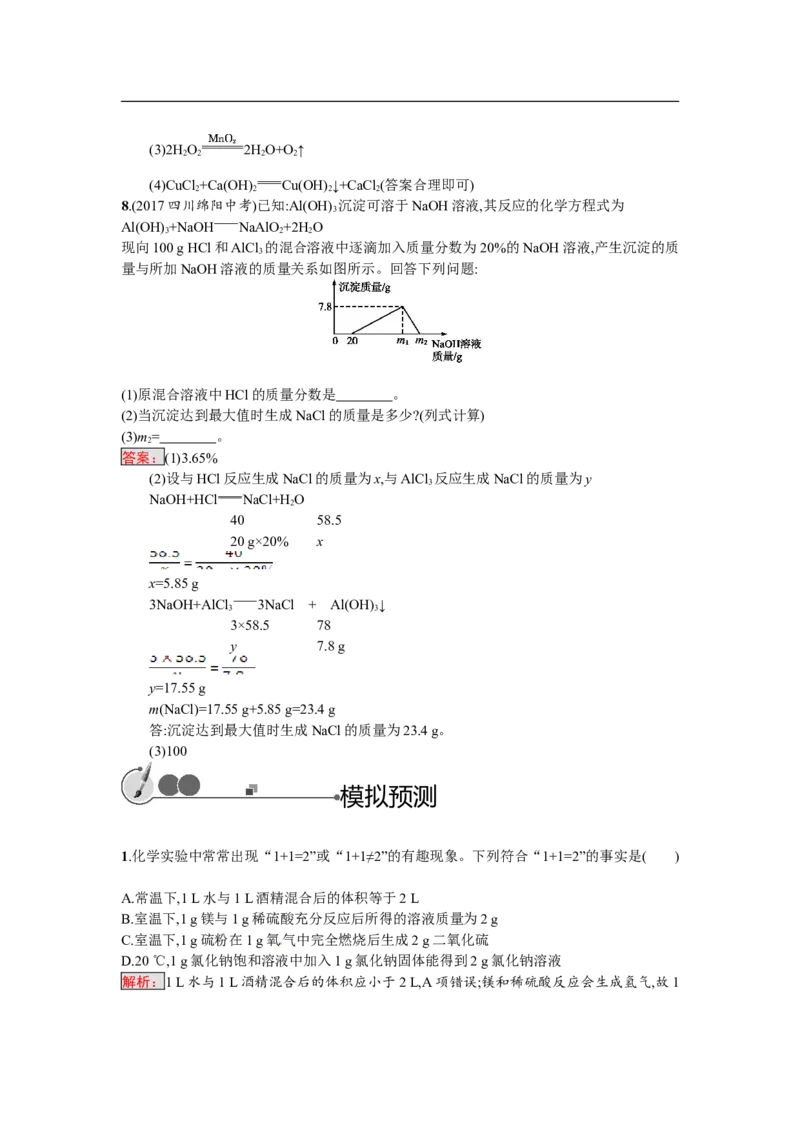
现向100 g HCl和AlCl 的混合溶液中逐滴加入质量分数为20%的NaOH溶液,产生沉淀的质
3
量与所加NaOH溶液的质量关系如图所示。回答下列问题:
(1)原混合溶液中HCl的质量分数是 。
(2)当沉淀达到最大值时生成NaCl的质量是多少?(列式计算)
(3)m= 。
2
答案:(1)3.65%
[来源:学科网ZXXK]
(2)设与HCl反应生成NaCl的质量为x,与AlCl 反应生成NaCl的质量为y
3
NaOH+HCl NaCl+H O
2
40 58.5
20 g×20% x
x=5.85 g
3NaOH+AlCl 3NaCl + Al(OH) ↓
3 3
3×58.5 78
y 7.8 g
y=17.55 g
m(NaCl)=17.55 g+5.85 g=23.4 g
[来源:学+科+网Z+X+X+K]
答:沉淀达到最大值时生成NaCl的质量为23.4 g。
(3)100
模拟预测
1.化学实验中常常出现“1+1=2”或“1+1≠2”的有趣现象。下列符合“1+1=2”的事实是( )
A.常温下,1 L水与1 L酒精混合后的体积等于2 L
B.室温下,1 g镁与1 g稀硫酸充分反应后所得的溶液质量为2 g
C.室温下,1 g硫粉在1 g氧气中完全燃烧后生成2 g二氧化硫
D.20 ℃,1 g氯化钠饱和溶液中加入1 g氯化钠固体能得到2 g氯化钠溶液
解析:1 L水与1 L酒精混合后的体积应小于2 L,A项错误;镁和稀硫酸反应会生成氢气,故1g镁与1 g稀硫酸充分反应后所得的溶液质量小于2 g,故B项错误;由硫在氧气中燃烧的化学
方程式可知,在该反应中硫与氧气的质量之比为1∶1,所以1 g硫粉在1 g氧气中完全燃烧,两
者恰好完全反应,生成二氧化硫的质量正好为2 g,C项正确;20 ℃,1 g氯化钠饱和溶液中加入
1 g氯化钠固体,氯化钠不再溶解,故氯化钠的质量仍为1 g,所以D项错误。
答案:C
2.钛具有硬度大、密度小、熔点高、抗腐蚀性强等优良性能,被誉为“未来金属”。钛铁矿石的
主要成分是钛酸亚铁(FeTiO),冶炼金属钛时,主要发生以下两个反应:
3
①2FeTiO+6C+7Cl 2X+2TiCl +6CO,②TiCl +2Mg Ti+2MgCl ,则X为( )
3 2 4 4 2
A.FeCl B.FeCl C.Fe O D.FeCO
2 3 2 3 3
解析:在2FeTiO+6C+7Cl 2X+2TiCl +6CO反应中,反应前铁原子是2个,钛原子是2个,
3 2 4
氧原子是6个,碳原子是6个,氯原子是14个,反应后钛原子是2个,氯原子是8个,碳原子是6
个,氧原子是6个,所以①反应方程式中1个“X”分子中含有1个铁原子和3个氯原子,故其化
学式为FeCl 。
3
答案:B
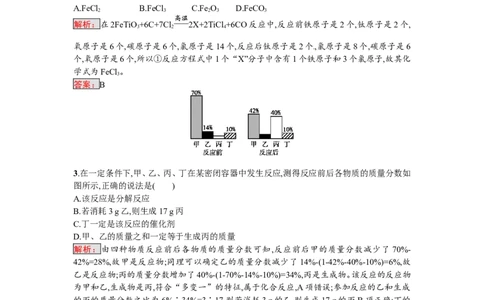
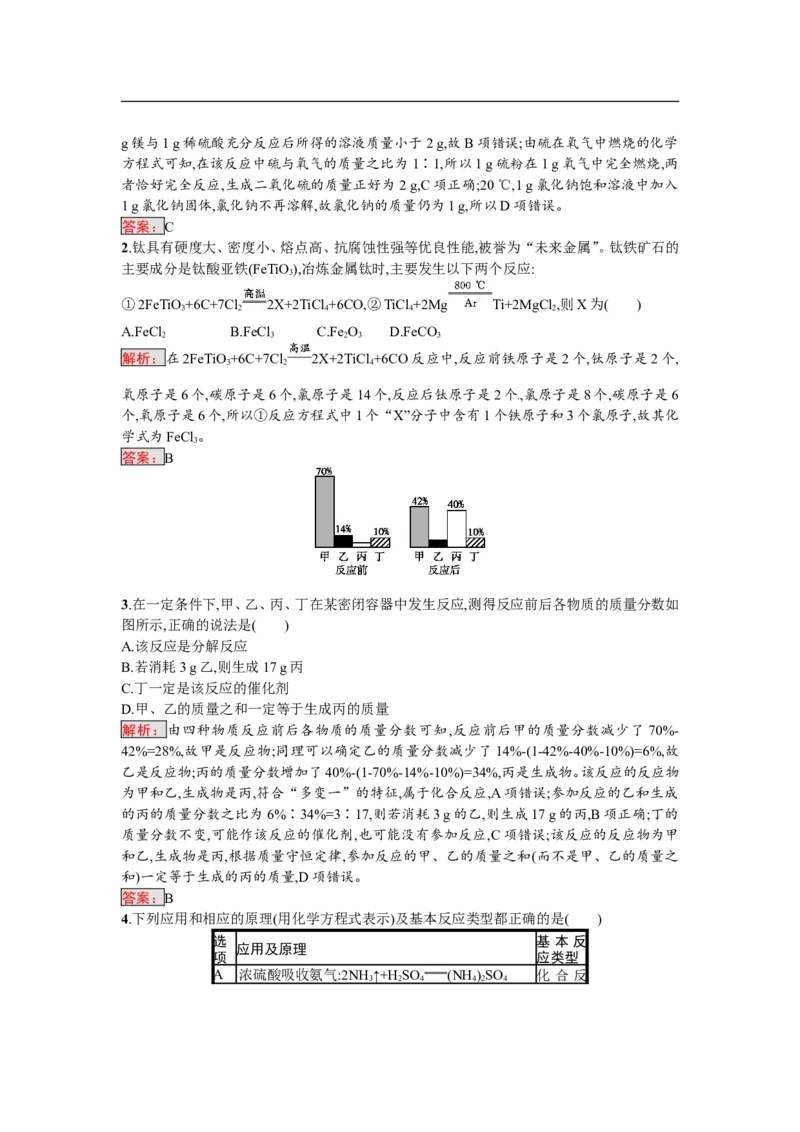
3.在一定条件下,甲、乙、丙、丁在某密闭容器中发生反应,测得反应前后各物质的质量分数如
图所示,正确的说法是( )
A.该反应是分解反应
B.若消耗3 g乙,则生成17 g丙
C.丁一定是该反应的催化剂
D.甲、乙的质量之和一定等于生成丙的质量
解析:由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了 70%-
42%=28%,故甲是反应物;同理可以确定乙的质量分数减少了14%-(1-42%-40%-10%)=6%,故
乙是反应物;丙的质量分数增加了40%-(1-70%-14%-10%)=34%,丙是生成物。该反应的反应物
为甲和乙,生成物是丙,符合“多变一”的特征,属于化合反应,A项错误;参加反应的乙和生成
的丙的质量分数之比为6%∶34%=3∶17,则若消耗3 g的乙,则生成17 g的丙,B项正确;丁的
质量分数不变,可能作该反应的催化剂,也可能没有参加反应,C项错误;该反应的反应物为甲
和乙,生成物是丙,根据质量守恒定律,参加反应的甲、乙的质量之和(而不是甲、乙的质量之
和)一定等于生成的丙的质量,D项错误。
答案:B
4.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
选 基 本 反
应用及原理
项 应类型
A 浓硫酸吸收氨气:2NH↑+H SO (NH )SO 化 合 反
3 2 4 4 2 4应
复 分 解
B 盐酸除铁锈:6HCl+Fe O 2FeCl +3H O
2 3 3 2 反应
氢 氧 化 钠 处 理 工 厂 废 气 中 的 二 氧 化复 分 解
C
硫:2NaOH+SO NaSO +H O 反应
2 2 4 2
化 合 反
D 用熟石灰制生石灰:CaO+H O Ca(OH)
2 2 应
解析:浓硫酸吸收氨气的化学方程式为2NH +H SO (NH )SO ,反应物是两种,生成物是
3 2 4 4 2 4
一种,属于化合反应,但反应物氨气后面不应该加↑,A项错误;氢氧化钠处理工厂废气中的二
氧化硫的化学方程式为2NaOH+SO NaSO +H O,该反应没有相互交换成分,因此不属于
2 2 3 2
复分解反应,C项错误;生石灰是CaO的俗名,而熟石灰是Ca(OH) 的俗名,即可以用生石灰来
2
制熟石灰,D项错误。
答案:B
5.(双选)下列说法正确的是( )
A.等质量的CO和CO 中氧元素的质量比为11∶14
2
B.等质量的Al和Mg分别与足量稀硫酸充分反应,生成H 的质量相等
2
C.等质量的NaHCO 和MgCO 分别与足量稀盐酸充分反应,生成CO 的质量相等
3 3 2
D.等质量的溶质质量分数均为4%氢氧化钠溶液与稀盐酸充分反应后,所得溶液显中性
解析:等质量的CO和CO 中氧元素的质量比= =11∶14;等质量的Al和Mg分别与足量
2
稀硫酸充分反应,生成H 的质量不相等,铝得到的氢气质量大;等质量的NaHCO 和MgCO 分
2 3 3
别与足量稀盐酸充分反应,生成CO 的质量相等,因为二者的相对分子质量相等;等质量的溶
2
质质量分数均为4%氢氧化钠溶液与稀盐酸充分反应,所得溶液显酸性。故选AC。
答案:AC
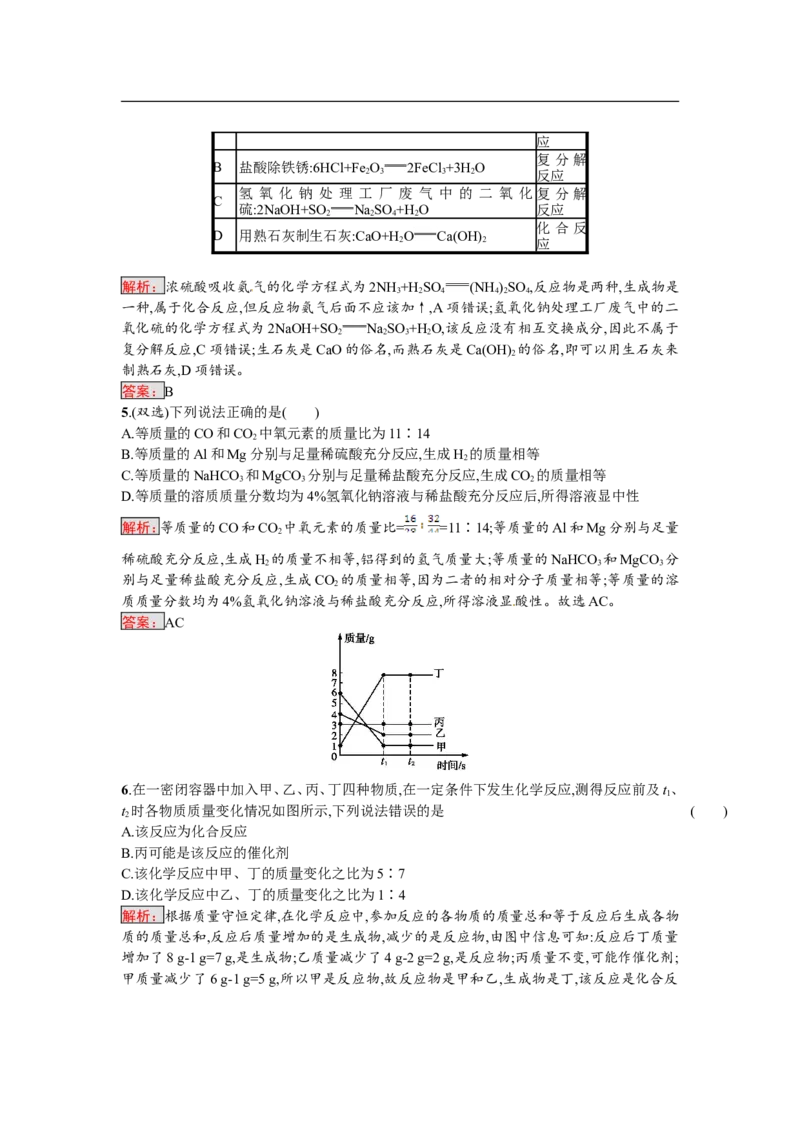
6.在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前及t、
1
t 时各物质质量变化情况如图所示,下列说法错误的是 ( )
2
A.该反应为化合反应
B.丙可能是该反应的催化剂
C.该化学反应中甲、丁的质量变化之比为5∶7
D.该化学反应中乙、丁的质量变化之比为1∶4
解析:根据质量守恒定律,在化学反应中,参加反应的各物质的质量总和等于反应后生成各物
质的质量总和,反应后质量增加的是生成物,减少的是反应物,由图中信息可知:反应后丁质量
增加了8 g-1 g=7 g,是生成物;乙质量减少了4 g-2 g=2 g,是反应物;丙质量不变,可能作催化剂;
甲质量减少了6 g-1 g=5 g,所以甲是反应物,故反应物是甲和乙,生成物是丁,该反应是化合反应。反应中甲、丁的质量变化之比为5∶7;乙、丁的质量变化之比为2∶7,故只有D不正确。
答案:D
7.在宏观、微观和符号之间建立联系是化学学科的特点。
甲、乙、丙、丁表示四种物质,它们的部分化学式和微观示意图分别列于下表。
物
甲 乙 丙 丁
质
化
学
H
2 C
H图例:
[来源:学科网]
O
式 2
微
观
示 [来源:Zxxk.Com]
意
图
(1)请写出丙物质的化学式 ,画出丁物质的微观示意图 。
(2)构成甲物质的粒子是 (填“分子”或“原子”),四种物质中属于氧化物的是
(填化学式)。
(3)甲和乙在一定条件下反应生成丙和丁,所属的基本反应类型为 。若20 g甲与
12 g乙充分反应,可生成丙物质的质量为 g。
解析:(1)由丙的微观示意图可知,一个丙物质的分子中有1个C原子和1个O原子,故其则化
学式为CO,丁物质为氢气,1个氢分子中含有2个氢原子,则微粒的微观示意图为 ;(2)甲物质
为水,丙物质是一氧化碳,它们都属于氧化物;乙是碳,丁是氢气,它们都属于单质;(3)根据题意
可知,水与碳在一定条件下反应生成一氧化碳和氢气,其反应的化学方程式为 C+H O
2
CO+H,该反应是单质和化合物反应生成单质和化合物,故属于置换反应;由反应可
2
知12 g碳和18 g水恰好完全反应,若20 g甲(水)与12 g乙(碳)充分反应,则水有剩余,12 g碳完
全反应。
设生成CO的质量为x,则
C+H O CO+H
2 2
12 28
12 g x
解得x=28 g
答案:(1)CO
(2)分子 HO、CO
2
(3)置换反应 28
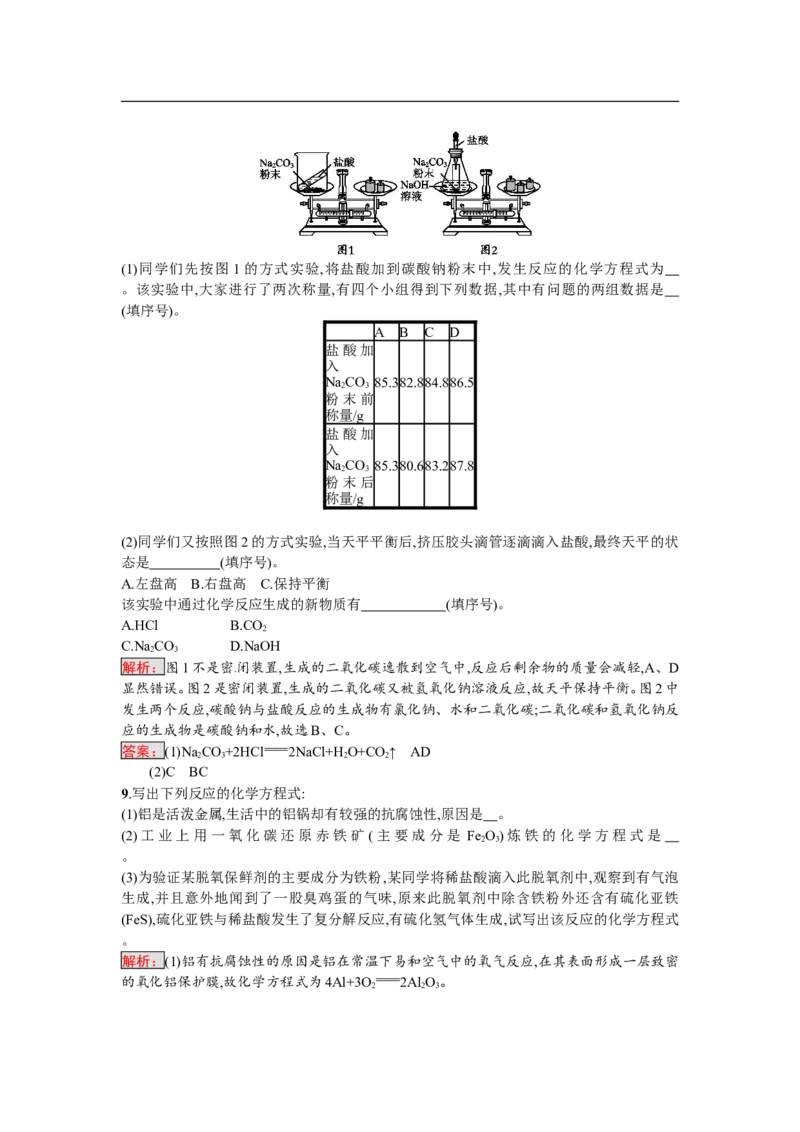
8.某班同学按下图所示的实验探究质量守恒定律。(1)同学们先按图1的方式实验,将盐酸加到碳酸钠粉末中,发生反应的化学方程式为
。该实验中,大家进行了两次称量,有四个小组得到下列数据,其中有问题的两组数据是
(填序号)。
A B C D
盐酸加
入
NaCO 85.382.884.886.5
2 3
粉末前
称量/g
盐酸加
入
NaCO 85.380.683.287.8
2 3
粉末后
称量/g
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴入盐酸,最终天平的状
态是 (填序号)。
A.左盘高 B.右盘高 C.保持平衡
该实验中通过化学反应生成的新物质有 (填序号)。
A.HCl B.CO
2
C.NaCO D.NaOH
2 3
解析:图1不是密闭装置,生成的二氧化碳逸散到空气中,反应后剩余物的质量会减轻,A、D
显然错误。图2是密闭装置,生成的二氧化碳又被氢氧化钠溶液反应,故天平保持平衡。图2中
发生两个反应,碳酸钠与盐酸反应的生成物有氯化钠、水和二氧化碳;二氧化碳和氢氧化钠反
应的生成物是碳酸钠和水,故选B、C。
答案:(1)Na CO+2HCl 2NaCl+H O+CO↑ AD
2 3 2 2
(2)C BC
9.写出下列反应的化学方程式:
(1)铝是活泼金属,生活中的铝锅却有较强的抗腐蚀性,原因是 。
(2)工业上用一氧化碳还原赤铁矿(主要成分是 Fe O)炼铁的化学方程式是
2 3
。
(3)为验证某脱氧保鲜剂的主要成分为铁粉,某同学将稀盐酸滴入此脱氧剂中,观察到有气泡
生成,并且意外地闻到了一股臭鸡蛋的气味,原来此脱氧剂中除含铁粉外还含有硫化亚铁
(FeS),硫化亚铁与稀盐酸发生了复分解反应,有硫化氢气体生成,试写出该反应的化学方程式
。
解析:(1)铝有抗腐蚀性的原因是铝在常温下易和空气中的氧气反应,在其表面形成一层致密
的氧化铝保护膜,故化学方程式为4Al+3O 2Al O。
2 2 3(2)赤铁矿的主要成分是Fe O,炼铁的化学方程式是3CO+Fe O 2Fe+3CO 。
2 3 2 3 2
(3)硫化亚铁与稀盐酸发生复分解反应,根据其交换成分的特点,可知产物为FeCl 和HS,
2 2
且由题意知硫化氢为气体,故化学方程式为2HCl+FeS FeCl +H S↑。
2 2
答案:(1)4Al+3O 2Al O
2 2 3
(2)3CO+Fe O 2Fe+3CO
2 3 2
(3)FeS+2HCl FeCl +H S↑
2 2
10.将一定质量的金属锌投入63.7 g稀硫酸中,恰好完全反应,放出气体的质量与反应时间的
关系如图所示。试求(计算结果精确到0.1%):
(1)完全反应后生成氢气的质量为 g;
(2)反应结束后所得溶液的溶质质量分数。(写出计算过程)
解析:(1)根据图中数据可以判断完全反应后生成氢气的质量;(2)根据氢气的质量可以计算反
应生成硫酸锌的质量,反应的锌的质量,进一步可以计算反应结束后所得溶液的溶质的质量
分数。
答案:(1)0.2
(2)解:设反应的锌的质量为x,生成的硫酸锌的质量为y。
Zn+H SO ZnSO+H ↑
2 4 4 2
65 161 2
x y 0.2 g
解得x=6.5 g
解得y=16.1 g
反应结束后所得溶液的质量为6.5 g+63.7 g-0.2 g=70.0 g,
反应结束后所得溶液的溶质质量分数为 ×100%=23.0%
答:反应结束后所得溶液的溶质质量分数为23.0%。
11.某碳酸钠样品中含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配制成100 g溶
液,将其全部加入到100 g一定质量分数的HSO 溶液中,恰好完全反应,生成的气体全部逸出
2 4
后,所得溶液质量是195.6 g,将溶液蒸干,得到15.6 g硫酸钠。计算:
(1)加入的HSO 溶液的溶质质量分数;
2 4
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
答案:解:根据质量守恒定律知,生成二氧化碳的质量为100 g+100 g-195.6 g=4.4 g
设样品中NaCO 的质量为x,反应的硫酸质量为y,生成NaSO 的质量为z。
2 3 2 4NaCO+H SO NaSO +H O+CO↑
2 3 2 4 2 4 2 2
106 98 142 44
x y z 4.4 g
列比例式得:
解得:x=10.6 g,y=9.8 g,z=14.2 g。
HSO 溶液中溶质的质量分数: ×100%=9.8%。
2 4
原样品的质量为10.6 g+(15.6 g-14.2 g)=12 g,
原样品中碳酸钠的质量分数为 ×100%=88.3%。
答:(1)加入的HSO 溶液的溶质质量分数为9.8%;
2 4
(2)原碳酸钠样品中碳酸钠的质量分数为88.3%。