文档内容
第十一单元 盐 化肥
知能优化训练
中考回顾
1.(2017重庆中考B卷)氯化铵(NH Cl)是“侯氏制碱法”的一种副产品。已知氯化铵的水溶
4
液呈酸性,下列关于氯化铵的说法正确的是( )
A.氯化铵属于酸
B.氯化铵是一种复合肥
C.氯化铵与熟石灰混合使用可提高肥效
D.氯化铵溶液与硝酸银溶液混合会产生白色沉淀
[来源:学科网]
答案:D
2.(2017湖南邵阳中考)在“粗盐难溶性杂质的去除”实验中,操作步骤为溶解、过滤、蒸发、
计算产率。下列各步骤中的一些做法正确的是( )
A.溶解:用玻璃棒搅拌以加速溶解
B.过滤:直接将粗盐水倒入漏斗中
C.蒸发:等蒸发皿中水分蒸干便停止加热
D.计算产率:将精盐直接转移到天平的托盘上称量
答案:A
3.(2017南京中考)下列各组离子在水中能大量共存的是 ( )
A.Cu2+、Na+、Cl-、OH- B.H+、K+、N 、S
C.Na+、N 、N 、OH- D.Ag+、Ba2+、N 、Cl-
答案:B
4.(2017广州中考)下列物质的性质和用途表述没有直接联系的是( )
选
性质 用途
项
活性炭有吸附脱色制白
A
性 糖
小苏打能与盐治疗胃酸
B
酸反应 过多
碳酸氢铵受热
C 作化肥
易分解
CO 具有还原
D 工业炼铁
性
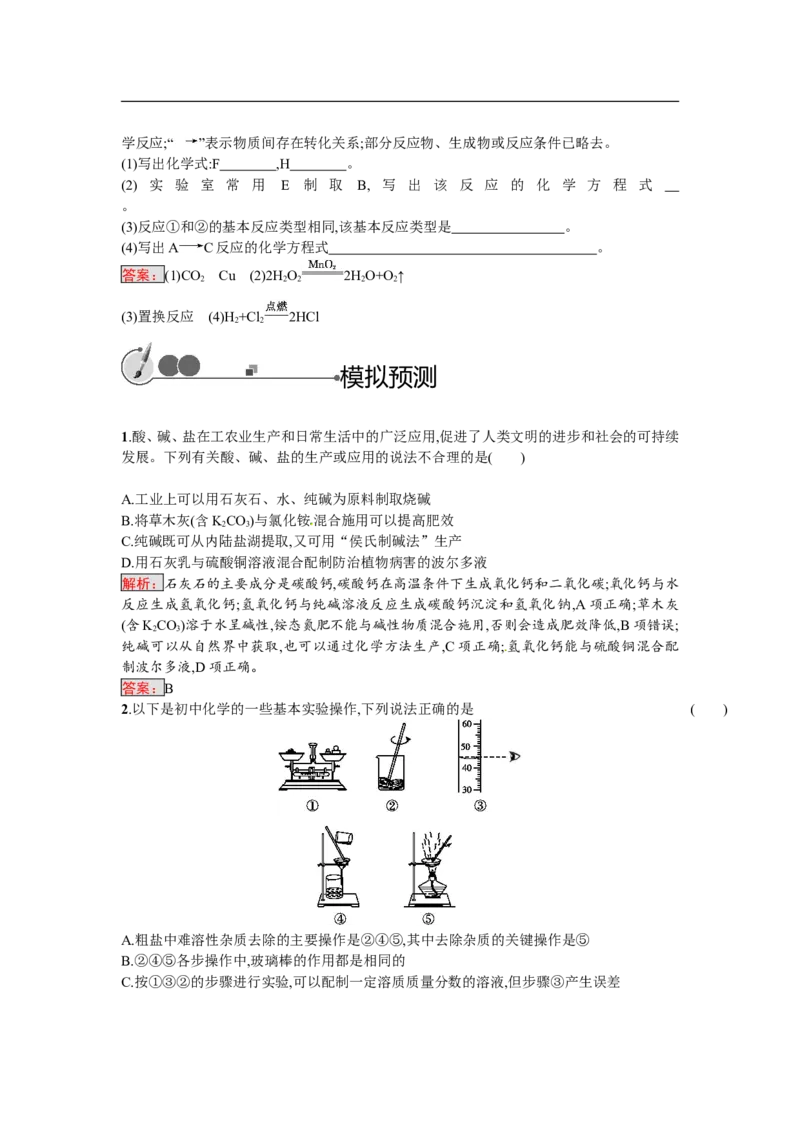
答案:C5.(2017山东青岛中考)为除去粗盐中含有的氯化镁、硫酸钠、氯化钙等杂质,应加入过量的氢
氧化钠、氯化钡、碳酸钠等物质,将杂质转化为沉淀。过滤去除沉淀后,再向滤液中加入适量的
盐酸得到精盐水。实验操作过程如图所示:
下列说法错误的是( )
A.实验操作步骤也可以是①③④②⑤⑥
B.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
C.在实验操作过程中,氯化钡和碳酸钠溶液的添加顺序可以颠倒
D.操作⑤得到的沉淀中共有四种物质
答案:C
6.(2017呼和浩特中考)某工厂排出的废水中,可能含有AgNO、Ba(NO )、FeCl 、Cu(NO )、
3 3 2 2 3 2
NaSO 中的几种物质。某化学兴趣小组做如下实验,探究工厂废水中含有的物质并设计实验
2 4
方案处理废水。
【查阅资料】①白色的Fe(OH) 沉淀在潮湿空气中迅速转化为红褐色Fe(OH) ;
2 3
②Ba的金属活动性比Fe强。
(1)取少量废水,加入过量稀盐酸,产生白色沉淀,沉淀化学式为 ;过滤,将滤液分成两份,
一 份 加 入 稀 硫 酸 , 产 生 白 色 沉 淀 , 反 应 的 化 学 方 程 式 为
;另一份加入过量氢氧化钠溶液,产生蓝色沉淀,该过程中与OH-反应的离子有 (写离
子符号)。
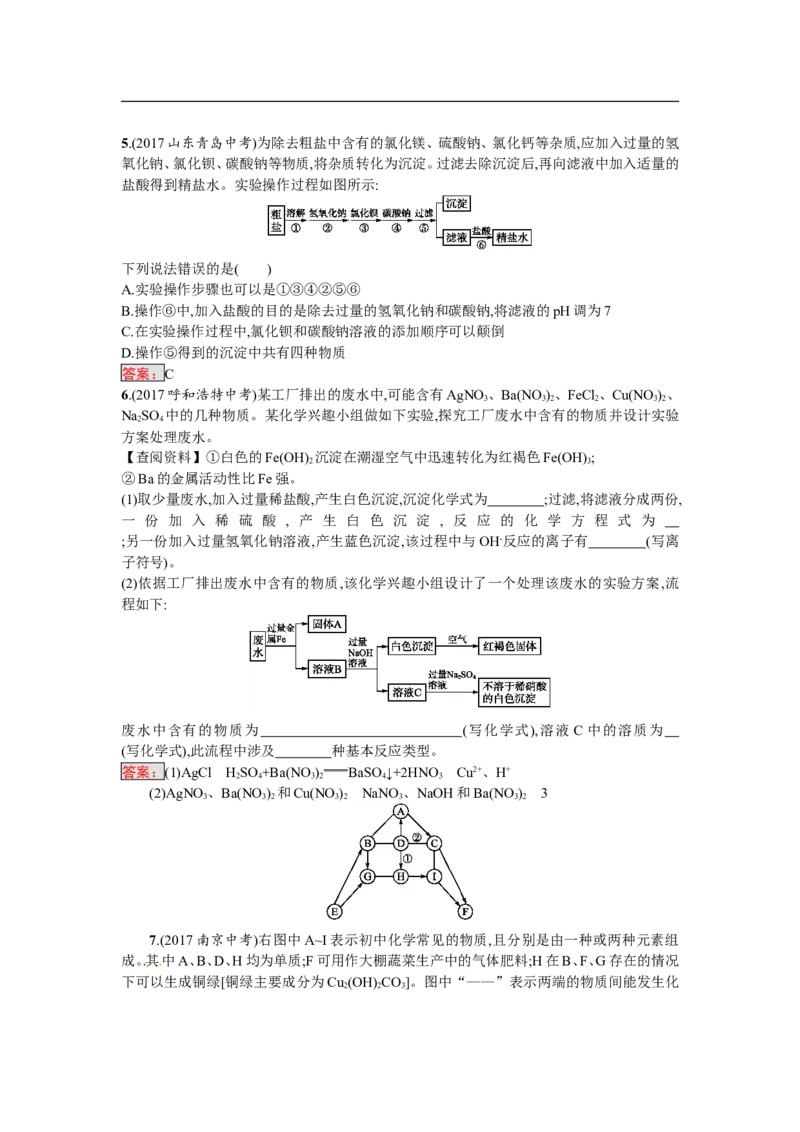
(2)依据工厂排出废水中含有的物质,该化学兴趣小组设计了一个处理该废水的实验方案,流
程如下:
废水中含有的物质为 (写化学式),溶液 C 中的溶质为
(写化学式),此流程中涉及 种基本反应类型。
答案:(1)AgCl HSO +Ba(NO) BaSO↓+2HNO Cu2+、H+
2 4 3 2 4 3
(2)AgNO、Ba(NO ) 和Cu(NO ) NaNO 、NaOH和Ba(NO ) 3
3 3 2 3 2 3 3 2
7.(2017南京中考)右图中A~I表示初中化学常见的物质,且分别是由一种或两种元素组
成。其中A、B、D、H均为单质;F可用作大棚蔬菜生产中的气体肥料;H在B、F、G存在的情况
下可以生成铜绿[铜绿主要成分为Cu (OH) CO]。图中“——”表示两端的物质间能发生化
2 2 3学反应;“ ”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)写出化学式:F ,H 。
(2) 实 验 室 常 用 E 制 取 B, 写 出 该 反 应 的 化 学 方 程 式
。
(3)反应①和②的基本反应类型相同,该基本反应类型是 。
(4)写出A C反应的化学方程式 。
答案:(1)CO Cu (2)2H O 2HO+O↑
2 2 2 2 2
(3)置换反应 (4)H +Cl 2HCl
2 2
模拟预测
1.酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续
发展。下列有关酸、碱、盐的生产或应用的说法不合理的是( )
A.工业上可以用石灰石、水、纯碱为原料制取烧碱
B.将草木灰(含KCO)与氯化铵混合施用可以提高肥效
2 3
C.纯碱既可从内陆盐湖提取,又可用“侯氏制碱法”生产
[来源:学|科|网]
D.用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液
解析:石灰石的主要成分是碳酸钙,碳酸钙在高温条件下生成氧化钙和二氧化碳;氧化钙与水
反应生成氢氧化钙;氢氧化钙与纯碱溶液反应生成碳酸钙沉淀和氢氧化钠,A项正确;草木灰
(含KCO)溶于水呈碱性,铵态氮肥不能与碱性物质混合施用,否则会造成肥效降低,B项错误;
2 3
纯碱可以从自然界中获取,也可以通过化学方法生产,C项正确;氢氧化钙能与硫酸铜混合配
制波尔多液,D项正确。
答案:B
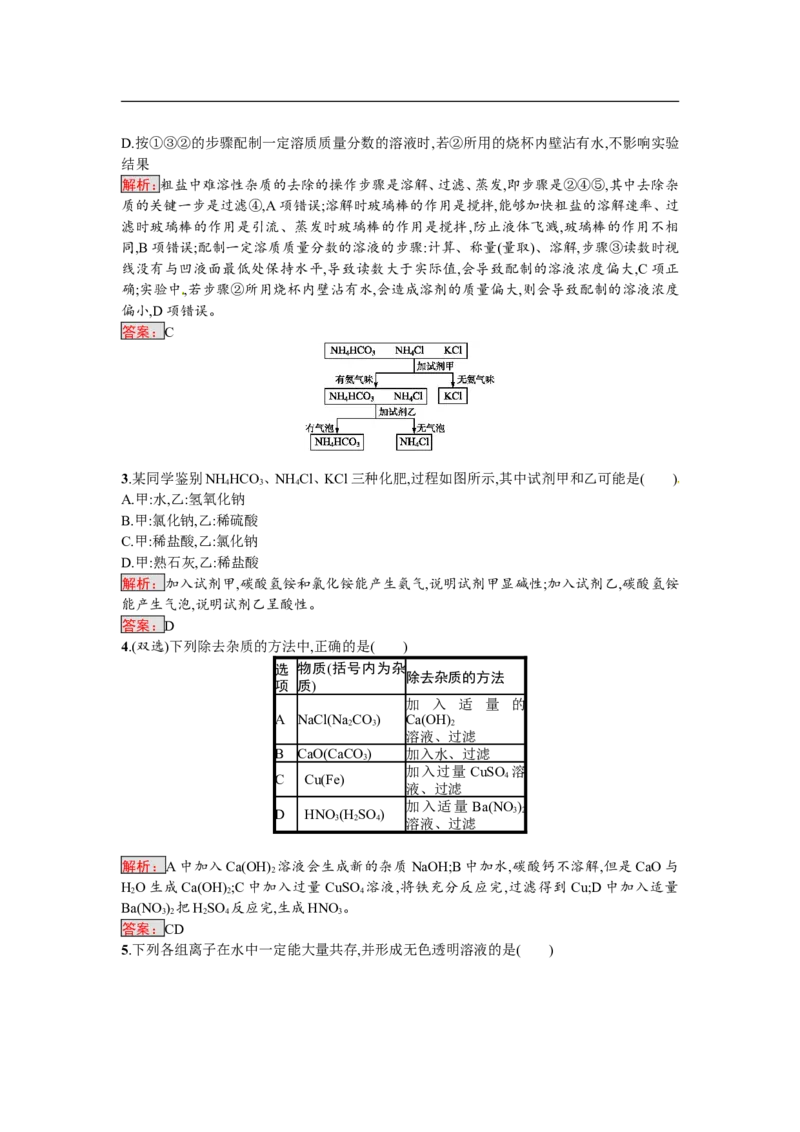
2.以下是初中化学的一些基本实验操作,下列说法正确的是 ( )
A.粗盐中难溶性杂质去除的主要操作是②④⑤,其中去除杂质的关键操作是⑤
B.②④⑤各步操作中,玻璃棒的作用都是相同的
C.按①③②的步骤进行实验,可以配制一定溶质质量分数的溶液,但步骤③产生误差D.按①③②的步骤配制一定溶质质量分数的溶液时,若②所用的烧杯内壁沾有水,不影响实验
结果
解析:粗盐中难溶性杂质的去除的操作步骤是溶解、过滤、蒸发,即步骤是②④⑤,其中去除杂
质的关键一步是过滤④,A项错误;溶解时玻璃棒的作用是搅拌,能够加快粗盐的溶解速率、过
滤时玻璃棒的作用是引流、蒸发时玻璃棒的作用是搅拌,防止液体飞溅,玻璃棒的作用不相
同,B项错误;配制一定溶质质量分数的溶液的步骤:计算、称量(量取)、溶解,步骤③读数时视
线没有与凹液面最低处保持水平,导致读数大于实际值,会导致配制的溶液浓度偏大,C项正
确;实验中,若步骤②所用烧杯内壁沾有水,会造成溶剂的质量偏大,则会导致配制的溶液浓度
偏小,D项错误。
答案:C
3.某同学鉴别NH HCO 、NH Cl、KCl三种化肥,过程如图所示,其中试剂甲和乙可能是( )
4 3 4
A.甲:水,乙:氢氧化钠
B.甲:氯化钠,乙:稀硫酸
C.甲:稀盐酸,乙:氯化钠
D.甲:熟石灰,乙:稀盐酸
解析:加入试剂甲,碳酸氢铵和氯化铵能产生氨气,说明试剂甲显碱性;加入试剂乙,碳酸氢铵
能产生气泡,说明试剂乙呈酸性。
答案:D
4.(双选)下列除去杂质的方法中,正确的是( )
选 物质(括号内为杂
除去杂质的方法
项 质)
加 入 适 量 的
A NaCl(Na CO) Ca(OH)
2 3 2
溶液、过滤
B CaO(CaCO) 加入水、过滤
3
加入过量 CuSO 溶
C Cu(Fe) 4
液、过滤
加入适量 Ba(NO )
D HNO(H SO ) 3 2
3 2 4 溶液、过滤
解析:A中加入Ca(OH) 溶液会生成新的杂质NaOH;B中加水,碳酸钙不溶解,但是CaO与
2
HO生成Ca(OH) ;C中加入过量CuSO 溶液,将铁充分反应完,过滤得到Cu;D中加入适量
2 2 4
Ba(NO ) 把HSO 反应完,生成HNO。
3 2 2 4 3
答案:CD
5.下列各组离子在水中一定能大量共存,并形成无色透明溶液的是( )A.H+、Cl-、HC B.Ca2+、C 、Cl-
C.K+、OH-、Na+ D.Cu2+、S 、Na+
解析:H+、HC 会生成二氧化碳气体和水,不能共存,A项错误;Ca2+、C 会反应产生碳酸钙沉
淀,不能共存,B项错误;三种离子间不能结合成沉淀、气体或水,能大量共存,且不存在有色离
子,C项正确;铜离子溶于水为蓝色,D项错误。
答案:C
6.右图表示初中化学常见物质的相互转化关系(反应条件已省略)。下列说法错误的是 ( )
A.圈Ⅰ中发生的反应可能都是分解反应
B.利用反应②可检验二氧化碳气体
C.圈Ⅱ中的化学反应说明氧气具有可燃性
D.利用反应①可制得烧碱
解析:
正
解释
误
A √ 圈Ⅰ中2HO 2H↑+O ↑、2HO 2HO+O↑都是分解反应
2 2 2 2 2 2 2
二氧化碳与澄清石灰水反应生成碳酸钙白色沉淀是二氧化碳的特性,故
B √
用澄清石灰水来检验二氧化碳气体
C × 圈Ⅱ中的化学反应说明氧气支持燃烧,具有助燃性,但不具有可燃性
D √ Ca(OH) 与NaCO 反应生成NaOH,故可以利用①制得烧碱
2 2 3
答案:C
7.有甲、乙、丙、丁四种无色溶液,它们分别是HCl、HSO 、BaCl 、NaCO 溶液中的一种。为区
2 4 2 2 3
别这四种溶液,现将它们两两混合并得到下面现象,则甲、乙、丙、丁分别是( )
溶 甲 乙 丙 甲
液 +乙 +丙+丁+丁
白 白 无
无明
现 色 色 色
显
象 沉 沉 气
现象
淀 淀 体
A.HCl、BaCl 、HSO 、NaCO
2 2 4 2 3
B.HSO 、HCl、BaCl 、NaCO
2 4 2 2 3
C.HCl、HSO 、BaCl 、NaCO
2 4 2 2 3
D.HSO 、NaCO、HCl、BaCl
2 4 2 3 2解析:四物质中只有BaCl 与HSO 和NaCO 会生成白色沉淀,因此丙为BaCl ,则乙和丁分
2 2 4 2 3 2
别是HSO 、NaCO 中的一种,故甲是HCl。HCl分别与HSO 、NaCO 混合,产生的现象分别
2 4 2 3 2 4 2 3
为无明显现象和无色气体,故乙是HSO ,丁是NaCO。
2 4 2 3
答案:C
8.我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:
(1)反应①的化学方程式为 ,反应②的基本反应类型为 。
(2)工业上用分离液态空气的方法制取氮气,属于 (填“物理”或“化学”)变化。
(3)操作a的名称是 ,实验室进行此操作时所需的玻璃仪器有烧杯、玻璃棒、 。
(4)写出NH Cl的一种用途: 。
4
解析:(1)由图示信息可知,碳酸钙在高温下反应生成氧化钙和二氧化碳;反应②是NaHCO 受
3
热分解生成纯碱、CO 和HO,符合“一变多”的特点,故属于分解反应;(2)工业上利用氮气、
2 2
氧气沸点不同,分离液态空气制取氮气,该过程中没有新物质生成,故属于物理变化;(3)操作a
是将碳酸氢钠固体和氯化铵溶液分离,故采用过滤的方法;实验室进行此操作时所需的玻璃仪
器有烧杯、玻璃棒、漏斗;(4)NH Cl含有农作物生长需要的氮元素,故可以用作氮肥。
4
答案:(1)CaCO CaO+CO ↑ 分解反应 (2)物理
3 2
(3)过滤 漏斗 (4)可以用作氮肥
9.小煜通过学习知道:Na CO、NaHCO 均能与盐酸反应,Na CO 溶液还会与石灰水反应。
2 3 3 2 3
【产生疑问】NaHCO 溶液也能与石灰水发生反应吗?如果能反应,生成物可能是什么?
3
【进行实验】小煜将NaHCO 溶液与石灰水混合,结果产生白色沉淀,已知Ca(HCO ) 能溶于水,
3 3 2
碳酸氢盐在碱溶液中会生成碳酸盐。此白色沉淀是 ,证明NaHCO 溶液与
3
Ca(OH) 溶液也能发生反应。为了进一步了解生成的含钠化合物有什么,继续探究:
2
【作出猜想】①只有NaOH ②有NaCO 和NaOH ③
2 3
【实验设计】步骤1:取少量上述实验后的上层清液于试管中,再滴加足量的CaCl 溶液(中性),
2
观察到产生白色沉淀,由此可知生成的含钠化合物一定含有 ;
[来源:Z.xx.k.Com]
步骤2:将步骤1中反应后的混合物过滤,往滤液中先滴加几滴酚酞溶液,再滴加足量的稀盐酸,
观察到溶液颜色变化情况为 ,整个实验过程中无气泡产生,由此
可知猜想②成立。
【拓展提高】若步骤1中未出现白色沉淀,则此时NaHCO 溶液与Ca(OH) 溶液反应的化学方
3 2
程式为
。
解析:对生成的含钠化合物进行猜想有三种情况:只有NaOH,只有NaCO 和NaCO、NaOH
2 3 2 3
的混合物;向滤液中加入足量的CaCl 溶液有白色沉淀产生,说明生成的含钠化合物一定有
2
NaCO,再取滤液滴加酚酞溶液和稀盐酸,观察到溶液由无色变为红色,再由红色变无色,说明
2 3
有NaOH和NaCO;步骤1未出现白色沉淀,故无NaCO 生成,而生成CaCO 、NaOH和HO。
2 3 2 3 3 2答案:【进行实验】CaCO (或碳酸钙)
3
【作出猜想】只有NaCO
2 3
【实验设计】NaCO 溶液先由无色变红色,然后由红色变无色
2 3
【拓展提高】Ca(OH) +NaHCO CaCO ↓+NaOH+HO
2 3 3 2
10.某复合肥的部分说明书如图所示。请回答:
(1)从肥效的角度看,共有 种有效元素。
(2)该复合肥的有效成分之一是尿素[CO(NH)],则尿素中碳、氧、氮、氢的原子个数比为 。
2 2
(3)一袋该化肥至少含PO kg。
2 5
(4)从“注意事项”看,该复合肥料的物理性质是 ,化学性质是
。(各写一种)
解析:(1)从肥效的角度看,共有氮、磷、钾三种有效元素。
(2)1个尿素分子是由1个碳原子、1个氧原子、2个氮原子和4个氢原子构成的,则碳、氧、
氮、氢四种原子个数比为1∶1∶2∶4。
(3)一袋该化肥至少含PO 的质量为50 kg×25%× =2.5 kg。
2 5
(4)从“注意事项”看,该复合肥料的物理性质是易潮解,化学性质是受热易分解。
答案:(1)3 (2)1∶1∶2∶4 (3)2.5 (4)易潮解 受热易分解
11.某固体物质可能含有NaSO 、NaCO、CaCl 、CuSO 、KCl和KOH中的一种或几种。为探
2 4 2 3 2 4
究其组成,进行如下实验,流程和现象记录如下:
【资料】CaCl 、BaCl 、KCl三种溶液均呈中性。
2 2
(1)依据步骤①的实验现象得出固体物质中一定不含 (填化学式)。
(2)步骤②中发生反应的化学方程式为
。
(3)根据上述实验得出固体物质中一定含有 (填化学式,下同),可能含有 。
为进一步确定可能含有的物质,采用的方法是
(写出实验的操作、现象和结论)。
答案:(1)CuSO (2)Na CO+BaCl BaCO ↓+2NaCl (3)Na CO、KOH KCl 取少量无
4 2 3 2 3 2 3色溶液A于试管中,加入足量的稀硝酸,然后滴加硝酸银溶液,若产生白色沉淀,则固体中一定
含有KCl,否则不含KCl
12.尿素[CO(NH)]是氮肥中最主要的一种,其含氮量高,在土壤中不残留任何有害物质,长期
2 2
施用没有不良影响。计算:
(1)CO(NH) 中共含有 (写数字)种元素;
2 2
(2)CO(NH) 的相对分子质量是 ;
2 2
(3)若CO(NH) 中含有3 g氮元素,则该CO(NH) 的质量为 g(计算结果精确到
2 2 2 2
0.1 g)。
答案:(1)4 (2)60 (3)6.4