文档内容
阶段检测二 物质构成的奥秘 自然界的水
化学方程式
(时间:90分钟 满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 K 39 Mn 55
一、选择题(每小题只有一个选项符合题意,每小题3分,共45分)
1.下列有关分子、原子和离子的说法正确的是( )
A.保持氮气化学性质的粒子是氮原子
B.原子的质子数决定原子的化学性质
C.氯化钠是由离子构成的化合物
D.原子可以构成分子,但不可形成离子
解析:氮气是由氮分子构成的,所以保持氮气化学性质的粒子是氮分子,故A错误;原子的化
学性质主要取决于原子最外层的电子数,故B错误;原子可以构成分子,同样原子得失电子后
可以形成离子,故D错误。
答案:C
2.下列粒子可以通过得到电子变成原子的是( )
A.Cl B.O2- C. +12 D. +9
解析:A.Cl表示氯原子,既不需要得电子,也不需要失电子;B.O2-需要失去两个电子变成原
子;C.图中表示的是镁离子,需要得到两个电子变成原子;D.图中表示的是氟原子,既不需要得
电子,也不需要失电子。
答案:C
3.对下列事实的微观解释错误的是( )
选
事实 解释
项
两种物质的分子构成不
A 一氧化碳有毒而二氧化碳无毒
同
受热情况下,分子运动速
B 品红在热水中扩散速度更快
率加快
盐酸、稀硫酸都能使紫色石蕊溶
C 两种溶液中都含有H+
液变红
受热时原子间的间隔增
D 温度计中的酒精受热膨胀
大
解析:温度计中的酒精受热膨胀是由于酒精受热分子间的间隔增大。
答案:D
[来源:Z_xx_k.Com]
4.钛和钛合金被认为是21世纪的重要金属材料,它们具有熔点高、密度小、抗腐蚀性能好等
优良性能,被广泛用于火箭、航天飞机、船舶和化工等。如图是钛元素在元素周期表中的相关信息及其原子结构示意图。下列说法正确的是( )
+22
[来源:学,科,网Z,X,X,K]
A.钛元素的相对原子质量为47.87 g
B.钛合金可做保险丝
C.钛元素原子在化学反应中易失电子
D.钛原子核内有22个中子
解析:根据元素周期表中的相关信息,可知该元素的相对原子质量为47.87,相对原子质量单
位是“1”,不是“g”,A项错误;钛合金不能做保险丝,因为它的熔点高,B项错误;根据钛元素在
元素周期表中的相关信息可知,钛元素的原子序数为22,相对原子质量为47.87约为48,根据
原子序数=核电荷数=质子数,则该元素的原子核内质子数为22,又根据相对原子质量=质子数
+中子数可知,中子数=相对原子质量-质子数,故中子数=48-22=26,D项错误。
答案:C
5.稀土元素铕(Eu)是激光及原子能应用的重要材料。已知氯化铕的化学式为EuCl,则氧化铕
3
的化学式为( )
A.EuO B.EuO
2 3
C.EuO D.EuO
3 2 3
解析:氯化铕的化学式为EuCl,氯元素显-1价,设铕元素的化合价是x,根据在化合物中,所含
3
元素正负化合价代数和为零,可得:x+(-1)×3=0,则x=+3。氧化铕中铕元素显+3价,氧元素显-2
价,故其化学式为EuO。
2 3
答案:B
6.尼古丁(C H N)会使人上瘾或产生依赖性(最难戒除的毒瘾之一),大剂量的尼古丁会引起
10 14 2
呕吐以及恶心,严重时人会死亡。下列有关C H N 的说法正确的是( )
10 14 2
A.尼古丁是由C、H、N三种元素构成的
B.尼古丁由26个原子构成
C.尼古丁由10个碳原子、14个氢原子、2个氮原子构成
D.尼古丁中氢元素的含量最低
[来源:学&科&网]
解析:尼古丁是由C、H、N三种元素组成的,不是构成的,A项错误;C H N 是由尼古丁分子
10 14 2
构成的,B项错误;1个尼古丁分子由10个碳原子、14个氢原子、2个氮原子构成,C项错误;尼
古丁中碳原子的相对原子质量之和为12×10=120,氢原子的相对原子质量之和为1×14=14,氮
原子的相对原子质量之和为14×2=28,氢元素的相对原子质量之和最小,则氢元素的质量分数
最小,D项正确。
答案:D
7.物质的化学式和相应的名称均正确的是( )
A.O 氧气
3
B.MgCl 氯化镁
2
C.OFe 氧化铁
4 3D.Fe(OH) 氢氧化铁
2
答案:B
8.甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如下:
根据以上微观示意图得出的结论中,正确的是( )
A.水煤气的成分是一氧化碳和氧气
B.反应中含氢元素的化合物有三种
C.反应前后碳元素的化合价没有发生变化
D.反应中甲和丙的质量之比为4∶7
解析:据图可以看出,该反应是甲烷与水在一定条件下反应生成氢气和一氧化碳,该反应的化
学方程式为CH+H O CO+3H 。水煤气的成分是一氧化碳和氢气的混合气体,故A
4 2 2
错误;反应中含有氢元素的化合物是甲烷和水,是两种,故B错误;反应前甲烷中碳元素的化合
价是-4价,反应后一氧化碳中碳元素的化合价是+2价,碳元素的化合价发生了改变,故C错误;
反应中甲烷和一氧化碳的质量比为16∶28=4∶7,故D正确。
答案:D
9.下列各组物质,按单质、化合物、混合物顺序排列的是 ( )
A.氢气、干冰、冰水共存物
B.天然气、煤、石油
C.液态氧、二氧化硫、生铁
D.稀有气体、酒精、碳酸钙
解析:氢气属于单质,干冰、冰水共存物都属于化合物,A项错误;天然气、煤、石油都属于混合
物,B项错误;稀有气体属于混合物,酒精、碳酸钙属于化合物,D项错误。
答案:C
10.在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基
本类型的关系如图所示,下列示例中错误的是( )
A.阴影1:C+O CO
2 2
B.阴影2:2H O 2H↑+O ↑
2 2 2
C.阴影3:Mg(OH) +2HCl MgCl +2H O
2 2 2
D.阴影4:Fe+CuSO FeSO +Cu
4 4
解析:由Mg(OH) +2HCl MgCl +2H O知各元素化合价均无变化,故它不是氧化还原反应。
2 2 2
答案:C11.下列化学方程式与事实相符且正确的是( )
A.治疗胃酸过多:Mg(OH) +H SO MgSO +2H O
2 2 4 4 2
B.用铁和硫酸铜溶液反应制备铜:Fe+CuSO Cu+FeSO
4 4
C.用一氧化碳还原氧化铁炼铁:Fe O+CO 2Fe+CO
2 3 2
D.洗去试管壁上附着的铜:Cu+H SO CuSO +H ↑
2 4 4 2 [来源:学科网]
解析:胃酸是盐酸,而不是硫酸;一氧化碳还原氧化铁的化学方程式没有配平;铜排在金属活动
性顺序中氢的后面,不能与稀硫酸反应。
答案:B
12.下列叙述正确的是( )
A.酸、碱、盐之间都能发生复分解反应
B.金属单质都能与酸溶液发生置换反应,生成盐和氢气
C.20 ℃时,氯化钠的溶解度是36 g,此时溶液的溶质质量分数为36%
D.质量守恒定律是物质发生化学变化所遵循的基本定律
解析:酸、碱、盐之间发生复分解反应需要一定的条件,即生成物中有气体、水或沉淀,因此酸、
碱、盐之间不一定都能发生复分解反应,故A错误;在金属活动性顺序中,通常排在氢前面的金
属能与酸溶液发生置换反应,生成盐和氢气,故B错误;20 ℃时,氯化钠的溶解度是36 g,由于不
知溶液是否饱和,故无法计算溶液的溶质质量分数,故C错误。
答案:D
13.在反应X+2Y R+2M中,已知R和M的相对分子质量之比为22∶9,当1.6 g X与Y完
全反应后,生成4.4 g R,则在此反应中Y和M的质量比是( )
A.16∶9 B.23∶9
C.32∶9 D.46∶9
解析:在反应X+2Y R+2M中,当1.6 g X与Y完全反应后,生成4.4 g R,且反应生成R和M
的质量比为11∶9,则生成M的质量为4.4 g× =3.6 g;由质量守恒定律,则参加反应的Y的质
量为4.4 g+3.6 g-1.6 g=6.4 g,则在此反应中Y和M的质量之比为6.4 g∶3.6 g=16∶9,故选A。
答案:A
14.今有四种粒子的结构示意图,下列说法正确的是( )
① +8 ② +12 ③ +11 ④ +12
A.它们表示四种元素
B.②表示的阳离子
C.④表示的元素是金属元素
D.①④表示的是阳离子解析:不同种元素最本质的区别是质子数不同,②和④核内质子数相同,属于同一种元素,图中
共表示3种元素,A项错误;在②中核内质子数=核外电子数=12,为镁原子,B项错误;粒子④的
质子数是12,属于镁元素,是金属元素,C项正确;粒子①质子数=8,核外电子数=10,质子数<核
外电子数,为阴离子,D项错误。
答案:C
15.如图是实验室制取氧气时,各物质的质量随加热时间的变化关系,下列叙述正确的是( )
A.①表示反应物高锰酸钾
B.②表示催化剂
C.③表示生成物氧气
D.④表示反应物氯酸钾
解析:由图像可知,反应后,②③的质量增加,故②③是生成物;①的质量减少,故①是反应物;④
的质量不变,可能是催化剂,也可能不参加反应。
高锰酸钾分解生成三种物质,由以上分析可知,生成物是两种,故①表示反应物氯酸钾,A
错误;由以上分析可知,②表示生成物,故B错误;氯酸钾分解时生成的氧气的质量小于氯化钾
的质量,故③表示氧气的质量,C正确;④的质量不变,不可能是反应物,可能是催化剂,故D错误。
答案:C
二、填空题(本题包括5个小题,共23分)
16.(7分)请按要求填空:
(1)请写出相应的化学符号或名称:
①2个硫原子 ;②+2价的镁元素 ;③2Cl- ;④HO 。
2 2
(2)请从H、C、O、Na 4种元素中选择恰当的元素,组成符合下列要求的物质,并将其化学式填
写在相应的空格上:
①能燃烧的固态非金属单质是 ;
②一种有毒的气态氧化物,可用于炼铁的是 ;
③三种元素组成的盐,其溶液呈碱性,还可以作洗涤剂的是 ;
④参与植物的光合作用,可以作农作物气体肥料的是 ;
⑤最简单的有机物,是天然气的主要成分 。
答案:(1)①2S ② g ③2个氯离子 ④过氧化氢 (2)①C ②CO ③NaCO ④CO
2 3 2
⑤CH
4
17.(3分)生活离不开水,净化水的知识在日常生活中有着广泛的应用。
(1)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是
。
(2)自制净水器中常加入 ,用于除去水中的异味和色素。(3)自来水厂用二氧化氯消毒杀菌,二氧化氯的化学式为 。
解析:(1)茶杯内的纱网,可将茶叶与茶水分离,该设计利用的化学原理是过滤;(2)活性炭可吸
附异味和色素等,所以可用于自制净水器中;(3)1个二氧化氯分子是由1个氯原子和2个氧原
子构成的,故其化学式为ClO 。
2
答案:(1)过滤
(2)活性炭
(3)ClO
2
18.(5分)下图为六种常见元素的原子结构示意图,依据图中信息回答下列问题:
H N F Na Al Cl
(1)上述六种元素中属于金属元素的是 (填元素名称),己元素的化学性质与以上
(填元素符号)元素相似。
(2)在化学反应中,戊元素的原子容易 (填“失去”或“得到”)电子形成阳离子,该元素
的 离 子 符 号 是 。 该 元 素 单 质 与 氧 气 反 应 的 化 学 方 程 式 是
。
(3)甲、乙元素和碳元素、氧元素组成的一种常见氮肥的化学式为 。
解析:(1)除最外层是第一层外,一般情况下,金属元素最外层电子数小于4,故上述六种元素中
属于金属元素的是丁和戊;元素的化学性质由原子最外层的电子数决定,己元素的原子最外层
有7个电子,丙元素的原子最外层也有7个电子,故它们的化学性质相同;(2)戊元素的原子最
外层有3个电子,在化学反应中容易失去3个电子,变成带3个正电荷的铝离子;铝与氧气在点
燃的条件下生成氧化铝,其反应化学方程式为4Al+3O 2Al O;(3)氢、氮、碳、氧四种元素
2 2 3
组成的常见氮肥的化学式为NH HCO 或(NH )CO、CO(NH)。
4 3 4 2 3 2 2
答案:(1)钠、铝 F
(2)失去 Al3+ 4Al+3O 2Al O(反应条件可不写)
2 2 3
(3)NH HCO [或(NH )CO、CO(NH)]
4 3 4 2 3 2 2
19.(4分)甲醇(CHOH)有毒,误饮可使眼睛失明甚至死亡。最新研究证明用氨气(NH )处理含
3 3
有甲醇的工业废水,可使甲醇转变为无毒的物质,反应的化学方程式为5CHOH+12O +
3 2NH 3N+5CO +19H O。
3 2 2 2
(1)甲醇中碳元素、氢元素和氧元素的质量比为 (填最简整数比)。
(2)上述化学反应方程式中氨分子前的化学计量数为 。
(3)上述化学反应前后分子数目 (填“增加”“不变”或“减少”)。
(4)NH 中氮元素的化合价是 价。
3
解析:(1)甲醇中碳元素、氢元素和氧元素的质量比=12∶(1×4)∶16=3∶1∶4;(2)由
5CHOH+12O +6NH 3N+5CO +19H O可推知氨分子前的化学计量数为6,化学反应前后
3 2 3 2 2 2
分子数目增加;(4)NH 中氮元素的化合价是-3价。
3
答案:(1)3∶1∶4 (2)6 (3)增加 (4)-3
20.(4分)元素M是地壳中含量居第二位的金属元素;M单质是世界上年产量最高的金属,也是
现实生活中使用最广泛的金属。M单质能在纯氧中燃烧;古代曾用M单质与硫酸铜溶液反应
制取铜;生活中可用稀盐酸除去M单质表面因锈蚀而生成的氧化物;M的碳酸盐(MCO )在高
3
温条件下能分解生成M的低价氧化物和另一种气态氧化物。请分析推断M元素,按下列要求
写出上述中涉及的化学方程式:
(1)化合反应 ;
(2)分解反应 ;
(3)置换反应 ;
(4)复分解反应 。
解析:元素M是地壳中含量居第二位的金属元素,故M为铁元素。再根据题意即可写出有关
的化学方程式。
答案:(1)3Fe+2O Fe O
2 3 4
(2)FeCO FeO+CO↑
3 2 [来源:学科网ZXXK]
(3)Fe+CuSO FeSO +Cu
4 4
(4)Fe O+6HCl 2FeCl +3H O
2 3 3 2
三、简答题(本题包括2个小题,共10分)
21.(4分)请用分子、原子、离子、元素的相关知识解释下列问题:
(1)化学反应前后物质总质量不变。
。
(2)分别加热高锰酸钾、氯酸钾或电解水,都能生成氧气。
。
(3)金刚石、石墨都是由碳元素组成的单质,但物理性质有很大的差异。 。
(4)钠原子和钠离子属于同种元素。
。
答案:(1)在化学反应前后,元素种类不变,原子个数不变,原子质量不变 (2)三种物质中都含
有氧元素 (3)碳原子排列方式不同 (4)核内质子数相同(或核电荷数相同)
22.(6分)人类的日常生活和工农业生产离不开水。请回答:
(1)水 (填“属于”或“不属于”)人类所需的六大基本营养素之一。(2)含有较多可溶性钙、镁化合物的水叫做 (填“软水”或“硬水”)。
(3)下列净化水的单一操作中,相对净化程度较高的是 (填字母)。
A.静置沉淀
B.吸附沉淀
C.蒸馏
(4) 水 在 通 电 的 条 件 下 可 以 分 解 , 写 出 该 反 应 的 化 学 方 程 式 :
。
解析:人类所需的六大基本营养素有蛋白质、脂肪、糖类、维生素、水和无机盐,故水属于人类
所需的六大基本营养素之一;含有较多可溶性钙、镁化合物的水叫做硬水;净化水的单一操作
中,相对净化程度较高的是蒸馏,能够得到纯净的水;水在通电的条件下可以分解生成氢气和
氧气,该反应的化学方程式:2H O 2H↑+O ↑。
2 2 2
答案:(1)属于
(2)硬水
(3)C
(4)2H O 2H↑+O ↑
2 2 2
四、实验探究题(本题包括2个小题,共16分)
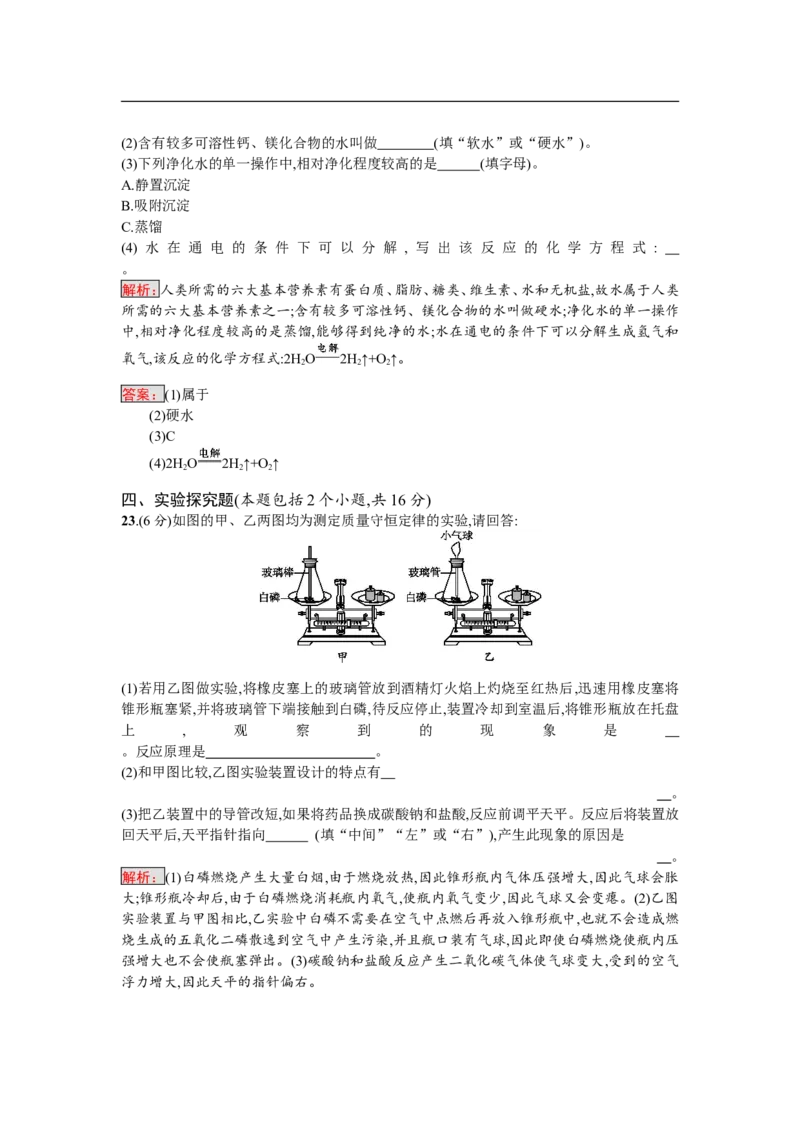
23.(6分)如图的甲、乙两图均为测定质量守恒定律的实验,请回答:
(1)若用乙图做实验,将橡皮塞上的玻璃管放到酒精灯火焰上灼烧至红热后,迅速用橡皮塞将
锥形瓶塞紧,并将玻璃管下端接触到白磷,待反应停止,装置冷却到室温后,将锥形瓶放在托盘
上 , 观 察 到 的 现 象 是
。反应原理是 。
(2)和甲图比较,乙图实验装置设计的特点有
。
(3)把乙装置中的导管改短,如果将药品换成碳酸钠和盐酸,反应前调平天平。反应后将装置放
回天平后,天平指针指向 (填“中间”“左”或“右”),产生此现象的原因是
。
解析:(1)白磷燃烧产生大量白烟,由于燃烧放热,因此锥形瓶内气体压强增大,因此气球会胀
大;锥形瓶冷却后,由于白磷燃烧消耗瓶内氧气,使瓶内氧气变少,因此气球又会变瘪。(2)乙图
实验装置与甲图相比,乙实验中白磷不需要在空气中点燃后再放入锥形瓶中,也就不会造成燃
烧生成的五氧化二磷散逸到空气中产生污染,并且瓶口装有气球,因此即使白磷燃烧使瓶内压
强增大也不会使瓶塞弹出。(3)碳酸钠和盐酸反应产生二氧化碳气体使气球变大,受到的空气
浮力增大,因此天平的指针偏右。答案:(1)白磷燃烧生成了大量白烟,气球先变鼓后变瘪,天平平衡 4P+5O 2PO
2 2 5
(2)密闭性好,有利于环保,胶塞不易弹出
(3)右 碳酸钠和盐酸反应产生二氧化碳气体使气球变鼓,受到的空气浮力增大,使锥形
瓶对左边托盘的压力减小
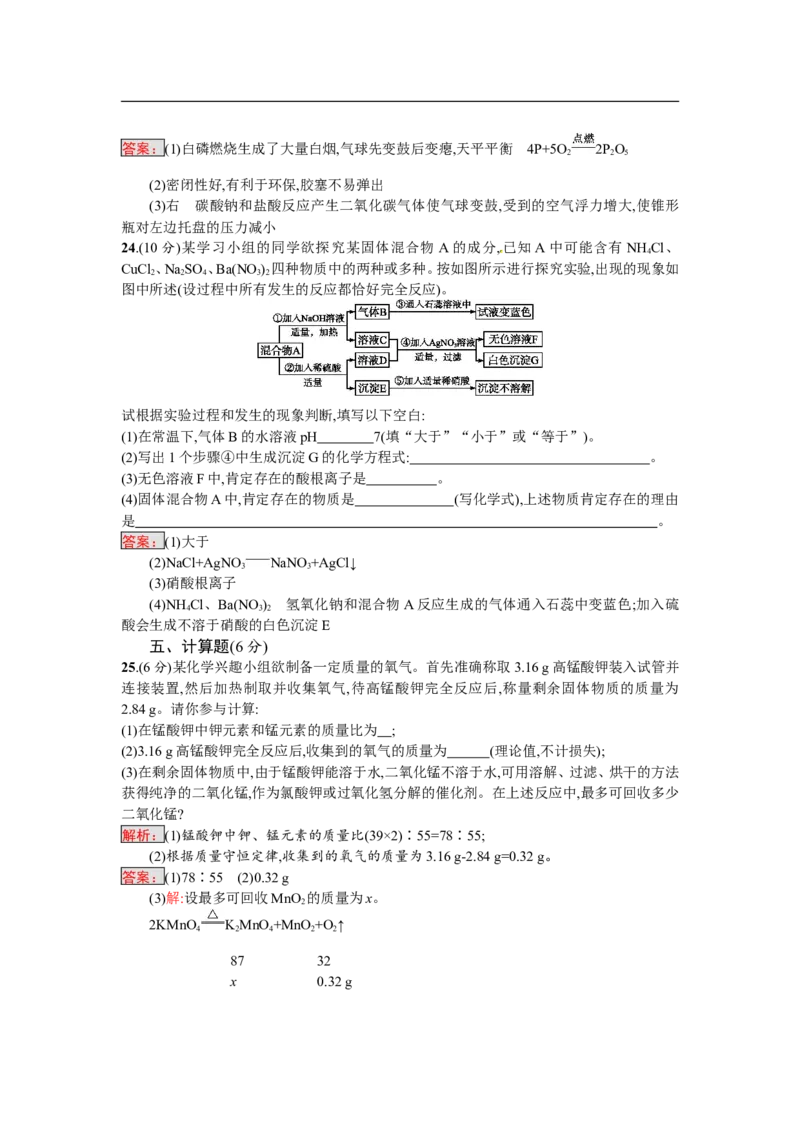
24.(10分)某学习小组的同学欲探究某固体混合物 A的成分,已知A中可能含有NH Cl、
4
CuCl 、NaSO 、Ba(NO ) 四种物质中的两种或多种。按如图所示进行探究实验,出现的现象如
2 2 4 3 2
图中所述(设过程中所有发生的反应都恰好完全反应)。
试根据实验过程和发生的现象判断,填写以下空白:
(1)在常温下,气体B的水溶液pH 7(填“大于”“小于”或“等于”)。
(2)写出1个步骤④中生成沉淀G的化学方程式: 。
(3)无色溶液F中,肯定存在的酸根离子是 。
(4)固体混合物A中,肯定存在的物质是 (写化学式),上述物质肯定存在的理由
是 。
答案:(1)大于
(2)NaCl+AgNO NaNO +AgCl↓
3 3
(3)硝酸根离子
(4)NH Cl、Ba(NO ) 氢氧化钠和混合物A反应生成的气体通入石蕊中变蓝色;加入硫
4 3 2
酸会生成不溶于硝酸的白色沉淀E
五、计算题(6分)
25.(6分)某化学兴趣小组欲制备一定质量的氧气。首先准确称取3.16 g高锰酸钾装入试管并
连接装置,然后加热制取并收集氧气,待高锰酸钾完全反应后,称量剩余固体物质的质量为
2.84 g。请你参与计算:
(1)在锰酸钾中钾元素和锰元素的质量比为 ;
(2)3.16 g高锰酸钾完全反应后,收集到的氧气的质量为 (理论值,不计损失);
(3)在剩余固体物质中,由于锰酸钾能溶于水,二氧化锰不溶于水,可用溶解、过滤、烘干的方法
获得纯净的二氧化锰,作为氯酸钾或过氧化氢分解的催化剂。在上述反应中,最多可回收多少
二氧化锰?
解析:(1)锰酸钾中钾、锰元素的质量比(39×2)∶55=78∶55;
(2)根据质量守恒定律,收集到的氧气的质量为3.16 g-2.84 g=0.32 g。
答案:(1)78∶55 (2)0.32 g
(3)解:设最多可回收MnO 的质量为x。
2
2KMnO KMnO +MnO+O ↑
4 2 4 2 2
87 32
x 0.32 g解得x=0.87 g,
答:最多可回收MnO 的质量为0.87 g。
2