文档内容
阶段检测三 碳和碳的氧化物 燃料及其利用
(时间:90分钟 满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Cl 35.5
Ca 40
一、选择题(每小题只有一个选项符合题意,每小题3分,共45分)
1.石墨烯是由碳原子构成的单层片状结构的新材料,它是一种透明的良好导体,也是最薄、最
硬的纳米材料。下列关于石墨烯的说法不正确的是( )
A.为白色固体 B.硬度较大
C.具有良好的导电性 D.燃烧能生成二氧化碳
解析:石墨烯是由碳元素组成的,不是白色,A项错误。
答案:A
2.下列说法中,正确的是( )
A.金刚石、石墨都是由碳原子构成的,硬度很大
B.木炭不完全燃烧时会生成一氧化碳,同时吸收大量的热
C.单质碳具有氧化性,没有还原性
D.固态二氧化碳俗称“干冰”,可用于人工降雨
解析:金刚石、石墨都是由碳原子构成的单质,金刚石很硬,石墨很软,A项错误;木炭不完全燃
烧时会生成一氧化碳,同时放出大量的热,B项错误;单质碳具有还原性,不具有氧化性,C项错
误;固态二氧化碳俗称“干冰”,升华时吸收大量的热,可用于人工降雨,D项正确。
答案:D
3.下列有关二氧化碳的检验、制备和用途能达到目的的是 ( )
A.二氧化碳气体通入紫色石蕊溶液中,溶液变蓝
[来源:Z+xx+k.Com]
B.将燃着的木条伸入集气瓶,火焰立即熄灭,证明瓶内原有气体就是二氧化碳
C.用块状石灰石和稀硫酸迅速制备大量二氧化碳
D.可以用澄清石灰水检验二氧化碳的生成
解析:由于二氧化碳与水反应生成的是碳酸,因此将二氧化碳气体通入紫色石蕊溶液中,溶液
变红,A项错误;由于二氧化碳既不燃烧也不支持燃烧,因此将燃着的木条伸入到有二氧化碳
的集气瓶中时,木条会熄灭,但能使木条熄灭的不一定是二氧化碳气体,也有可能是氮气,B项
错误;由于稀硫酸和石灰石反应时生成的硫酸钙微溶于水,会覆盖在石灰石的表面,阻碍反应
的进行,因此在实验室中制取二氧化碳不能用石灰石和稀硫酸,而是用石灰石和稀盐酸,C项
错误;因为二氧化碳能使澄清石灰水变浑浊,因此可用澄清石灰水检验二氧化碳的生成,D项
正确。
答案:D
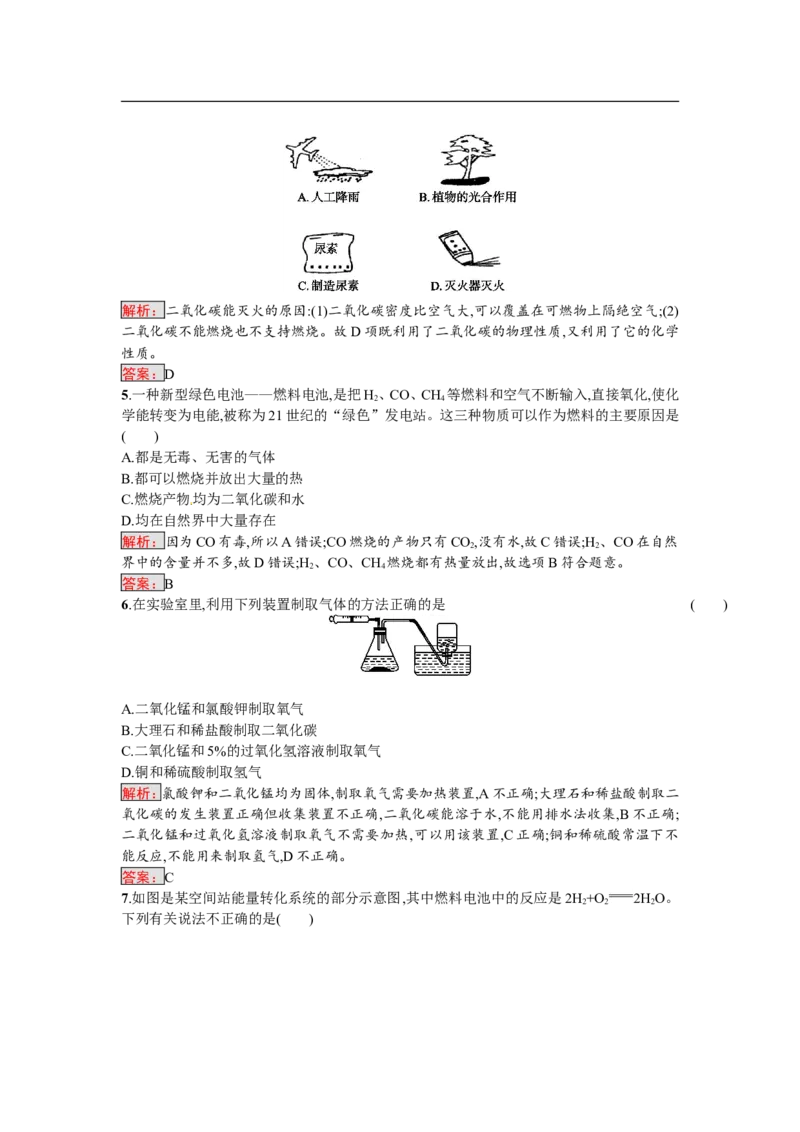
4.如图所示是二氧化碳的几种用途,其中既利用了它的物理性质,又利用了它的化学性质的是
( )解析:二氧化碳能灭火的原因:(1)二氧化碳密度比空气大,可以覆盖在可燃物上隔绝空气;(2)
二氧化碳不能燃烧也不支持燃烧。故D项既利用了二氧化碳的物理性质,又利用了它的化学
性质。
答案:D
5.一种新型绿色电池——燃料电池,是把H、CO、CH 等燃料和空气不断输入,直接氧化,使化
2 4
学能转变为电能,被称为21世纪的“绿色”发电站。这三种物质可以作为燃料的主要原因是
( )
A.都是无毒、无害的气体
B.都可以燃烧并放出大量的热
C.燃烧产物均为二氧化碳和水
D.均在自然界中大量存在
解析:因为CO有毒,所以A错误;CO燃烧的产物只有CO,没有水,故C错误;H 、CO在自然
2 2
界中的含量并不多,故D错误;H 、CO、CH 燃烧都有热量放出,故选项B符合题意。
2 4
答案:B
6.在实验室里,利用下列装置制取气体的方法正确的是 ( )
A.二氧化锰和氯酸钾制取氧气
B.大理石和稀盐酸制取二氧化碳
C.二氧化锰和5%的过氧化氢溶液制取氧气
D.铜和稀硫酸制取氢气
解析:氯酸钾和二氧化锰均为固体,制取氧气需要加热装置,A不正确;大理石和稀盐酸制取二
氧化碳的发生装置正确但收集装置不正确,二氧化碳能溶于水,不能用排水法收集,B不正确;
二氧化锰和过氧化氢溶液制取氧气不需要加热,可以用该装置,C正确;铜和稀硫酸常温下不
能反应,不能用来制取氢气,D不正确。
答案:C
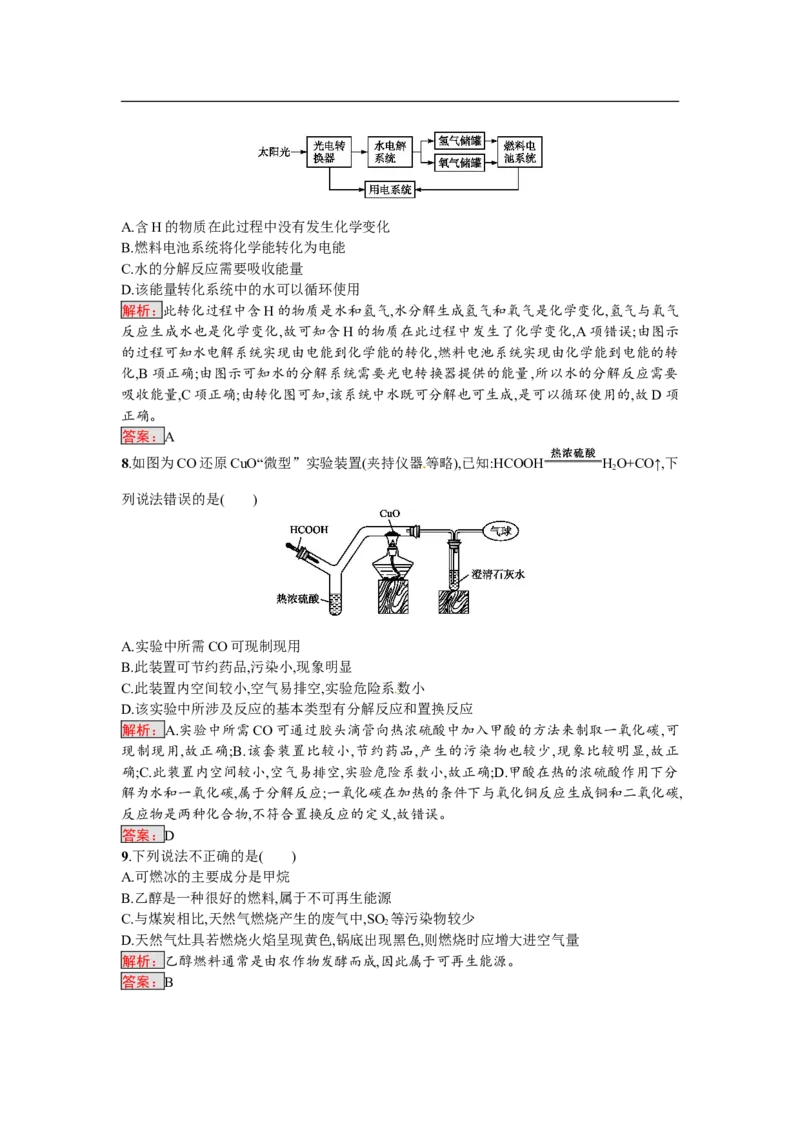
7.如图是某空间站能量转化系统的部分示意图,其中燃料电池中的反应是2H+O 2HO。
2 2 2
下列有关说法不正确的是( )A.含H的物质在此过程中没有发生化学变化
B.燃料电池系统将化学能转化为电能
C.水的分解反应需要吸收能量
D.该能量转化系统中的水可以循环使用
解析:此转化过程中含H的物质是水和氢气,水分解生成氢气和氧气是化学变化,氢气与氧气
反应生成水也是化学变化,故可知含H的物质在此过程中发生了化学变化,A项错误;由图示
的过程可知水电解系统实现由电能到化学能的转化,燃料电池系统实现由化学能到电能的转
化,B项正确;由图示可知水的分解系统需要光电转换器提供的能量,所以水的分解反应需要
吸收能量,C项正确;由转化图可知,该系统中水既可分解也可生成,是可以循环使用的,故D项
正确。
答案:A
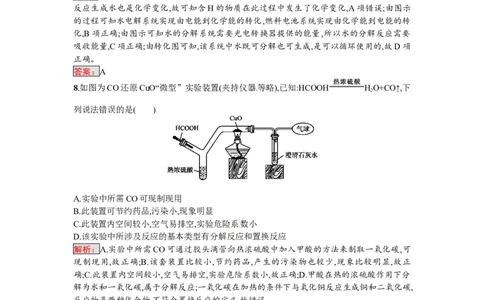
8.如图为CO还原CuO“微型”实验装置(夹持仪器等略),已知:HCOOH HO+CO↑,下
2
列说法错误的是( )
A.实验中所需CO可现制现用
[来源:Z_xx_k.Com]
B.此装置可节约药品,污染小,现象明显
C.此装置内空间较小,空气易排空,实验危险系数小
D.该实验中所涉及反应的基本类型有分解反应和置换反应
解析:A.实验中所需CO可通过胶头滴管向热浓硫酸中加入甲酸的方法来制取一氧化碳,可
现制现用,故正确;B.该套装置比较小,节约药品,产生的污染物也较少,现象比较明显,故正
确;C.此装置内空间较小,空气易排空,实验危险系数小,故正确;D.甲酸在热的浓硫酸作用下分
解为水和一氧化碳,属于分解反应;一氧化碳在加热的条件下与氧化铜反应生成铜和二氧化碳,
反应物是两种化合物,不符合置换反应的定义,故错误。
答案:D
[来源:Z|xx|k.Com]
9.下列说法不正确的是( )
A.可燃冰的主要成分是甲烷
B.乙醇是一种很好的燃料,属于不可再生能源
C.与煤炭相比,天然气燃烧产生的废气中,SO 等污染物较少
2
D.天然气灶具若燃烧火焰呈现黄色,锅底出现黑色,则燃烧时应增大进空气量
解析:乙醇燃料通常是由农作物发酵而成,因此属于可再生能源。
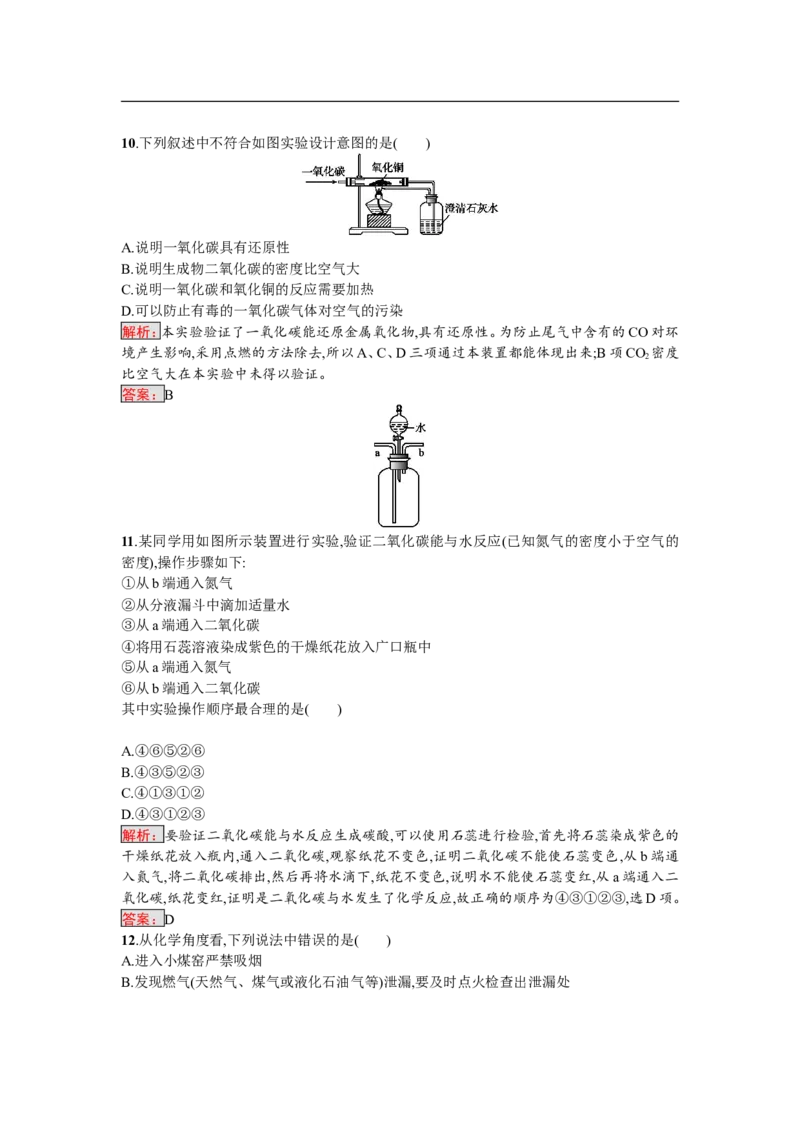
答案:B10.下列叙述中不符合如图实验设计意图的是( )
A.说明一氧化碳具有还原性
B.说明生成物二氧化碳的密度比空气大
C.说明一氧化碳和氧化铜的反应需要加热
D.可以防止有毒的一氧化碳气体对空气的污染
解析:本实验验证了一氧化碳能还原金属氧化物,具有还原性。为防止尾气中含有的CO对环
境产生影响,采用点燃的方法除去,所以A、C、D三项通过本装置都能体现出来;B项CO 密度
2
比空气大在本实验中未得以验证。
答案:B
11.某同学用如图所示装置进行实验,验证二氧化碳能与水反应(已知氮气的密度小于空气的
密度),操作步骤如下:
①从b端通入氮气
②从分液漏斗中滴加适量水
③从a端通入二氧化碳
④将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
⑤从a端通入氮气
⑥从b端通入二氧化碳
其中实验操作顺序最合理的是( )
A.④⑥⑤②⑥
B.④③⑤②③
C.④①③①②
D.④③①②③
解析:要验证二氧化碳能与水反应生成碳酸,可以使用石蕊进行检验,首先将石蕊染成紫色的
干燥纸花放入瓶内,通入二氧化碳,观察纸花不变色,证明二氧化碳不能使石蕊变色,从b端通
入氮气,将二氧化碳排出,然后再将水滴下,纸花不变色,说明水不能使石蕊变红,从a端通入二
氧化碳,纸花变红,证明是二氧化碳与水发生了化学反应,故正确的顺序为④③①②③,选D项。
答案:D
12.从化学角度看,下列说法中错误的是( )
A.进入小煤窑严禁吸烟
B.发现燃气(天然气、煤气或液化石油气等)泄漏,要及时点火检查出泄漏处C.炒菜时油锅着火,可用锅盖盖灭火焰
D.面粉厂、加油站严禁烟火
答案:B
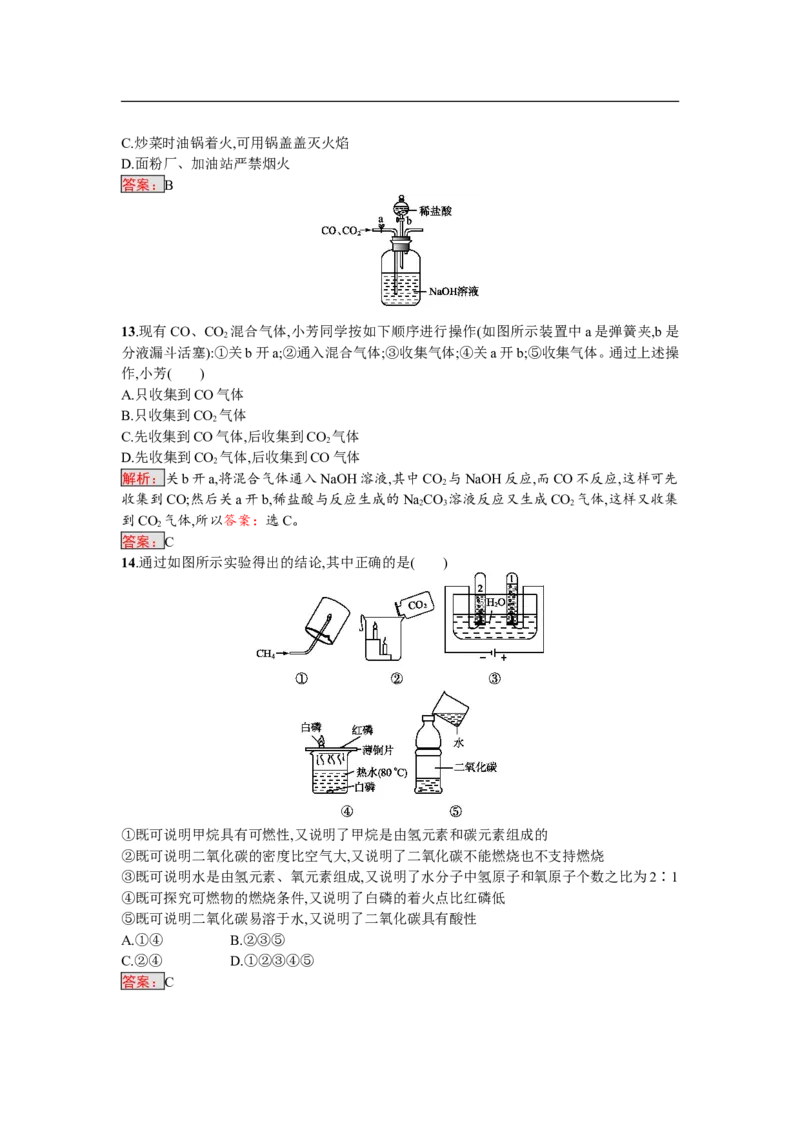
13.现有CO、CO 混合气体,小芳同学按如下顺序进行操作(如图所示装置中a是弹簧夹,b是
2
分液漏斗活塞):①关b开a;②通入混合气体;③收集气体;④关a开b;⑤收集气体。通过上述操
作,小芳( )
A.只收集到CO气体
B.只收集到CO 气体
2
C.先收集到CO气体,后收集到CO 气体
2
D.先收集到CO 气体,后收集到CO气体
2
解析:关b开a,将混合气体通入NaOH溶液,其中CO 与NaOH反应,而CO不反应,这样可先
2
收集到CO;然后关a开b,稀盐酸与反应生成的NaCO 溶液反应又生成CO 气体,这样又收集
2 3 2
到CO 气体,所以答案:选C。
2
答案:C
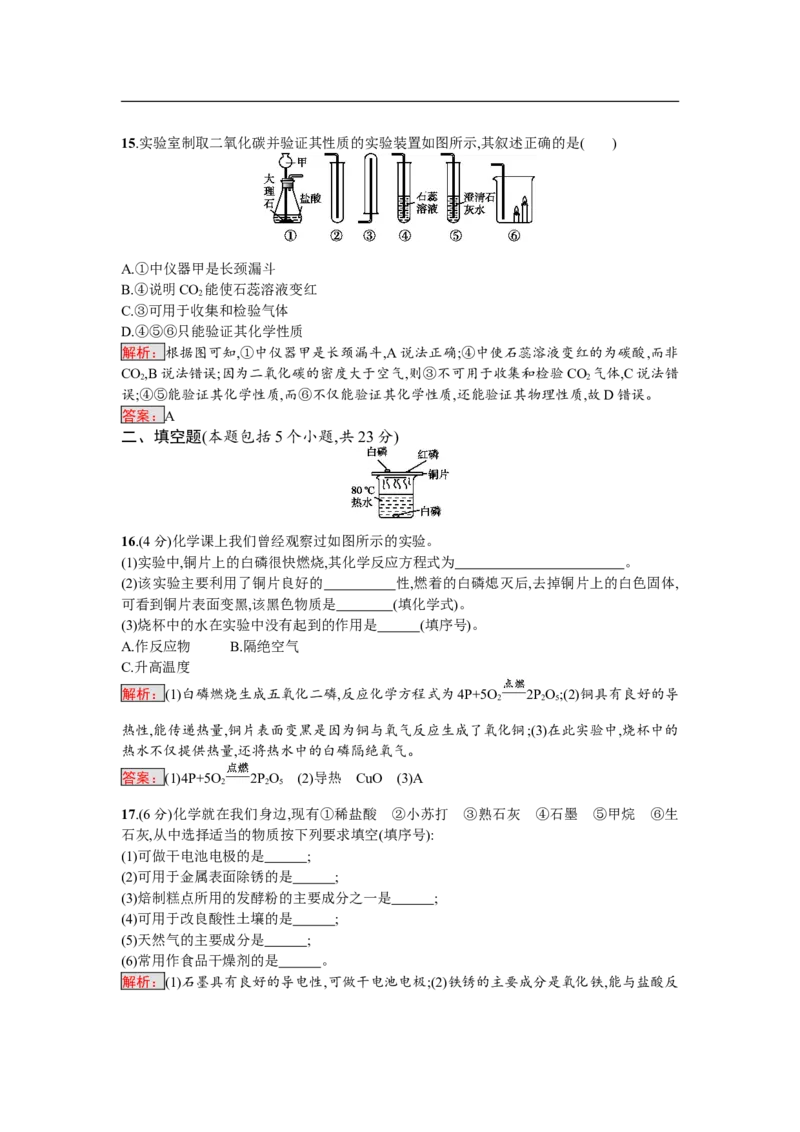
14.通过如图所示实验得出的结论,其中正确的是( )
①既可说明甲烷具有可燃性,又说明了甲烷是由氢元素和碳元素组成的
②既可说明二氧化碳的密度比空气大,又说明了二氧化碳不能燃烧也不支持燃烧
③既可说明水是由氢元素、氧元素组成,又说明了水分子中氢原子和氧原子个数之比为2∶1
④既可探究可燃物的燃烧条件,又说明了白磷的着火点比红磷低
⑤既可说明二氧化碳易溶于水,又说明了二氧化碳具有酸性
A.①④ B.②③⑤
C.②④ D.①②③④⑤
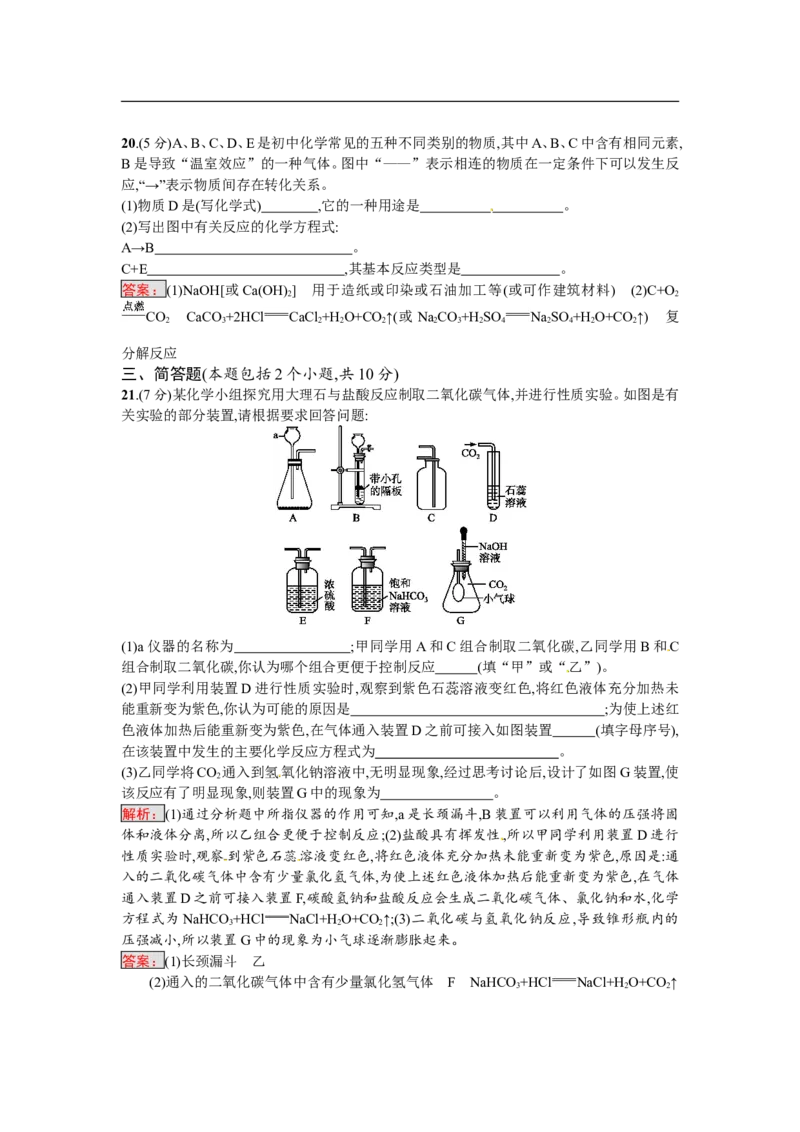
答案:C15.实验室制取二氧化碳并验证其性质的实验装置如图所示,其叙述正确的是( )
A.①中仪器甲是长颈漏斗
B.④说明CO 能使石蕊溶液变红
2
C.③可用于收集和检验气体
D.④⑤⑥只能验证其化学性质
解析:根据图可知,①中仪器甲是长颈漏斗,A说法正确;④中使石蕊溶液变红的为碳酸,而非
CO,B说法错误;因为二氧化碳的密度大于空气,则③不可用于收集和检验CO 气体,C说法错
2 2
误;④⑤能验证其化学性质,而⑥不仅能验证其化学性质,还能验证其物理性质,故D错误。
答案:A
二、填空题(本题包括5个小题,共23分)
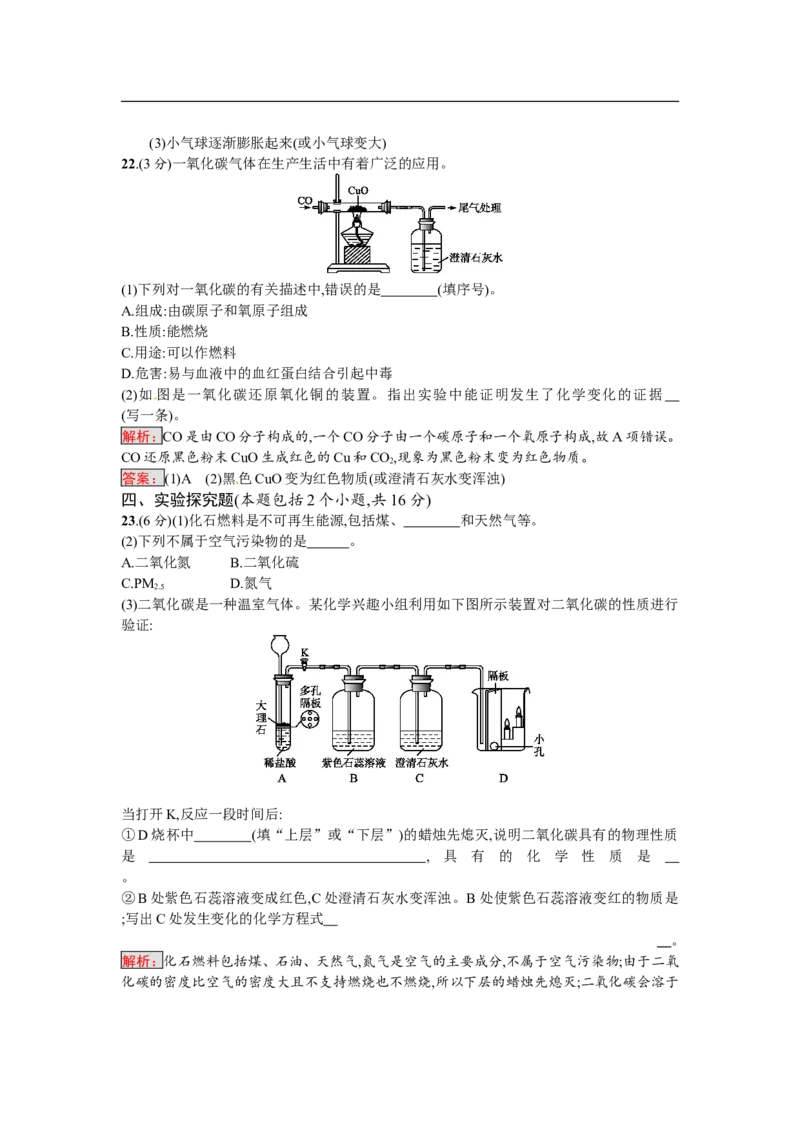
16.(4分)化学课上我们曾经观察过如图所示的实验。
(1)实验中,铜片上的白磷很快燃烧,其化学反应方程式为 。
(2)该实验主要利用了铜片良好的 性,燃着的白磷熄灭后,去掉铜片上的白色固体,
可看到铜片表面变黑,该黑色物质是 (填化学式)。
(3)烧杯中的水在实验中没有起到的作用是 (填序号)。
A.作反应物 B.隔绝空气
C.升高温度
解析:(1)白磷燃烧生成五氧化二磷,反应化学方程式为4P+5O 2PO;(2)铜具有良好的导
2 2 5
热性,能传递热量,铜片表面变黑是因为铜与氧气反应生成了氧化铜;(3)在此实验中,烧杯中的
热水不仅提供热量,还将热水中的白磷隔绝氧气。
答案:(1)4P+5O 2PO (2)导热 CuO (3)A
2 2 5
17.(6分)化学就在我们身边,现有①稀盐酸 ②小苏打 ③熟石灰 ④石墨 ⑤甲烷 ⑥生
石灰,从中选择适当的物质按下列要求填空(填序号):
(1)可做干电池电极的是 ;
(2)可用于金属表面除锈的是 ;
(3)焙制糕点所用的发酵粉的主要成分之一是 ;
(4)可用于改良酸性土壤的是 ;
(5)天然气的主要成分是 ;
(6)常用作食品干燥剂的是 。
解析:(1)石墨具有良好的导电性,可做干电池电极;(2)铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁和水;(3)小苏打是碳酸氢钠的俗称,是焙制糕点所用的发酵粉的主要成分之一;
(4)氢氧化钙具有碱性,可用于改良酸性土壤;(5)天然气的主要成分是甲烷;(6)生石灰能与水反
应,常用作食品干燥剂。
答案:(1)④ (2)① (3)② (4)③ (5)⑤ (6)⑥
18.(3分)木炭在一定条件下燃烧既有CO 生成,也有CO生成。若要证明两种气体都存在,应先
2
将气体通入澄清石灰水,澄清石灰水变浑浊,证明有CO 存在。写出CO 与澄清石灰水反应的
2 2
化学方程式:
。 然 后 将 气 体 干 燥 后 通 过 灼 热 的 氧 化 铜 , 观 察 到
,证明有 CO 存在。实验后向燃着的木炭上洒水使其熄灭 ,其灭火的原理是
。
答案:CO+Ca(OH) CaCO ↓+H O 黑色粉末变为红色 把可燃物的温度降到着火点以
2 2 3 2
下
19.(5分)能源和环境问题日益成为人们关注的焦点。
(1)常见的化石燃料有煤、 和天然气等。天然气(主要成分是CH)在空气中完全燃烧
4
的化学方程式是 。
(2)燃煤会影响环境。下列环境问题与燃煤没有直接关系的是 (填序号,下同)。
A.酸雨
B.温室效应
C.臭氧层破坏
D.可吸入颗粒物增加
(3)大气中CO 含量不断升高,使全球气候问题日趋严重。如图为CO 参与的一种“碳转化”。
2 2
①下列物质中,属于有机物的是 。
A.CaCO B.C HOH C.CO
3 2 5
②CO 和H 在催化剂和加热条件下,可以转化为化工原料乙烯(C H),请将该反应的化学方
2 2 2 4
程式补充完整:
2CO+6H C H+4 。
2 2 2 4
解析:(1)煤、石油、天然气属于化石燃料;甲烷燃烧会生成二氧化碳和水,其方程式为CH+2O
4 2
CO+2H O;(2)煤燃烧能生成二氧化碳、二氧化硫等物质,还能产生大量的灰尘,生成的二
2 2
氧化碳能产生温室效应,生成的二氧化硫能形成酸雨,产生的大量灰尘增加了空气中的可吸入
颗粒物;(3)①含有碳元素的化合物属于有机物,一氧化碳、二氧化碳、碳酸盐等除外,所以乙醇
属于有机物;②根据质量守恒定律可知,元素种类、原子种类和个数在反应前后不变,可以判断
出生成物是乙烯和水,其反应化学方程式为2CO+6H C H+4H O。
2 2 2 4 2
答案:(1)石油 CH+2O CO+2H O (2)C (3)①B ②HO
4 2 2 2 220.(5分)A、B、C、D、E是初中化学常见的五种不同类别的物质,其中A、B、C中含有相同元素,
B是导致“温室效应”的一种气体。图中“——”表示相连的物质在一定条件下可以发生反
应,“→”表示物质间存在转化关系。
(1)物质D是(写化学式) ,它的一种用途是 。
(2)写出图中有关反应的化学方程式:
A→B 。
C+E ,其基本反应类型是 。
答案:(1)NaOH[或Ca(OH) ] 用于造纸或印染或石油加工等(或可作建筑材料) (2)C+O
2 2
CO CaCO +2HCl CaCl +H O+CO↑(或 NaCO+H SO NaSO +H O+CO↑) 复
2 3 2 2 2 2 3 2 4 2 4 2 2
分解反应
三、简答题(本题包括2个小题,共10分)
21.(7分)某化学小组探究用大理石与盐酸反应制取二氧化碳气体,并进行性质实验。如图是有
关实验的部分装置,请根据要求回答问题:
(1)a仪器的名称为 ;甲同学用A和C组合制取二氧化碳,乙同学用B和C
组合制取二氧化碳,你认为哪个组合更便于控制反应 (填“甲”或“乙”)。
(2)甲同学利用装置D进行性质实验时,观察到紫色石蕊溶液变红色,将红色液体充分加热未
能重新变为紫色,你认为可能的原因是 ;为使上述红
色液体加热后能重新变为紫色,在气体通入装置D之前可接入如图装置 (填字母序号),
在该装置中发生的主要化学反应方程式为 。
(3)乙同学将CO 通入到氢氧化钠溶液中,无明显现象,经过思考讨论后,设计了如图G装置,使
2
该反应有了明显现象,则装置G中的现象为 。
解析:(1)通过分析题中所指仪器的作用可知,a是长颈漏斗,B装置可以利用气体的压强将固
体和液体分离,所以乙组合更便于控制反应;(2)盐酸具有挥发性,所以甲同学利用装置D进行
性质实验时,观察到紫色石蕊溶液变红色,将红色液体充分加热未能重新变为紫色,原因是:通
入的二氧化碳气体中含有少量氯化氢气体,为使上述红色液体加热后能重新变为紫色,在气体
通入装置D之前可接入装置F,碳酸氢钠和盐酸反应会生成二氧化碳气体、氯化钠和水,化学
方程式为NaHCO +HCl NaCl+H O+CO↑;(3)二氧化碳与氢氧化钠反应,导致锥形瓶内的
3 2 2
压强减小,所以装置G中的现象为小气球逐渐膨胀起来。
答案:(1)长颈漏斗 乙
(2)通入的二氧化碳气体中含有少量氯化氢气体 F NaHCO +HCl NaCl+H O+CO↑
3 2 2(3)小气球逐渐膨胀起来(或小气球变大)
22.(3分)一氧化碳气体在生产生活中有着广泛的应用。
(1)下列对一氧化碳的有关描述中,错误的是 (填序号)。
A.组成:由碳原子和氧原子组成
B.性质:能燃烧
C.用途:可以作燃料
D.危害:易与血液中的血红蛋白结合引起中毒
(2)如图是一氧化碳还原氧化铜的装置。指出实验中能证明发生了化学变化的证据
(写一条)。
解析:CO是由CO分子构成的,一个CO分子由一个碳原子和一个氧原子构成,故A项错误。
CO还原黑色粉末CuO生成红色的Cu和CO,现象为黑色粉末变为红色物质。
2
答案:(1)A (2)黑色CuO变为红色物质(或澄清石灰水变浑浊)
四、实验探究题(本题包括2个小题,共16分)
23.(6分)(1)化石燃料是不可再生能源,包括煤、 和天然气等。
(2)下列不属于空气污染物的是 。
A.二氧化氮 B.二氧化硫
C.PM D.氮气
2.5
(3)二氧化碳是一种温室气体。某化学兴趣小组利用如下图所示装置对二氧化碳的性质进行
验证:
当打开K,反应一段时间后:
①D烧杯中 (填“上层”或“下层”)的蜡烛先熄灭,说明二氧化碳具有的物理性质
是 , 具 有 的 化 学 性 质 是
。
②B处紫色石蕊溶液变成红色,C处澄清石灰水变浑浊。B处使紫色石蕊溶液变红的物质是
;写出C处发生变化的化学方程式
。
解析:化石燃料包括煤、石油、天然气,氮气是空气的主要成分,不属于空气污染物;由于二氧
化碳的密度比空气的密度大且不支持燃烧也不燃烧,所以下层的蜡烛先熄灭;二氧化碳会溶于水生成碳酸,碳酸使紫色石蕊溶液变红,而不是二氧化碳,因为二氧化碳不具有酸性;二氧化碳
与澄清石灰水反应的化学方程式为Ca(OH) +CO CaCO ↓+H O。
2 2 3 2
答案:(1)石油
(2)D
(3)①下层 密度比空气的大 不燃烧也不支持燃烧 ②碳酸(H CO) CO+Ca(OH)
2 3 2 2
CaCO ↓+H O
3 2
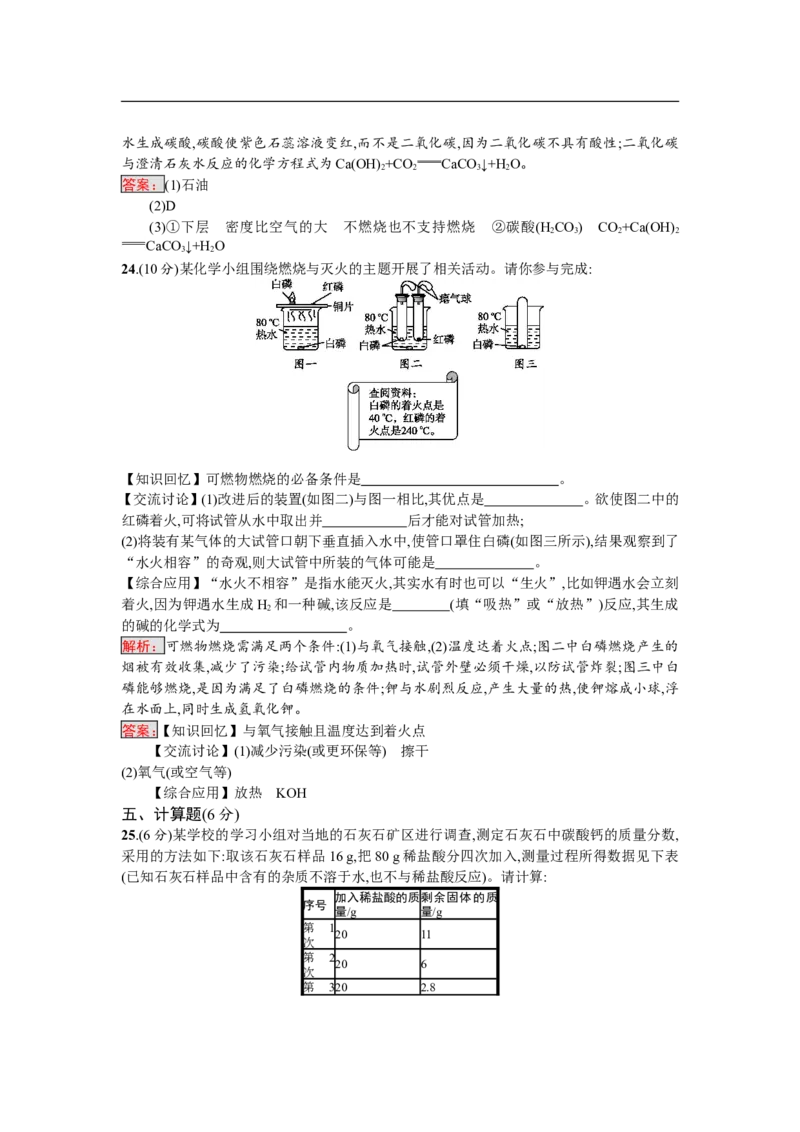
24.(10分)某化学小组围绕燃烧与灭火的主题开展了相关活动。请你参与完成:
【知识回忆】可燃物燃烧的必备条件是 。
【交流讨论】(1)改进后的装置(如图二)与图一相比,其优点是 。欲使图二中的
红磷着火,可将试管从水中取出并 后才能对试管加热;
(2)将装有某气体的大试管口朝下垂直插入水中,使管口罩住白磷(如图三所示),结果观察到了
“水火相容”的奇观,则大试管中所装的气体可能是 。
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻
着火,因为钾遇水生成H 和一种碱,该反应是 (填“吸热”或“放热”)反应,其生成
2
的碱的化学式为 。
解析:可燃物燃烧需满足两个条件:(1)与氧气接触,(2)温度达着火点;图二中白磷燃烧产生的
烟被有效收集,减少了污染;给试管内物质加热时,试管外壁必须干燥,以防试管炸裂;图三中白
磷能够燃烧,是因为满足了白磷燃烧的条件;钾与水剧烈反应,产生大量的热,使钾熔成小球,浮
在水面上,同时生成氢氧化钾。
答案:【知识回忆】与氧气接触且温度达到着火点
【交流讨论】(1)减少污染(或更环保等) 擦干
(2)氧气(或空气等)
【综合应用】放热 KOH
五、计算题(6分)
25.(6分)某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,
采用的方法如下:取该石灰石样品16 g,把80 g稀盐酸分四次加入,测量过程所得数据见下表
(已知石灰石样品中含有的杂质不溶于水,也不与稀盐酸反应)。请计算:
加入稀盐酸的质剩余固体的质
序号
量/g 量/g
第 1
20 11
次
第 2
20 6
次
第 320 2.8次
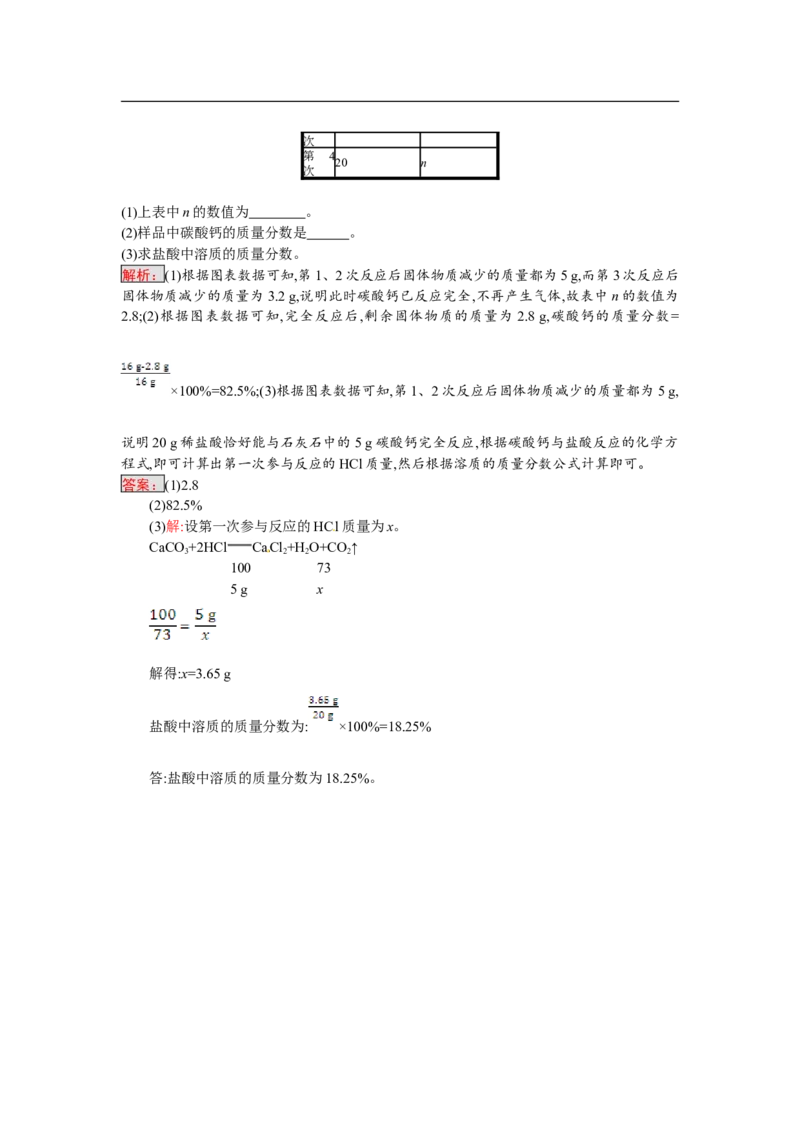
第 4
20 n
次
(1)上表中n的数值为 。
(2)样品中碳酸钙的质量分数是 。
(3)求盐酸中溶质的质量分数。
[来源:学|科|网Z|X|X|K]
解析:(1)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5 g,而第3次反应后
固体物质减少的质量为3.2 g,说明此时碳酸钙已反应完全,不再产生气体,故表中n的数值为
2.8;(2)根据图表数据可知,完全反应后,剩余固体物质的质量为 2.8 g,碳酸钙的质量分数=
×100%=82.5%;(3)根据图表数据可知,第1、2次反应后固体物质减少的质量都为5 g,
说明20 g稀盐酸恰好能与石灰石中的5 g碳酸钙完全反应,根据碳酸钙与盐酸反应的化学方
程式,即可计算出第一次参与反应的HCl质量,然后根据溶质的质量分数公式计算即可。
答案:(1)2.8
(2)82.5%
(3)解:设第一次参与反应的HCl质量为x。
CaCO +2HCl CaCl+H O+CO↑
3 2 2 2 [来源:学#科#网Z#X#X#K]
100 73
5 g x
解得:x=3.65 g
盐酸中溶质的质量分数为: ×100%=18.25%
答:盐酸中溶质的质量分数为18.25%。