文档内容
阶段检测六 酸和碱 盐 化肥 化学与生活
(时间:90分钟 满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16
Cl 35.5 Ca 40
一、选择题(每小题3分,共45分)
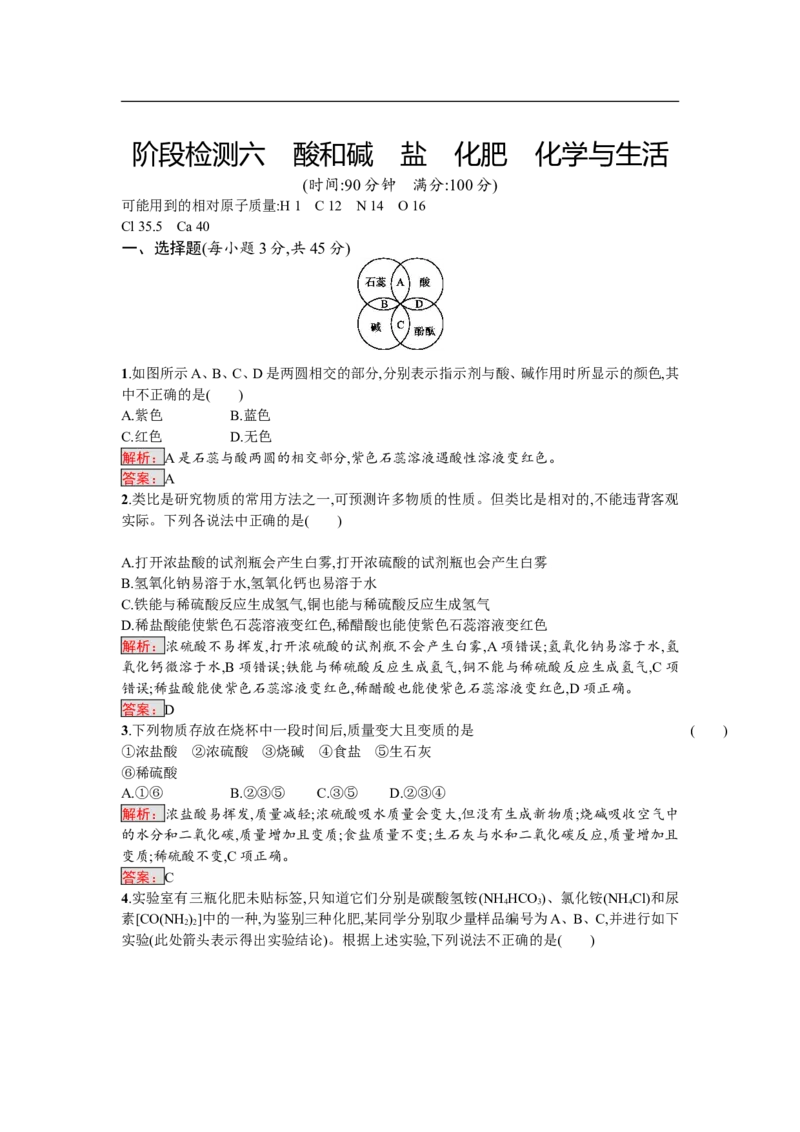
1.如图所示A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱作用时所显示的颜色,其
中不正确的是( )
A.紫色 B.蓝色
C.红色 D.无色
解析:A是石蕊与酸两圆的相交部分,紫色石蕊溶液遇酸性溶液变红色。
答案:A
2.类比是研究物质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观
实际。下列各说法中正确的是( )
A.打开浓盐酸的试剂瓶会产生白雾,打开浓硫酸的试剂瓶也会产生白雾
[来源:学科网]
B.氢氧化钠易溶于水,氢氧化钙也易溶于水
C.铁能与稀硫酸反应生成氢气,铜也能与稀硫酸反应生成氢气
D.稀盐酸能使紫色石蕊溶液变红色,稀醋酸也能使紫色石蕊溶液变红色
解析:浓硫酸不易挥发,打开浓硫酸的试剂瓶不会产生白雾,A项错误;氢氧化钠易溶于水,氢
氧化钙微溶于水,B项错误;铁能与稀硫酸反应生成氢气,铜不能与稀硫酸反应生成氢气,C项
错误;稀盐酸能使紫色石蕊溶液变红色,稀醋酸也能使紫色石蕊溶液变红色,D项正确。
答案:D
3.下列物质存放在烧杯中一段时间后,质量变大且变质的是 ( )
①浓盐酸 ②浓硫酸 ③烧碱 ④食盐 ⑤生石灰
⑥稀硫酸
A.①⑥ B.②③⑤ C.③⑤ D.②③④
解析:浓盐酸易挥发,质量减轻;浓硫酸吸水质量会变大,但没有生成新物质;烧碱吸收空气中
的水分和二氧化碳,质量增加且变质;食盐质量不变;生石灰与水和二氧化碳反应,质量增加且
变质;稀硫酸不变,C项正确。
答案:C
4.实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH HCO )、氯化铵(NH Cl)和尿
4 3 4
素[CO(NH)]中的一种,为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如下
2 2
实验(此处箭头表示得出实验结论)。根据上述实验,下列说法不正确的是( )A.B物质为碳酸氢铵
B.A物质为尿素,属于有机物
C.常温下如要鉴别B、C两种样品,能采取闻气味的方法
D.如果实验Ⅱ中B、C两种样品没有另取,则会使检验结果不准确
解析:因为碳酸氢铵与盐酸反应产生氯化铵、水、二氧化碳,氯化铵与盐酸不反应,所以B物质
为碳酸氢铵,A项正确;碳酸氢铵(NH HCO )、氯化铵(NH Cl)和尿素[CO(NH)]三种物质中,加
4 3 4 2 2
熟石灰无刺激性气味的是尿素,而碳酸氢铵和氯化铵中含有铵根离子,会和熟石灰反应产生有
刺激性气味的氨气,故A物质是尿素,属于有机物,B项正确;因为碳酸氢铵、氯化铵都是铵态
氮肥,但是碳酸氢铵能分解,而氯化铵常温不分解,所以能采取闻气味的方法鉴别,C项正确;碳
酸氢铵与盐酸反应产生氯化铵、水、二氧化碳,氯化铵与盐酸不反应,所以只要含有碳酸氢铵
和氯化铵,就能通过加入盐酸的方式来鉴别,D项错误。
答案:D
5.分类是学习和研究化学的常用方法。下列分类中正确的是( )
A.合成材料:合金、合成橡胶、合成纤维
B.有机物:甲烷、乙醇、葡萄糖(C H O)
6 12 6
C.混合物:煤、石油、冰水共存物
D.复合肥料:尿素、硝酸钾、磷酸氢二铵
解析:合成橡胶、合成纤维属于合成材料,合金属于金属材料,A项错误;甲烷、乙醇、葡萄糖
(C H O)均为含碳元素的化合物,均为有机物,B项正确;煤、石油均属于混合物,冰是固态的水,
6 12 6
冰水共存物属于纯净物,C项错误;尿素中含有氮元素,属于氮肥,不属于复合肥,硝酸钾中含有
钾元素和氮元素,属于复合肥,磷酸氢二铵中含有磷元素和氮元素,属于复合肥,D项错误。
答案:B
6.健康是人类永恒的主题。下列有关叙述中正确的是( )
①蛋白质和糖类都是由碳、氢、氧元素组成的;
②铁是血红蛋白的成分,能帮助运输氧气,缺铁会患坏血病;
③淀粉、蛋白质、油脂都是有机高分子化合物;
④维生素有20多种,它们多数在人体内不能合成;
⑤蔬菜、水果和粗粮等都含有较多的纤维素。
A.①②③④ B.②④⑤
C.④⑤ D.②③⑤
解析:①蛋白质主要由C、H、O、N组成,糖类由C、H、O组成,该说法错误;②缺铁会患贫血,该
说法错误;③淀粉、蛋白质是有机高分子化合物,油脂不是有机高分子化合物,该说法错误;④
维生素有20多种,它们多数在人体内不能合成,该说法正确;⑤蔬菜、水果和粗粮等都含有较
多的纤维素,该说法正确。
答案:C
7.酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不
属于酸的共同性质的是( )A.能使紫色石蕊溶液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
解析:盐酸能使紫色石蕊溶液变红,其他酸也能使紫色石蕊溶液变红,属于酸的共同性质,故A
错误;盐酸能与氢氧化钠溶液反应生成水,酸能与碱发生中和反应,其他酸也能与氢氧化钠溶
液反应生成水,属于酸的共同性质,故B错误;盐酸能与硝酸银溶液反应生成氯化银沉淀,表现
为氯离子的特征,因此硫酸、硝酸等不能与硝酸银溶液反应生成氯化银沉淀,则该性质不属于
酸的共同性质,故C正确;盐酸能与活泼金属反应产生氢气,其他的酸也能与活泼金属反应产
生氢气,属于酸的共同性质,故D错误。
答案:C
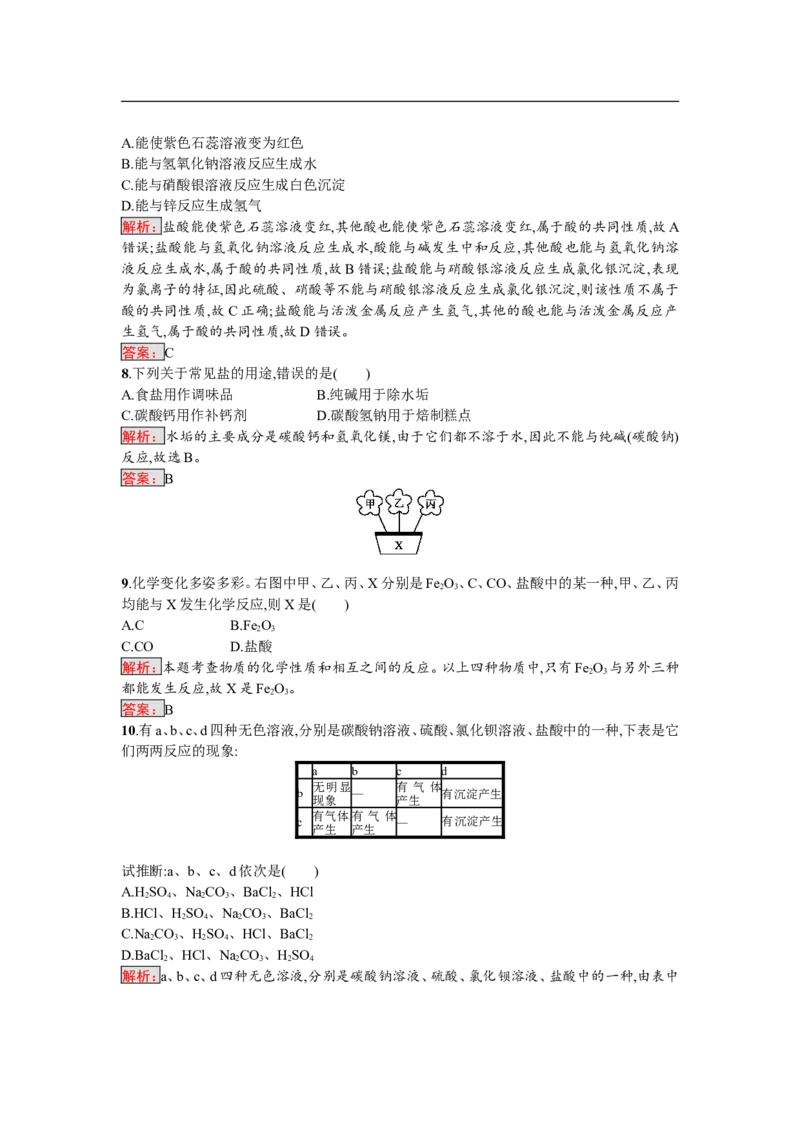
8.下列关于常见盐的用途,错误的是( )
A.食盐用作调味品 B.纯碱用于除水垢
C.碳酸钙用作补钙剂 D.碳酸氢钠用于焙制糕点
解析:水垢的主要成分是碳酸钙和氢氧化镁,由于它们都不溶于水,因此不能与纯碱(碳酸钠)
反应,故选B。
答案:B
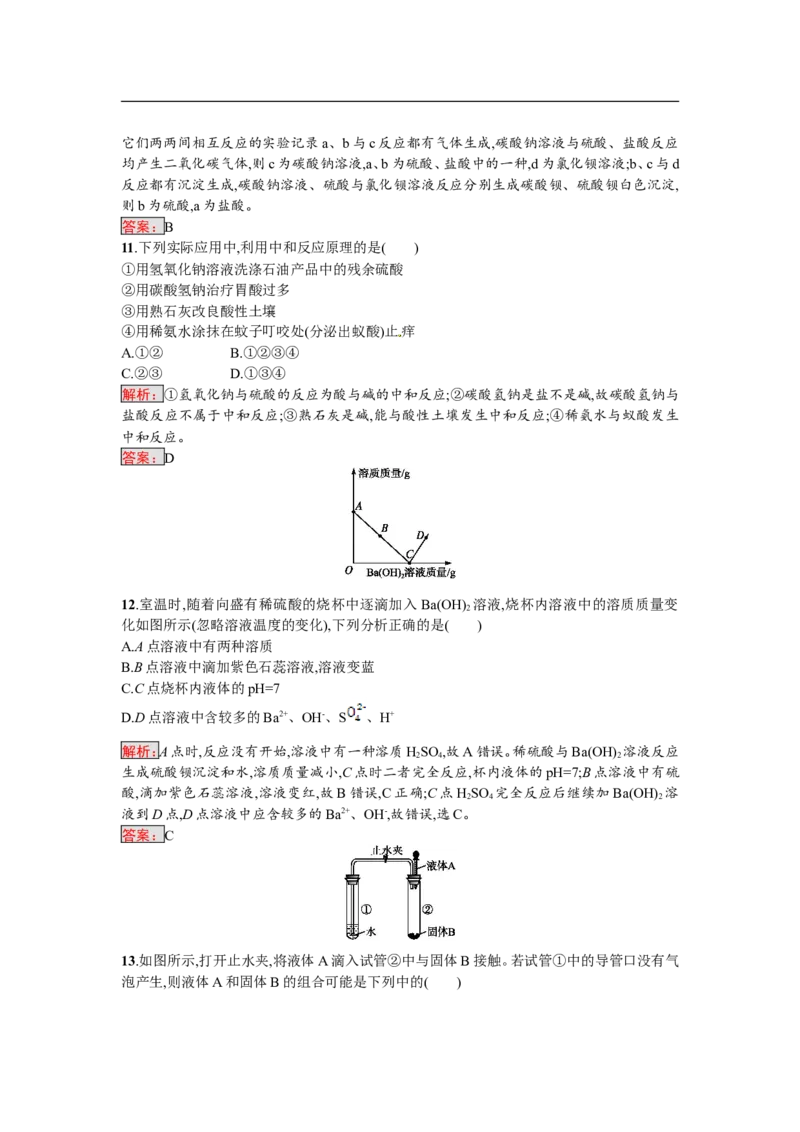
9.化学变化多姿多彩。右图中甲、乙、丙、X分别是Fe O、C、CO、盐酸中的某一种,甲、乙、丙
2 3
均能与X发生化学反应,则X是( )
A.C B.Fe O
2 3
C.CO D.盐酸
解析:本题考查物质的化学性质和相互之间的反应。以上四种物质中,只有Fe O 与另外三种
2 3
都能发生反应,故X是Fe O。
2 3
答案:B
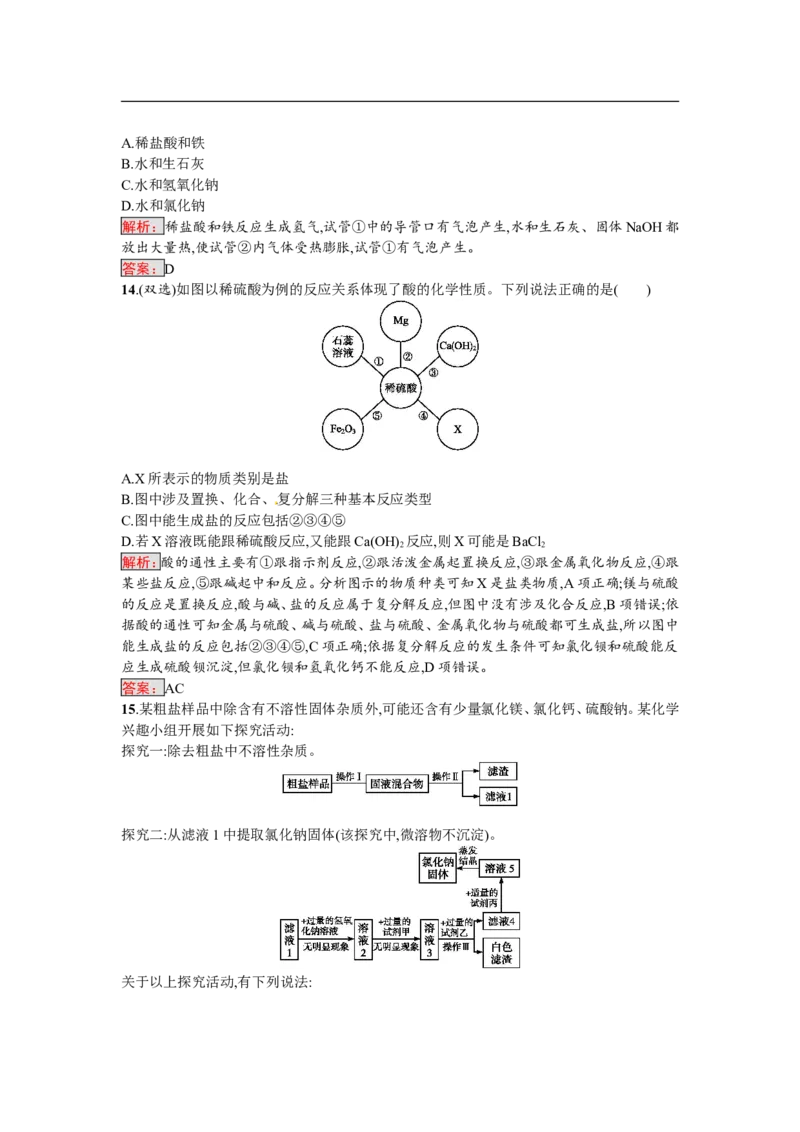
10.有a、b、c、d四种无色溶液,分别是碳酸钠溶液、硫酸、氯化钡溶液、盐酸中的一种,下表是它
们两两反应的现象:
a b c d
无明显 有 气 体
b — 有沉淀产生
现象 产生
有气体有 气 体
c — 有沉淀产生
产生 产生 [来源:学科网ZXXK]
试推断:a、b、c、d依次是( )
A.HSO 、NaCO、BaCl 、HCl
2 4 2 3 2
B.HCl、HSO 、NaCO、BaCl
2 4 2 3 2
C.NaCO、HSO 、HCl、BaCl
2 3 2 4 2
D.BaCl 、HCl、NaCO、HSO
2 2 3 2 4
解析:a、b、c、d四种无色溶液,分别是碳酸钠溶液、硫酸、氯化钡溶液、盐酸中的一种,由表中它们两两间相互反应的实验记录a、b与c反应都有气体生成,碳酸钠溶液与硫酸、盐酸反应
均产生二氧化碳气体,则c为碳酸钠溶液,a、b为硫酸、盐酸中的一种,d为氯化钡溶液;b、c与d
反应都有沉淀生成,碳酸钠溶液、硫酸与氯化钡溶液反应分别生成碳酸钡、硫酸钡白色沉淀,
则b为硫酸,a为盐酸。
答案:B
11.下列实际应用中,利用中和反应原理的是( )
①用氢氧化钠溶液洗涤石油产品中的残余硫酸
②用碳酸氢钠治疗胃酸过多
③用熟石灰改良酸性土壤
④用稀氨水涂抹在蚊子叮咬处(分泌出蚁酸)止痒
A.①② B.①②③④
C.②③ D.①③④
解析:①氢氧化钠与硫酸的反应为酸与碱的中和反应;②碳酸氢钠是盐不是碱,故碳酸氢钠与
盐酸反应不属于中和反应;③熟石灰是碱,能与酸性土壤发生中和反应;④稀氨水与蚁酸发生
中和反应。
答案:D
12.室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH) 溶液,烧杯内溶液中的溶质质量变
2
化如图所示(忽略溶液温度的变化),下列分析正确的是( )
A.A点溶液中有两种溶质
B.B点溶液中滴加紫色石蕊溶液,溶液变蓝
C.C点烧杯内液体的pH=7
D.D点溶液中含较多的Ba2+、OH-、S 、H+
解析:A点时,反应没有开始,溶液中有一种溶质HSO ,故A错误。稀硫酸与Ba(OH) 溶液反应
2 4 2
生成硫酸钡沉淀和水,溶质质量减小,C点时二者完全反应,杯内液体的pH=7;B点溶液中有硫
酸,滴加紫色石蕊溶液,溶液变红,故B错误,C正确;C点HSO 完全反应后继续加Ba(OH) 溶
2 4 2
液到D点,D点溶液中应含较多的Ba2+、OH-,故错误,选C。
答案:C
13.如图所示,打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中的导管口没有气
泡产生,则液体A和固体B的组合可能是下列中的( )A.稀盐酸和铁
B.水和生石灰
C.水和氢氧化钠
D.水和氯化钠
解析:稀盐酸和铁反应生成氢气,试管①中的导管口有气泡产生,水和生石灰、固体NaOH都
放出大量热,使试管②内气体受热膨胀,试管①有气泡产生。
答案:D
14.(双选)如图以稀硫酸为例的反应关系体现了酸的化学性质。下列说法正确的是( )
A.X所表示的物质类别是盐
B.图中涉及置换、化合、复分解三种基本反应类型
C.图中能生成盐的反应包括②③④⑤
D.若X溶液既能跟稀硫酸反应,又能跟Ca(OH) 反应,则X可能是BaCl
2 2
解析:酸的通性主要有①跟指示剂反应,②跟活泼金属起置换反应,③跟金属氧化物反应,④跟
某些盐反应,⑤跟碱起中和反应。分析图示的物质种类可知X是盐类物质,A项正确;镁与硫酸
的反应是置换反应,酸与碱、盐的反应属于复分解反应,但图中没有涉及化合反应,B项错误;依
据酸的通性可知金属与硫酸、碱与硫酸、盐与硫酸、金属氧化物与硫酸都可生成盐,所以图中
能生成盐的反应包括②③④⑤,C项正确;依据复分解反应的发生条件可知氯化钡和硫酸能反
应生成硫酸钡沉淀,但氯化钡和氢氧化钙不能反应,D项错误。
答案:AC
15.某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠。某化学
兴趣小组开展如下探究活动:
探究一:除去粗盐中不溶性杂质。
探究二:从滤液1中提取氯化钠固体(该探究中,微溶物不沉淀)。
关于以上探究活动,有下列说法:①试剂甲是碳酸钠溶液,试剂乙是氯化钡溶液
②滤液1中的溶质一定有氯化钠,可能有氯化钙
③若向探究二所得的白色滤渣中加入过量的稀盐酸,滤渣不溶解
[来源:学科网ZXXK]
④往滤液4中加入适量的试剂丙时有中和反应发生
上述说法中正确的是( )
A.①③ B.①④ C.②③ D.②④
解析:某粗盐样品中除含有不溶性固体杂质外,可能还含有少量氯化镁、氯化钙、硫酸钠。溶
解过滤得到滤液1,则滤液1一定有氯化钠;往滤液1中加过量的氢氧化钠溶液,无明显现象,说
明没有氯化镁;硫酸根离子可用BaCl 溶液除去,钙离子可用碳酸钠溶液来除去,但是加入碳酸
2
钠溶液要在加入氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡。往溶液2中加过量
的试剂甲,试剂甲是氯化钡溶液,试剂乙是碳酸钠溶液;由反应现象是无明显现象,说明不含硫
酸钠;往溶液3中加过量的试剂乙(碳酸钠溶液),出现白色沉淀,该沉淀肯定含有过量的氯化钡
与碳酸钠溶液反应生成的碳酸钡白色沉淀,可能存在氯化钙与碳酸钠反应生成的碳酸钙白色
沉淀,滤液1中的溶质一定有氯化钠,可能有氯化钙;若向探究二所得的白色滤渣中加入过量
的稀盐酸,由于该滤渣中含有碳酸钡,可能含有碳酸钙,加入过量的稀盐酸,滤渣全部溶解;往滤
液4中加入适量的试剂丙,丙应为稀盐酸,氢氧化钠与稀盐酸反应生成氯化钠和水,属于中和
反应。由上述分析,②④说法正确。故选D。
答案:D
二、填空题(本题包括5个小题,共23分)
16.(5分)化学源于生活,生活中蕴含着许多化学知识。
(1)醋酸具有挥发性,打开盛装醋酸的瓶盖,会闻到酸味,这是由于分子具有 的性质,醋
酸的pH (填“>”“<”或“=”)7。
(2)用洗涤剂清洗油污,是利用了洗涤剂的 作用。
(3)牛奶中富含的营养物质是 。牛奶常用塑料袋盛装,聚乙烯塑料无毒,用来生产食
品袋、保鲜膜,聚乙烯塑料属于 (填序号)。
①金属材料 ②无机非金属材料 ③合成材料
解析:分子在不停地运动,所以我们会闻到醋酸的酸味。牛奶中富含人体需要的蛋白质,聚乙
烯塑料属于有机合成材料。
答案:(1)不断运动 < (2)乳化 (3)蛋白质 ③
17.(4分)生活、生产、环保等都离不开化学。我们学习了化学知识后,观察物质世界就要从化
学视角来看问题。节假日里,某班同学去郊外进行野炊活动。请回答下列问题:
(1)他们所带的下列物品中,主要材料属于有机合成高分子材料的是 (填序号)。
A.纯净水 B.棉布围裙
C.铝合金锅 D.塑料凳子
(2)学生野炊的食谱如下:
主
馒头
食
配 红烧肉、豆腐汤、牛
菜 肉干
从膳食平衡角度来看,你认为应补充的营养物质是 。
(3)洗涤剂可用来洗碗,是因为它对油污具有 功能。(4)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),可涂抹下列物质之一以减轻疼痛,该物质是
(填序号)。
A.食醋(pH<7)
B.食盐水(pH=7)
C.肥皂水(pH>7)
解析:(1)纯净水属于无机物,棉布属于天然材料,铝合金属于金属材料,塑料属于有机合成材
料;(2)馒头富含糖类,红烧肉富含蛋白质和油脂,豆腐汤含有蛋白质、水和无机盐,牛肉干含有
蛋白质,缺少的营养物质是维生素;(3)洗涤剂可用来洗碗,是因为它对油污具有乳化作用;(4)蚊
虫能分泌出蚁酸,需要涂抹碱性的物质,肥皂水的pH大于7,呈碱性。
答案:(1)D (2)维生素 (3)乳化 (4)C
18.(5分)使用适量的化肥可以让花开得更好。
(1)不同的花卉需要施用不同的化肥,下列属于复合肥的是 (填字母)。
A.硝酸钾(KNO)
3
B.尿素[CO(NH)]
2 2
C.磷酸二氢钙[Ca(HPO )]
2 4 2
D.磷酸氢二铵[(NH )HPO ]
4 2 4
(2)在施用氯化铵时, (填“能”或“不能”)同时施用草木灰等碱性物质,写出氯化铵和
熟石灰反应的化学方程式 。
(3)月季花被称为“花中皇后”,偏碱性的土壤可让它长得更好。如何测定土壤的酸碱度?
;如果土壤呈酸性,则需加入 降低土壤的酸性。
解析:(1)KNO 中含有钾元素和氮元素,属于复合肥,CO(NH ) 中含有氮元素,属于氮
3 2 2
肥,Ca(H PO ) 中含有磷元素,属于磷肥,(NH)HPO 中含有氮元素和磷元素,属于复合肥;(2)铵
2 4 2 4 2 4
态氮肥不能与碱性肥料混合施用,草木灰属于碱性肥料,所以不能混合施用;反应物是氯化铵
和氢氧化钙,生成物是氯化钙、氨气和水,反应的化学方程式是 2NH Cl+Ca(OH)
4 2
CaCl +2H O+2NH ↑;(3)常用pH试纸测定土壤的酸碱度;生活中常用熟石灰改良土壤的酸性。
2 2 3
答案:(1)AD
(2)不能 2NH Cl+Ca(OH) CaCl +2H O+2NH ↑
4 2 2 2 3
(3)用pH试纸测定土壤的酸碱度 熟石灰
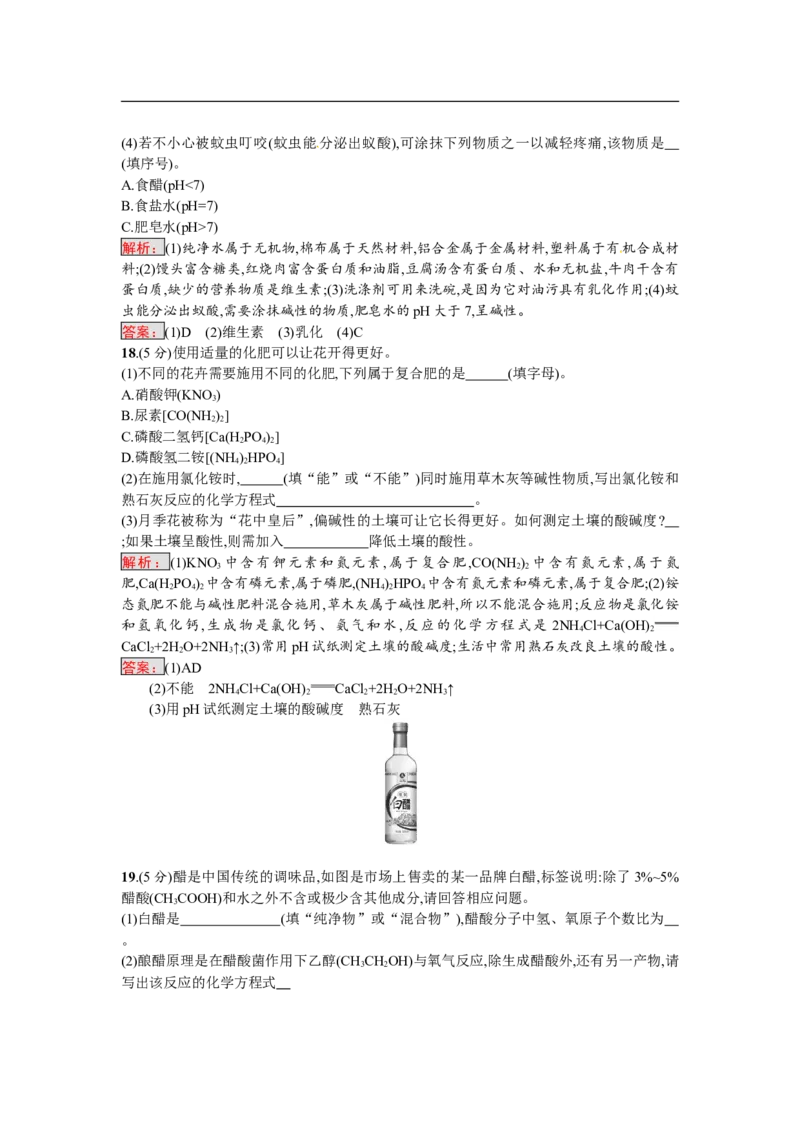
19.(5分)醋是中国传统的调味品,如图是市场上售卖的某一品牌白醋,标签说明:除了3%~5%
醋酸(CHCOOH)和水之外不含或极少含其他成分,请回答相应问题。
3
(1)白醋是 (填“纯净物”或“混合物”),醋酸分子中氢、氧原子个数比为
。
(2)酿醋原理是在醋酸菌作用下乙醇(CHCHOH)与氧气反应,除生成醋酸外,还有另一产物,请
3 2
写出该反应的化学方程式。
(3)已知:HNO 是一元酸,H SO 是二元酸,某同学对白醋性质进行如下探究。
3 2 4
实验操作 实验现象实验结论与解释
观 察 到
①向白醋中滴入 溶 液 变 白醋显酸性
红
②向镁粉中滴加白醋直至过量 白醋能与活泼金属反应
③100 g含醋酸3%的白醋恰好与20 g
— 醋酸为 元酸(填一、二等数字)
10%的NaOH溶液中和
有 少 量
④将白醋滴加到碳酸钙表面 气 泡 产 反应的化学方程式是
生
解析:(1)混合物是由两种或两种以上纯净物混合而成,白醋除了3%~5%醋酸(CHCOOH)和
3
水之外不含或极少含其他成分,所以白醋属于混合物,醋酸分子中氢、氧原子个数比为
4∶2=2∶1。
(2)乙醇和氧气在醋酸菌的作用下生成乙酸和水,化学方程式为CHCHOH+O
3 2 2
CHCOOH+H O。
3 2
(3)酸能使紫色石蕊溶液变红色,醋酸和镁反应会生成醋酸镁和氢气,NaOH为一元碱,根
据CHCOOH和NaOH的质量及反应的化学方程式可知CHCOOH为一元酸,碳酸钙和醋酸
3 3
反应生成醋酸钙、水和二氧化碳。
答案:(1)混合物 2∶1
(2)CH CHOH+O CHCOOH+H O
3 2 2 3 2
(3)①紫色石蕊溶液 ②有气泡产生 ③一
④CaCO +2CH COOH (CHCOO) Ca+CO ↑+H O
3 3 3 2 2 2
20.(4分)盐酸、硫酸、氢氧化钠和氢氧化钙是初中化学中常见的物质,它们有着较广泛的用途。
(1)酸与碱之间能发生 反应,写出一个上述四种物质之间能发生反应的化学方程式:
。
(2)氢氧化钙可以用来调节土壤的 性,它的水溶液常用来检验 气体的存在。
(3)将一定量的稀硫酸与氢氧化钠溶液混合,滴入几滴酚酞溶液,混合液显红色,可推断该溶液
的 pH 7(填“>”“<”或“=”)。要准确测定该溶液的 pH,需要用到的仪器是
。
解析:(1)酸与碱能够发生中和反应生成盐和水,盐酸分别能和氢氧化钠、氢氧化钙发生中和
反应,硫酸分别能与氢氧化钠、氢氧化钙发生中和反应;(2)氢氧化钙常用来改良酸性土壤,由于
二氧化碳具有能使澄清石灰水变浑浊的特性,因此常用澄清石灰水来检验二氧化碳气体的存
在;(3)能使酚酞溶液变红色,说明稀硫酸和氢氧化钠溶液的混合溶液呈碱性,溶液的pH>7,用
pH计可以准确测定溶液的pH。
答案:(1)中和 NaOH+HCl NaCl+H O(合理答案均给分)
2
(2)酸 CO(或二氧化碳)
2
(3)> pH计
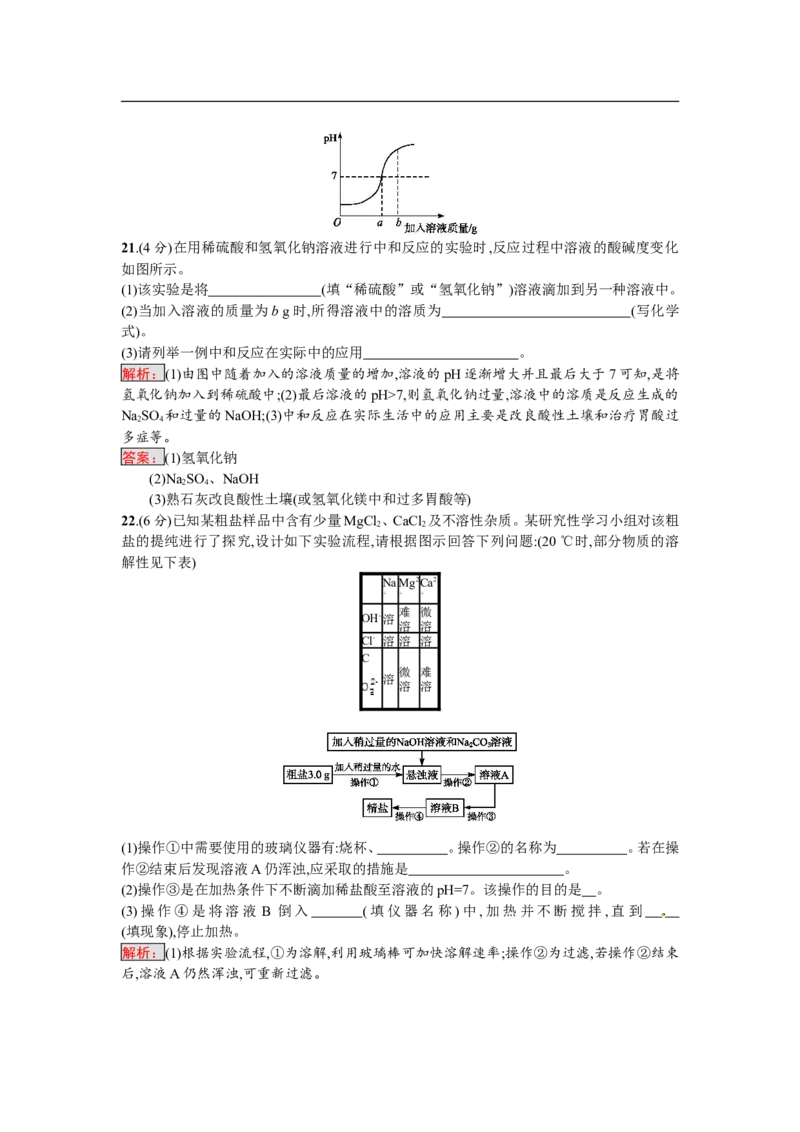
三、简答题(本题包括2个小题,共10分)21.(4分)在用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化
如图所示。
(1)该实验是将 (填“稀硫酸”或“氢氧化钠”)溶液滴加到另一种溶液中。
(2)当加入溶液的质量为b g时,所得溶液中的溶质为 (写化学
式)。
(3)请列举一例中和反应在实际中的应用 。
解析:(1)由图中随着加入的溶液质量的增加,溶液的pH逐渐增大并且最后大于7可知,是将
氢氧化钠加入到稀硫酸中;(2)最后溶液的pH>7,则氢氧化钠过量,溶液中的溶质是反应生成的
NaSO 和过量的NaOH;(3)中和反应在实际生活中的应用主要是改良酸性土壤和治疗胃酸过
2 4
多症等。
答案:(1)氢氧化钠
(2)Na SO 、NaOH
2 4
(3)熟石灰改良酸性土壤(或氢氧化镁中和过多胃酸等)
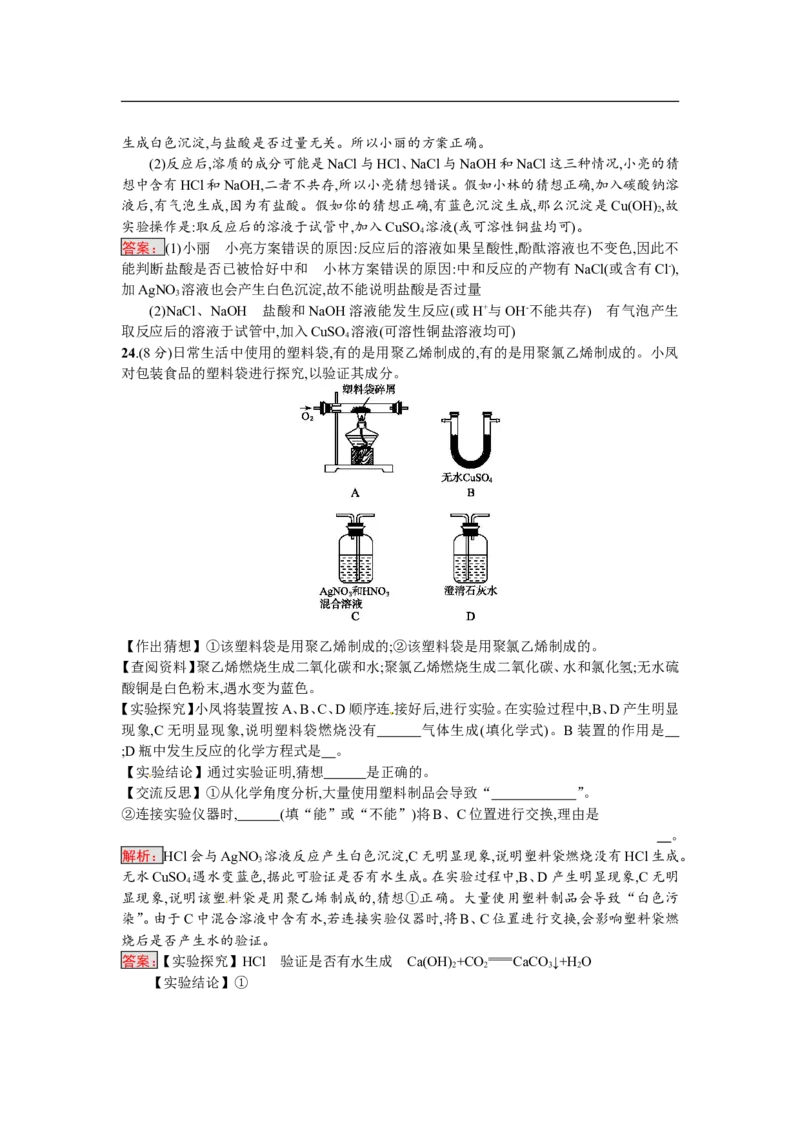
22.(6分)已知某粗盐样品中含有少量MgCl 、CaCl 及不溶性杂质。某研究性学习小组对该粗
2 2
盐的提纯进行了探究,设计如下实验流程,请根据图示回答下列问题:(20 ℃时,部分物质的溶
解性见下表)
NaMg2Ca2
+ + +
难 微
OH-溶
溶 溶
Cl- 溶溶 溶
C
微 难
溶
溶 溶
(1)操作①中需要使用的玻璃仪器有:烧杯、 。操作②的名称为 。若在操
作②结束后发现溶液A仍浑浊,应采取的措施是 。
(2)操作③是在加热条件下不断滴加稀盐酸至溶液的pH=7。该操作的目的是 。
(3)操作④是将溶液 B 倒入 (填仪器名称)中,加热并不断搅拌,直到
(填现象),停止加热。
解析:(1)根据实验流程,①为溶解,利用玻璃棒可加快溶解速率;操作②为过滤,若操作②结束
后,溶液A仍然浑浊,可重新过滤。(2)操作③是由于加入过量的NaOH和NaCO,可加入稀盐酸与NaOH和NaCO 反应,从
2 3 2 3
而除去过量的NaOH和NaCO。
2 3
(3)操作④为滤液的蒸发,蒸发需用蒸发皿,当出现较多量固体时停止加热,利用余热蒸干
即可得到精盐。
答案:(1)玻璃棒 过滤 重新过滤 (2)除去过量的NaOH和NaCO (3)蒸发皿 蒸发皿中
2 3
出现较多量固体
四、实验探究题(本题包括2个小题,共16分)
23.(8分)某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请同学
们一起参与此次探究之旅。
[来源:Z,xx,k.Com]
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小亮、小丽、小林三位同学设计了如下方案进行探究:
方 案
方案预
设 方案步骤 方案预估现象
估结论
计者
取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞溶液, 酚酞溶液不变恰好完
小亮
振荡 色 全中和
用一根洁净的玻璃棒蘸取反应后的溶液点在pH试纸上,把试纸呈现的颜 恰好完
小丽 pH=7
色与标准比色卡对照 全中和
盐 酸 过
有白色沉淀生量,
小林 取少量反应后的溶液于一支试管中,并向试管中滴加稀硝酸和硝酸银溶液
成 没有完
全中和
【方案评价】请判断以上设计的三个方案中, 同学的方案是正确的。
【方案反思】请分析另外两个方案错误的原因:
;
。
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有 (填化学式)
小丽认为小亮的猜想是错误的,她的理由是
。
【实验设计及验证】请你将下列实验报告填写完整:
实验现实验结
实验操作
象 论
取反应后的溶液
于试 小林猜
管中,加入碳酸钠 想正确
溶液
有蓝色
你的猜
沉
想正确
淀生成
解析:(1)三种方案中,溶液使酚酞溶液不变色,可能是酸性或中性,所以小亮的结论错误;小丽
用pH试纸检测,pH=7说明溶液显中性,恰好完全反应;溶液中只要有氯离子,加入硝酸银就能生成白色沉淀,与盐酸是否过量无关。所以小丽的方案正确。
(2)反应后,溶质的成分可能是NaCl与HCl、NaCl与NaOH和NaCl这三种情况,小亮的猜
想中含有HCl和NaOH,二者不共存,所以小亮猜想错误。假如小林的猜想正确,加入碳酸钠溶
液后,有气泡生成,因为有盐酸。假如你的猜想正确,有蓝色沉淀生成,那么沉淀是Cu(OH) ,故
2
实验操作是:取反应后的溶液于试管中,加入CuSO 溶液(或可溶性铜盐均可)。
4
答案:(1)小丽 小亮方案错误的原因:反应后的溶液如果呈酸性,酚酞溶液也不变色,因此不
能判断盐酸是否已被恰好中和 小林方案错误的原因:中和反应的产物有NaCl(或含有Cl-),
加AgNO 溶液也会产生白色沉淀,故不能说明盐酸是否过量
3
(2)NaCl、NaOH 盐酸和NaOH溶液能发生反应(或H+与OH-不能共存) 有气泡产生
取反应后的溶液于试管中,加入CuSO 溶液(可溶性铜盐溶液均可)
4
24.(8分)日常生活中使用的塑料袋,有的是用聚乙烯制成的,有的是用聚氯乙烯制成的。小凤
对包装食品的塑料袋进行探究,以验证其成分。
【作出猜想】①该塑料袋是用聚乙烯制成的;②该塑料袋是用聚氯乙烯制成的。
【查阅资料】聚乙烯燃烧生成二氧化碳和水;聚氯乙烯燃烧生成二氧化碳、水和氯化氢;无水硫
酸铜是白色粉末,遇水变为蓝色。
【实验探究】小凤将装置按A、B、C、D顺序连接好后,进行实验。在实验过程中,B、D产生明显
现象,C无明显现象,说明塑料袋燃烧没有 气体生成(填化学式)。B装置的作用是
;D瓶中发生反应的化学方程式是 。
【实验结论】通过实验证明,猜想 是正确的。
【交流反思】①从化学角度分析,大量使用塑料制品会导致“ ”。
②连接实验仪器时, (填“能”或“不能”)将B、C位置进行交换,理由是
。
解析:HCl会与AgNO 溶液反应产生白色沉淀,C无明显现象,说明塑料袋燃烧没有HCl生成。
3
无水CuSO 遇水变蓝色,据此可验证是否有水生成。在实验过程中,B、D产生明显现象,C无明
4
显现象,说明该塑料袋是用聚乙烯制成的,猜想①正确。大量使用塑料制品会导致“白色污
染”。由于C中混合溶液中含有水,若连接实验仪器时,将B、C位置进行交换,会影响塑料袋燃
烧后是否产生水的验证。
答案:【实验探究】HCl 验证是否有水生成 Ca(OH) +CO CaCO ↓+H O
2 2 3 2
【实验结论】①【交流反思】①白色污染 ②不能 如果将B、C位置进行交换,气体从C中出来再检验
到有水分,就不能充分说明水是燃烧时生成的,还是从C装置中带出来的
五、计算题(6分)
25.(6分)将250 g含杂质(杂质不参加反应,也不溶于水)40%的大理石放到500 g稀盐酸中,恰
好完全反应。求:
(1)生成二氧化碳多少克?
(2)所用稀盐酸的溶质质量分数是多少?
(3)所得溶液的溶质质量分数是多少?
解析:由碳酸钙的质量及化学方程式CaCO +2HCl CaCl +H O+CO↑,求出参加反应HCl
3 2 2 2
的质量以及生成二氧化碳和氯化钙的质量,然后求出所用稀盐酸的溶质质量分数以及所得溶
液的溶质质量分数。
答案:解:样品中碳酸钙的质量为250 g×(1-40%)=150 g
设稀盐酸中溶质的质量为x,生成二氧化碳的质量为y,生成氯化钙的质量为z。
CaCO +2HCl CaCl +H O+CO↑
3 2 2 2
100 73 111 44
150 g x z y
解得:x=109.5 g
解得:y=66 g
解得:z=166.5 g
所用稀盐酸的溶质质量分数是 ×100%=21.9%,
所得溶液中溶质质量分数为 ×100%≈28.5%。
答:(1)生成二氧化碳的质量为66 g。
(2)稀盐酸中溶质的质量分数为21.9%。
(3)所得溶液中溶质的质量分数为28.5%。