文档内容
阶段检测四 金属和金属材料
(时间:90分钟 满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cu 64 Zn 65 Ag 108
一、选择题(每小题只有一个选项符合题意,每小题3分,共45分)
1.为了减缓铁制品的锈蚀,下列做法不当的是( )
[来源:学_科_网]
A.在车、船的表面喷涂油漆
B.将使用后的菜刀用布擦干
C.洗净铁制品表面的油膜
D.在铁制品表面镀上一层锌
解析:A.在车、船的表面喷涂油漆能够防止生锈,做法正确;B.将使用后的菜刀用布擦干,能减
缓铁制品的锈蚀,做法正确;C.洗净铁制品表面的油膜,使铁与氧气和水接触,容易生锈,做法错
误;D.在铁制品表面镀上一层锌,能够防止生锈,做法正确。
答案:C
2.人们常把金、银、铜、铁、锡五种金属统称为“五金”。下列相关叙述错误的是( )
A.铁锅应用了铁的导热性
B.金的化学性质最不活泼
C.金属银可与硝酸铜溶液发生置换反应
D.焊锡(锡铅合金)比锡熔点要低
解析:通过金属活动性顺序分析可知,银的金属活动性比铜弱,所以金属银不与硝酸铜溶液发
生置换反应,C项错误。
答案:C
[来源:学科网]
3.将少量灰黑色的生铁粉末,投入到盛有过量稀硫酸的烧杯中,充分搅拌,待完全反应后过滤,
滤纸上留有黑色的残渣。该黑色残渣的主要成分是( )
A.铁 B.碳
C.铁、碳混合物 D.硫酸亚铁
解析:生铁是铁碳合金,故生铁中除铁以外的物质主要是碳,因为硫酸过量,铁完全反应,所以
剩余的黑色残渣主要成分是碳。
答案:B
4.下列有关金属材料的说法正确的是( )
A.硬铝片比纯铝片硬度小
B.钢的性能优良,是很纯的铁
C.沙漠地区的铁制品锈蚀较快
D.为防止钢铁生锈,可在其表面涂油
解析:合金比组成它的纯金属硬度大,因此硬铝片比纯铝片硬度大,故A错误;钢的性能优良,
它是铁的合金不是纯铁,故B错误;沙漠地区空气干燥,因此铁制品锈蚀较慢,故C正确;在钢铁
表面涂油,可以防止钢铁与水、氧气接触,防止生锈,故D正确。
答案:D
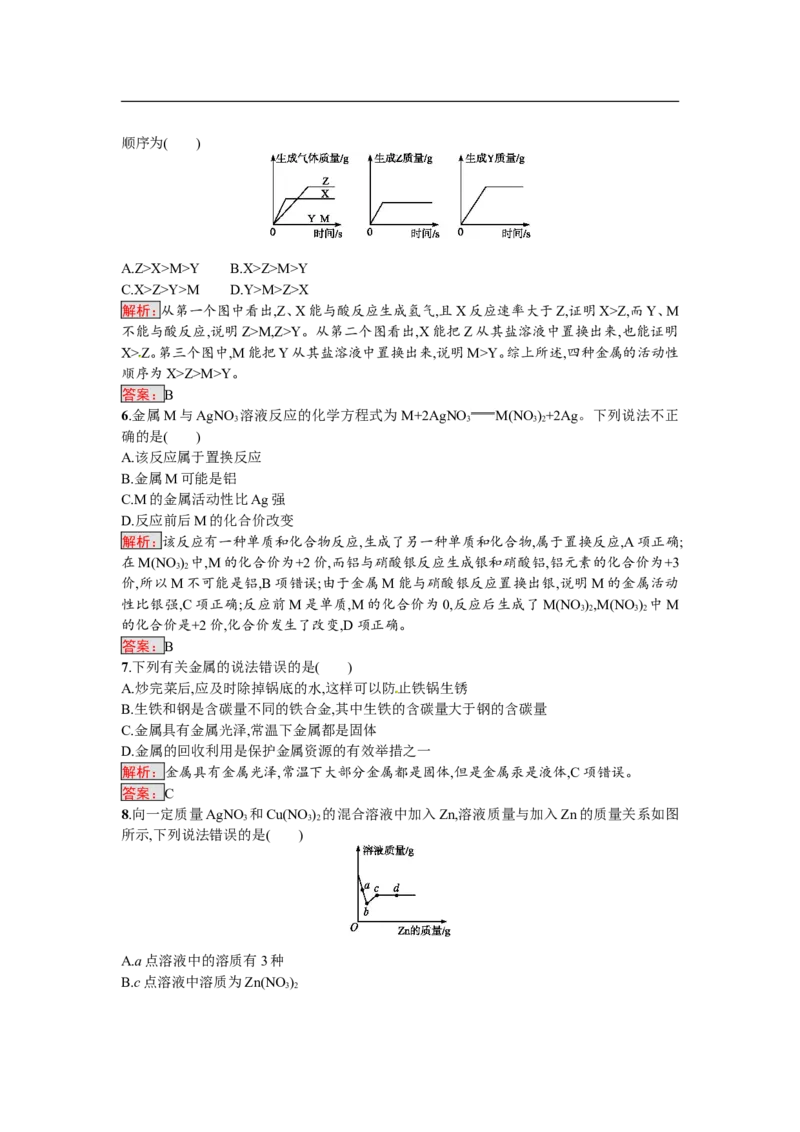
5.把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中,再把X加入
到Z(NO ) 溶液中,M加入到YNO 溶液中。反应关系如图所示。据此判断四种金属的活动性
3 2 3顺序为( )
A.Z>X>M>Y B.X>Z>M>Y
C.X>Z>Y>M D.Y>M>Z>X
解析:从第一个图中看出,Z、X能与酸反应生成氢气,且X反应速率大于Z,证明X>Z,而Y、M
不能与酸反应,说明Z>M,Z>Y。从第二个图看出,X能把Z从其盐溶液中置换出来,也能证明
X>Z。第三个图中,M能把Y从其盐溶液中置换出来,说明M>Y。综上所述,四种金属的活动性
顺序为X>Z>M>Y。
答案:B
6.金属M与AgNO 溶液反应的化学方程式为M+2AgNO M(NO)+2Ag。下列说法不正
3 3 3 2
确的是( )
A.该反应属于置换反应
B.金属M可能是铝
C.M的金属活动性比Ag强
D.反应前后M的化合价改变
解析:该反应有一种单质和化合物反应,生成了另一种单质和化合物,属于置换反应,A项正确;
在M(NO) 中,M的化合价为+2价,而铝与硝酸银反应生成银和硝酸铝,铝元素的化合价为+3
3 2
价,所以M不可能是铝,B项错误;由于金属M能与硝酸银反应置换出银,说明M的金属活动
性比银强,C项正确;反应前M是单质,M的化合价为0,反应后生成了M(NO),M(NO ) 中M
3 2 3 2
的化合价是+2价,化合价发生了改变,D项正确。
答案:B
7.下列有关金属的说法错误的是( )
A.炒完菜后,应及时除掉锅底的水,这样可以防止铁锅生锈
B.生铁和钢是含碳量不同的铁合金,其中生铁的含碳量大于钢的含碳量
C.金属具有金属光泽,常温下金属都是固体
D.金属的回收利用是保护金属资源的有效举措之一
解析:金属具有金属光泽,常温下大部分金属都是固体,但是金属汞是液体,C项错误。
答案:C
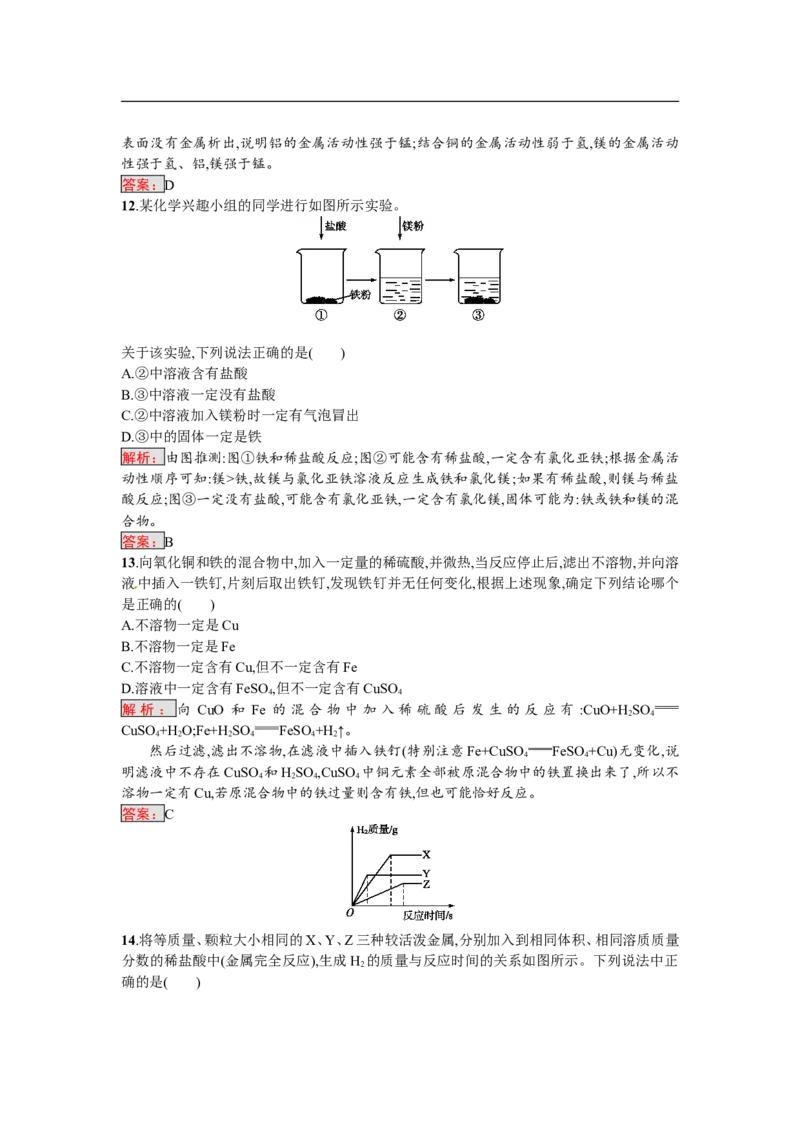
8.向一定质量AgNO 和Cu(NO ) 的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图
3 3 2
所示,下列说法错误的是( )
A.a点溶液中的溶质有3种
B.c点溶液中溶质为Zn(NO )
3 2C.若取b~c段溶液,滴加稀盐酸,不会产生白色沉淀
D.取d点时的固体,加入稀盐酸,无气泡产生
解析:在金属活动性顺序中,Zn>Cu>Ag,向一定质量AgNO 和Cu(NO ) 的混合溶液中加入
3 3 2
Zn,Zn与AgNO 和Cu(NO ) 两种溶质依次发生反应。
3 3 2
Zn+2AgNO Zn(NO )+2Ag
3 3 2
65 216
所以析出银的过程是溶液质量减少的过程;
Zn+Cu(NO ) Zn(NO )+Cu
3 2 3 2
65 64
所以析出铜的过程是溶液质量增加的过程。
在a点时,硝酸银没有全部参加反应,溶液中含有硝酸银、硝酸铜和生成的硝酸锌,溶质是
3种,A项正确;c点时硝酸铜恰好完全反应,溶液中只有硝酸锌,B项正确;b~c段是硝酸银全部
参加反应完后,锌和硝酸铜反应的过程,因此滴加稀盐酸,不会产生白色沉淀,C项正确;d点时
锌过量,因此加入稀盐酸会产生氢气,D项错误。
答案:D
9.小明发现月饼盒里的脱氧剂部分呈红褐色,查阅资料得知脱氧剂中含有铁粉和活性炭。他
猜想这包脱氧剂中可能含有:① Cu 和 C;② Fe O 和 C;③ Fe O 和 C;④ Fe O 、C 和 Fe;
2 3 3 4 3 4
⑤Fe O、C和Fe。其中猜想合理的是( )
2 3
A.①③⑤ B.②④⑤
C.②⑤ D.④⑤
解析:脱氧剂是在常温下能与氧气发生反应的物质,该脱氧剂与氧气反应后生成红色物质。①
不合理;②中Fe O 是红色物质,合理;Fe O 是黑色,③④不合理;脱氧剂中的铁可能部分生锈,
2 3 3 4
⑤合理。故选C。
答案:C
10.(2016河北中考)下列验证Zn、Fe、Ag三种金属活动性顺序的实验方案中(“—”表示未进行
金属与盐溶液之间的实验),不能达到实验目的的是( )
选项
A B C D
金属
盐溶液
ZnSO 溶
4 —FeAgFe
液
FeSO 溶
4 ZnAgZn—
液
AgNO 溶
3 Fe——Fe
液
答案:C
11.硬铝的组成金属有铝、镁、铜、锰等。已知:锰丝放入稀硫酸中,有气泡产生;锰丝放入硫酸铝
溶液中,表面没有金属析出。结合我们所学金属在溶液中的活动性顺序,下列有关金属的活动
性强弱判断错误的是( )
A.Mn强于Cu B.Al强于Mn
C.Mg强于Al D.Mn强于Mg
解析:锰丝放入稀硫酸中,有气泡产生,说明锰的金属活动性强于氢;锰丝放入硫酸铝溶液中,表面没有金属析出,说明铝的金属活动性强于锰;结合铜的金属活动性弱于氢,镁的金属活动
性强于氢、铝,镁强于锰。
[来源:Z#xx#k.Com]
答案:D
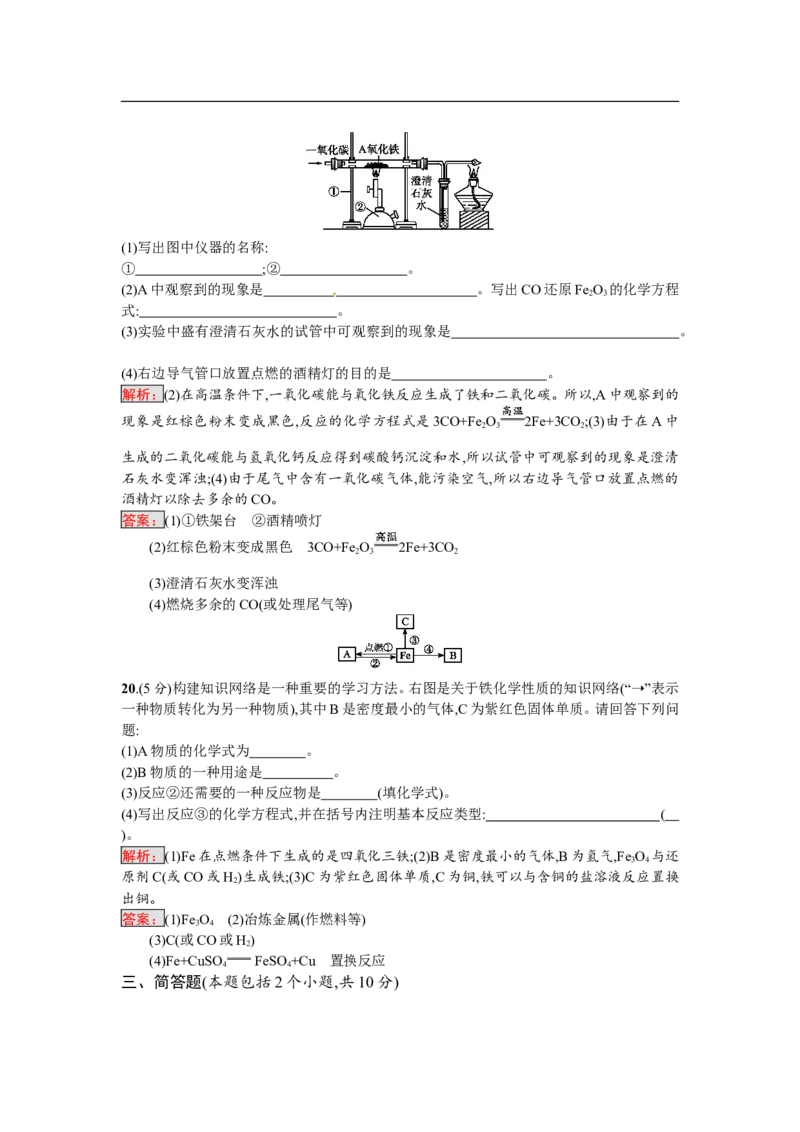
12.某化学兴趣小组的同学进行如图所示实验。
关于该实验,下列说法正确的是( )
A.②中溶液含有盐酸
B.③中溶液一定没有盐酸
C.②中溶液加入镁粉时一定有气泡冒出
D.③中的固体一定是铁
解析:由图推测:图①铁和稀盐酸反应;图②可能含有稀盐酸,一定含有氯化亚铁;根据金属活
动性顺序可知:镁>铁,故镁与氯化亚铁溶液反应生成铁和氯化镁;如果有稀盐酸,则镁与稀盐
酸反应;图③一定没有盐酸,可能含有氯化亚铁,一定含有氯化镁,固体可能为:铁或铁和镁的混
合物。
答案:B
13.向氧化铜和铁的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向溶
液中插入一铁钉,片刻后取出铁钉,发现铁钉并无任何变化,根据上述现象,确定下列结论哪个
是正确的( )
A.不溶物一定是Cu
B.不溶物一定是Fe
C.不溶物一定含有Cu,但不一定含有Fe
D.溶液中一定含有FeSO ,但不一定含有CuSO
4 4
解析: 向 CuO 和 Fe 的混合物中加入稀硫酸后发生的反应有 :CuO+H SO
2 4
CuSO +H O;Fe+H SO FeSO +H ↑。
4 2 2 4 4 2
然后过滤,滤出不溶物,在滤液中插入铁钉(特别注意Fe+CuSO FeSO +Cu)无变化,说
4 4
明滤液中不存在CuSO 和HSO ,CuSO 中铜元素全部被原混合物中的铁置换出来了,所以不
4 2 4 4
溶物一定有Cu,若原混合物中的铁过量则含有铁,但也可能恰好反应。
答案:C
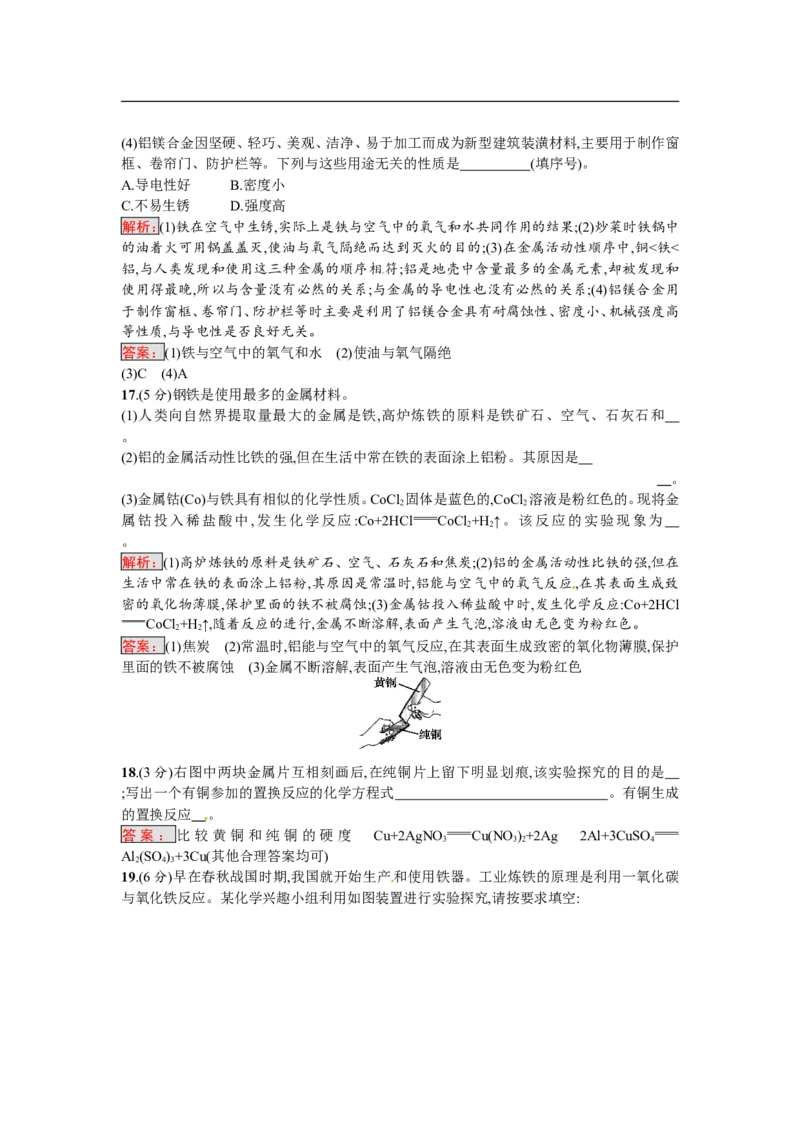
14.将等质量、颗粒大小相同的X、Y、Z三种较活泼金属,分别加入到相同体积、相同溶质质量
分数的稀盐酸中(金属完全反应),生成H 的质量与反应时间的关系如图所示。下列说法中正
2
确的是( )A.消耗稀盐酸的质量顺序为Z>Y>X
B.产生氢气的速率顺序为X>Y>Z
C.三种金属的活动性顺序为Y>X>Z
D.相对原子质量由大到小的顺序为Z>Y>X
解析:由生成H 的质量与反应时间的关系图可知,三种金属完全反应放出氢气的质量由大到
2
小的顺序为X>Y>Z,则消耗稀盐酸的质量顺序为X>Y>Z,A项错误;同一时间内,产生氢气由
多到少的顺序为Y>X>Z,因此产生氢气的速率顺序应为Y>X>Z,同时可判断三种金属的活动
性顺序为Y>X>Z,B项错误,C项正确;由生成H 的质量与反应时间的关系图可知,三种等质量
2
的金属完全反应放出氢气的质量由大到小的顺序为X>Y>Z,根据一定量金属完全反应产生
氢气质量= ×金属的质量可知,要比较相对原子质量大小还需要知道三种金
属的化合价,因此,无法比较三种金属相对原子质量的大小,D项错误。
答案:C
15.为从废铜屑中得到较纯的单质铜,某探究小组设计了如下方案。有关说法正确的是( )
废铜屑 氧化铜 氯化铜 铜
A.若X是铁,第③步反应还会生成氯化铁
B.X还可以是锌,但不能是银
C.仅用第②③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
解析:若X为铁,与氯化铜反应生成铜和氯化亚铁,A项错误;锌的金属活动性比铜的强,可以
置换出铜,但银的金属活动性比铜的弱,不能置换出铜,所以X可以是锌,不能是银,B项正确;铜
在金属活动性顺序中,排在氢的后面,不能直接与盐酸反应,仅用②③步操作不能达到实验目
的,C项错误;第②步反应后的溶液中含有氯化铜,加入的硝酸银溶液与氯化铜反应可生成白
色沉淀,故不能证明盐酸过量,D项错误。
答案:B
二、填空题(本题包括5个小题,共23分)
[来源:Zxxk.Com]
16.(4分)人类的生产、生活离不开金属。如图是铁锅示意图。
(1)铁锅生锈实际是 发生化学反应所致。
(2)炒菜时铁锅里的油着火可用锅盖盖灭的原因是 。
(3)铜、铁、铝三种金属,依次被人类发现和利用。以下三个选项中与人类大规模发现和使用金
属最有关的是 (填序号)。
A.地壳中金属元素的含量
B.金属的导电性
C.金属活动性(4)铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗
框、卷帘门、防护栏等。下列与这些用途无关的性质是 (填序号)。
A.导电性好 B.密度小
C.不易生锈 D.强度高
解析:(1)铁在空气中生锈,实际上是铁与空气中的氧气和水共同作用的结果;(2)炒菜时铁锅中
的油着火可用锅盖盖灭,使油与氧气隔绝而达到灭火的目的;(3)在金属活动性顺序中,铜<铁<
铝,与人类发现和使用这三种金属的顺序相符;铝是地壳中含量最多的金属元素,却被发现和
使用得最晚,所以与含量没有必然的关系;与金属的导电性也没有必然的关系;(4)铝镁合金用
于制作窗框、卷帘门、防护栏等时主要是利用了铝镁合金具有耐腐蚀性、密度小、机械强度高
等性质,与导电性是否良好无关。
答案:(1)铁与空气中的氧气和水 (2)使油与氧气隔绝
(3)C (4)A
17.(5分)钢铁是使用最多的金属材料。
(1)人类向自然界提取量最大的金属是铁,高炉炼铁的原料是铁矿石、空气、石灰石和
。
(2)铝的金属活动性比铁的强,但在生活中常在铁的表面涂上铝粉。其原因是
。
(3)金属钴(Co)与铁具有相似的化学性质。CoCl 固体是蓝色的,CoCl 溶液是粉红色的。现将金
2 2
属钴投入稀盐酸中,发生化学反应:Co+2HCl CoCl +H ↑。该反应的实验现象为
2 2
。
解析:(1)高炉炼铁的原料是铁矿石、空气、石灰石和焦炭;(2)铝的金属活动性比铁的强,但在
生活中常在铁的表面涂上铝粉,其原因是常温时,铝能与空气中的氧气反应,在其表面生成致
密的氧化物薄膜,保护里面的铁不被腐蚀;(3)金属钴投入稀盐酸中时,发生化学反应:Co+2HCl
CoCl +H ↑,随着反应的进行,金属不断溶解,表面产生气泡,溶液由无色变为粉红色。
2 2
答案:(1)焦炭 (2)常温时,铝能与空气中的氧气反应,在其表面生成致密的氧化物薄膜,保护
里面的铁不被腐蚀 (3)金属不断溶解,表面产生气泡,溶液由无色变为粉红色
18.(3分)右图中两块金属片互相刻画后,在纯铜片上留下明显划痕,该实验探究的目的是
;写出一个有铜参加的置换反应的化学方程式 。有铜生成
的置换反应 。
答案: 比较黄铜和纯铜的硬度 Cu+2AgNO Cu(NO )+2Ag 2Al+3CuSO
3 3 2 4
Al (SO )+3Cu(其他合理答案均可)
2 4 3
19.(6分)早在春秋战国时期,我国就开始生产和使用铁器。工业炼铁的原理是利用一氧化碳
与氧化铁反应。某化学兴趣小组利用如图装置进行实验探究,请按要求填空:(1)写出图中仪器的名称:
① ;② 。
(2)A中观察到的现象是 。写出CO还原Fe O 的化学方程
2 3
式: 。
(3)实验中盛有澄清石灰水的试管中可观察到的现象是 。
(4)右边导气管口放置点燃的酒精灯的目的是 。
解析:(2)在高温条件下,一氧化碳能与氧化铁反应生成了铁和二氧化碳。所以,A中观察到的
现象是红棕色粉末变成黑色,反应的化学方程式是3CO+Fe O 2Fe+3CO ;(3)由于在A中
2 3 2
生成的二氧化碳能与氢氧化钙反应得到碳酸钙沉淀和水,所以试管中可观察到的现象是澄清
石灰水变浑浊;(4)由于尾气中含有一氧化碳气体,能污染空气,所以右边导气管口放置点燃的
酒精灯以除去多余的CO。
答案:(1)①铁架台 ②酒精喷灯
(2)红棕色粉末变成黑色 3CO+Fe O 2Fe+3CO
2 3 2
(3)澄清石灰水变浑浊
(4)燃烧多余的CO(或处理尾气等)
20.(5分)构建知识网络是一种重要的学习方法。右图是关于铁化学性质的知识网络(“➝”表示
一种物质转化为另一种物质),其中B是密度最小的气体,C为紫红色固体单质。请回答下列问
题:
(1)A物质的化学式为 。
(2)B物质的一种用途是 。
(3)反应②还需要的一种反应物是 (填化学式)。
(4)写出反应③的化学方程式,并在括号内注明基本反应类型: (
)。
解析:(1)Fe在点燃条件下生成的是四氧化三铁;(2)B是密度最小的气体,B为氢气,Fe O 与还
3 4
原剂C(或CO或H)生成铁;(3)C为紫红色固体单质,C为铜,铁可以与含铜的盐溶液反应置换
2
出铜。
答案:(1)Fe O (2)冶炼金属(作燃料等)
3 4
(3)C(或CO或H)
2
(4)Fe+CuSO FeSO+Cu 置换反应
4 4
三、简答题(本题包括2个小题,共10分)21.(4分)某地根据当地资源特点将石灰石的开采、加工和高炉炼铁连在一起形成联产。
(1)炼铁的固体原料有铁矿石、焦炭和 。请写出炼铁过程中CO和Fe O 反应的化学
2 3
方程式: 。
(2)高炉炼铁排放的废气中含有大量的高温一氧化碳,可作为能源用来煅烧石灰石。请写出煅
烧石灰石的化学方程式: 。
(3)此联产方式的主要优点是 。(答出一点即可)
答案:(1)石灰石 3CO+Fe O 2Fe+3CO
2 3 2
(2)CaCO CaO+CO ↑
3 2
(3)降低成本(变废为宝,节约能源)
22.(6分)某工业废料含氧化铜和氧化铁,经过处理后可得到铜和硫酸亚铁溶液,主要流程如图。
已知:CuO+H SO CuSO +H O Fe+Fe (SO ) 3FeSO
2 4 4 2 2 4 3 4
(1) 过 程 Ⅰ 中 氧 化 铁 溶 解 的 化 学 方 程 式 是
。
(2)过程Ⅱ充分反应后,还应有的实验操作是 ,该过程中发生的化
学基本反应类型是 (填基本反应类型名称)。
(3)过程Ⅲ加入适量A的作用是 ;该过程中的实验现
象是
。
(4)A~F中含铁元素的有 (填序号)。
解析:(1)要最终得到铜和硫酸亚铁,则溶解氧化铜和氧化铁使用的酸是稀硫酸,氧化铁能与稀
硫酸反应生成硫酸铁和水;(2)由于溶液B中含有硫酸铜、硫酸铁和稀硫酸,要得到铜和硫酸亚
铁溶液,就要除去稀硫酸,因此要加入过量的铁,然后过滤得到固体铜和铁的混合物D以及硫
酸亚铁F,该过程中发生两个反应,铁与硫酸铜反应生成硫酸亚铁和铜,该反应是置换反应;铁
与硫酸铁反应生成硫酸亚铁,该反应是化合反应;(3)为了除去铜中的铁,并将铁转化为硫酸亚
铁,需要加入稀硫酸将过量的铁除去;铁与硫酸反应生成硫酸亚铁和氢气,硫酸亚铁的溶液呈
浅绿色;(4)根据分析推断,A中含有硫酸,B中含有硫酸铜和硫酸铁,C是铁,D中含有铁和铜,E
是铜,F中含有硫酸亚铁。
答案:(1)Fe O+3H SO Fe (SO )+3H O
2 3 2 4 2 4 3 2
(2)过滤 化合反应、置换反应
(3)除去剩余的铁,得到纯净的铜 有气体生成,溶液由无色逐渐变为浅绿色
(4)BCDF
四、实验探究题(本题包括2个小题,共16分)
23.(6分)黄铜是铜锌合金。黄铜渣中除含Cu、Zn外,还含ZnO和CuO。处理黄铜渣可得到硫
酸锌,其主要流程如下:(1)步骤Ⅰ、Ⅱ中进行的操作为 。
(2)步骤Ⅰ实验中也可验证两种金属的活动性顺序,写出判断依据 。
(3)为什么步骤Ⅱ中加入过量的锌?
(4)若将黄铜渣中的ZnO和CuO除去得到黄铜合金,写出实验操作步骤及预期现象。
解析:(1)从流程图看出:步骤Ⅰ、Ⅱ都需要进行分离液体与固体混合物的操作,因而是过滤。
(2)金属活动性顺序中,排在氢前面的金属可以将酸中的氢置换出来,排在氢后面的金属
不能置换酸中的氢,步骤Ⅰ中加入稀硫酸,锌会与硫酸反应生成硫酸锌和氢气,铜不会与稀硫
酸反应,可以判断出锌的活动性比铜强。
(3)加入过量的锌既可以将CuSO 中的Cu置换出来,又可以使溶液A中的硫酸完全反应。
4
(4)某些金属氧化物在高温条件下会与碳反应生成相应金属和二氧化碳,所以操作步骤是:
取样品,加入木炭粉高温加热,黑色的氧化铜和白色的氧化锌会转化为金黄色的金属混合物。
答案:(1)过滤
(2)锌会与硫酸反应生成硫酸锌和氢气,铜不会与硫酸反应
(3)置换出CuSO 中的Cu并使溶液A中的硫酸完全反应。
4
(4)取样品,加入木炭粉高温加热,黑色的氧化铜和白色的氧化锌会转化为金黄色的金属
混合物。
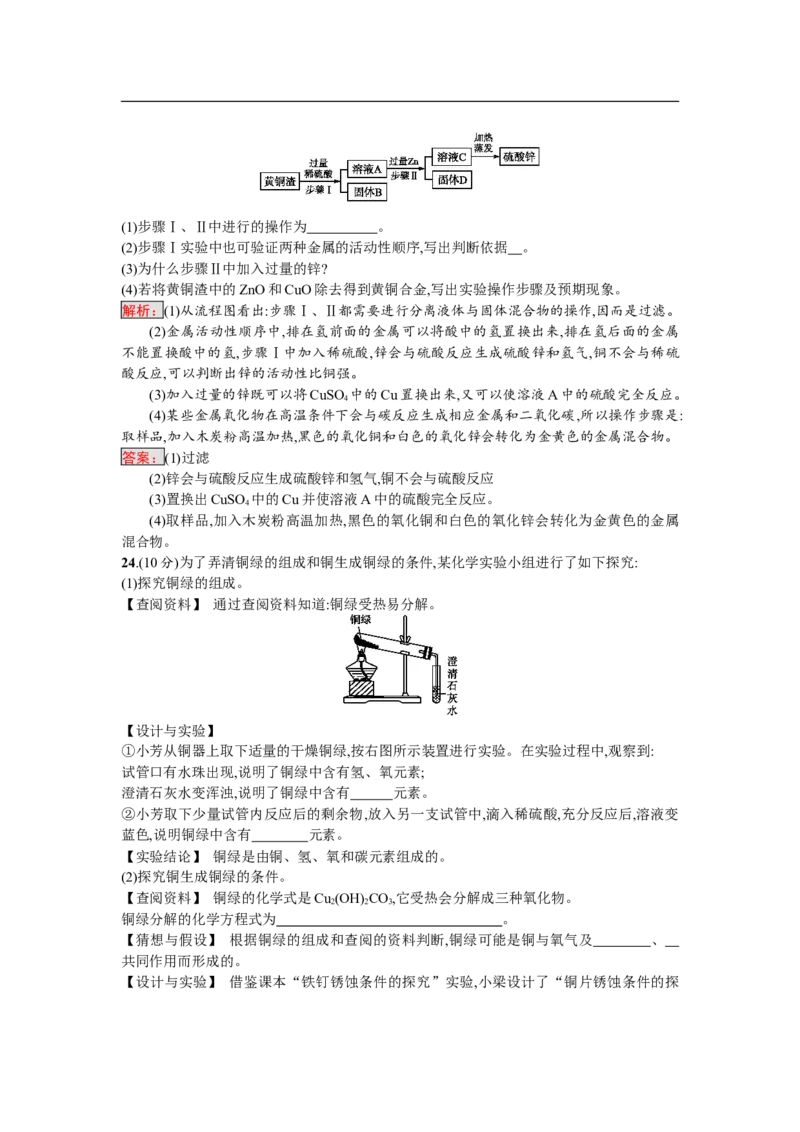
24.(10分)为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
(1)探究铜绿的组成。
【查阅资料】 通过查阅资料知道:铜绿受热易分解。
【设计与实验】
①小芳从铜器上取下适量的干燥铜绿,按右图所示装置进行实验。在实验过程中,观察到:
试管口有水珠出现,说明了铜绿中含有氢、氧元素;
澄清石灰水变浑浊,说明了铜绿中含有 元素。
②小芳取下少量试管内反应后的剩余物,放入另一支试管中,滴入稀硫酸,充分反应后,溶液变
蓝色,说明铜绿中含有 元素。
【实验结论】 铜绿是由铜、氢、氧和碳元素组成的。
(2)探究铜生成铜绿的条件。
【查阅资料】 铜绿的化学式是Cu (OH) CO,它受热会分解成三种氧化物。
2 2 3
铜绿分解的化学方程式为 。
【猜想与假设】 根据铜绿的组成和查阅的资料判断,铜绿可能是铜与氧气及 、
共同作用而形成的。
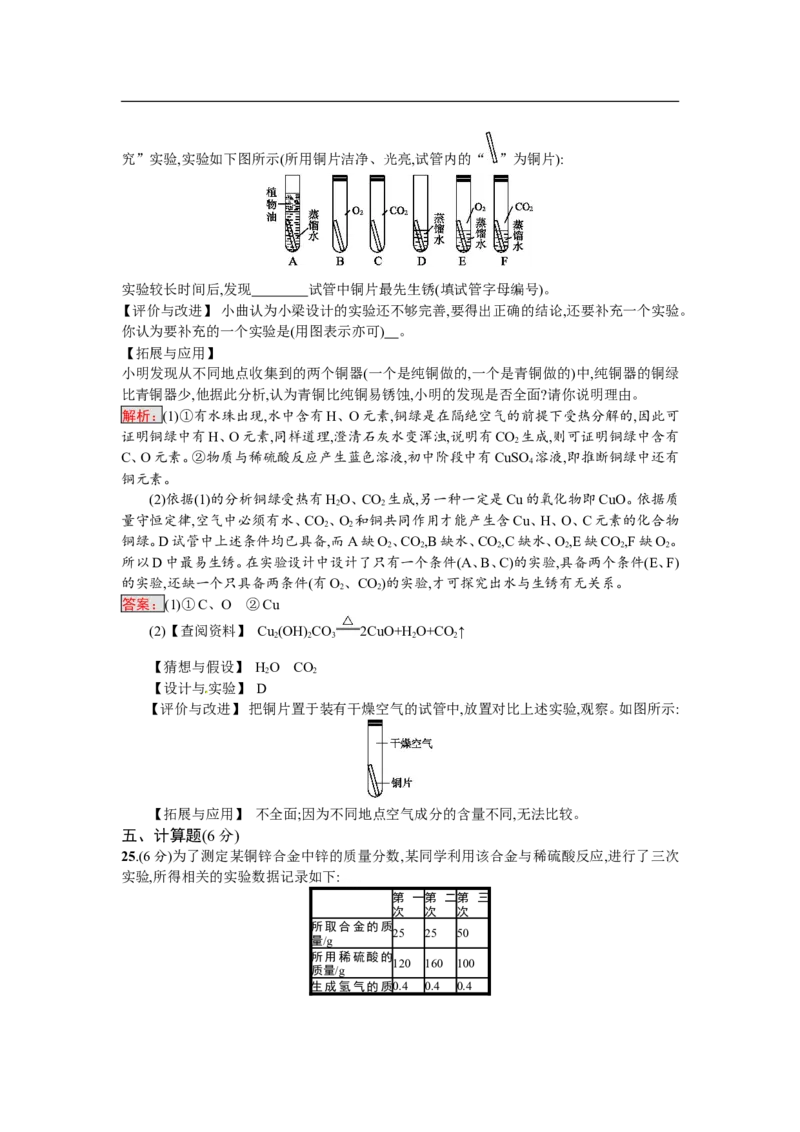
【设计与实验】 借鉴课本“铁钉锈蚀条件的探究”实验,小梁设计了“铜片锈蚀条件的探究”实验,实验如下图所示(所用铜片洁净、光亮,试管内的“ ”为铜片):
实验较长时间后,发现 试管中铜片最先生锈(填试管字母编号)。
【评价与改进】 小曲认为小梁设计的实验还不够完善,要得出正确的结论,还要补充一个实验。
你认为要补充的一个实验是(用图表示亦可) 。
【拓展与应用】
小明发现从不同地点收集到的两个铜器(一个是纯铜做的,一个是青铜做的)中,纯铜器的铜绿
比青铜器少,他据此分析,认为青铜比纯铜易锈蚀,小明的发现是否全面?请你说明理由。
解析:(1)①有水珠出现,水中含有H、O元素,铜绿是在隔绝空气的前提下受热分解的,因此可
证明铜绿中有H、O元素,同样道理,澄清石灰水变浑浊,说明有CO 生成,则可证明铜绿中含有
2
C、O元素。②物质与稀硫酸反应产生蓝色溶液,初中阶段中有CuSO 溶液,即推断铜绿中还有
4
铜元素。
(2)依据(1)的分析铜绿受热有HO、CO 生成,另一种一定是Cu的氧化物即CuO。依据质
2 2
量守恒定律,空气中必须有水、CO、O 和铜共同作用才能产生含Cu、H、O、C元素的化合物
2 2
铜绿。D试管中上述条件均已具备,而A缺O、CO,B缺水、CO,C缺水、O,E缺CO,F缺O。
2 2 2 2 2 2
所以D中最易生锈。在实验设计中设计了只有一个条件(A、B、C)的实验,具备两个条件(E、F)
的实验,还缺一个只具备两条件(有O、CO)的实验,才可探究出水与生锈有无关系。
2 2
答案:(1)①C、O ②Cu
(2)【查阅资料】 Cu (OH) CO 2CuO+HO+CO↑
2 2 3 2 2
【猜想与假设】 HO CO
2 2
【设计与实验】 D
【评价与改进】 把铜片置于装有干燥空气的试管中,放置对比上述实验,观察。如图所示:
【拓展与应用】 不全面;因为不同地点空气成分的含量不同,无法比较。
五、计算题(6分)
25.(6分)为了测定某铜锌合金中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次
实验,所得相关的实验数据记录如下:
[来源:Z|xx|k.Com]
第 一第 二第 三
次 次 次
所取合金的质
25 25 50
量/g
所用稀硫酸的
120 160 100
质量/g
生成氢气的质0.4 0.4 0.4量/g
(1)从上表数据分析,当所取合金与所用的稀硫酸的质量比为 时,表示合金中的锌
与稀硫酸中的硫酸恰好完全反应。
(2)试计算该铜锌合金中锌的质量分数。
解析:(1)铜锌合金中铜和稀硫酸不反应,只有锌和稀硫酸反应,第二次和第一次所取的合金质
量相同,第二次所用的稀硫酸比第一次多,而两次生成的气体质量相同,说明两次所取的合金
中的锌都完全反应了,由此可以知道25 g合金只能生成0.4 g氢气;第三次所取的合金是前两
次的2倍,如果合金中的锌完全反应,应该产生0.8 g气体,而实际上产生的气体和前两次相同
只有0.4 g,说明第三次反应中稀硫酸不足量,由此可以知道100 g稀硫酸只能产生0.4 g氢气,
综上可以知道:25 g合金中的锌和100 g 稀硫酸可恰好完全反应,即合金和稀硫酸的质量比为
25 g∶100 g=1∶4;(2)根据氢气的质量结合反应的化学方程式可以计算出锌的质量,进而求出
锌的质量分数即可。
答案:(1)1∶4
(2)解:设25 g铜锌合金中含有锌的质量为x。
Zn+H SO ZnSO+H ↑
2 4 4 2
65 2
x 0.4 g
解得:x=13 g
铜锌合金中锌的质量分数为: ×100%=52%
答:铜锌合金中锌的质量分数为52%。