文档内容
2019 年浙江省绍兴市中考化学试卷
一、单选题(本大题共4小题,共16.0分)
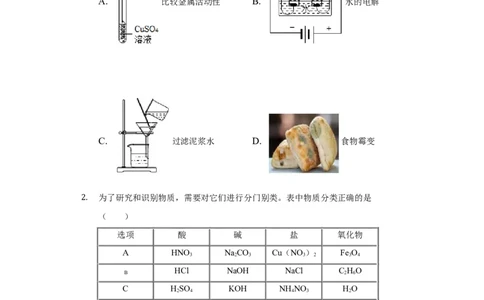
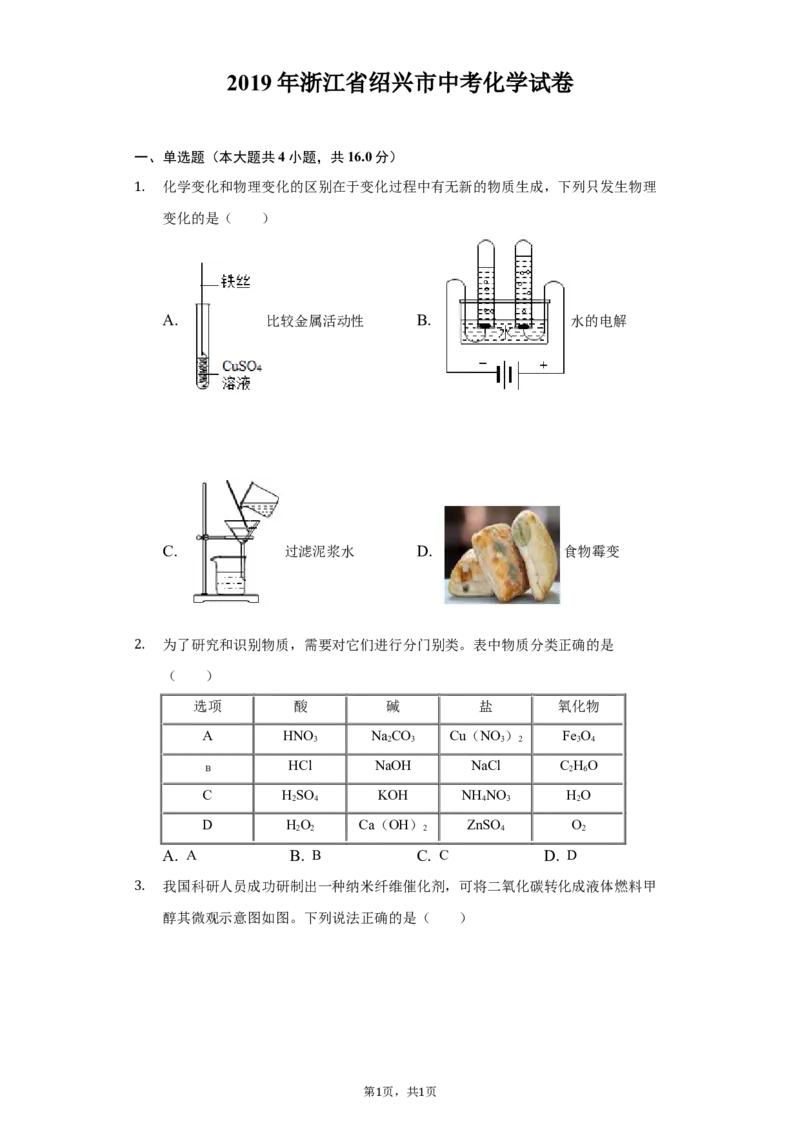
化学变化和物理变化的区别在于变化过程中有无新的物质生成,下列只发生物理
1. 变化的是( )
A. 比较金属活动性 B. 水的电解
C. 过滤泥浆水 D. 食物霉变
为了研究和识别物质,需要对它们进行分门别类。表中物质分类正确的是
2. ( )
选项 酸 碱 盐 氧化物
A HNO NaCO Cu(NO ) Fe O
3 2 3 3 2 3 4
HCl NaOH NaCl C HO
B 2 6
C HSO KOH NH NO HO
2 4 4 3 2
D HO Ca(OH) ZnSO O
2 2 2 4 2
A. A B. B C. C D. D
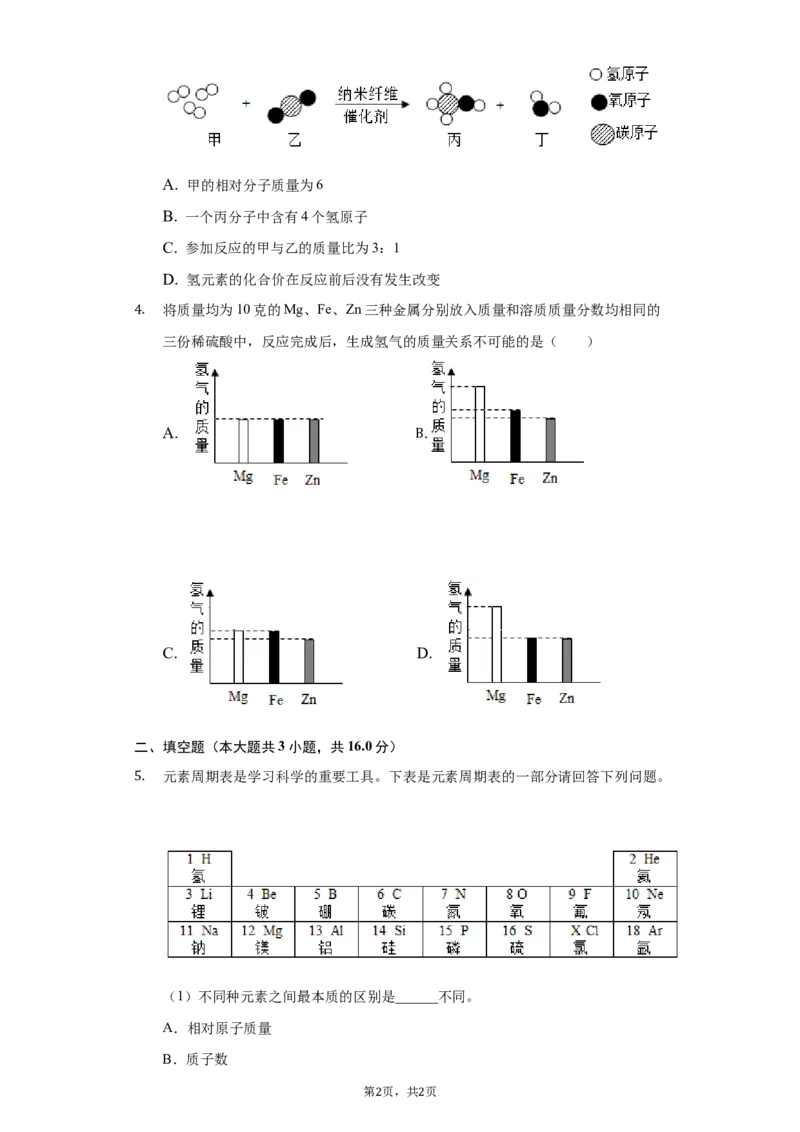
我国科研人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲
3. 醇其微观示意图如图。下列说法正确的是( )
第 页,共 页
1 1A. 甲的相对分子质量为6
B. 一个丙分子中含有4个氢原子
C. 参加反应的甲与乙的质量比为3:1
D. 氢元素的化合价在反应前后没有发生改变
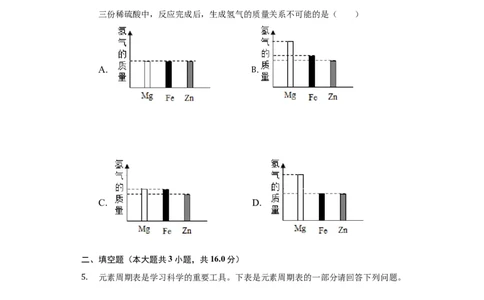
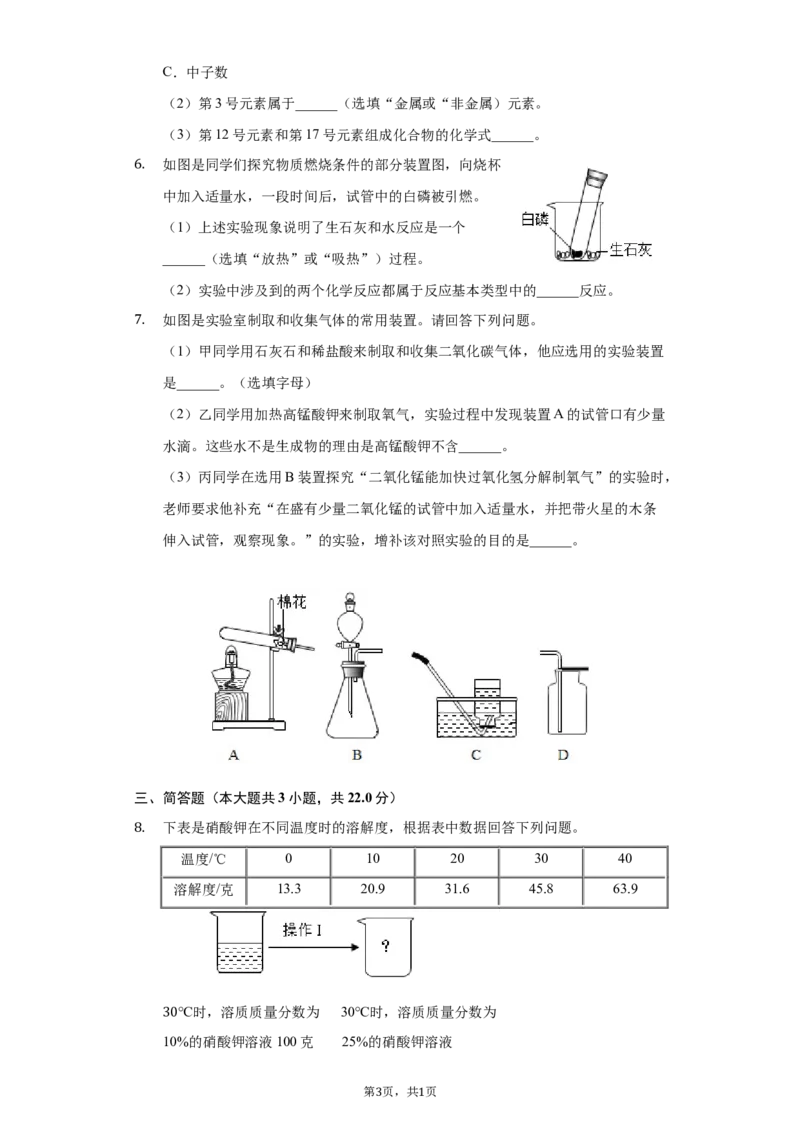
将质量均为10克的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的
4. 三份稀硫酸中,反应完成后,生成氢气的质量关系不可能的是( )
A. .
B
C. D.
二、填空题(本大题共3小题,共16.0分)
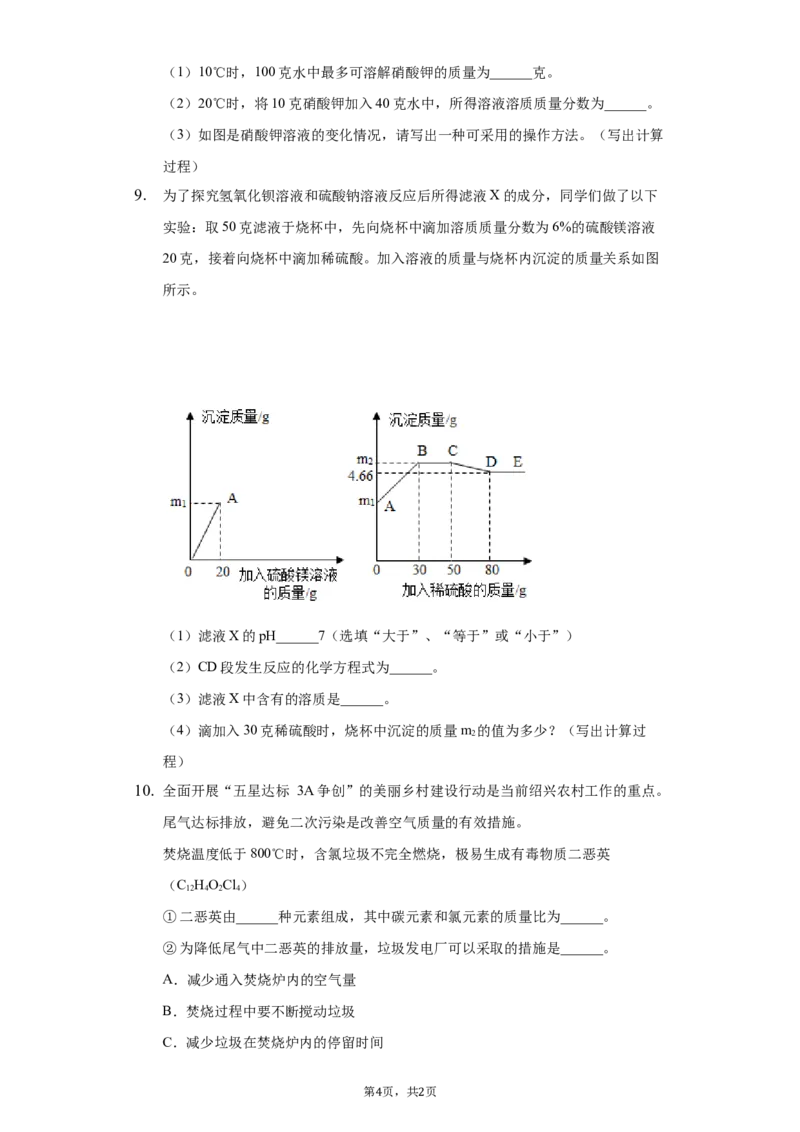
元素周期表是学习科学的重要工具。下表是元素周期表的一部分请回答下列问题。
5.
(1)不同种元素之间最本质的区别是______不同。
A.相对原子质量
B.质子数
第 页,共 页
2 2C.中子数
(2)第3号元素属于______(选填“金属或“非金属)元素。
(3)第12号元素和第17号元素组成化合物的化学式______。
如图是同学们探究物质燃烧条件的部分装置图,向烧杯
6. 中加入适量水,一段时间后,试管中的白磷被引燃。
(1)上述实验现象说明了生石灰和水反应是一个
______(选填“放热”或“吸热”)过程。
(2)实验中涉及到的两个化学反应都属于反应基本类型中的______反应。
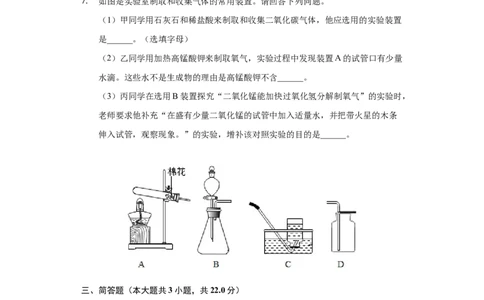
如图是实验室制取和收集气体的常用装置。请回答下列问题。
7. (1)甲同学用石灰石和稀盐酸来制取和收集二氧化碳气体,他应选用的实验装置
是______。(选填字母)
(2)乙同学用加热高锰酸钾来制取氧气,实验过程中发现装置A的试管口有少量
水滴。这些水不是生成物的理由是高锰酸钾不含______。
(3)丙同学在选用B装置探究“二氧化锰能加快过氧化氢分解制氧气”的实验时,
老师要求他补充“在盛有少量二氧化锰的试管中加入适量水,并把带火星的木条
伸入试管,观察现象。”的实验,增补该对照实验的目的是______。
三、简答题(本大题共3小题,共22.0分)
下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
8. 温度/℃ 0 10 20 30 40
溶解度/克 13.3 20.9 31.6 45.8 63.9
℃时,溶质质量分数为 30℃时,溶质质量分数为
3100%的硝酸钾溶液100克 25%的硝酸钾溶液
第 页,共 页
3 1(1)10℃时,100克水中最多可溶解硝酸钾的质量为______克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为______。
(3)如图是硝酸钾溶液的变化情况,请写出一种可采用的操作方法。(写出计算
过程)
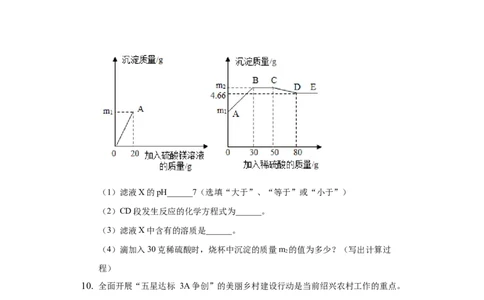
9. 为了探究氢氧化钡溶液和硫酸钠溶液反应后所得滤液X的成分,同学们做了以下
实验:取50克滤液于烧杯中,先向烧杯中滴加溶质质量分数为6%的硫酸镁溶液
20克,接着向烧杯中滴加稀硫酸。加入溶液的质量与烧杯内沉淀的质量关系如图
所示。
(1)滤液X的pH______7(选填“大于”、“等于”或“小于”)
(2)CD段发生反应的化学方程式为______。
(3)滤液X中含有的溶质是______。
(4)滴加入30克稀硫酸时,烧杯中沉淀的质量m 的值为多少?(写出计算过
2
程)
10. 全面开展“五星达标 3A争创”的美丽乡村建设行动是当前绍兴农村工作的重点。
尾气达标排放,避免二次污染是改善空气质量的有效措施。
焚烧温度低于800℃时,含氯垃圾不完全燃烧,极易生成有毒物质二恶英
(C HOCl)
12 4 2 4
①二恶英由______种元素组成,其中碳元素和氯元素的质量比为______。
②为降低尾气中二恶英的排放量,垃圾发电厂可以采取的措施是______。
A.减少通入焚烧炉内的空气量
B.焚烧过程中要不断搅动垃圾
C.减少垃圾在焚烧炉内的停留时间
第 页,共 页
4 2D.升高垃圾焚烧炉内的温度
四、探究题(本大题共1小题,共12.0分)
11. 材料一:1673年,玻义耳曾经做过一个实验:在密闭的曲颈瓶中加热金属时,得
到了金属灰,冷却后打开容器,称量金属灰的质量,发现与原来金属相比质量增
加了。
材料二:1703年,施塔尔提出“燃素学说”,其主要观点有:①燃素是组成物体
的一种成分,一般条件下被禁锢在可燃物中;②燃素在可燃物燃烧时会分离出来,
且燃素可穿透一切物质。
材料三:1756年,罗蒙诺索夫重做了玻义耳的实验。他将金属铅装入容器后密封、
称量。然后把容器放到大火上加热,银白色的金属变成了灰黄色,待容器冷却后
再次称量,发现容器的总质量没有发生变化。罗蒙诺索夫对此的解释是:“容器
里原来有一定量的空气,且容器中的空气质量减少多少,金属灰的质量就比金属
增加多少,在化学变化中物质的质量是守恒的。”后来,拉瓦锡等科学家经过大
量的定量实验,推翻了”燃素学说”,质量守恒定律得到公认。
(1)由“燃素学说”可知,物质燃烧后质量应该减少。请根据所学知识写出一个
可以推翻“燃素学说”的事实
:______。
(2)罗蒙诺索夫重做了玻义耳的实验是基于金属加热后,增加的质量并非来自燃
素而是来自______的假设。
(3)对比材料一和材料三,玻义耳错过了发现质量守恒定律的一个重要原因是
______。
(4)质量守恒定律的发现过程,给我们的启示是______。
A.分析问题应该全面、严谨
B.实验的成功与否,取决于药品的选择
C.定量方法是科学研究的重要方法
D.科学研究既要尊重事实,也要勇于创新
第 页,共 页
5 1第 页,共 页
6 22019 年浙江省绍兴市中考化学试卷
参考答案与试题解析
1.【答案】C
解:A、铁与硫酸铜反应生成铜和硫酸亚铁,属于化学变化,故A错;
B、电解水生成氢气和氧气,属于化学变化,故B错;
C、过滤只是除去不溶性杂质,没有新物质生成,属于物理变化,故C正确;
D、食物霉变有菌类物质生成,属于化学变化,故D错。
故选:C。
2.【答案】C
解:A、硝酸是由氢离子和酸根离子构成的化合物,属于酸;Na CO 是由钠离
2 3
子和碳酸根离子构成的化合物,属于盐,故选项错误。
B、盐酸是由氢离子和酸根离子构成的化合物,属于酸;NaOH是由钠离子和
氢氧根离子组成的化合物,属于碱;NaCl是由钠离子和氯离子构成的化合物,
属于盐;C H O是由碳、氢、氧三种元素组成的化合物,不属于氧化物;故选
2 6
项错误。
C、硫酸是由氢离子和酸根离子构成的化合物,属于酸;KOH是由钾离子和氢
氧根离子组成的化合物,属于碱;NH NO 是由铵根离子和硝酸根离子构成的
4 3
第 页,共 页
7 1化合物,属于盐;H O是由两种元素组成的且有一种是氧元素的化合物,属于
2
氧化物;故选项正确。
D、过氧化氢不属于酸,故选项错误。
故选:C。
3.【答案】B
解:由题目信息和质量守恒定律可知,该反应的方程式为:二氧化碳和氢气在
催化剂作用下反应生成甲醇和水的化学方程式为:CO +3H
2 2
CH OH+H O。
3 2
A、甲为氢气,甲的相对分子质量为2,故A不正确;
B、由微粒的构成可知,一个丙分子中含有4个氢原子,故B正确;
C、由上述反应可知,参加反应的甲、乙两物质的分子个数比为3:1,质量比
是(2×3):44=3:22,故C不正确;
D、该反应由氢气单质参加反应,氢元素的化合价一定发生了变化,故D不正
确。
故选:B。
4.【答案】D
解:Mg+H SO =MgSO +H ↑
2 4 4 2
24 98
10g 40.8g
第 页,共 页
8 2Fe+H SO =FeSO +H ↑
2 4 4 2
56 98
10g 17.5g
Zn+H SO =ZnSO +H ↑
2 4 4 2
65 98
10g 15.1g
酸的质量小于15.1g,酸完全反应,生成的氢气质量相等;
酸的质量介于17.5g和15.1g之间时,镁=铁>锌;
酸的质量介于17.5g和40.8g之间时,镁>铁>锌;
故选:D。
5.【答案】B 金属 MgCl
2
解:(1)不同种元素之间最本质的区别是核内质子数不同。
故填:B。
(2)第3号元素是锂元素,属于金属元素。
故填:金属。
(3)第12号元素(镁元素)和第17号元素(氯元素)组成化合物是氯化镁,氯化
镁中镁元素化合价是+2,氯元素化合价是-1,根据化合物中元素化合价代数
和为零可知,氯化镁的化学式是MgCl 。
2
故填:MgCl 。
2
元素周期表中,方格中左上角是原子序数,右上角是元素符号,中间是元素
第 页,共 页
9 1名称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
除汞外,金属元素的名称都带金字旁,非金属元素的名称不带金字旁;
化合物中元素化合价代数和为零;
元素是具有相同质子数的一类原子的总称;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中
容易得到电子,等于4的,既不容易得到电子,也不容易失去电子,因此最外
层电子数相等的元素化学性质相似,最外层电子数是8的是一种稳定结构,
第一层也是最外层时,达到2个电子也是一种稳定结构。
元素周期表反映了元素之间的内在联系,要注意理解和应用。
6.【答案】放热 化合
解:(1)向烧杯中加入适量水,一段时间后,试管中的白磷被引燃,说明符合
了燃烧的三个条件,说明温度达到了着火点,即说明了生石灰和水反应是一
个放热反应。
(2)生石灰与水反应生成氢氧化钙、白磷与氧气反应生成五氧化二磷,反应均
符合“多变一”的形式,均符合化合反应的特征,均属于化合反应。
故答案为:
第 页,共 页
10 2(1)放热;
(2)化合。
(1)向烧杯中加入适量水,一段时间后,试管中的白磷被引燃,说明符合了燃
烧的三个条件,进行分析解答。
(2)根据生石灰与水反应生成氢氧化钙、白磷与氧气反应生成五氧化二磷,进
行分析解答。
7.【答案】BD 氢元素 排除水中加入二氧化锰也会产生氧气
解:(1)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳
2
酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能
溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:
BD;
(2)乙同学用加热高锰酸钾来制取氧气,实验过程中发现装置A的试管口有
少量水滴。这些水不是生成物的理由是高锰酸钾不含氢元素;故答案为:氢元
素;
(3)增补该对照实验的目的是:排除水中加入二氧化锰也会产生氧气;故答案
为:排除水中加入二氧化锰也会产生氧气;
(1)实验室制取CO ,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸
2
钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热。二氧化碳能溶
于水,密度比空气的密度大,因此只能用向上排空气法收集。
第 页,共 页
11 1(2)制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就
不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热。氧气的密度比空
气的密度大,不易溶于水,因此能用向上排空气法和排水法收集。
(3)增补该对照实验的目的是:排除水中加入二氧化锰也会产生氧气。
8.【答案】12.64 20%
解:(1)10 时,硝酸钾人溶解度是20.9g,也就是说,100g水中最多可以溶解
℃
20.9g硝酸钾;
(2)20 时,硝酸钾人溶解度是31.6g,40g水中最多可以溶解硝酸钾的质量为:
℃
=12.64g,
10克硝酸钾能完全溶于40克水中,所得溶液中溶质的质量分数为:
=20%;
(3)设要加入硝酸钾的质量为x。
=25%
x=20g
答:要加入硝酸钾的质量为20g。
或者设蒸发掉水的质量为y。
25%
y=60g
第 页,共 页
12 2答:蒸发掉水的质量为60g
故答案为:
(1)12.64;
(2)20%;
(3)加入硝酸钾的质量为20g或蒸发掉水的质量为60g。
(1)根据固体物质溶解度的定义进行分析;
(2)根据20 时硝酸钾的溶解度进行相关的计算;
℃
(3)根据增加溶质的质量分数的方法进行分析。
9.【答案】大于 Mg(OH)+H SO =MgSO +2H O Ba(OH)、NaOH
2 2 4 4 2 2
解:(1)由于由于氢氧化钡和硫酸钠反应生成氢氧化钠,且加入硫酸镁有沉淀
生成,且后期加入硫酸导致沉淀质量减少一部分,所以滤液X含有氢氧化钠,
所以pH 大于7;
(2)CD段是氢氧化镁和硫酸反应生成硫酸镁和水,对应的化学方程式为Mg
(OH) +H SO =MgSO +2H O。
2 2 4 4 2
(3)加入硫酸镁有沉淀生成,且后期加入硫酸导致沉淀质量减少一部分,所以
基友氢氧化钠也有钡离子,所以滤液X中含有的溶质是Ba(OH) 、NaOH。
2
(4)滴加入30克稀硫酸时,烧杯中沉淀的质量m 的值为多少?(写出计算
2
设加入20g硫酸镁生成的氢氧化镁的质量为x
第 页,共 页
13 1Ba(OH) +MgSO =Mg(OH) +↓+BaSO ↓
2 4 2 4
120 58
20g×6% x
=
x=0.58g
m 的值为4.66g+0.58g=5.24g
2
故答案为:
(1)大于;
(2)Mg(OH) +H SO =MgSO +2H O。
2 2 4 4 2
(3)Ba(OH) 、NaOH。
2
(4)5.24。
10.【答案】4 72:71 BD
解:
二恶英由碳氢氧氯 4种元素组成,其中碳元素和氯元素的质量比为
①
(12×12):(35.5×4)=72:71。
为降低尾气中二恶英的排放量,垃圾发电厂可以采取的措施是 BD。
②
A.减少通入焚烧炉内的空气量,造成含氯垃圾不完全燃烧,极易生成有毒物
质二恶英。错误;
B.焚烧过程中要不断搅动垃圾,含氯垃圾完全燃烧,不易生成有毒物质二恶
英。正确;
第 页,共 页
14 2C.减少垃圾在焚烧炉内的停留时间,造成含氯垃圾不完全燃烧,极易生成有
毒物质二恶英。错误;
D.升高垃圾焚烧炉内的温度,含氯垃圾完全燃烧,不易生成有毒物质二恶英。
正确;
故选:BD。
故答案为:
4; 72:71。
BD。
①
11.【答案】铁丝燃烧后固体质量增大 空气 打开容器前没有称量容器的总质量
②
ACD
解:(1)可以推翻“燃素学说”的事实:铁丝燃烧后固体质量增大。
故填:铁丝燃烧后固体质量增大。
(2)罗蒙诺索夫重做了玻义耳的实验是基于金属加热后,增加的质量并非来
自燃素而是来自空气的假设。
故填:空气。
(3)对比材料一和材料三,玻义耳错过了发现质量守恒定律的一个重要原因
是打开容器前没有称量容器的总质量。
故填:打开容器前没有称量容器的总质量。
(4)质量守恒定律的发现过程,给我们的启示是:分析问题应该全面、严谨,
第 页,共 页
15 1定量方法是科学研究的重要方法,科学研究既要尊重事实,也要勇于创新。
故填:ACD。
第 页,共 页
16 2