文档内容
优秀领先 飞翔梦
想
第十单元检测卷
班级:__________ 姓名:__________
考生注意:1.本卷共三大题,满分60分。考试时间为45分钟。
2.可能用到的相对原子质量:H—1 O—16 Na—23 Cl—35.5
题号 一 二 三 总分
得分
一、本大题包括10小题,每小题2分,共20分。每小题的4个选项中只有1个符合题意。
1.下列物质的水溶液不能使紫色石蕊试液变红的是( )
A.稀硫酸
B.氧化钙
C.浓盐酸
D.二氧化碳
2.下列溶液中不能导电的是( )
A.澄清石灰水
B.稀硫酸
C.酒精溶液
D.食盐水
3.人被蚊虫叮咬后,皮肤红肿疼痛,这是因为被注入了一种叫蚁酸的酸性物质。为缓解
疼痛,可涂抹下列物质中的( )
A.食醋
B.肥皂水
C.食盐水
D.白糖水
4.下列图示的实验操作,正确的是( )
5.醋酸(CHCOOH)是食醋的成分,它溶于水时能解离出H+和CHCOO-。下列说法中正
3 3
确的是( )
A.醋酸中含有5种元素
B.食醋是一种酸
C.醋酸与氢氧化钠溶液反应生成CHCOONa与HO
3 2
D.食醋可使无色酚酞变红
6.对物质进行分类是化学学习中重要的环节,下列物质分类错误的一组是( )
A.单质:H、O、N
2 2 2
B.酸:HCl、HSO 、HO
2 4 2
C.碱:NaOH、Ba(OH) 、NH ·H O
2 3 2
D.混合物:空气、合金、溶液
7.一些食物和生活中的物质的pH大致如下图。下列说法正确的是( )
www.youyi100.com
第 1 页 共 6 页优秀领先 飞翔梦
想
A.草木灰可用于改良碱性土壤
B.肥皂水可使石蕊试液变红
C.胃液过多的人不宜多吃苹果
D.西瓜比酱油的酸性强
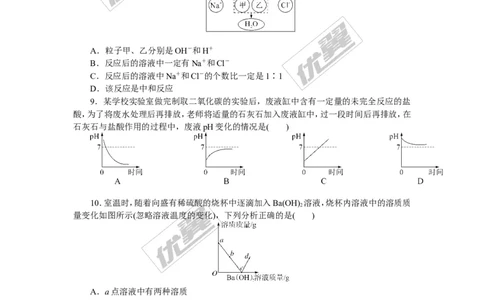
8.如图为氢氧化钠溶液与稀盐酸反应的微观图解,下列有关该反应的说法中错误的是(
)
A.粒子甲、乙分别是OH-和H+
B.反应后的溶液中一定有Na+和Cl-
C.反应后的溶液中Na+和Cl-的个数比一定是1∶1
D.该反应是中和反应
9.某学校实验室做完制取二氧化碳的实验后,废液缸中含有一定量的未完全反应的盐
酸,为了将废水处理后再排放,老师将适量的石灰石加入废液缸中,过一段时间后再排放,在
石灰石与盐酸作用的过程中,废液pH变化的情况是( )
10.室温时,随着向盛有稀硫酸的烧杯中逐滴加入Ba(OH) 溶液,烧杯内溶液中的溶质质
2
量变化如图所示(忽略溶液温度的变化),下列分析正确的是( )
A.a点溶液中有两种溶质
B.b点溶液中滴加紫色石蕊溶液,溶液变蓝
C.c点烧杯内液体的pH=7
D.d点溶液中有较多的Ba2+、OH-、SO、H+
二、本大题包括5小题,共34分。
11.(6分)春节期间小明对当地雨水的酸碱度进行了检测。他将收集的雨水,每隔5min用
pH计检测一次,其pH值如表。
测定时间 8:05 8:10 8:15 8:20 8:25 8:30
www.youyi100.com
第 2 页 共 6 页优秀领先 飞翔梦
想
pH 4.94 4.92 4.90 4.88 4.86 4.85
(1)为了判断雨水酸度是否正常,他做了如下对比实验:将足量CO 气体通入蒸馏水中,
2
检测所得溶液的pH为5.60,有关反应的化学方程式为____________________________。据
此得出,他收集的雨水是否为酸雨?________(选填“是”或“否”)。在检测期间,雨水的酸
度随着时间的变化逐渐________________(选填“增强”或“减弱”);
(2)经调查,近几天空气中SO 、NO 含量明显增多,小明很纳闷:春节期间,工厂大多停
2 2
产,运输车辆也比往日减少,空气中SO 、NO 怎么会增多呢?耳边鸣响的鞭炮声使他恍然大
2 2
悟,鞭炮爆炸会产生SO 、NO 等污染物,小明通过查询资料得知,SO (或NO )的化学性质与
2 2 2 2
CO 相似。他设计用氢氧化钠溶液来吸收鞭炮爆炸时产生的SO (或NO ),请写出有关反应的
2 2 2
化学方程式:________________________________________。
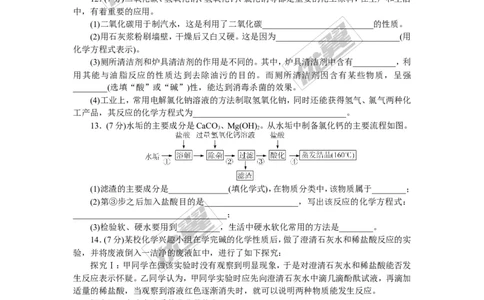
12.(7分)二氧化碳、氢氧化钠、氢氧化钙、氯化钠等都是重要的化工原料,在生产和生活
中,有着重要的应用。
(1)二氧化碳用于制汽水,这是利用了二氧化碳__________________________的性质。
(2)用石灰浆粉刷墙壁,干燥后又白又硬。这是因为_____________________________(用
化学方程式表示)。
(3)厕所清洁剂和炉具清洁剂的作用是不同的。其中,炉具清洁剂中含有__________,利
用其能与油脂反应的性质达到去除油污的目的。而厕所清洁剂因含有某些物质,呈强
________(选填“酸”或“碱”)性,能达到消毒杀菌的效果。
(4)工业上,常用电解氯化钠溶液的方法制取氢氧化钠,同时还能获得氢气、氯气两种化
工产品,其反应的化学方程式为____________________________________。
13.(7分)水垢的主要成分是CaCO 、Mg(OH) 。从水垢中制备氯化钙的主要流程如图。
3 2
(1)滤渣的主要成分是______________(填化学式),在物质分类中,该物质属于________;
(2)第③步之后加入盐酸目的是______________________,写出该反应的化学方程式:
____________________________________;
(3)检验软、硬水要用到__________,生活中硬水软化常用的方法是________。
14.(7分)某校化学兴趣小组在学完碱的化学性质后,做了澄清石灰水和稀盐酸反应的实
验,并将废液倒入一洁净的废液缸中,进行了如下探究:
探究Ⅰ:甲同学在做该实验时没有观察到明显现象,于是对澄清石灰水和稀盐酸能否发
生反应表示怀疑。乙同学认为,甲同学实验时应先向澄清石灰水中滴几滴酚酞试液,再滴加
适量的稀盐酸,当观察到溶液红色逐渐消失时,就可以说明两种物质能发生反应。
探究Ⅱ:废液中溶质的成分是什么?
【查阅资料】CaCl +NaCO===CaCO ↓+2NaCl。
2 2 3 3
【做出猜想】猜想一:CaCl ;猜想二:CaCl ,HCl;猜想三:CaCl 、HCl、Ca(OH) ;
2 2 2 2
你的猜想:____________________________________________________。
丙同学认为猜想三是错误的,理由是______________________________________(用化
学方程式解释)。
【实验设计】
设计者 实验操作 实验现象 实验结论
丁同学 取少量废液于一支试管中,向其中加入足 有白色沉淀生成 猜想一正确
www.youyi100.com
第 3 页 共 6 页优秀领先 飞翔梦
想
量的碳酸钠溶液
取几粒锌粒于一支试管中,向其中加入少
戊同学 ________________ 猜想二正确
量废液
【评价与反思】
请判断以上设计的两个方案中,__________同学的方案合理,请分析另一个方案不合理
的理由:_____________________________________________________________________。
【表达与交流】
若实验证明猜想二是正确的,你认为该废液未经处理直接倒入下水道,可能造成的危害
是________________________________(填一点)。
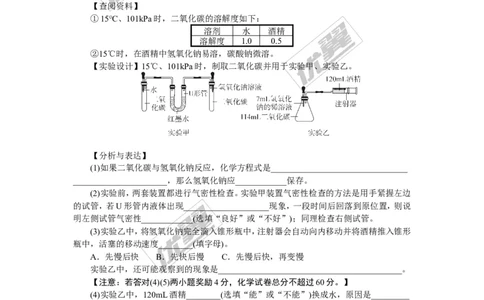
15.(7分)某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究。
【提出问题】二氧化碳与氢氧化钠反应,还是溶解在水中?
【查阅资料】
①15℃、101kPa时,二氧化碳的溶解度如下:
溶剂 水 酒精
溶解度 1.0 0.5
②15℃时,在酒精中氢氧化钠易溶,碳酸钠微溶。
【实验设计】15℃、101kPa时,制取二氧化碳并用于实验甲、实验乙。
【分析与表达】
(1)如果二氧化碳与氢氧化钠反应,化学方程式是________________________________
______________________,那么氢氧化钠应____________保存。
(2)实验前,两套装置都进行气密性检查。实验甲装置气密性检查的方法是用手紧握左边
的试管,若U形管内液体出现____________________现象,一段时间后回落到原位置,则说
明左侧试管气密性____________(选填“良好”或“不好”);同理检查右侧试管。
(3)实验乙中,将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形
瓶中,活塞的移动速度________(填字母)。
A.先慢后快 B.先快后慢 C.先慢后快,再变慢
实验乙中,还可能观察到的现象是___________________________________________。
【注意:若答对(4)(5)两小题奖励4分,化学试卷总分不超过60分。】
(4)实验乙中,120mL酒精________(选填“能”或“不能”)换成水,原因是_________
_________________________________________________________________。
(5)由以上探究可知,二氧化碳能溶于水,也能与氢氧化钠反应,但实验乙的数据还不够
准确,造成实验乙误差的原因可能有____________________________________________
______________________________________________________________________。(写一条)
三、本大题共6分。
16.(6分)将5%的NaOH溶液逐滴加入10g稀盐酸中,边滴加边搅拌,随着NaOH溶液的
加入,溶液pH的变化如图所示,请回答:
www.youyi100.com
第 4 页 共 6 页优秀领先 飞翔梦
想
(1)当恰好完全反应时,消耗NaOH溶液的质量为________g;
(2)计算稀盐酸中溶质的质量分数。
www.youyi100.com
第 5 页 共 6 页优秀领先 飞翔梦
想
参考答案与点拨
1.B 2.C 3.B 4.D 5.C 6.B 7.C 8.C 9.B
10.C 点拨:a点时,反应没有开始,溶液中有一种溶质HSO ;b点溶液中硫酸有剩余,
2 4
滴加紫色石蕊溶液,溶液变红;c点稀HSO 与Ba(OH) 完全反应,杯内液体的pH=7;d点
2 4 2
Ba(OH) 溶液过量,溶液中有Ba2+、OH-,无SO、H+。
2
11.(1)CO +HO===H CO 是 增强
2 2 2 3
(2)SO +2NaOH===Na SO +HO(合理即可)
2 2 3 2
12.(1)可与水反应生成碳酸
(2)Ca(OH) +CO===CaCO ↓+HO
2 2 3 2
(3)氢氧化钠(或NaOH) 酸
(4)2NaCl+2HO=====2NaOH+H↑+Cl↑
2 2 2
13.(1)Mg(OH) 碱
2
(2)除去未反应的氢氧化钙
Ca(OH) +2HCl===CaCl +2HO
2 2 2
(3)肥皂水 煮沸
14.【做出猜想】氯化钙、氢氧化钙
2HCl+Ca(OH) ===CaCl +2HO
2 2 2
【实验设计】有气泡产生
【评价与反思】戊 氢氧化钙过量时,其与CaCl 一样能与碳酸钠反应生成沉淀
2
【表达与交流】导致水或土壤污染
15.(1)2NaOH+CO===Na CO+HO 密封
2 2 3 2
(2)右高左低 良好
(3)B 在锥形瓶中观察到白色浑浊现象
(4)不能 二氧化碳在水中的溶解度大于在酒精中的溶解度
(5)水分子和酒精分子的间隔不同,酒精具有挥发性
16.(1)16
(2)解:设稀盐酸中氯化氢的质量为x。
NaOH+HCl===NaCl+HO
2
40 36.5
16g×5% x
=
x=0.73g
稀盐酸中溶质的质量分数为×100%=7.3%
答:稀盐酸中溶质的质量分数为7.3%。
www.youyi100.com
第 6 页 共 6 页