文档内容
专题五 科学探究
一、选择题
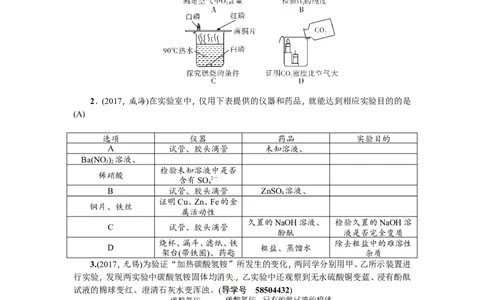
1.如图的实验设计不能实现其对应实验目的的是(A)(导学号 58504431)
2.(2017,威海)在实验室中,仅用下表提供的仪器和药品,就能达到相应实验目的的是
(A)
选项 仪器 药品 实验目的
A 试管、胶头滴管 未知溶液、
Ba(NO ) 溶液、
3 2
检验未知溶液中是否
稀硝酸
含有SO 2-
4
B 试管、胶头滴管 ZnSO 溶液、
4
证明Cu、Zn、Fe的金
铜片、铁丝
属活动性
久置的NaOH溶液、 检验久置的NaOH溶
C 试管、胶头滴管
酚酞 液是否完全变质
烧杯、漏斗、滤纸、铁 除去粗盐中的难溶性
D 粗盐、蒸馏水
架台(带铁圈)、药匙 杂质
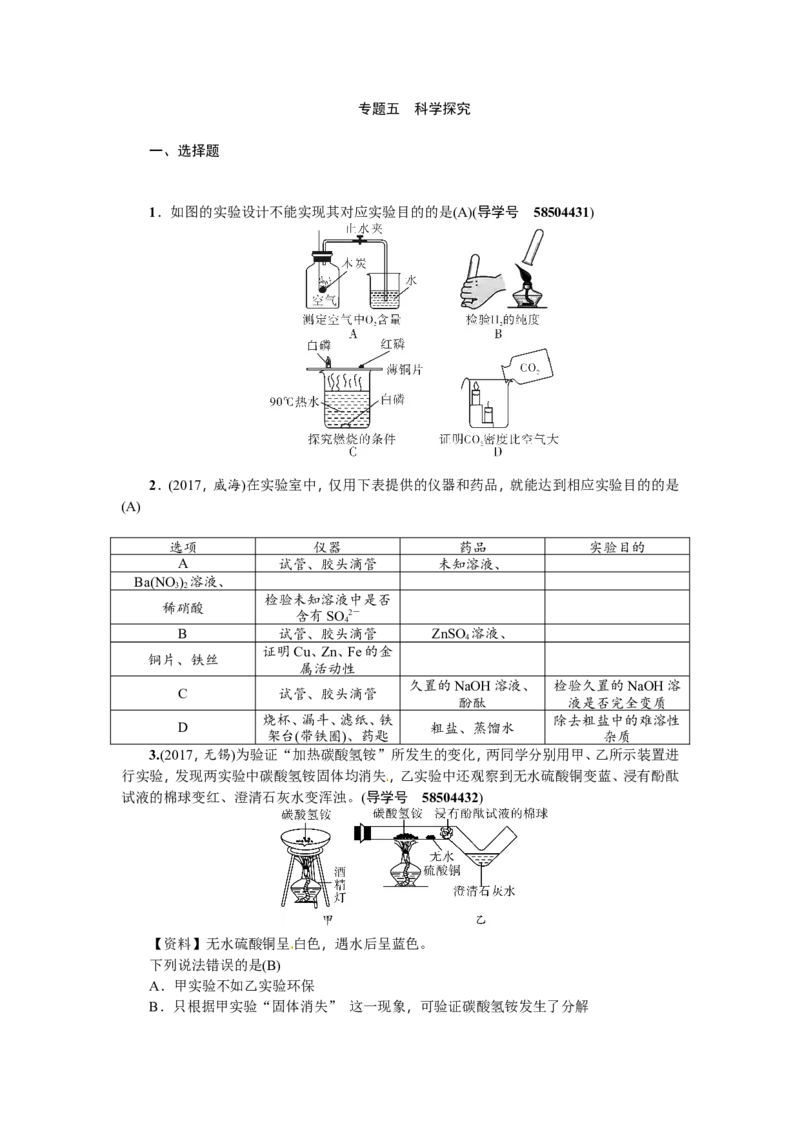
3.(2017,无锡)为验证“加热碳酸氢铵”所发生的变化,两同学分别用甲、乙所示装置进
行实验,发现两实验中碳酸氢铵固体均消失,乙实验中还观察到无水硫酸铜变蓝、浸有酚酞
试液的棉球变红、澄清石灰水变浑浊。(导学号 58504432)
【资料】无水硫酸铜呈白色,遇水后呈蓝色。
下列说法错误的是(B)
A.甲实验不如乙实验环保
B.只根据甲实验“固体消失” 这一现象,可验证碳酸氢铵发生了分解C.乙实验有利于学生分析“固体消失” 的原因
D.只根据乙实验的现象,可验证NH HCO =====NH ↑+CO↑+HO
4 3 3 2 2
二、实验探究题
4.(2017,孝感)小明同学欲回收中考化学实验操作考试(考题:鉴别碳酸钠和氯化钠两瓶
白色固体)用剩的药品。他对其中的一瓶药品是否纯净产生质疑,于是他在老师的指导下对其
成分展开了如下探究:(导学号 58504433)
【猜想与假设】猜想一:白色固体为碳酸钠;
猜想二:白色固体为氯化钠;
猜想三:白色固体为碳酸钠和氯化钠的混合物。
【设计与实验】
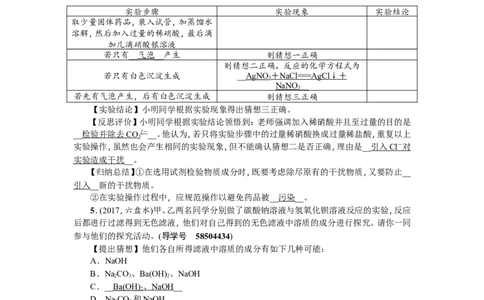
实验步骤 实验现象 实验结论
取少量固体药品,装入试管,加蒸馏水
溶解,然后加入过量的稀硝酸,最后滴
加几滴硝酸银溶液
若只有__气泡__产生 则猜想一正确
则猜想二正确。反应的化学方程式为
若只有白色沉淀生成 __AgNO + NaC l == =AgC l ↓ +
3
NaNO __
3
若先有气泡产生,后有白色沉淀生成 则猜想三正确
【实验结论】小明同学根据实验现象得出猜想三正确。
【反思评价】小明同学根据实验结论领悟到:老师强调加入稀硝酸并且至过量的目的是
__ 检验并除去 CO 2-__。他认为,若只将实验步骤中的过量稀硝酸换成过量稀盐酸,重复以上
3
实验操作,虽然也会产生相同的实验现象,但不能确认猜想二是否正确,理由是__ 引入 C l - 对
实验造成干扰__。
【归纳总结】①在选用试剂检验物质成分时,既要考虑除尽原有的干扰物质,又要防止__
引入__新的干扰物质。
②在实验操作过程中,应规范操作以避免药品被__污染__。
5.(2017,六盘水)甲、乙两名同学分别做了碳酸钠溶液与氢氧化钡溶液反应的实验,反应
后都进行过滤得到无色滤液,他们对自己得到的无色滤液中溶质的成分进行探究。请你一同
参与他们的探究活动。(导学号 58504434)
【提出猜想】他们各自所得滤液中溶质的成分有如下几种可能:
[来源:学,科,网]
A.NaOH
B.NaCO、Ba(OH) 、NaOH
2 3 2
C.__Ba(OH) 、 NaOH __
2
D.NaCO 和NaOH
2 3
【讨论交流】上述猜想中,肯定不成立的是__B__(填猜想序号),其理由是__NaCO 和
2 3
Ba(OH) 能发生反应__。
2
【实验探究】甲、乙两同学为了验证各自所得滤液的成分,分别进行了如下实验:
实验操作 实验现象 实验结论
取少量滤液于试管中,加
滤液中溶质的成分与猜想
甲同学 入足量的__NaCO__溶 __产生白色沉淀
2 3 C对应
液
取少量滤液于试管中,加 滤液中溶质的成分与猜想
乙同学 无明显实验现象
入足量的NaCO 溶液 A 对应
2 3
【反思与评价】经过讨论,大家一致认为甲同学的实验结论是正确的,乙同学的实验结论不一定正确。请你帮乙同学设计实验,进一步确定乙同学得到的滤液中溶质的成分。
实验操作及实验现象 实验结论
__ 取少量滤液于试管中 , 加入 Ba(OH ) 溶液或
2 滤液中溶质的成分与猜想__A__对应
Ca (OH) 溶液 , 无明显现象 __
2
6.(2017,青岛)某研究性学习小组通过查阅资料获知以下信息:将二氧化碳气体慢慢地
通入一定量的氢氧化钠溶液中,在溶液中先后发生以下两个化学反应:(导学号 58504435)
2NaOH + CO === NaCO + HO (先发生反应)
2 2 3 2
NaCO+ CO+ HO ===2NaHCO (后发生反应)
2 3 2 2 3
同学们开展了下列探究活动:
【提出问题】将二氧化碳气体慢慢地通入一定量的氢氧化钠溶液中, 反应后所得溶液中
溶质的成分有哪些
【猜想假设】Ⅰ.NaOH 和NaCO;
2 3
Ⅱ.只有 NaCO;
2 3
Ⅲ.__NaHCO __;
3
Ⅳ.__NaCO 和 NaHCO __。
2 3_ 3
【实验探究】将二氧化碳气体慢慢地通入一定量的某氢氧化钠溶液中,再将反应后所得
溶液按下列流程进行实验并测出相关数据:
【查阅资料】 碳酸盐一般不易溶于水, 如 CaCO 难溶; 碳酸氢盐绝大多数易溶于水,
3
如Ca(HCO ) 易溶。
3 2
【获得结论】根据上述信息, 分析反应后所得溶液中溶质的成分并计算溶质的质量,
将结果填入下表:
溶质的化学式 溶质的质量/g
__NaCO __ __10.6_g__
2 3_
__NaHCO __ __16.8_g__
3
(填表说明: ①不写计算过程, 计算结果保留一位小数。②如果溶质的成分只有一种,
请填写在第一行;如果溶质的成分有两种,请分别在两行中各填写一种物质。)
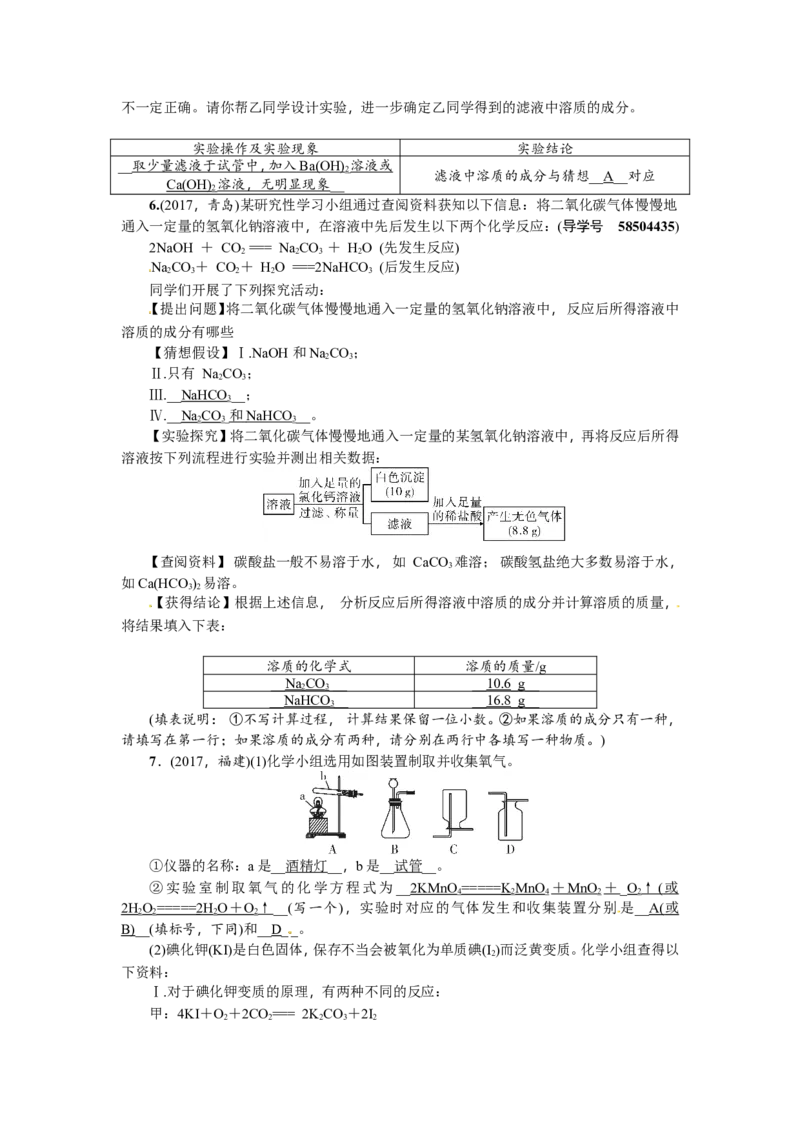
7.(2017,福建)(1)化学小组选用如图装置制取并收集氧气。
①仪器的名称:a是__酒精灯__,b是__试管__。
②实验室制取氧气的化学方程式为__2KMnO ===== K MnO + MnO +_O ↑ ( 或
4 2 4 2 2
2HO ===== 2 H O + O ↑__(写一个),实验时对应的气体发生和收集装置分别是__ A( 或
2 2 2 2
B)__(填标号,下同)和__D__。
(2)碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I)而泛黄变质。化学小组查得以
2
下资料:
Ⅰ.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O+2CO=== 2KCO+2I
2 2 2 3 2乙:4KI+O+2H O===4KOH+2I
2 2 2
Ⅱ.KOH与NaOH的化学性质相似。
为探究碘化钾变质原理的合理性,开展以下实验。
【实验过程】
[实验1]取适量碘化钾固体暴露于空气一小段时间,观察到固体泛黄。往泛黄的固体中加
入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。
①石灰水变浑浊的原理是__CO + Ca(OH ) == =CaCO ↓ + H O__(用化学方程式表示)。
2 2 3 2
②化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论。
理由是__ 无法判断 K CO 是按反应甲原理产生 , 还是按 反应乙原理生成的 KOH 吸收空气中
2 3
的 CO 而产生的 ( 或其他合理答案 )__。
2
图1 图2
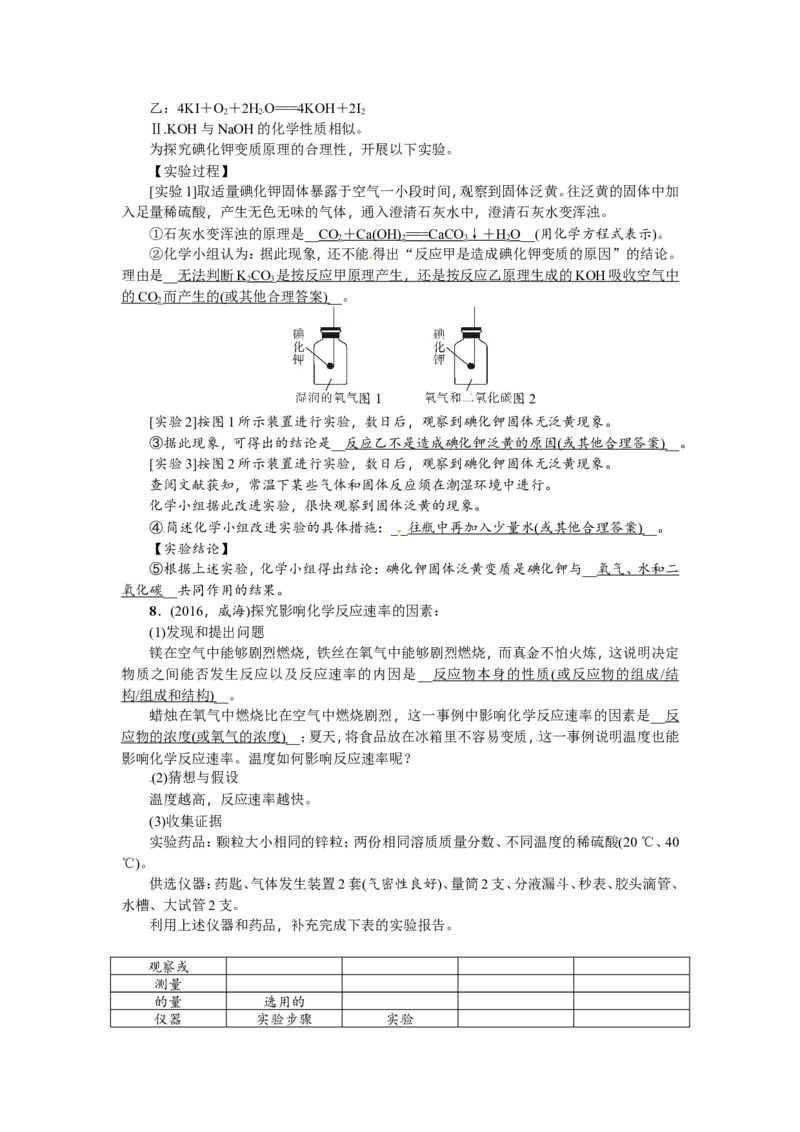
[实验2]按图1所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
③据此现象,可得出的结论是__ 反应乙不是造成碘化钾泛黄的原因 ( 或其他合理答案 )__。
[实验3]按图2所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
查阅文献获知,常温下某些气体和固体反应须在潮湿环境中进行。
化学小组据此改进实验,很快观察到固体泛黄的现象。
④简述化学小组改进实验的具体措施:__ 往瓶中再加入少量水 ( 或其他合理答案 )__。
【实验结论】
⑤根据上述实验,化学小组得出结论:碘化钾固体泛黄变质是碘化钾与__氧气、水和二
氧化碳__共同作用的结果。
8.(2016,威海)探究影响化学反应速率的因素:
(1)发现和提出问题
[来源:学.科.网Z.X.X.K]
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定
物质之间能否发生反应以及反应速率的内因是__ 反应物本身的性质 ( 或反应物的组成 / 结
构 / 组成和结构 )__。
蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是__反
应物的浓度 ( 或氧气的浓度 )__;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能
影响化学反应速率。温度如何影响反应速率呢?
(2)猜想与假设
温度越高,反应速率越快。
(3)收集证据
实验药品:颗粒大小相同的锌粒;两份相同溶质质量分数、不同温度的稀硫酸(20 ℃、40
℃)。
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、
水槽、大试管2支。
利用上述仪器和药品,补充完成下表的实验报告。
观察或
测量
的量 选用的
仪器 实验步骤 实验现象 实验结论
__ 1 . 分别取相同
数量 ( 或质量 ) 的
锌粒于两套气体
发生装置中; 2 .
气体发生装置、
分别取相同体 温度高的 , 收集 温度越高,反应
产生相同体积的 秒表、胶头滴管、
积、不同温度的 一试管气体所需 速率越快。反应
气体所需时间 水槽、大试管、药
稀硫酸加入到两 的时间短 的化学方程式是
匙、量筒
套气体发生装置
中; 3 . 记录收集
一试管气体所需
的时间__
Zn +
HSO == = _ZnSO
2 4
+ H ↑__。
4 2
该实验可以观察或测量的量有多种,除了上述观测点外,可以观察或测量的量还有
(写一条)__ 相同时间内收集气体的体积 ( 或反应结束所需的时间或消耗等量锌粒所需的时间
或消耗等量的稀硫酸所需的时间 )__等。
(4)结论与解释
从微观的角度分析“温度越高,反应速率越快”的原因是__ 温度越高 , 微粒运动速率加
快 , 有效碰撞机会增多 __。
(5)拓展分析
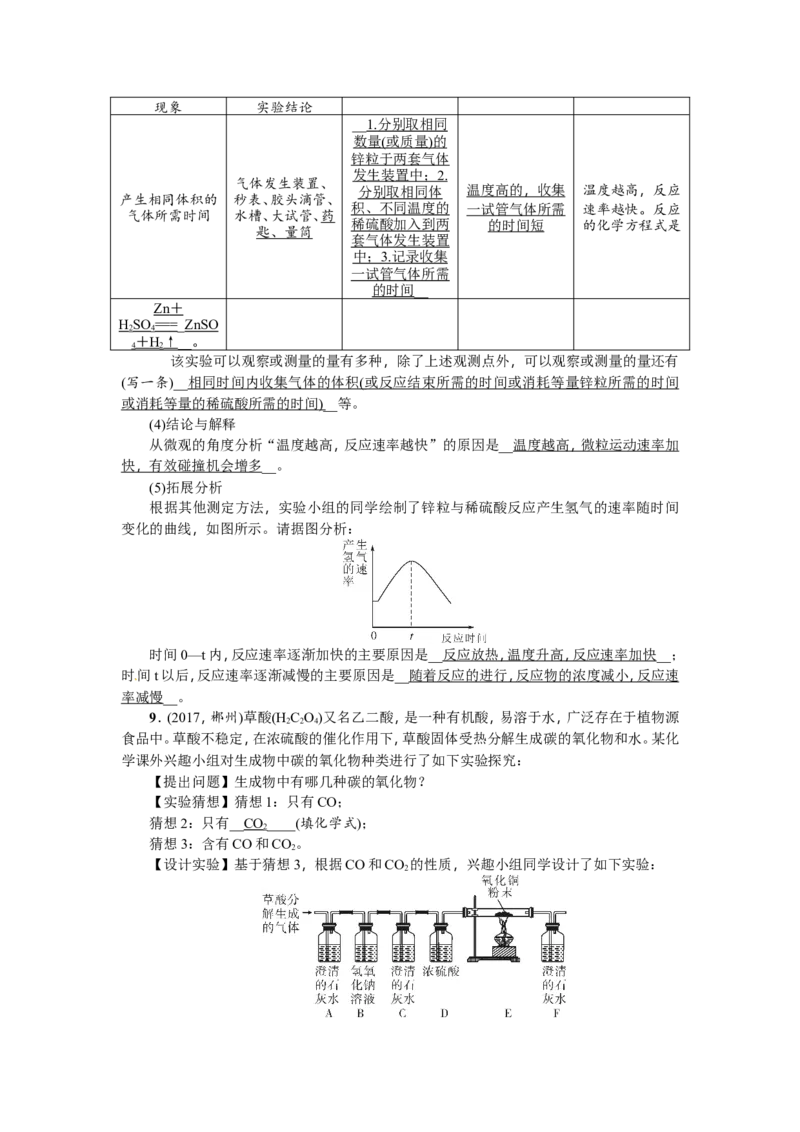
根据其他测定方法,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间
变化的曲线,如图所示。请据图分析:
时间0—t内,反应速率逐渐加快的主要原因是__ 反应放热 , 温度升高 , 反应速率加快 __;
时间t以后,反应速率逐渐减慢的主要原因是__ 随着反应的进行 , 反应物的浓度减小 , 反应速
率减慢__。
9.(2017,郴州)草酸(H C O)又名乙二酸,是一种有机酸,易溶于水,广泛存在于植物源
2 2 4
食品中。草酸不稳定,在浓硫酸的催化作用下,草酸固体受热分解生成碳的氧化物和水。某化
学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究:
【提出问题】生成物中有哪几种碳的氧化物?
【实验猜想】猜想1:只有CO;
猜想2:只有__CO____(填化学式);
2
猜想3:含有CO和CO。
2
【设计实验】基于猜想3,根据CO和CO 的性质,兴趣小组同学设计了如下实验:
2【实验探究】
(1)观察到A装置中的澄清石灰水变浑浊,证明草酸分解有CO 气体生成,请写出A装置
2
中的化学反应方程式:__Ca(OH) + CO == =CaCO ↓ + H O__。
2 2 3 2
(2)有两种实验现象都能分别证明草酸分解的气体中含有CO:
①C装置中澄清石灰水不变浑浊,F装置中出现__ 澄 清石灰水变浑浊 __的现象;
②E装置中出现__黑色粉末变红色____的现象。
【实验结论】通过实验探究证明:猜想3成立。
草酸分解的化学方程式是__HC O ===== CO ↑ + CO ↑ + H O__。
2 2 4 2 2
(1)B装置的作用是__除去二氧化碳气体__。
(2)C装置的作用是__检验二氧化碳气体是否除尽__。
(3)该实验装置的设计还有一处明显不足(实验前已排尽装置内的空气),请提出改进措施:
__ 在 F 装置后设置尾气处理装置 __(任写一条)。
10.(2017,泰安)某兴趣小组在探究浓硫酸的化学性质时,将浓硫酸滴加到氯化钠固体中
并小心的加热,发现有剌激性气味的气体产生,同时发现有白雾。经查阅资料了解到浓硫酸
与氯化钠在加热时会发生反应 ,写出该反应的化学方程式: __HSO ( 浓 ) +
2 4
2NaCl ===== Na SO _ + 2HC l ↑ ( 或 H SO ( 浓 ) + NaCl ===== NaHSO _ + HC l ↑ )__,该兴趣小组
2 4 2 4 4
对产生的氯化氢(HCl)气体是否显酸性进行了相关探究。
【进行实验】同学们根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染
成蓝紫色的纸质干燥小花进行如图1的三个实验:(导学号 58504436)
图1
【实验现象】Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色。
【査阅资料】图2是同学们査阅的氯化氢气体溶于水的示意图。
图2
【实验结论】氯化氢气体不显酸性。
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是__ 在氯化氢气体中 , 氯化氢气体是由
氯化氢分子构成的 , 没有解离出氢离子 , 所以氯化氢气体不显酸性 __。
(2)小明向实验Ⅲ中变红的小花上喷足量的稀氢氧化钠溶液,发现小花最后变成黄绿色,
写出相关反应的化学方程式:__ NaOH + HCl == =NaCl + H O__。
2(3)紫甘蓝的汁液在酸性溶液中显__红__色。
(4)下列实验可以用来说明氯化氢气体不显酸性的是__B__(填字母号)。
A.测试盐酸的导电性,盐酸能导电
B.干燥的碳酸钠粉末放入氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体
D.干燥的碳酸钠粉末放入盐酸中,能反应
【拓展应用】
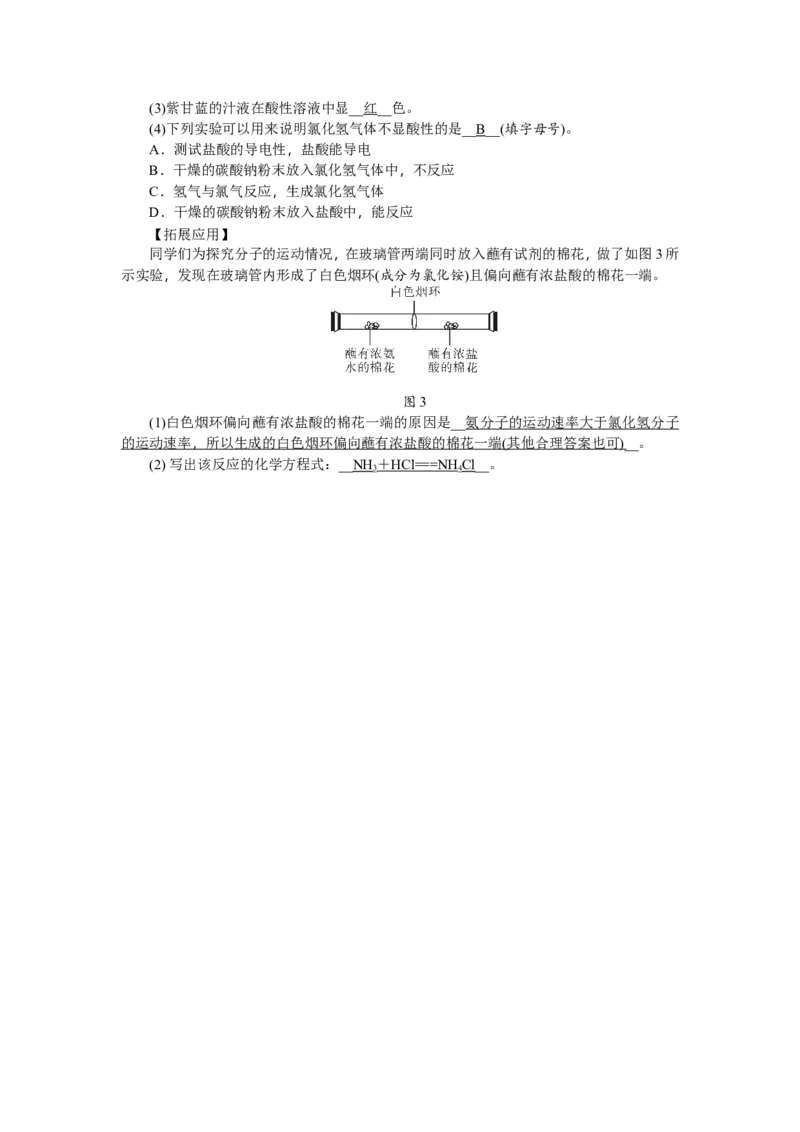
同学们为探究分子的运动情况,在玻璃管两端同时放入蘸有试剂的棉花,做了如图3所
示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端。
图3
(1)白色烟环偏向蘸有浓盐酸的棉花一端的原因是__氨分子的运动速率大于氯化氢分子
的运动速率 , 所以生成的白色烟环偏向蘸有浓盐酸的棉花一端 ( 其他合理答案也可 )__。
(2) 写出该反应的化学方程式:__NH + HC l == =NH Cl__。
3 4