文档内容
专题六 化学计算
一、选择题
1.(2017,滨州)我市邹平特产“长山山药”中含有被医学界称为“药用黄金”的薯蓣皂
素,其化学式为C H O。下列有关薯蓣皂素的说法正确的是(A)
27 42 3
A.薯蓣皂素中质量分数最大的是碳元素
B.薯蓣皂素的相对分子质量为228
C.薯蓣皂素中含有21个氢分子
D.薯蓣皂素是由27个碳原子、42个氢原子和3个氧原子构成的
2.(多选)(2017,天津)下列说法中正确的是(AC)(导学号 58504437)
A.质量相等的氧化镁和硫酸镁中镁元素的质量比为3∶1
B.质量相等的硫和碳分别在氧气中充分燃烧,硫比碳消耗氧气的质量大
C.硝酸铵和氯化钾的混合物中氮元素质量分数为14%,该混合物中硝酸铵的质量分数为
40%
D.质量和质量分数均相等的氢氧化钠溶液和稀硫酸,充分反应后,向所得溶液中滴加硫
酸铜溶液,不会出现蓝色沉淀
3.(2017,烟台)在托盘天平的两盘上各放一只质量相同的烧杯,分别加入等质量、等溶质
质量分数的足量稀盐酸,将天平调节至平衡。然后向左盘的烧杯中加入4.0 g含钙元素的质量
分数为50%的碳酸钙与氧化钙的固体混合物,使之完全反应。欲使天平恢复平衡,可向右盘的
烧杯中加入(B)(导学号 58504438)
A.3.5 g氢氧化钠溶液 B.2.8 g氧化铁
C.2.8 g碳酸钠溶液 D.2.4 g镁
二、填空题
4.(2017,内江)一种新型环保材料被塑胶跑道工程广泛应用,合成这种新材料的原料是二
甲苯烷二异氰酸酯(其分子式为C H NO)。请回答下列问题:(导学号 58504439)
15 10 2 2
(1)二甲苯烷二异氰酸酯(C H NO)中氢、氧元素的质量比为__ 5 ∶ 16 __(填最简整数比)。
15 10 2 2
(2)二甲苯烷二异氰酸酯(C H NO)的相对分子质量为__250__。
15 10 2 2
(3)500 g二甲苯烷二异氰酸酯中含氮元素的质量为__56__ g。
三、计算题
5.(2017,德州)硫酸亚铁在工农业生产中有重要用途,也有较高的医用价值。工业上用废
铁屑和含硫酸的废液来制取硫酸亚铁,变废为宝。现用5.6 t铁屑与100 t废液恰好完全反应
(已知铁屑只和废液中的硫酸反应),请你计算:(导学号 58504440)
(1)可生成硫酸亚铁的质量。
(2)所用废液中硫酸的溶质质量分数。
解:设生成硫酸亚铁的质量为x,100 t废液中硫酸的质量为y。
Fe + HSO ===FeSO + H↑
2 4 4 2
56 98 152
5.6 t y x
==
解得:x=15.2 t y=9.8 t
废液中硫酸的质量分数为×100%=9.8%
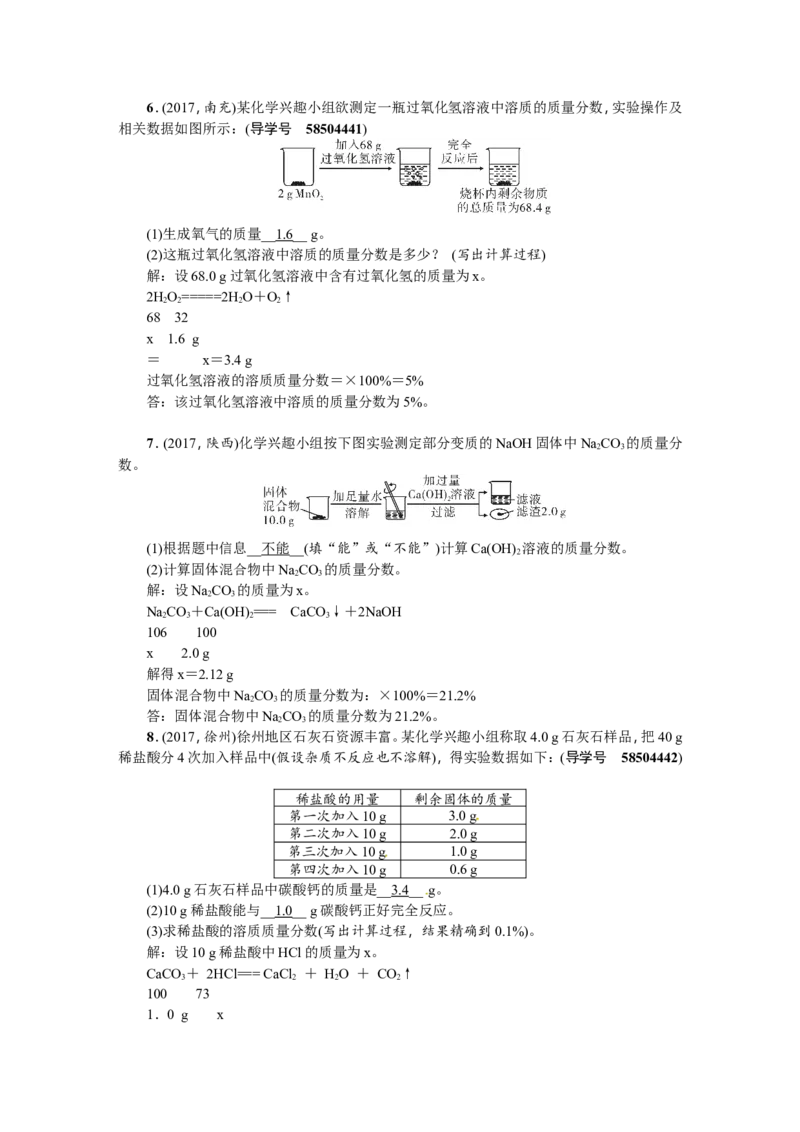
答:(1)可制得硫酸亚铁15.2 t;(2)废液中硫酸的溶质质量分数为9.8%。6.(2017,南充)某化学兴趣小组欲测定一瓶过氧化氢溶液中溶质的质量分数,实验操作及
相关数据如图所示:(导学号 58504441)
(1)生成氧气的质量__1.6__ g。
(2)这瓶过氧化氢溶液中溶质的质量分数是多少? (写出计算过程)
解:设68.0 g过氧化氢溶液中含有过氧化氢的质量为x。
2HO=====2HO+O↑
2 2 2 2
68 32
x 1.6 g
= x=3.4 g
过氧化氢溶液的溶质质量分数=×100%=5%
[来源:Zxxk.Com]
答:该过氧化氢溶液中溶质的质量分数为5%。
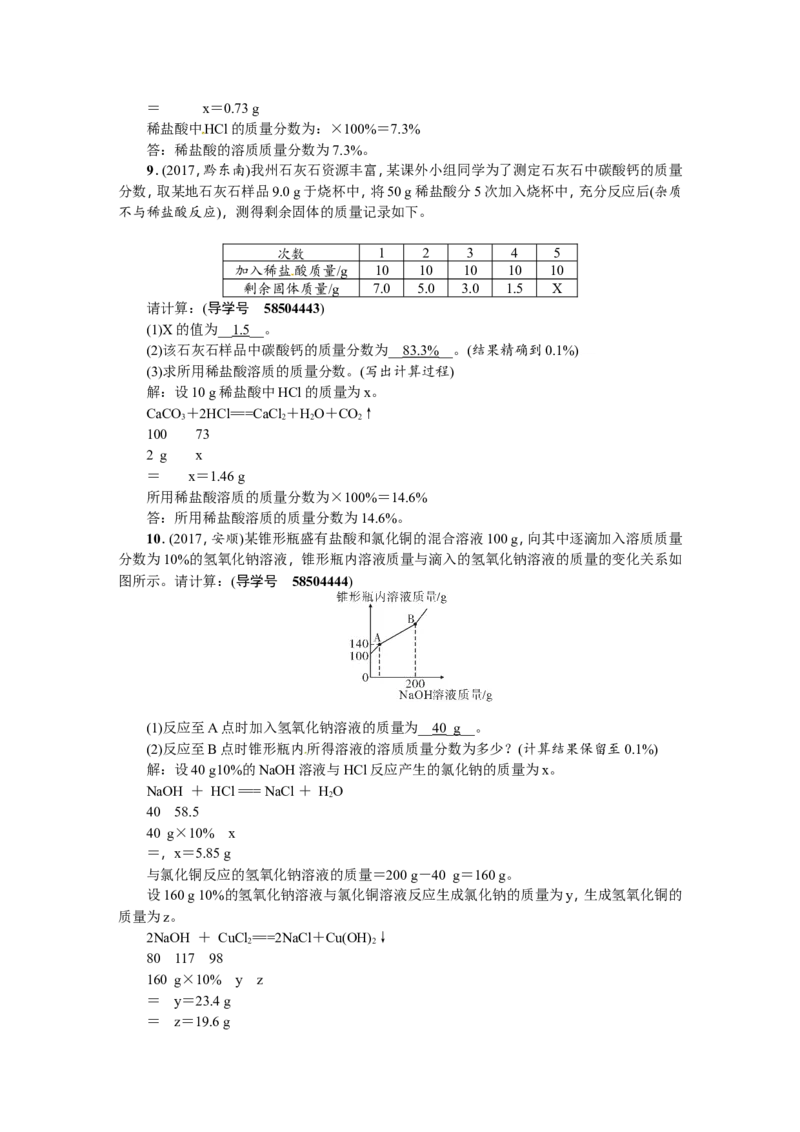
7.(2017,陕西)化学兴趣小组按下图实验测定部分变质的NaOH固体中NaCO 的质量分
2 3
数。
(1)根据题中信息__不能__(填“能”或“不能”)计算Ca(OH) 溶液的质量分数。
2
(2)计算固体混合物中NaCO 的质量分数。
2 3
解:设NaCO 的质量为x。
2 3
NaCO+Ca(OH) === CaCO ↓+2NaOH
2 3 2 3
106 100
x 2.0 g
解得x=2.12 g
固体混合物中NaCO 的质量分数为:×100%=21.2%
2 3
答:固体混合物中NaCO 的质量分数为21.2%。
2 3 [来源:Zxxk.Com]
8.(2017,徐州)徐州地区石灰石资源丰富。某化学兴趣小组称取4.0 g石灰石样品,把40 g
稀盐酸分4次加入样品中(假设杂质不反应也不溶解),得实验数据如下:(导学号 58504442)
稀盐酸的用量 剩余固体的质量
第一次加入10 g 3.0 g
第二次加入10 g 2.0 g
第三次加入10 g 1.0 g
第四次加入10 g 0.6 g
(1)4.0 g石灰石样品中碳酸钙的质量是__3.4__ g。
(2)10 g稀盐酸能与__1.0__ g碳酸钙正好完全反应。
(3)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
[来源:Zxxk.Com]
解:设10 g稀盐酸中HCl的质量为x。
CaCO + 2HCl=== CaCl + HO + CO↑
3 2 2 2
100 73
1.0 g x= x=0.73 g
稀盐酸中HCl的质量分数为:×100%=7.3%
答:稀盐酸的溶质质量分数为7.3%。
9.(2017,黔东南)我州石灰石资源丰富,某课外小组同学为了测定石灰石中碳酸钙的质量
分数,取某地石灰石样品9.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质
不与稀盐酸反应),测得剩余固体的质量记录如下。
次数 1 2 3 4 5
加入稀盐酸质量/g 10 10 10 10 10
剩余固体质量/g 7.0 5.0 3.0 1.5 X
请计算:(导学号 58504443)
(1)X的值为__1.5__。
(2)该石灰石样品中碳酸钙的质量分数为__83.3%__。(结果精确到0.1%)
[来源:学科网]
(3)求所用稀盐酸溶质的质量分数。(写出计算过程)
解:设10 g稀盐酸中HCl的质量为x。
CaCO +2HCl===CaCl +HO+CO↑
3 2 2 2
100 73
2 g x
= x=1.46 g
所用稀盐酸溶质的质量分数为×100%=14.6%
答:所用稀盐酸溶质的质量分数为14.6%。
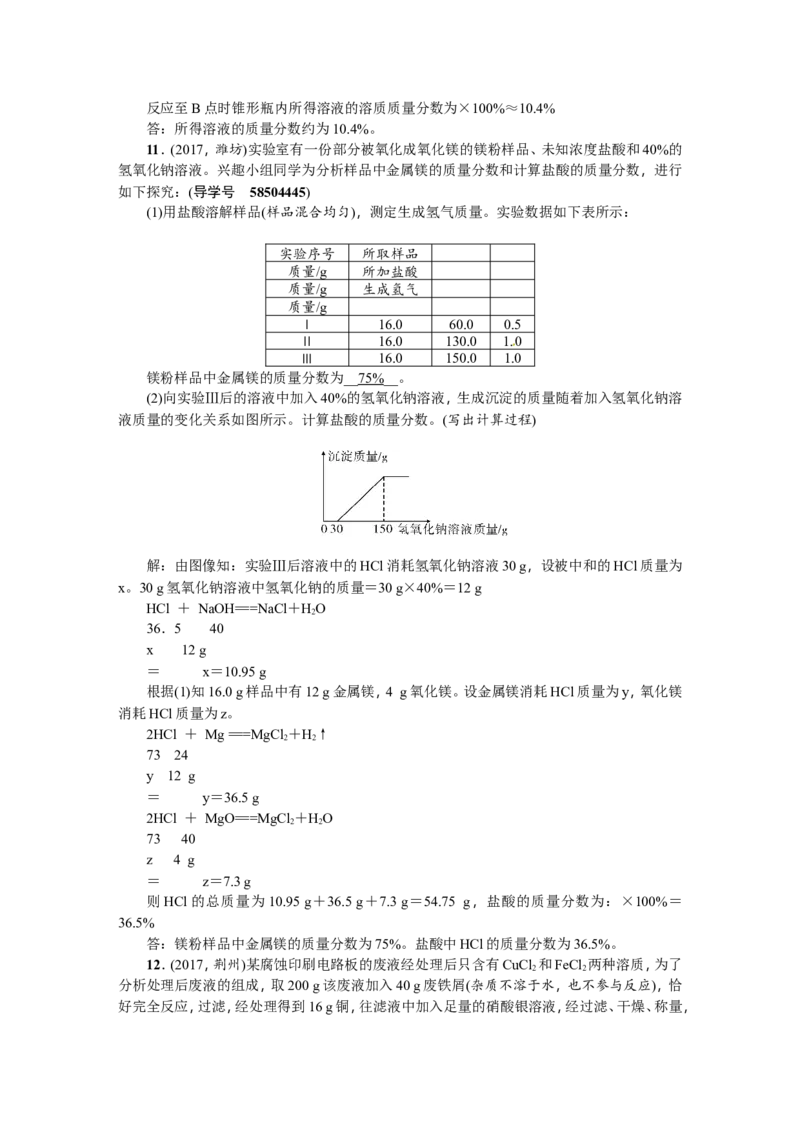
10.(2017,安顺)某锥形瓶盛有盐酸和氯化铜的混合溶液100 g,向其中逐滴加入溶质质量
分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如
图所示。请计算:(导学号 58504444)
(1)反应至A点时加入氢氧化钠溶液的质量为__40_g__。
(2)反应至B点时锥形瓶内所得溶液的溶质质量分数为多少?(计算结果保留至0.1%)
解:设40 g10%的NaOH溶液与HCl反应产生的氯化钠的质量为x。
NaOH + HCl === NaCl + HO
2
40 58.5
40 g×10% x
=,x=5.85 g
与氯化铜反应的氢氧化钠溶液的质量=200 g-40 g=160 g。
设160 g 10%的氢氧化钠溶液与氯化铜溶液反应生成氯化钠的质量为y,生成氢氧化铜的
质量为z。
2NaOH + CuCl ===2NaCl+Cu(OH) ↓
2 2
80 117 98
160 g×10% y z
= y=23.4 g
= z=19.6 g反应至B点时锥形瓶内所得溶液的溶质质量分数为×100%≈10.4%
答:所得溶液的质量分数约为10.4%。
11.(2017,潍坊)实验室有一份部分被氧化成氧化镁的镁粉样品、未知浓度盐酸和40%的
氢氧化钠溶液。兴趣小组同学为分析样品中金属镁的质量分数和计算盐酸的质量分数,进行
如下探究:(导学号 58504445)
(1)用盐酸溶解样品(样品混合均匀),测定生成氢气质量。实验数据如下表所示:
实验序号 所取样品
质量/g 所加盐酸
质量/g 生成氢气
质量/g
Ⅰ 16.0 60.0 0.5
Ⅱ 16.0 130.0 1.0
Ⅲ 16.0 150.0 1.0
镁粉样品中金属镁的质量分数为__75%__。
(2)向实验Ⅲ后的溶液中加入40%的氢氧化钠溶液,生成沉淀的质量随着加入氢氧化钠溶
液质量的变化关系如图所示。计算盐酸的质量分数。(写出计算过程)
[来源:学科网ZXXK]
解:由图像知:实验Ⅲ后溶液中的HCl消耗氢氧化钠溶液30 g,设被中和的HCl质量为
x。30 g氢氧化钠溶液中氢氧化钠的质量=30 g×40%=12 g
HCl + NaOH===NaCl+HO
2
36.5 40
x 12 g
= x=10.95 g
根据(1)知16.0 g样品中有12 g金属镁,4 g氧化镁。设金属镁消耗HCl质量为y,氧化镁
消耗HCl质量为z。
2HCl + Mg ===MgCl +H↑
2 2
73 24
y 12 g
= y=36.5 g
2HCl + MgO===MgCl +HO
2 2
73 40
z 4 g
= z=7.3 g
则HCl的总质量为10.95 g+36.5 g+7.3 g=54.75 g,盐酸的质量分数为:×100%=
36.5%
答:镁粉样品中金属镁的质量分数为75%。盐酸中HCl的质量分数为36.5%。
12.(2017,荆州)某腐蚀印刷电路板的废液经处理后只含有CuCl 和FeCl 两种溶质,为了
2 2
分析处理后废液的组成,取200 g该废液加入40 g废铁屑(杂质不溶于水,也不参与反应),恰
好完全反应,过滤,经处理得到16 g铜,往滤液中加入足量的硝酸银溶液,经过滤、干燥、称量,最终得到114.8 g AgCl固体。回答下列问题:(导学号 58504446)
(1)往废液中加入废铁屑发生反应的化学方程式为__Fe_+_CuCl == =FeCl _+_Cu__;往
2_ 2
滤液中加入硝酸银溶液发生反应的化学方程式为__FeCl _+_2AgNO == =2AgCl ↓ _+
2 3
_Fe(NO )__。
3 2
(2)求滤液中溶质的质量分数(精确到1%)。
(3)求200 g废液中FeCl 的质量分数(精确到1%)。
2
解:(2)设滤液中氯化亚铁的质量为x,与氯化铜反应的铁的质量为y,铁与氯化铜反应生
成氯化亚铁的质量为z。
Fe + CuCl ===FeCl + Cu
2 2
56 127 64
y z 16 g
==
解得:y=14 g z=31.75 g
所以滤液的质量为200 g+14 g-16 g=198 g
FeCl + 2AgNO ===2AgCl↓ + Fe(NO )
2 3 3 2
127 287
x 114.8 g
=
解得:x=50.8 g
所以滤液中溶质的质量分数为×100%≈26%
(3)原废液中氯化亚铁的质量为50.8 g-31.75 g=19.05 g
所以原废液中FeCl 的质量分数为×100%≈10%
2
答:(2)滤液中溶质的质量分数约为26%;(3)原废液中氯化亚铁的质量分数约为10%。