文档内容
九年级化学金属和金属材料检测题附参考答案
试卷说明:本试卷分为第Ⅰ卷、第Ⅱ卷,共17个小题。满分60分。
答题时间为50分钟。
可能用到的相对原子质量 Mg-24 H-1 S-32 O-16 Fe-56 Cl-35.5 Zn-65
第Ⅰ卷(选择题,共16分)
每小题只有1个选项符合题意,共8个小题,每小题2分,共16分。
( )1.铜能够制成铜片或拉成铜丝,是因为铜具有良好的
A.导热性 B.导电性 C.延展性 D.金属活动性
( )2.下列常见材料中,属于金属材料的是
A.不锈钢 B.玻璃钢 C.大理石 D.“塑料王”聚四氟乙烯
( )3.铁制品在通常情况下很易生锈,制造时往往在铁制品表面电镀一层铜起防锈
作用。下列说法正确的是
A.镀铜铁制品不可以在弱酸性条件下使用
B.镀铜铁制容器可盛硝酸银溶液
C.镀铜铁制品不易生锈的原因之一是使铁隔绝了空气
D.镀铜铁制品是一种合金
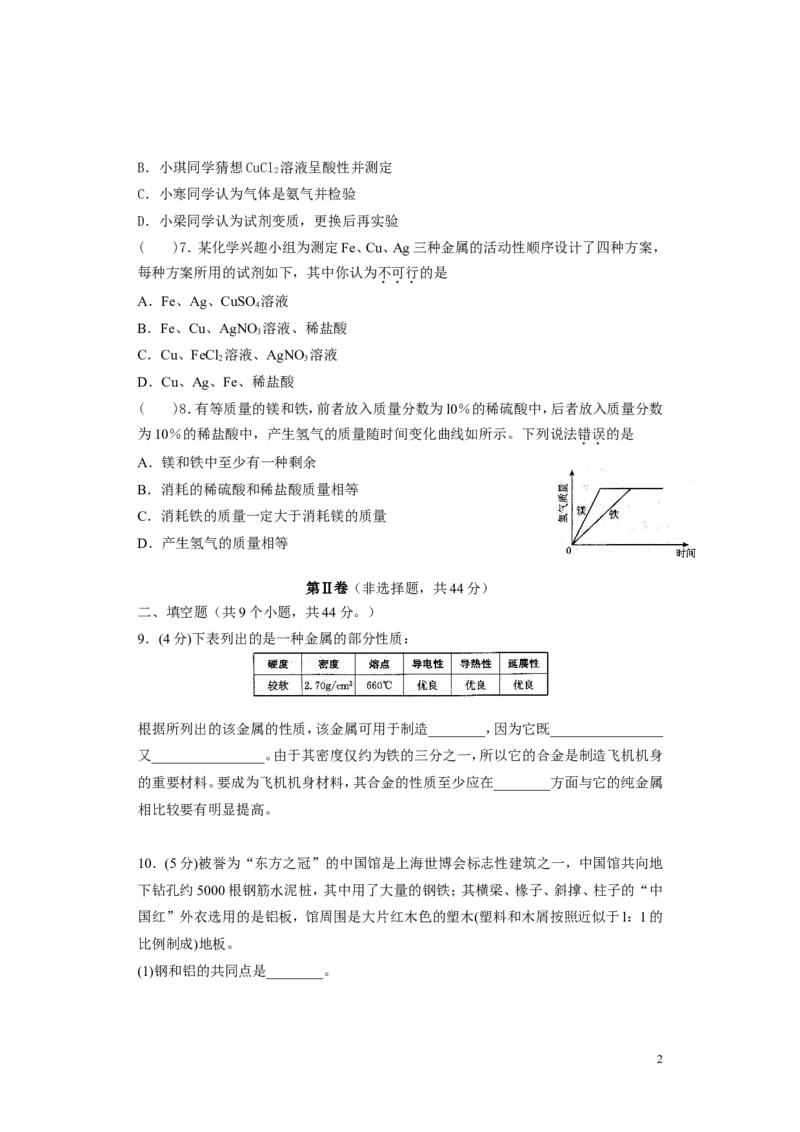
( )4.如图所示是探究铁锈蚀条件的装置。调节L端与R端的液面高度一致,塞紧
木塞,一周后观察。下列推断错误的是
A.b管中铁钉不会锈蚀
B.L端与R端液面高度仍然保持一致
C.该实验说明铁锈蚀与空气、水有关
D.若将a管中的水改为食盐水能加快铁的锈蚀
( )5.下列有关金属的说法错误的是
A.金属具有金属光泽,常温下金属都是固体
B.生铁和钢是含碳量不同的铁合金,其中生铁的含碳量大于钢的含碳量
C.炒完菜后,应及时除掉锅底的水,这样可以防止铁锅生锈
D.金属的回收利用是保护金属资源的有效途径之一
( )6.把铝箔放入CuCl 溶液中,铝箔表面覆盖了红色物质,一会儿又有大量气泡冒
2
出。同学们对“放出气体”这一异常现象进行猜想、实验。其中没有价值的是
( )
A.小宇同学推测气体是氢气并检验
1B.小琪同学猜想CuCl 溶液呈酸性并测定
2
C.小寒同学认为气体是氨气并检验
D.小梁同学认为试剂变质,更换后再实验
( )7.某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,
每种方案所用的试剂如下,其中你认为不可行的是
A.Fe、Ag、CuSO 溶液
4
B.Fe、Cu、AgNO 溶液、稀盐酸
3
C.Cu、FeCl 溶液、AgNO 溶液
2 3
D.Cu、Ag、Fe、稀盐酸
( )8.有等质量的镁和铁,前者放入质量分数为l0%的稀硫酸中,后者放入质量分数
为10%的稀盐酸中,产生氢气的质量随时间变化曲线如所示。下列说法错误的是
A.镁和铁中至少有一种剩余
B.消耗的稀硫酸和稀盐酸质量相等
C.消耗铁的质量一定大于消耗镁的质量
D.产生氢气的质量相等
第Ⅱ卷(非选择题,共44分)
二、填空题(共9个小题,共44分。)
9.(4分)下表列出的是一种金属的部分性质:
根据所列出的该金属的性质,该金属可用于制造________,因为它既________________
又________________。由于其密度仅约为铁的三分之一,所以它的合金是制造飞机机身
的重要材料。要成为飞机机身材料,其合金的性质至少应在________方面与它的纯金属
相比较要有明显提高。
10.(5分)被誉为“东方之冠”的中国馆是上海世博会标志性建筑之一,中国馆共向地
下钻孔约5000根钢筋水泥桩,其中用了大量的钢铁;其横梁、椽子、斜撑、柱子的“中
国红”外衣选用的是铝板,馆周围是大片红木色的塑木(塑料和木屑按照近似于l:1的
比例制成)地板。
(1)钢和铝的共同点是________。
2A.都是单质 B.都是合金 C.都能导电
(2)铝能与NaOH溶液反应,化学方程式为:2A1 + 2NaOH + 2H O = 2NaAlO + 3X,X的
2 2
化学式为________。
(3)每年世界上钢铁的产量很高,钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中
锈蚀,实际上是铁跟空气中的________和________共同作用的结果;
(4)为了防止钢铁锈蚀,人们常采用________________的方法(任写一种)来达到目的。
11.(3分)小思实验操作考试的题目是探究金属的化学性质,内容包括:铜在空气中灼烧、
锌与稀硫酸反应、铝丝与硫酸铜溶液反应。如图所示是他实验操作考试中的部分情景。
(1)上图中有一处错误的操作,该操作是________(填序号);
(2)操作A的现象是________________;
(3) 他 将 铝 丝 插 入 到 硫 酸 铜 溶 液 中 , 未 出 现 任 何 现 象 , 其 原 因 是
________________________。
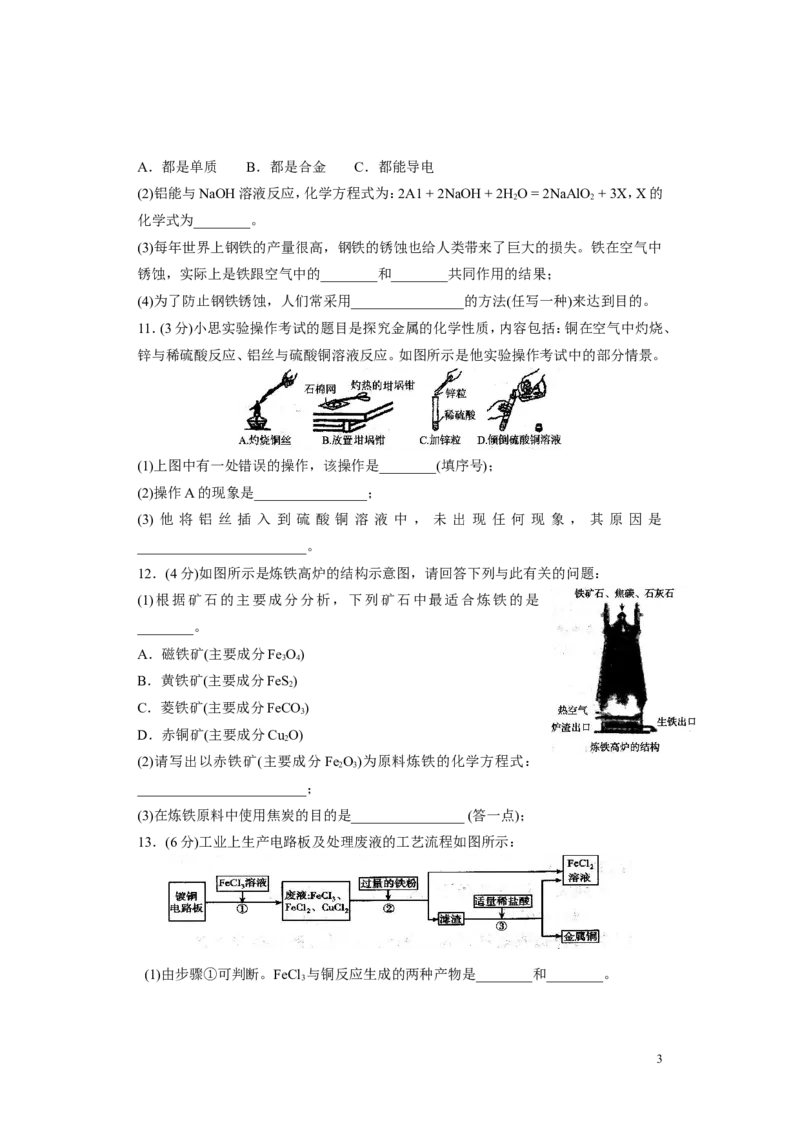
12.(4分)如图所示是炼铁高炉的结构示意图,请回答下列与此有关的问题:
(1)根据矿石的主要成分分析,下列矿石中最适合炼铁的是
________。
A.磁铁矿(主要成分Fe O)
3 4
B.黄铁矿(主要成分FeS)
2
C.菱铁矿(主要成分FeCO)
3
D.赤铜矿(主要成分Cu O)
2
(2)请写出以赤铁矿(主要成分Fe O)为原料炼铁的化学方程式:
2 3
________________________;
(3)在炼铁原料中使用焦炭的目的是________________ (答一点);
13.(6分)工业上生产电路板及处理废液的工艺流程如图所示:
(1)由步骤①可判断。FeCl 与铜反应生成的两种产物是________和________。
3
3(2)步骤②加入过量的铁粉,除能与废液中FeCl 反应外,还可发生反应的化学方程式
3
为________________________________________。
(3)步骤③加入稀盐酸,充分搅拌,当观察到________________现象时,说明滤渣只剩铜。
(4)步骤②③所得FeCl 可与一种单质发生化合反应生成FeCl ,实现循环使用。根据质
2 3
量守恒定律可推测该单质的化学式为________。
14.(7分)小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起
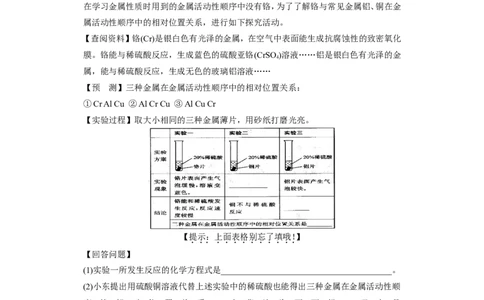
在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金
属活动性顺序中的相对位置关系,进行如下探究活动。
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化
膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO )溶液……铝是银白色有光泽的金
4
属,能与稀硫酸反应,生成无色的玻璃铝溶液……
【预 测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
【提示:上面表格别忘了填哦!】
【回答问题】
(1)实验一所发生反应的化学方程式是________________________________________。
(2)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺
序 的 相 对 位 置 关 系 , 小 燕 认 为 不 可 行 , 理 由 是
________________________________________。
(3)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相
对位置关系,这三种药品可以是________。
15.(6分)某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密
性良好)。一段时间后,进行观察。请你一起参与分析,并完成后续实验设计。
[观察现象]①装置中右侧导管中的液面升高。
4②铁钉生锈,试管底部有黑色固体物质。
[提出问题]导管中液面为何升高?黑色固体物质又是什么?
[理论分析]小组同学根据已学习过的知识分析得知,液面上升的原因是
________________________________________。
[猜想与假设]小组中的小明同学猜测该黑色固体可能含有:①Fe、②Fe O、③FeCl 、④
3 4 3
C四种物质。
[分析与验证]小组同学根据小明的四种猜测做了以下分析:
(1)小强同学认为一定含有碳,该结论也得到小组同学的认可,理由是
________________。
(2)小组同学不能确定是否含有铁,请你帮他们设计方案进行确认:
【提示:上面表格别忘了填哦!】
[知识链接]相信你一定在家中做过铁钉分别在水以及食盐水中生锈的实验,你的结论之
一是铁钉在________(填“水”或“食盐水”)中生锈快。
16.(5分)做完“铁在氧气里燃烧”实验后,小冬同学有两个疑惑不解的问题,于是她进
行了以下探究活动,请你一同参与。
[问题]铁燃烧的产物为什么不是Fe O 呢?
2 3
[查阅资料]
(1)Fe O 和Fe O 的分解温度、铁的熔点见下表:
3 4 2 3
(2) Fe O 高温时分解成Fe O。
2 3 3 4
[理论探讨]
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温应在________之
间,在此温度范围内Fe O 已分解,所以铁在氧气里燃烧的产物是Fe O。
2 3 3 4
[拓展延伸]
实验中为了防止集气瓶炸裂,必须________;
Fe O 高温时会分解成 Fe O 和一种气体,请写出此反应的化学方程式
2 3 3 4
5_________________;
有些超市的食品密封包装盒的透明盖内放有黑色的 FeO 粉末,若粉末的颜色
_____________,
就说明包装盒破损进气,这样售货员就能及时发现并处理。
17.(4分)Cu与Zn的合金称为黄铜,有优良韵导热性和耐腐蚀性,可用作各种仪器零件。
某化学兴趣小组的同学为了测定某黄铜的组成,取20g该黄铜样品于烧杯中,向其中分
5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固
体的质 量记录于下表:
试回答下列问题:
(1)上述表格中m的值为________;
(2)黄铜样品中锌的质量分数为________;
(3)在这5次实验中,第________次实验金属过量,硫酸完全反应了?这几次实验中参加
反应的硫酸的质量都是________?
参 考 答 案
一、选择题(每小题只有1个选项符合题意,共8个小题,每小题2分,共16分。)
1 2 3 4 5 6 7 8
C A C B A C D B
二、填空题(共9个小题,共44分。)
9.(4分) 导线 , 具有优良的导电性 , 具有优良的延展性 ; 硬度 。
10.(5分) ⑴ C ,
⑵ H ,
2
⑶ 水 氧气 ,
⑷ 喷漆等合理答案 。
611.(3分) ⑴ C ;
⑵ 铜丝表面变黑 ;
⑶ 铝丝表面的氧化膜未处理 。
12.(4分) ⑴ A ;
高温
⑵ 3CO + Fe O = 2Fe + 3CO ,
2 3 2
⑶ 做燃料提供热量(或提供还原剂一氧化碳)。
13.(6分) ⑴ FeCl CuCl ;
2 2
⑵ Fe + CuCl = FeCl + Cu ;
2 2
⑶ 不再有气泡产生 ;
⑷ Cl 。
2
14.(7分) 填表 :无现象 铝能与稀硫酸发生反应,反应速度较快
Al Cr Cu
⑴ Cr + H SO = CrSO + H ↑,
2 4 4 2
⑵ 无法比较铬和铝的金属活动性强弱 ,
⑶ Al CrSO 溶液 Cu等合理答案。
4
15.(6分) [理论分析]:铁钉生锈消耗了试管内的氧气,使试管内压强低于大气压 ;
[分析与验证] ⑴ 铁钉是铁合金,含有碳 ;
⑵ 填表 :稀盐酸 有气泡产生(或无气泡产生)
含有(或不含有)
[知识链接]:食盐水 。
16.(4分) [理论探讨]:1535~1538℃ ,
7[拓展延伸]:在集气瓶底部放少量的水或铺一层细沙 ,
高温
6Fe O = 4Fe O + O ↑,
2 3 3 4 2
由黑色变成红棕色 。
17.(4分) ⑴ 12.0 ,
⑵ 40% ,
⑶ 1、2、3次 3.92g
8