文档内容
第六单元碳和碳的氧化物 课题1 金刚石、石墨和C
学习内容 60
第1学时
知识与技能
1、知道不同元素可以形成不同物质,同种元素也可以形成不同物质;了解
金刚石、石墨和C 都是由碳元素形成的单质;
60
2、了解木炭、活性炭的吸附性
过程与方法
1、通过对金刚石、石墨和C 中碳原子排列方式的分析,懂得物质结构、
学习目标 60
性质和用途之间的关系;
2、通过木炭、活性炭对红墨水的西服实验,学会用对比实验的方法来解
决实际问题。
情感、态度与价值观
通过对C 、碳钠米管的发现及研究的介绍,学会用发展的眼光看问题、
60
提高学生的科学素质。
重点:金刚石、石墨和C 中原子排列方式的分析,物质的结构、性质和
60
学习重难点 用途之间的关系。
难点:物质的结构、性质和用途之间的关系
导学过程 自主空间
一、课前先学
1、阅读教材P 几种常见的碳单质,了解其物理性质、用途及结构的不同;木
104—106
炭、活性炭具有疏松多孔的结构,使得它们具有 性质,常利用这一性质
来 、 ,金刚石、石墨、C 的物理性质相差较大的原因是
60
。
2、阅读课本P 碳单质的化学性质。回答下列问题:
107—108
(1)在常温下,碳的化学性质 ,如古代的字画多年不褪色等。
(2)碳与 反应,化学方程式:充分燃烧 ;不充分燃
烧 。
(3)碳与某些 反应,写出三个不同化学方程式: ;
; 。
二、课堂探究
合作探究-:几种碳单质的物理性质及用途
1、学生展示自己收集的或身边有碳单质制品:如玻璃刻刀、铅笔芯、干电池等,
自学、讨论交流碳单质的物理性质及用途有关知识。
2、多媒体展示表格,有小组抢答
3、小组完成木炭吸附性实验
4、小组提问:有不清楚提出问,然后已搞懂小组给予回答,老师给予补充。
5、老师提问:⑴石墨在一定条件下转化成金刚石是什么变化?
⑵一种元素组成的物质一定是单质吗?
⑶自然界中元素的种类和物质的种类哪一个大⑷金刚石是钢吗?铅笔芯是铅
吗?
合作探究二:碳的化学性质
(一)常温下碳单质化学性质稳定
1、师投影展示一幅古代的字画:清明上河图,古代的字画一般是什么制作的?古
代的字画得以保存至今可以推测碳单质具有什么样的化学性质?
2、小组讨论并回答
学生再列举生活中利用碳单质在常温下化学性质稳定实例。
3、碳单质的化学性质在常温下为什么稳定?(提示:化学性质跟最外层电子数关
系密切)
(二)碳与氧气反应
1、学生回忆木炭在氧气中燃烧实验现象并完成课本P107表格
2、学习木炭不充分燃烧生成一氧化碳(煤炉在夜间封闭炉门的情况下主要生成一氧化碳)
3、学生默写化学方式,并标注变化前后碳的化合价。
4、说明指出:碳的单质在氧气中充分燃烧都生成二氧化碳
5、思考:如何从理论上证明金刚石和石墨都是碳元素组成的单质?
(三)碳与某些氧化物反应
1、[演示实验] 木炭粉与氧化铜的反应, 指导学生观察并归纳
现象:学生归纳、老师总结
2、反应方程式:C+2CuO 2Cu+CO↑
2
3、学生按小组分析这个反应发生的过程: 在这个反应中,氧化铜失去
氧变成铜,发生还原反应;木炭得到氧,发生氧化反应。这个实
验说明木炭具有还原性。
4、师提问: 上述反应在工业上有何用途?
(1)请你们思考,到目前为止,人类以有哪些炼铜的方法?
(2)如果将氧化铜换成氧化铁、三氧化钨,就可炼得铁和钨。请你们写出用木
炭炼铁、炼钨的化学方程式。
5、指导学生思考、交流、并动笔练习
合作探究三:归纳总结
1、碳单质的有关化学性质
2、联系实际指出碳单质的有关用途
3、让学生充分体会物质的性质决定物质的用途。
三、达标检测
1、金刚石和石墨的物理性质有很大差异的原因是( )
A.金刚石和石墨是由不同种元素组成的B.金刚石是单质,而石墨是化合物。
C.金刚石和石墨里碳原子的排方式不同D.金刚石不含杂质,而石墨含杂质。
2、近年来科学家们发现,除金刚石和石墨外,还有一些新的单质形式存在的碳。
其中发现较早并在研究中取得重要进展的是C ,下面有关C 的说法不正确的
60 60
是( )
A .它的一个分子里含有60个碳原子 B .它是一种新型的化合物
C .它的相对分子质量是720 D. 它是一种单质
3、在化学上把同种元素组成的不同的单质互称为同素异形体。下列各组物质不
是同素异形体的是( )
A .金刚石和石墨 B. 红磷和白磷C.氧气与臭氧(O) D.液氧和氧气
3
4、下列过程中发生了化学变化的是( )
A.石墨导电 B.金刚石切割金属
C.用铅笔写字 D.用焦炭冶炼
5、北约曾用“石墨炸弹”使南联盟的高压输变电线路短路,这是利用了石墨的(
)
A.可燃性 B.还原性 C.导电性 D.润滑性
6、用木材做木桩时,常把埋入地下的部分烧焦,目的是( )
A.烘干木材 B.使木桩变得更结实
C.烧死虫子 D.形成化学性质稳定的炭层
7、木炭粉、氢气分别与黑色氧化铜粉末反应时,下列叙述正确的是①反应都需
要加热或高温 ②都有红色物质生成 ( )
A.① B.② C.①② D.都不对
8、纳米材料被誉为21世纪最有前途的新型材料。纳米碳管是一种由碳原子构成
的直径为几个纳米的空心管(1 nm = 10-9m)。下列说法错误的是
A.纳米碳管是一种新型的有机化合物( )
B.纳米碳管材料如果完全燃烧,生成物是二氧化碳
C.纳米碳管材料管道多,表面积大,吸附能力强
D.纳米碳管在常温下化学性质稳定
学习反思第六单元碳和碳的氧化物
学习内容
课题2二氧化碳制取的研究 第2学时
知识和技能
1、了解实验室中制取二氧化碳的反应原理
2、探究实验室制取二氧化碳的装置,并利用设计的装置制取二氧化碳
3、了解实验室中制取气体的思路和方法
过程和方法
1、通过对获得二 氧化碳气体的途径的讨论与分析,探究实验室
学习目标
制取二氧化碳的理想药品,树立多角度、多层次的观察和分析问
题的意识。
、 让学生设计、组装实验装置,体验、反思和完善设计,掌握基本技能
情感、态度和价值观
1、增强对化学实验的好奇心和探究欲,激发学习化学的兴趣
2、培养合作、勤于思考、大胆实践的科学精神
重点:实验室制取二氧化碳的化学反应原理、实验装置和制取方法
学习重难点 难点:从实验室制取气体的思路出发,学习二氧化碳的实验室制
取方法
自主
导学过程
空间
一、课前先学
1.根据氧气的实验室制取的原理和教材P 页的相关内容回答:
100--111
确定气体发生装置时应考虑的因素是______ _____,
____ __。
收集气体的常用方法有______ ____法,________ ____法
和___________法;选择相应方法的依据是_____________________。
2.在家长的帮助下并利用各种媒体收集整理生活中产生CO 的例子。(看谁收集的
2
多!)
二、课堂探究
合作探究一:实验原理及相关资料(上网或书查阅)
1.除了生活中遇到的能产生CO 的例子外,我们在上节课也学到了能产生CO 的
2 2
反应,如__ __,
____ 。资料显示,含碳酸根离子的化合物(例如:碳酸
钠NaCO、大理石或石灰石或鸡蛋壳主要成分是CaCO,)同样能与稀、浓盐酸(HCl)
2 3 3
或稀硫酸(HSO)反应生成二氧化碳。
2 4
2.指导学生分组做一组对比的探究实验,并根据观察填写下表
碳酸钙粉末 石灰石(大理 石灰石(大理 碳酸钠粉末
反应物 与稀盐酸 石)和稀盐酸 石)和稀硫酸 与稀盐酸
反应现象
放出气泡的速度
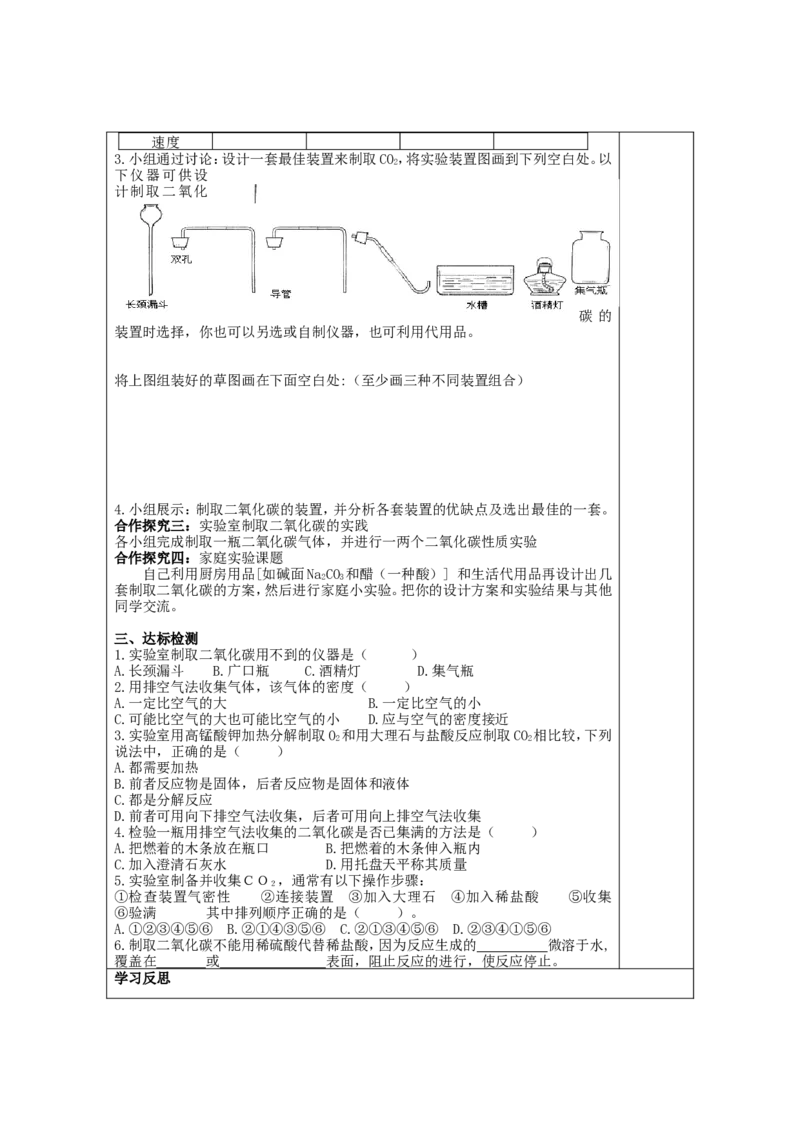
3.小组通过讨论:设计一套最佳装置来制取CO,将实验装置图画到下列空白处。以
2
下仪器可供设
计制取二氧化
碳 的
装置时选择,你也可以另选或自制仪器,也可利用代用品。
将上图组装好的草图画在下面空白处:(至少画三种不同装置组合)
4.小组展示:制取二氧化碳的装置,并分析各套装置的优缺点及选出最佳的一套。
合作探究三:实验室制取二氧化碳的实践
各小组完成制取一瓶二氧化碳气体,并进行一两个二氧化碳性质实验
合作探究四:家庭实验课题
自己利用厨房用品[如碱面NaCO 和醋(一种酸)] 和生活代用品再设计出几
2 3
套制取二氧化碳的方案,然后进行家庭小实验。把你的设计方案和实验结果与其他
同学交流。
三、达标检测
1.实验室制取二氧化碳用不到的仪器是( )
A.长颈漏斗 B.广口瓶 C.酒精灯 D.集气瓶
2.用排空气法收集气体,该气体的密度( )
A.一定比空气的大 B.一定比空气的小
C.可能比空气的大也可能比空气的小 D.应与空气的密度接近
3.实验室用高锰酸钾加热分解制取O 和用大理石与盐酸反应制取CO 相比较,下列
2 2
说法中,正确的是( )
A.都需要加热
B.前者反应物是固体,后者反应物是固体和液体
C.都是分解反应
D.前者可用向下排空气法收集,后者可用向上排空气法收集
4.检验一瓶用排空气法收集的二氧化碳是否已集满的方法是( )
A.把燃着的木条放在瓶口 B.把燃着的木条伸入瓶内
C.加入澄清石灰水 D.用托盘天平称其质量
5.实验室制备并收集CO ,通常有以下操作步骤:
2
①检查装置气密性 ②连接装置 ③加入大理石 ④加入稀盐酸 ⑤收集
⑥验满 其中排列顺序正确的是( )。
A.①②③④⑤⑥ B.②①④③⑤⑥ C.②①③④⑤⑥ D.②③④①⑤⑥
6.制取二氧化碳不能用稀硫酸代替稀盐酸,因为反应生成的 微溶于水,
覆盖在 或 表面,阻止反应的进行,使反应停止。
学习反思第六单元碳和碳的氧化物
学习内容
课题3 一氧化碳和二氧化碳(1) 第3学时
知识与技能:掌握二氧化碳的性质,通过对用途的学习,了解二氧化碳对
生活和环境的影响
过程与方法:通过实验探究二氧化碳化学性质,使学生经历科学探究的基本
学习目标 过程,体验探究的乐趣,教师应注意启发和引导,让学生对实验进行分析、推
理,得出结论
情感态度与价值观:通过实验探究二氧化碳的性质,增强学生学习化学的兴
趣,树立关注环境、热爱自然的意识。
重点:二氧化碳的性质和检验。
学习重难点
难点:二氧化碳与水、石灰水的反应。
导学过程 自主空间
一、课前先学
预习课本P113—117二氧化碳的性质和用途,并回答下列问题:
1、二氧化碳的物理性质有:在通常情况下,颜色 ,状态 ,气味
,密度比空气 , (易、可、微或难)溶于水。
2、二氧化碳的化学性质有:
①能否支持燃烧,能否燃烧?
②能与 反应,化学方程式
③与 反应,化学方程式 。
二、课堂探究
活动探究一
1、自主探究:实验[6-4]
实验现象
实验分析
实验结论
实验[6-5]
实验现象
实验分析
2、讨论、交流
根据实验[6-4][6-5]完成下表
密度 是否支
颜色 状态 气味 溶解性
(与空气相比) 持燃烧
CO
2
活动探究二
1.自主探究:实验[6-6]观察四朵花的颜色变化
(Ⅰ) (Ⅱ) (Ⅲ) (Ⅳ)
现象
分析
2.示范探究:将第一朵、第四朵小花分别放入干燥的大试管中加热,观察
现象
(Ⅰ) (Ⅳ)
现象分析
3.讨论交流
(1)通过对比分析,可知道二氧化碳的化学性质_______________ ,
反应的方程式________________________ _______。
(2)第四朵小花由红色重新变成紫色,说明___________ __ ___,
反应的方程式______________________ _____________。
活动探究三
1.展示:学生拿出自带的可口可乐、非常可乐、雪碧
2.师问:同学们是否能设计一个实验来证明这些饮料中有二氧化碳呢?指导
学生设计有效方案:
3.学生交流方案:
4、师生分析:澄清的石灰水变浑浊是因为CO 和C(OH) 反应生成了白色沉淀
2 a 2
碳酸钙的缘故
CO+ C(OH) = CCO↓+HO
2 a 2 a 3 2
用这个反应来检验CO
2
活动探究四
1.学生阅读:物质的性质决定了物质的用途。那么CO 有哪些用途呢?请同学们
2
阅读教材P —P
115 116
2.投影:大屏幕显示:CO 的用途
2
3.师生讨论:CO 的用途这么大,它对我们的生活和环境有没有负面的影响
2
呢?
大屏幕显示:漫画 全球变暖提问:地球为什么会大声喊救命?请同学们阅读
P
117
4.交流:谈谈温室效应对环境的影响以及防止温室效应进一步增强应采取什
么措施?
活动探究五
课外延伸:写一篇关于二氧化碳的小论文,题目有如下选择:
①二氧化碳的功与过②奇妙的二氧化碳③温室效应
三、达标检测
1.二氧化碳的下列用途,既跟它的物理性质有关,又跟它的化学性质有关的是
( )
A.灭火 B.制干冰 C.制化肥 D.温室肥料
2.下列说法不正确的是( )
A.温室里施用二氧化碳可提高农作物产量
B.干冰用于人工降雨和制冷剂,是利用它的化学性质
C.二氧化碳属于氧化物,也属于化合物和纯净物
D.将二氧化碳加压溶解可制成汽水
3.下列过程只发生物理变化的是( )。
A.二氧化碳通入水中
B.绿色植物吸收二氧化碳发生光合作用
C.刷过石灰浆的墙壁日久变硬
D.将二氧化碳加压、降温压缩成干冰
4.用玻璃管向盛有紫色石蕊试液的试管里吹气,过一会儿再给试管加热,试管
里溶液颜色变化情况是( )
A.紫色→红色→紫色 B.紫色→蓝色→红色
C.蓝色→红色→紫色 D.红色→紫色→蓝色
5.按要求写出下列反应的化学方程式:
(1)有二氧化碳生成的化合反应: ;
(2)有二氧化碳生成的置换反应: ;
(3)有二氧化碳生成的分解反应: ;
(4)有二氧化碳参加的化合反应:学习反思第六单元碳和碳的氧化物
学习内容
一氧化碳和二氧化碳(2) 第4学时
知识与技能
1、了解一氧化碳的性质;
2、 知道一氧化碳还原氧化铜的原理及使人中毒的原因
过程与方法
1、通过课件演示加深对一氧化碳毒性的理解,加强安全意识。
2、通过一氧化碳还原氧化铜实验的课件演示及因操作错误导致实验失
败的教训,强调实验操作的规范。
学习目标
3、通过讨论“一氧化碳还原氧化铜实验的尾气的处理?”让学生学会
发现问题、提出问题、主动讨论交流、解决问题的能力,逐步养成良好的学习
习惯和学习方法。
情感、态度和价值观
1、通过一氧化碳毒性、可燃性还原性的探究,懂得要一分为二地对待问题、
看待问题;培养勤于思考的科学习惯;
2、关注与一氧化碳有关的社会问题,主动参与社会决策、美化环境献计献策
重点:1.一氧化碳的物理性质;
学习重难点 2.一氧化碳的毒性、可燃性、还原性
难点:一氧化碳的还原性
导学过程 自主空间
一、课前先学
1.上网或查阅报刊,了解一氧化碳中毒事件。
2.阅读课本P117—118,并回答下列问题:
⑴一氧化碳的物理性质:颜色 ,状态 ,气味
,密度 。
⑵一氧化碳的化学性质有:
① ,
化学方程式 ;
② ,
化学方程式 。
二、课堂探究
活动与探究一:一氧化碳的可燃性
1.师引导:CO有什么样的化学性质呢?大家回忆一下,煤燃烧很旺时发出什么
颜色的火焰?请同学们观看大屏幕结合教材内容,尽可能地写出煤炉里发生
的化学反应方程式。
2.投影:大屏幕显示彩色图片:煤炉里煤层上方的蓝色火焰(见附2)
3. 学生观看图片,阅读教材,讨论交流,写出方程式。
点燃
1可燃性 2CO+ O====== 2CO
2 2
4.各小组互评互查后代表发言。
活动与探究二:一氧化碳的毒性
1、学生谈了解到的煤气中毒事件
2、学生分析煤气中毒:煤的燃烧产生了CO,因此冬天用煤火取暖或用煤气热水
器洗澡时,若室内不通风,容易发生煤气中毒。如刚才新闻报道中的煤气中毒
事件。同学们一定很想知道中毒的原因。请仔细观察实验。
3、演示:向新鲜的鸡血中(已加入抗凝剂了)通入CO,看血液颜色的变化
4、小结 CO的毒性
5、讨论如何防止煤气中毒
活动与探究三:一氧化碳的还原性
1、多媒体播放:动画演示一氧化碳还原氧化铜(附后4)
2、学生观看动画,
3、分析:认真观察其现象并记录,通过现象分析本质, 化学方程式。
4.学生分析反应的过程,讨论后得出CO和碳一样,具有还原性的正确结论。
5、讨论实验注意事项: 。
活动与探究四:一氧化碳的用途
1、根据性质决定用途,学生互相讨论一氧化碳的用途
2、学生得出结论: 。
活动与探究五:一氧化碳和二氧化碳的比较
对
CO CO
比 2
对
比 物
项
目
色、态、味
物 理
密度
性 质
溶解性
跟水反应
跟C(OH) 反应
化 学 a 2
性 质 可燃性
还原性
剧毒性
三、达标检测
1.5月31日是“世界无烟日”。吸烟对人体有害,吸烟产生的气体中含有一种
能与血液中血红蛋白结合的有毒气体,它是( )
A.CO B.SO C.CO D.HO
2 2 2
2.等质量的碳和一氧化碳分别与足量的氧气反应,下列说法中正确的
A.一氧化碳需要的氧气多 B.碳需要的氧气多( )
C.一氧化碳生成的二氧化碳多 D.生成的二氧化碳一样多
3.不能用来鉴别CO和CO 两种气体的方法是( )
2
A.通入澄清石灰水 B.观察颜色
C.通入紫色石蕊溶液 D.点燃
4.在一个密闭容器中,充入a个CO分子和b个O 分子。在一定条件下充分反应
2
后,容器内碳原子数和氧原子数之比为( )
A.a/b B.a/(a + 2b) C.a/2(a + b) D.a/2b
5.某同学为解决助力车污染空气问题,提出以下建议:①在公路上用灼热的
CuO与产生的CO反应;②在公路上喷洒石灰水吸收CO;③在助力车尾部点燃
CO;④改进助力车发动机的结构,提高燃料的燃烧效率;⑤控制行驶助力车的
数量。这些建议中,你认为切实可行的是( )
A.①② B.①②③ C.①②⑤ D.④⑤
6.某CO和CO 的混合气体中,碳的质量分数为36%。取5.0 g该气体混合物通
2
过足量灼热的氧化铜,再将气体通入足量的澄清石灰水中,得到白色沉淀的
质量为( )。
A.5 g B.10 g C.15 g D.20 g
学习反思