文档内容
金属和金属材料单元小结配套测试题(基础)
它们的载重量以及提高运行速度,并具有抗海水腐蚀、避磁性等特点。
一、金属材料
⑶铜合金:黄铜:铜、锌的合金;青铜:铜、锡的合金;白铜:铜、镍的合金。
⑷钛和钛合金:被认为是21世纪的重要金属材料。
1.金属材料包括__________和________两类。
性质:优异的耐腐蚀性,对海水、空气和若干腐蚀介质都稳定,可塑性好,强度大,有密度小,又称
2.在生活中,应用最广泛的金属(按使用历史长短,括号内填写最早使用历史时期)依次是_____(
亲生物金属。
)、______( )、______( );
用途:喷气式发动机、飞机机身、人造卫星外壳、火箭壳体、医学补形、造纸、人造骨、海水淡化设
3.目前,产量居前三位的金属依次是_______________。( 100多年前,开始了铝的使用,因铝具有
备、海轮、舰艇的外壳等。
____________和____________等许多优良性能,铝的产量已超过了______,位于第二位。)
二、金属的化学性质
4.金属共同的物理物理性质:①大多数金属都具有____________,不透明;②在室温下除_____为液体,
金属的化学性质体现在它们与____________反应,与_____________反应、与_____________反应。
其余金属均为________;③具有良好的__________和___________;④有良好的_________,适于机 1. 金属与氧气的反应
械加工;⑤密度_________,熔点_________。 ⑴_____________都能与氧气反应,但反应的难易和剧烈程度不同。_________等在常温下就能与
5.一些金属的特性:①铁、铝等大多数金属都呈______色,铜呈______色,金呈______色;②常温下大 氧气反应___________等在常温下几乎不能单独与氧气反应,但在点燃或加热的情况下可以发生反
多数金属都是固体,汞却是液体;③各种金属的导电性、导热性、密度、熔点、硬度等差异较大; 应;_______等在高温时也不与氧气反应【所以俗话说“___________________________”】。
______的密度最大,______的密度最小;______的熔点最高,______的熔点最低;______的导电性 ⑵铝在常温下与空气中的氧气反应,在其表面生成_________________________,从而
和导热性最好,______的硬度最大;地壳中含量最多的金属是______,人体中含量最多的金属是 _____________,因此铝具有很好的抗腐蚀性能。【镁与铝类似】
______,目前世界年产量最高的金属是______。 2.金属与酸的反应【分别写出镁、铝、锌、铁与稀盐酸和稀硫酸反应的方程式】
稀盐酸 稀硫酸
6.讨论题:⑴ 为什么菜刀、镰刀、锤子等用铁制而不用铅制?
镁
⑵银的导电性比铜好,为什么电线一般用铜制而不用银制?
铝
⑶为什么灯泡里的灯丝用钨制而不用锡制?如果用锡制的话,可能会出现什么情况?
为什么有的铁制品如水龙头等要镀铬?如果镀金会怎样? 锌
7.物质的用途主要由______________决定,但这不是唯一的决定因素,在考虑物质的用途时,还需要 铁
考虑__________、__________、是否美观、使用是否便利,以及__________________________和 3.金属与化合物溶液的反应
________________________等多种因素。 ⑴铁丝浸入硫酸铜溶液中,现象为浸入溶液中的铁钉表面覆盖_______________________,溶液由
8.合金:在金属中加热熔合某些__________________,形成具有____________的物质。
_______逐渐变为____________;反应的化学方程式为__________________________,反应后金属的
⑴金属在熔合了其它金属和非金属后,不仅组成上发生了变化,其内部组成结构也发生了改变,从 质量_________,溶液的质量_________。能否有铁制品盛放硫酸铜溶液(或农药波尔多液)________。
而引起性质的变化。如:合金的强度和硬度一般比组成它们的纯金属________,抗腐蚀性能
⑵铝丝浸入硫酸铜溶液中,现象为浸入溶液的铝丝表面覆盖一层紫红色的物质,溶液由_________
_________,熔点一般比组成它们的纯金属_________。
逐渐变为____________;反应的化学方程式为__________________________________,反应后金属的
⑵合金的很多性能与组成它们的纯金属不同,使合金更容易适于不同的用途。 质量_________,溶液的质量_________。
⑶日常使用的金属材料,大多数为合金。 ⑶铜丝浸入硝酸银溶液中,现象为浸入溶液中的铜丝表面覆盖_______________________,溶液由
⑷合金形成条件:其中任一金属的_______不能高于另一金属的_______(当两种金属形成合金时)。
_________逐渐变为____________;反应的化学方程式为__________________________,反应后金属
9.几种常见合金
的质量_________,溶液的质量_________。
⑴铁合金:主要包括__________和__________,它们的区别是_____________________,生铁含碳
⑷结论:①根据以上实验,说明铝、铁、铜、银四种金属的活动性由强到弱的顺序为:_____________;
量______________,钢的含碳量为______________。钢比生铁具有更多的优良性能,易于加工,用途更
②_____________的金属能把_____________的金属从其化合物溶液中置换出来。
为广泛。
⑸注意:①此类反应一定在溶液中进行,_____________的化合物一般不与金属反应。
⑵铝合金:铝中加入镁、铜、锌等金属形成合金。广泛应用于制造飞机、舰艇和载重汽车等,可增加
② K、Ca、Na活动性非常强,能同溶液中的水剧烈反应,不能用它们置换化合物溶液中的金属。
1⑹置换反应:由__________与一种_______反应,生成另一种_____________的反应叫做置换反应。 (3)主要设备:高炉
(4)冶炼过程中发生的化学反应:
三、金属活动性顺序
①在高温下,焦炭跟氧气反应生成二氧化碳,反应为:______________________________;
1.人们通过大量的实验验证,得到常见金属的活动性顺序为:
②二氧化碳被焦炭还原成一氧化碳,反应为:________________________________;
___________________________________
③一氧化碳再跟铁矿石中的氧化物反应,生成铁,反应为:__________________________;
(由强到弱,填元素符号)
练习:按如右图所示,写出有关化学方程式(注:②③要求各写三个):
2.应用:⑴在金属活动性顺序里,金属的位置__________,它的活动性__________。
Fe O
① 2 3
FeCl
⑵在金属活动性顺序里,______________________________能置换出盐酸、稀硫酸中的氢。 ② ③ ⑥ 2
①
⑶在金属活动性顺序里,____________________能把______________________________从它们 ③ F e 3 O 4 Fe ⑤ FeSO 4
②
化合物的溶液里置换出来(K、Ca、Na除外)。 ④ ④
Cu
四、矿石 ⑤ 铁锈
1.金属资源的存在方式:地球上的金属资源广泛存在于________________中,大多数金属性质较活泼,所以它们以⑥
六、金属的锈蚀和保护
2.常见矿石名称与其主要成分:赤铁矿的主要成分是___________;铝土矿的主要成分是___________;
常用的金属普遍有比较活泼的化学性质,所以大多数金属易被腐蚀,给人类造成巨大损失。
黄铁矿的主要成分是___________;磁铁矿的主要成分是___________。
1、钢铁的生锈实际上是铁跟空气中的_______、_______等物质发生一系列的化学反应,生成铁锈。
五、铁的冶炼
铁锈是一种复杂的铁的氧化物的水合物,可用______________表示。
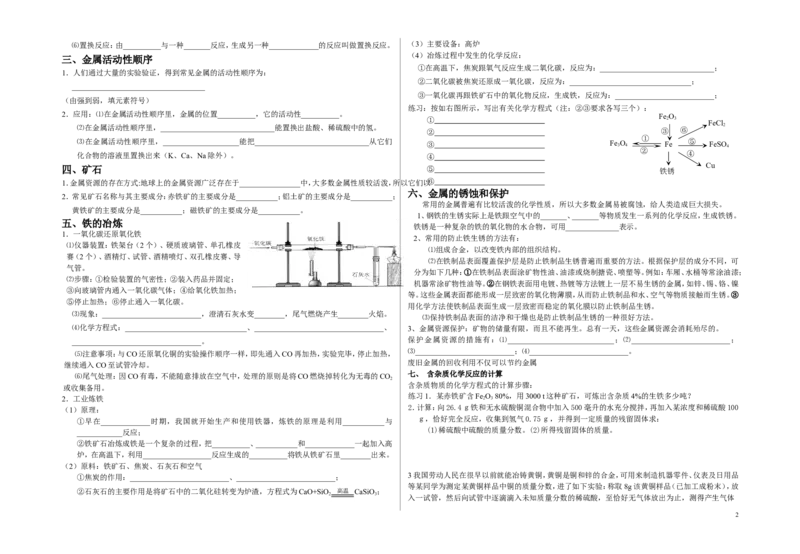
1.一氧化碳还原氧化铁
2、常用的防止铁生锈的方法有:
⑴仪器装置:铁架台(2个)、硬质玻璃管、单孔橡皮
⑴组成合金,以改变铁内部的组织结构。
赛(2个)、酒精灯、试管、酒精喷灯、双孔橡皮赛、导
⑵在铁制品表面覆盖保护层是防止铁制品生锈普遍而重要的方法。根据保护层的成分不同,可
气管。
分为如下几种:①在铁制品表面涂矿物性油、油漆或烧制搪瓷、喷塑等。例如:车厢、水桶等常涂油漆;
⑵步骤:①检验装置的气密性;②装入药品并固定;
机器常涂矿物性油等。②在钢铁表面用电镀、热镀等方法镀上一层不易生锈的金属,如锌、锡、铬、镍
③向玻璃管内通入一氧化碳气体;④给氧化铁加热;
等。这些金属表面都能形成一层致密的氧化物薄膜,从而防止铁制品和水、空气等物质接触而生锈。③
⑤停止加热;⑥停止通入一氧化碳。
用化学方法使铁制品表面生成一层致密而稳定的氧化膜以防止铁制品生锈。
⑶现象:__________________________,澄清石灰水变________,尾气燃烧产生________火焰。
⑶保持铁制品表面的洁净和干燥也是防止铁制品生锈的一种很好方法。
⑷化学方程式:________________________________、__________________________________、 3、金属资源保护:矿物的储量有限,而且不能再生。总有一天,这些金属资源会消耗殆尽的。
__________________________________。 保护金属资源的措施有:⑴____________________________;⑵__________________________;
⑶__________________________;⑷__________________________。
⑸注意事项:与CO还原氧化铜的实验操作顺序一样,即先通入CO再加热,实验完毕,停止加热,
废旧金属的回收利用不仅可以节约金属
继续通入CO至试管冷却。
七、 含杂质化学反应的计算
⑹尾气处理:因CO有毒,不能随意排放在空气中,处理的原则是将CO燃烧掉转化为无毒的CO
2
含杂质物质的化学方程式的计算步骤:
或收集备用。
练习1.某赤铁矿含Fe O 80%,用3000 t这种矿石,可炼出含杂质4%的生铁多少吨?
2.工业炼铁 2 3
2.计算:向26.4g铁和无水硫酸铜混合物中加入500毫升的水充分搅拌,再加入某浓度和稀硫酸100
(1)原理:
g,恰好完全反应,收集到氢气0.75g,并得到一定质量的残留固体求:
①早在_____________时期,我国就开始生产和使用铁器,炼铁的原理是利用___________与
(1)稀硫酸中硫酸的质量分数。(2)所得残留固体的质量。
____________反应;
②铁矿石冶炼成铁是一个复杂的过程,把__________、___________和_____________一起加入高
炉,在高温下,利用__________________反应生成的__________将铁从铁矿石里________出来。
(2)原料:铁矿石、焦炭、石灰石和空气
①焦炭的作用:__________________________、__________________________;
3我国劳动人民在很早以前就能冶铸黄铜,黄铜是铜和锌的合金,可用来制造机器零件、仪表及日用品
等某同学为测定某黄铜样品中铜的质量分数,进了如下实验:称取8g该黄铜样品(已加工成粉末),放
②石灰石的主要作用是将矿石中的二氧化硅转变为炉渣,方程式为CaO+SiO 高温 C aSiO ;
2 3
入一试管,然后向试管中逐滴滴入未知质量分数的稀硫酸,至恰好无气体放出为止,测得产生气体
20.1g
(1)通过计算求出该黄铜样品中铜的质量分数;(2)若想求出该稀硫酸中溶质的质量分数,你认为
还需测出哪些数据?
3