文档内容
二轮复习:中考化学实验物质的分离、检验、提纯
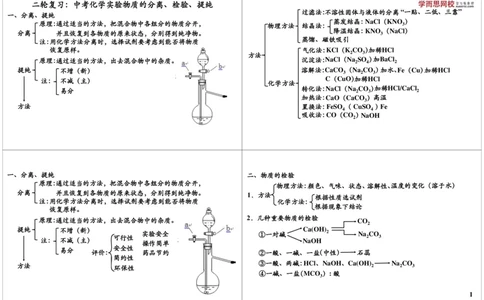
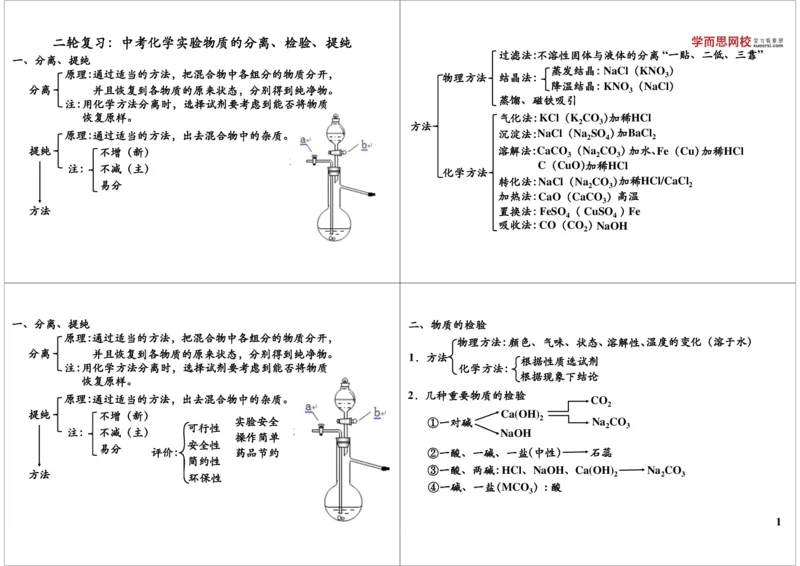
过滤法:不溶性固体与液体的分离“一贴、二低、三靠”
一、分离、提纯
蒸发结晶:NaCl(KNO )
原理:通过适当的方法,把混合物中各组分的物质分开, 物理方法 结晶法: 3
降温结晶:KNO (NaCl)
分离 并且恢复到各物质的原来状态,分别得到纯净物。 3
蒸馏、磁铁吸引
注:用化学方法分离时,选择试剂要考虑到能否将物质
恢复原样。 气化法:KCl(K CO )加稀HCl
2 3
方法
原理:通过适当的方法,出去混合物中的杂质。
沉淀法:NaCl(Na
2
SO
4
)加BaCl
2
提纯 不增(新) 溶解法:CaCO (Na CO )加水、Fe(Cu)加稀HCl
3 2 3
C(CuO)加稀HCl
注: 不减(主)
化学方法
转化法:NaCl(Na CO )加稀HCl/CaCl
易分 2 3 2
加热法:CaO(CaCO )高温
3
方法 置换法:FeSO (CuSO )Fe
4 4
吸收法:CO(CO )NaOH
2
一、分离、提纯 二、物质的检验
原理:通过适当的方法,把混合物中各组分的物质分开,
物理方法:颜色、气味、状态、溶解性、温度的变化(溶于水)
分离 并且恢复到各物质的原来状态,分别得到纯净物。 1.方法
根据性质选试剂
注:用化学方法分离时,选择试剂要考虑到能否将物质 化学方法:
根据现象下结论
恢复原样。
2.几种重要物质的检验
原理:通过适当的方法,出去混合物中的杂质。 CO
2
提纯 不增(新) Ca(OH)
实验安全 ①一对碱 2 Na CO
可行性 2 3
注: 不减(主) NaOH
操作简单
安全性
易分
评价: 药品节约 ②一酸、一碱、一盐(中性) 石蕊
简约性
③一酸、两碱:HCl、NaOH、Ca(OH) Na CO
方法 2 2 3
环保性
④一碱、一盐(MCO ):酸
3
1Cu2+ 蓝色 【例1】(2012东城一模)下列各组物质的两种鉴别方法都正确的是( )
Fe3+ 黄色 序号 物质 方法一 方法二
找颜色
Fe2+ 浅绿色 ① 一氧化碳和二氧化碳 点燃 闻气味
⑤不用试剂、组内鉴别 ② 食盐水和水 测pH 蒸发结晶
找特殊反应: ③ 氢氧化钠和碳酸钙 加水溶解 加入盐酸
④ 镁条和铝条 在空气中点燃 加入稀硫酸
⑥只用酚酞和组内试剂
A. ①和② B. ①和③ C. ②和④ D. ③和④
一酸、一碱、一盐 (中性) 【例2】某种混合气体中可能含有N 、HCl、CO中的一种或几种,为确定该混
2
合气体的成分,将混合气体依次通过NaHCO 溶液和灼热的Fe O ,气
3 2 3
体体积无变化但是有黑色物质生成;再通过NaOH溶液,气体体积明
显减小;将燃着的木条伸入装有剩余气体的集气瓶中,木条熄灭(假
设每步反应都是完全的),则下列说法中正确的是(提示:气体的分
子数之比等于体积比)( )
A. 一定有CO和HCl,肯定无N B. 一定有CO和N ,可能有HCl
2 2
C. 一定有CO和HCl,可能有N D. 一定有CO和N ,肯定无HCl
2 2
【例3】下列各组溶液中,必须另加试剂才能鉴别开来的一组是( ) 【例4】下列是分析已变质氢氧化钠溶液的相关实验,其中合理的是( )
A. NaOH、FeCl 、MgSO 、NaCl
3 4 序号 实验目的 实验过程
B. KOH、HCl、CuSO 、KNO
4 3 取少量溶液,滴加盐酸,将生成的气体通入
C. Na CO 、BaCl 、HCl、KCl ① 证明变质
2 3 2 石灰水
D. Na
2
CO
3
、KNO
3
、NaCl、CaCl
2 取少量溶液,加入石灰水,过滤,向滤液中
② 确定成分
【例4】(2013年朝阳一模)除去下列物质中所含的少量杂质,方法正确的是 滴加酚酞溶液
( ) 取一定量溶液,加入盐酸,用氢氧化钠固体
③ 测定纯度
吸收气体,称量
物质 所含杂质 除杂质的方法
④ 除去杂质 取溶液,滴加石灰水至恰好完全反应,过滤
A 二氧化锰 氯化钠 加水溶解,过滤,蒸发结晶
B 氯化钠溶液 碳酸钠 加入过量稀盐酸,加热蒸发
C 氯化钙溶液 稀盐酸 加入过量氢氧化钙,过滤
D 氢氧化钠溶液 碳酸钠 加入适量的石灰水
2