文档内容
二轮复习:中考化学实验气体的制备与净化
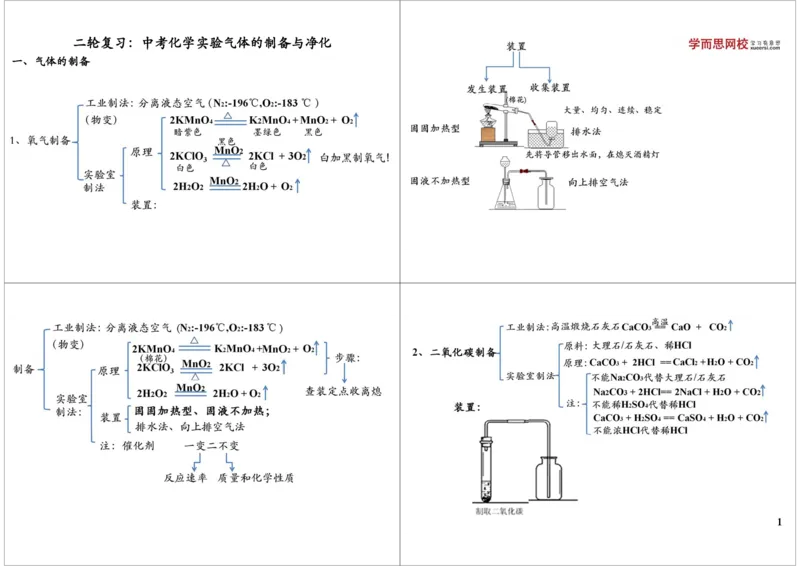
一、气体的制备
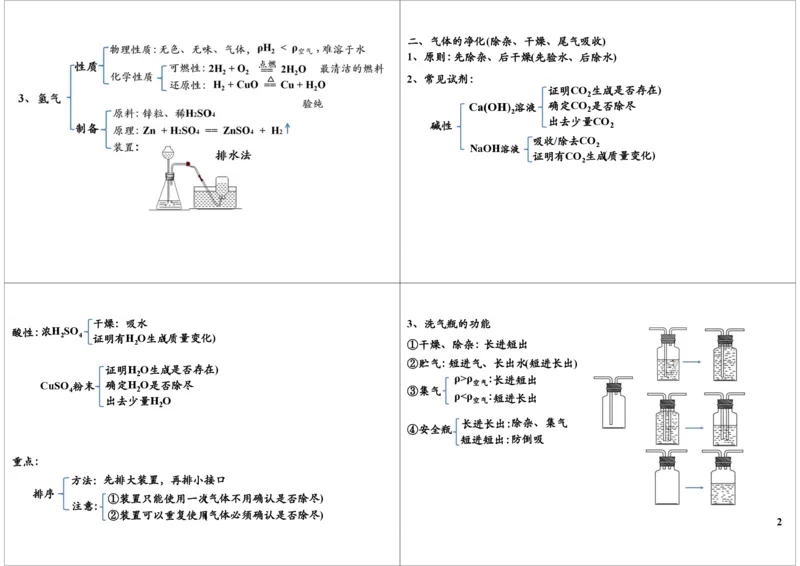
1二、气体的净化(除杂、干燥、尾气吸收)
1、原则:先除杂、后干燥(先验水、后除水)
2、常见试剂:
证明CO 生成(是否存在)
2
Ca(OH) 2 溶液 确定CO 2 是否除尽
出去少量CO
碱性 2
吸收/除去CO
NaOH溶液 2
证明有CO 生成(质量变化)
2
干燥:吸水 3、洗气瓶的功能
酸性:浓H SO
2 4 证明有H O生成(质量变化)
2 ①干燥、除杂:长进短出
②贮气:短进气、长出水(短进长出)
证明H O生成(是否存在)
2
ρ>ρ :长进短出
CuSO 粉末 确定H O是否除尽 空气
4 2 ③集气
出去少量H O
ρ<ρ
空气
:短进长出
2
长进长出:除杂、集气
④安全瓶
短进短出:防倒吸
重点:
方法:先排大装置,再排小接口
排序
①装置只能使用一次(气体不用确认是否除尽)
注意:
②装置可以重复使用(气体必须确认是否除尽)
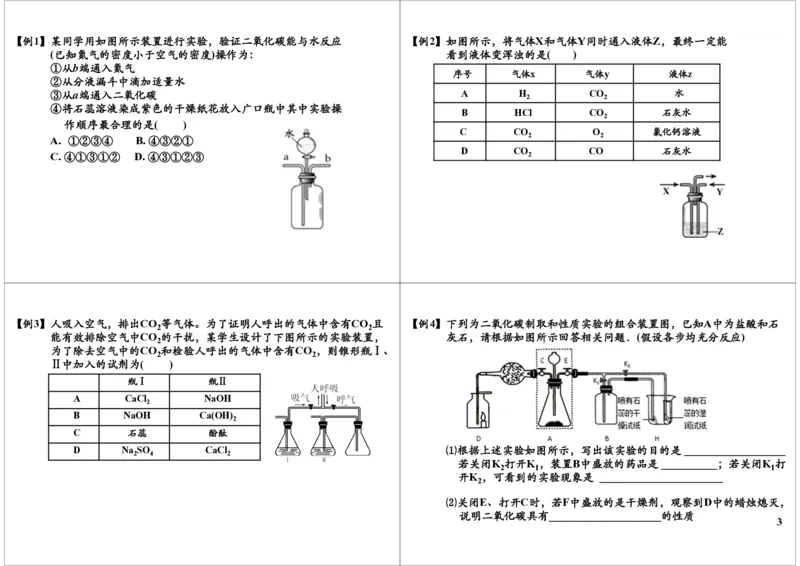
2【例1】某同学用如图所示装置进行实验,验证二氧化碳能与水反应 【例2】如图所示,将气体X和气体Y同时通入液体Z,最终一定能
(已知氮气的密度小于空气的密度)操作为: 看到液体变浑浊的是( )
①从b端通入氮气
序号 气体x 气体y 液体z
②从分液漏斗中滴加适量水
③从a端通入二氧化碳 A H CO 水
2 2
④将石蕊溶液染成紫色的干燥纸花放入广口瓶中其中实验操
B HCl CO 石灰水
2
作顺序最合理的是( )
C CO O 氯化钙溶液
2 2
A. ①②③④ B. ④③②①
D CO CO 石灰水
C. ④①③①② D. ④③①②③ 2
【例3】人吸入空气,排出CO 等气体。为了证明人呼出的气体中含有CO 且 【例4】下列为二氧化碳制取和性质实验的组合装置图,已知A中为盐酸和石
2 2
能有效排除空气中CO 的干扰,某学生设计了下图所示的实验装置, 灰石,请根据如图所示回答相关问题.(假设各步均充分反应)
2
为了除去空气中的CO 和检验人呼出的气体中含有CO ,则锥形瓶Ⅰ、
2 2
Ⅱ中加入的试剂为( )
瓶Ⅰ 瓶Ⅱ
A CaCl NaOH
2
B NaOH Ca(OH)
2
C 石蕊 酚酞
D Na SO CaCl ⑴根据上述实验如图所示,写出该实验的目的是__________________
2 4 2
若关闭K 打开K ,装置B中盛放的药品是__________;若关闭K 打
2 1 1
开K ,可看到的实验现象是 ______________________
2
⑵关闭E、打开C时,若F中盛放的是干燥剂,观察到D中的蜡烛熄灭,
说明二氧化碳具有____________________的性质
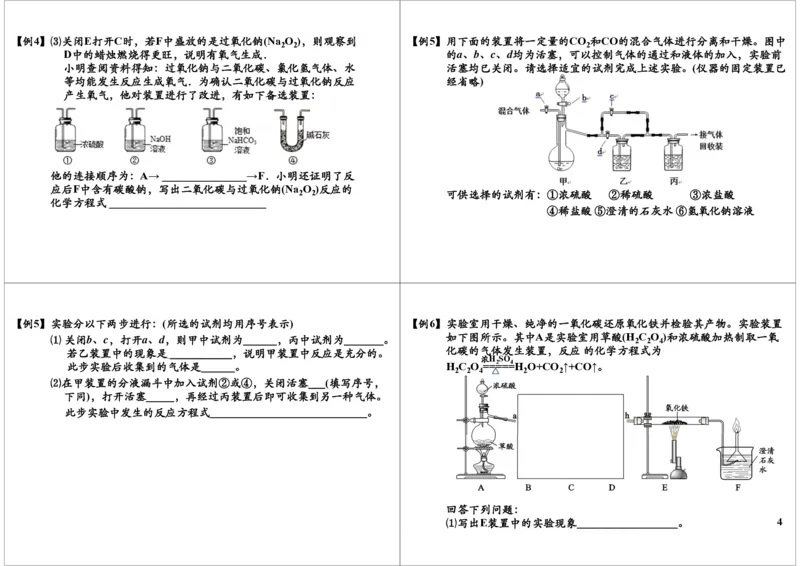
3【例4】⑶关闭E打开C时,若F中盛放的是过氧化钠(Na O ),则观察到 【例5】用下面的装置将一定量的CO 和CO的混合气体进行分离和干燥。图中
2 2 2
D中的蜡烛燃烧得更旺,说明有氧气生成. 的a、b、c、d均为活塞,可以控制气体的通过和液体的加入,实验前
小明查阅资料得知:过氧化钠与二氧化碳、氯化氢气体、水 活塞均已关闭。请选择适宜的试剂完成上述实验。(仪器的固定装置已
等均能发生反应生成氧气.为确认二氧化碳与过氧化钠反应 经省略)
产生氧气,他对装置进行了改进,有如下备选装置:
他的连接顺序为:A→ _______________→F.小明还证明了反
应后F中含有碳酸钠,写出二氧化碳与过氧化钠(Na O )反应的
2 2 可供选择的试剂有:①浓硫酸 ②稀硫酸 ③浓盐酸
化学方程式____________________________
④稀盐酸⑤澄清的石灰水⑥氢氧化钠溶液
【例5】实验分以下两步进行:(所选的试剂均用序号表示) 【例6】实验室用干燥、纯净的一氧化碳还原氧化铁并检验其产物。实验装置
⑴关闭b、c,打开a、d,则甲中试剂为______,丙中试剂为_______。 如下图所示。其中A是实验室用草酸(H
2
C
2
O
4
)和浓硫酸加热制取一氧
若乙装置中的现象是___________,说明甲装置中反应是充分的。 化碳的气体发生装置,反应的化学方程式为
浓HSO
此步实验后收集到的气体是______。 H C O ===2 ==4H O+CO ↑+CO↑。
2 2 4 2 2
⑵在甲装置的分液漏斗中加入试剂②或④,关闭活塞___(填写序号,
下同),打开活塞_____,再经过丙装置后即可收集到另一种气体。
此步实验中发生的反应方程式____________________________。
回答下列问题:
⑴写出E装置中的实验现象__________________。 4【例6】⑵请将下列装置正确的接入到B、C、D位置中,装置导管的接口顺序 【例7】正确连接如下图所示的装置进行实验,可以验证mg某混合气体的成分
是:a→__________________→h。 是CO 、H O和CO,并粗略测出每种气体的质量(每套装置限用一次)。
2 2
温馨小提示
1.通常情况下CO与
酸、碱、盐溶液均
不反应。
2.无水硫酸铜是白
色固体,遇到水蒸
气变成蓝色晶体。
⑶B装置中发生反应的化学方程式为_____________________。
⑷C装置无明显现象,C装置的作用是 请回答下列问题:
_______________________________________________________。 ⑴连接导管口(①-⑩)顺序:混合气体→_____________________→尾气
⑸F装置的作用是 处理。
_____________________________________________________________ ⑵证明原混合气体中CO存在的实验现象________________________;
_______________________。 证明CO存在的有关反应的化学方程式
____________________________、___________________________。
【例7】⑶欲粗略测得二氧化碳的质量应进行的操作 【例8】小勇看书得知:潜水艇中常用过氧化钠(Na O )作为供给人们呼吸的试
2 2
__________________________________________________________ 剂。知道Na O 是一种化学性质活泼的淡黄色颗粒状固体,在通常情
2 2
__________________________________________________________ 况下能分别跟H O和盐酸等发生化学反应,有O 生成。于是小勇想探
2 2
究CO 跟Na O 反应是否也能产生O ,小勇翻阅书籍,查到相关资料
2 2 2 2
如下:
CO 能与Na CO 水溶液反应生成NaHCO ,CO 在NaHCO 溶液中几
2 2 3 3 2 3
乎不溶解;NaHCO 与盐酸反应生成NaCl、H O和CO 。
3 2 2
并设计了实验方案:①用石灰石和浓盐酸制取二氧化碳;②将纯净、
干燥的二氧化碳通过过氧化钠(Na O )粉末;③验证产生的气体中是否
2 2
含有O ;在实验室中准备了如下图所示的装置,请你一起参与完成:
2
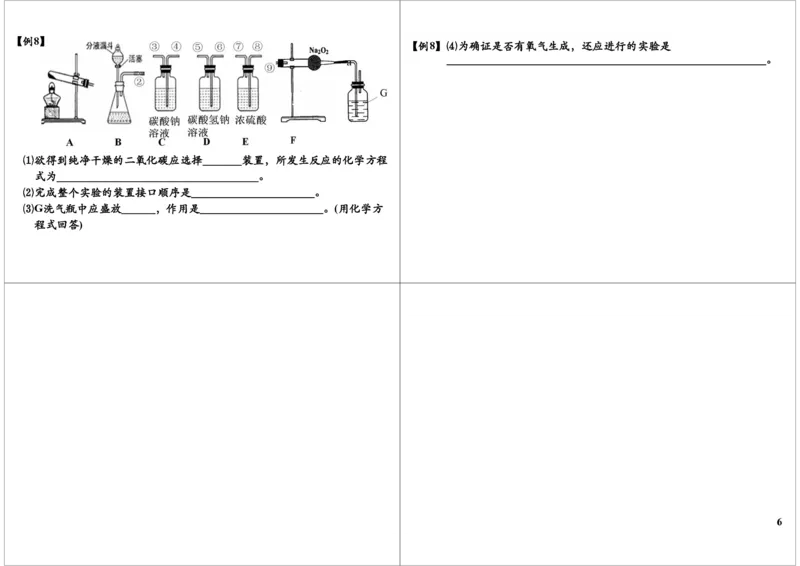
5【例8】
【例8】⑷为确证是否有氧气生成,还应进行的实验是
_________________________________________________________。
⑴欲得到纯净干燥的二氧化碳应选择_______装置,所发生反应的化学方程
式为____________________________________。
⑵完成整个实验的装置接口顺序是______________________。
⑶G洗气瓶中应盛放______,作用是______________________。(用化学方
程式回答)
6