文档内容
课后达标训练/训练·提升作业
【基础达标】
1.取四朵用石蕊溶液染成紫色的纸花,分别喷洒下列液体,能观察到纸花变红的
是( )
A.氢氧化钠溶液 B.稀盐酸
C.蒸馏水 D.食盐水
2.下列关于盐酸的描述中错误的是( )
A.盐酸中的溶质是HCl
B.盐酸能使石蕊溶液变蓝
C.人体胃液中含有盐酸,可帮助消化
D.打开装有浓盐酸的试剂瓶瓶盖,瓶口处有白雾出现
3.两只完全相同的烧杯,分别装有质量相等的浓盐酸和浓硫酸,将它们在空气中
放置一段时间,在这过程中( )
A.浓盐酸的溶质的质量分数逐渐增大
B.浓硫酸的溶质的质量分数逐渐增大
C.浓盐酸会变质
D.浓硫酸对杯底的压强逐渐增大
4.在某班举行的元旦晚会上,某同学为大家表演了小魔术,他将一张白纸展示给
大家,然后用喷壶向纸上喷了一些无色液体,“新年快乐”的红色大字立刻显现
于纸上。他所用的试剂可能是下列哪一组?( )
A.酚酞——盐酸溶液 B.酚酞——氢氧化钠溶液
C.石蕊——盐酸溶液 C.石蕊——氢氧化钠溶液
15.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不
容易被蚁酸腐蚀的是( )
A.镀锌水管 B.铜制塑像
C.大理石栏杆 D.铝合金门窗
6.将一定量的空气依次通过足量的石灰水及浓硫酸,分别被除去的是( )
A.氮气、氧气 B.二氧化碳、氮气
C.氮气、水蒸气 D.二氧化碳、水蒸气
7.向一定质量的稀盐酸中,加入足量的表面已经生锈的铁片,产生氢气的质量m
和时间t的关系图像正确的是( )
8.实验室有盐酸、白醋、柠檬酸三种溶液,回答下列问题:
(1)向三氧化二铁中放入足量盐酸,充分反应后,观察到的现象是__________
___________________________________________________________________,
反应的化学方程式是_________________________________________________。
(2)理论上溶解3.2 g三氧化二铁,需要36.5%的盐酸_____________ g。
9.“果导片”是一种常用缓泻剂,主要成分是酚酞。某同学欲将其作为酸碱指示
剂的替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上层清液滴入
白醋和食盐水中,看到______________________,滴入澄清石灰水中发现
______________________,确定“果导片”可作酸碱指示剂使用。当他用饮料吸
管向滴有“果导片”清液的澄清石灰水中吹气时,可观察到____________
2_____的现象。该反应的化学方程式为___________________________________。
10.为测定一瓶敞口放置的浓盐酸的溶质质量分数,某同学量取20 mL(密度为
1.1 g·mL-1)的该盐酸与大理石充分反应,共用去含碳酸钙85%的大理石7.1 g。
(1)浓盐酸需要密封保存的原因是___________________________________。
(2)计算该盐酸的溶质质量分数。
【知能提升】
1.下列物质中不能由金属和稀酸直接反应制得的是( )
A.AlCl B.ZnSO C.FeCl D.MgSO
3 4 3 4
2.进行下列实验,根据实验现象得出的结论中,错误的是( )
A.滴入紫色石蕊溶液,溶液颜色变红,则该溶液显酸性
B.滴入无色酚酞溶液,溶液保持无色,则该溶液显酸性
C.加入镁粉有气泡产生,则该溶液显酸性
D.加入石灰石,有气泡产生,则该溶液显酸性
3.下列区分物质的试剂或方法不正确的是( )
A.用水区分氯化钙和碳酸钙
B.用闻气味的方法区分白酒和白醋
C.用盐酸区分黄金和黄铜(含锌)
D.用酚酞溶液区分氯化钠溶液和盐酸
4.把铁粉和氧化铜的混合物加入到一定量的盐酸中,充分反应后过滤。在滤液中
加入少量铁粉,无现象。下列判断正确的是( )
A.滤渣中一定不含铜
B.滤渣可能是铜和铁的混合物
3C.滤液中含有FeCl 和盐酸
2
D.滤液中含有FeCl 和CuCl
2 2
5.如图所示,是两种稀释浓硫酸的操作,回答下列问题:
(1)B图中加水仪器的名称是_____________。
(2)B图锥形瓶内产生的现象是_____________________。产生这一现象的原因是
___________________________________________________________________。
(3)上边两幅图中,稀释浓硫酸操作正确的是_____________(填序号)。
(4)A图中玻璃棒的作用是_____________________________________________,
B图中的玻璃导管的作用是____________________________________________。
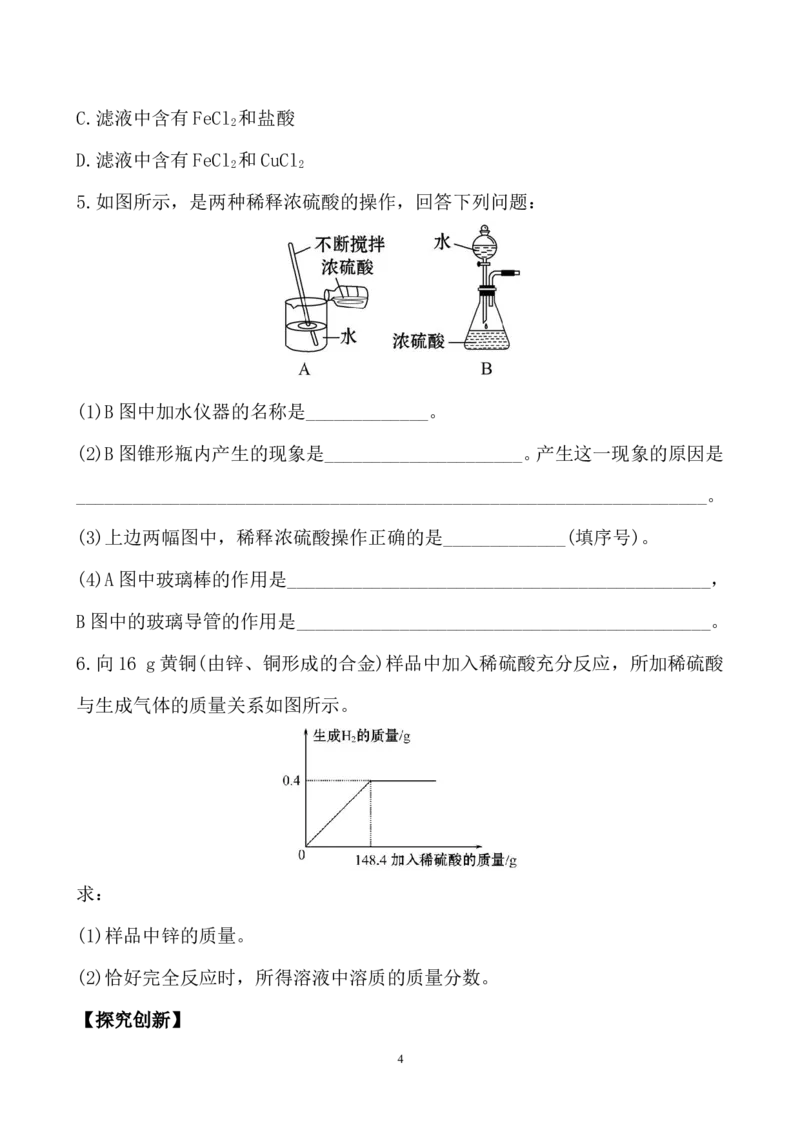
6.向16 g黄铜(由锌、铜形成的合金)样品中加入稀硫酸充分反应,所加稀硫酸
与生成气体的质量关系如图所示。
求:
(1)样品中锌的质量。
(2)恰好完全反应时,所得溶液中溶质的质量分数。
【探究创新】
4硫酸是常见的酸,也是常用的化工原料。由于浓度不同,浓硫酸与稀硫酸在性质
上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等。某课外兴趣小组
为了探究浓硫酸的某些特性做了如下一些实验。请结合有关实验,按要求回答下
列问题:
(1)用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由
于浓硫酸具有_____________性,使纸中的纤维素炭化的缘故;在洗气瓶中盛放
浓硫酸,除去氢气或氧气中的水分,是利用其_____________性。
(2)探究浓硫酸的吸水性。兴趣小组把98%的硫酸10 mL和63.3%的硫酸(用10
mL 98%的硫酸与10 mL水配成)约20 mL分别放入两个相同的大表面皿中,称量、
观察、记录、分析。根据室温环境下实验的数据绘成的曲线如图:
①稀释浓硫酸时,应将______________缓缓地注入盛有______________的烧杯
中并不断搅拌;
②由如图曲线你能得到的实验结论有哪些?
(写两点) ___________________________________________________________、
___________________________________________________________________。
(3)探究浓硫酸能否使铁钝化(钝化指在表面形成氧化膜保护层,使内层金属不
再发生变化)。
可选用的实验药品有:相同铁片若干、浓硫酸、稀硫酸、硫酸铜溶液等。实验仪器
5任选。
①兴趣小组已经完成下表实验Ⅰ和Ⅱ,请你帮他们将实验报告补充完整。
方案 实验假设 实验方案 实验现象与结论
取一铁片先插入浓硫酸中,一段时间 无明显变化,假设
Ⅰ 能发生钝化
后取出,再插入硫酸铜溶液中。 成立。
取两片相同的铁片,一片放入浓硫酸
______________,
Ⅱ 能发生钝化 中,一段时间后取出,与另一片同时
假设成立。
放入硫酸铜溶液中。
你认为方案Ⅱ与方案Ⅰ相比,方案Ⅱ的优点是_____________________________
___________________________________________________________________。
②请你选用提供的药品再设计一个实验,简述实验方案:__________________
____________________________________________________________________
___________________________________________________________________。
③某同学将一铁片插入盛有98%的浓硫酸的试管中,无明显变化,再给试管加热
一段时间后,发现溶液变色并有刺激性气味气体产生,此现象说明:___________
___________________________________________________________________。
6答案解析
【基础达标】
1.【解析】选B。酸能使紫色石蕊溶液变红色,所以观察到纸花变红的应是喷洒的
稀盐酸。
2.【解析】选B。盐酸中的溶质是HCl;酸能使石蕊溶液变红;人体胃液的主要成分
是盐酸,可帮助消化;浓盐酸具有挥发性,打开瓶盖,挥发出的HCl与空气里的水
蒸气接触形成盐酸小液滴,瓶口有白雾出现。
3.【解析】选D。浓盐酸易挥发而使溶质的质量分数逐渐变小,浓盐酸是变稀而不
是变质,浓硫酸有吸水性使溶质的质量分数逐渐变小,浓硫酸吸收水分,重量增
加,对杯底的压强逐渐增大。
4.【解析】选B。氢氧化钠溶液能使无色的酚酞溶液变红色,所以他所用的试剂可
能是酚酞与氢氧化钠溶液。
5.【解析】选B。由题目信息可知,蚁酸的化学性质与盐酸相似,由此推知,蚁酸能
与锌、铝、大理石反应,金属活动性顺序中铜在氢的后面,不能与蚁酸反应。故选
项B符合题意。
6.【解析】选D。石灰水能吸收空气中的二氧化碳,浓硫酸具有吸水性。
【拓展延伸】浓硫酸的三大特性
(1)吸水性:能吸收空气中的水分或其他气体中的水分,因而可做某些气体的干
燥剂,可干燥中性气体(如O 、N 、H 等)和酸性气体(如CO 、HCl等),不能干燥碱
2 2 2 2
性气体(如NH 等)。
3
(2)脱水性:能将一些有机物中的氢、氧元素按水的组成比脱去,生成黑色的炭,
这种作用通常叫做脱水作用(又称炭化),发生的是化学变化。
(3)氧化性:浓硫酸与金属反应一般生成水,而不生成氢气。
7.【解析】选B。表面已经生锈的铁片加入盐酸中,盐酸会先与铁锈反应,一开始
不会有氢气生成,当铁锈消耗完露出铁后,铁会与盐酸反应生成氢气,盐酸消耗
完毕,反应即停止,观察图像,只有B图与事实相符。
8.【解析】(1)三氧化二铁和稀盐酸反应生成氯化铁和水,氯化铁溶液呈黄色。
(2)根据Fe O +6HCl====2FeCl +3H O求出所用稀盐酸中氯化氢的质量,再除以盐
2 3 3 2
酸的溶质质量分数即可。
答案:(1)红色固体溶解,溶液由无色变为黄色 Fe O +6HCl====2FeCl +3H O
2 3 3 2
(2)12
9.【解析】酚酞溶液遇酸或中性溶液不变色,遇碱变红色;由于呼出气体中的二氧
7化碳能与石灰水反应,生成难溶于水的碳酸钙,因此澄清石灰水逐渐变为中性溶
液,同时会有浑浊现象出现。
答案:溶液无明显现象 溶液变红色 红色逐渐消失,溶液变浑浊
CO +Ca(OH) ====CaCO ↓+H O
2 2 3 2
10.【解析】浓盐酸具有挥发性,会挥发出氯化氢气体,所以需要密封保存。7.1 g
含碳酸钙85%的大理石中碳酸钙的质量=7.1 g×85%=6.035 g,根据碳酸钙的质
量可以求得HCl的质量,盐酸溶液的质量=溶液的体积×溶液的密度。HCl的质量
与盐酸溶液的质量之比就是盐酸的溶质质量分数。
答案:(1)浓盐酸易挥发
(2)解:设20 mL该盐酸中溶质的质量为x。
CaCO + 2HCl====CaCl +H O+CO ↑
3 2 2 2
100 73
7.1 g×85% x
100 7.1 g85%
x≈4.4 g
73 x
盐酸的溶质质量分数= 4.4 g ×100%=20%
20 mL1.1 gmL-1
答:该盐酸的溶质质量分数为20%。
【知能提升】
1.【解析】选C。铁与稀盐酸、稀硫酸反应时,生成物中铁元素显+2价,铁与稀盐酸
反应生成FeCl 。
2
2.【解析】选B。酚酞溶液在酸性和中性溶液中均为无色,故不能判断该溶液一定
是酸性溶液。
3.【解析】选D。氯化钙溶于水,碳酸钙不溶于水。白酒和白醋的味道不一样,用闻
气味的方法就可以区别开来。盐酸与黄金不反应,盐酸与黄铜(含锌)反应有气泡
冒出,是锌与盐酸反应有氢气生成。氯化钠溶液和盐酸均不使酚酞溶液变色,无
法区分。
4.【解析】选B。铁粉和CuO分别与盐酸反应生成FeCl 和CuCl ,滤液中加入铁粉
2 2
无现象,说明滤液中一定无剩余盐酸和CuCl ,否则会有气泡和红色物质产生,说
2
明生成的CuCl 又被铁粉全部置换生成铜,故滤渣中一定有铜。铁粉若过量,滤渣
2
中还会有铁。选项B符合题意。
5.【解析】(1)注意长颈漏斗与分液漏斗的区别,分液漏斗有开关旋钮。
(2)水注入浓硫酸中会发生暴沸,液滴飞溅。水的密度比浓硫酸的小,浓硫酸溶于
水会放出大量的热,使液体沸腾。
(3)稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中,并不断搅拌,千万不能
把水注入浓硫酸中。
(4)A图玻璃棒的作用是搅拌,使浓硫酸和水混合均匀,迅速放热,防止沸腾。B图
中玻璃导管的作用是维持内外气压平衡,防止因产生大量的蒸汽造成瓶内压强
增大,把瓶塞冲开。
答案:(1)分液漏斗
(2)液体沸腾,产生大量蒸汽 水的密度比浓硫酸小,且浓硫酸溶于水放出大量
的热
(3)A
(4)搅拌,防止局部温度过高而造成液滴飞溅 维持内外气压平衡,防止冲开瓶
8塞
6.【解析】解:由图分析可知产生氢气的总质量为0.4 g。
设样品中锌的质量为x,生成硫酸锌的质量为y。
Zn+H SO ====ZnSO +H ↑
2 4 4 2
65 161 2
x y 0.4 g
65 x
2 0.4 g
650.4 g
x 13 g
2
161 y
2 0.4 g
1610.4 g
y 32.2 g
2
所得硫酸锌溶液中溶质的质量分数为
32.2 g ×100%=20%
13 g148.4 g-0.4 g
答案:(1)13 g (2)20%
【探究创新】
【解析】(1)浓硫酸具有吸水性和脱水性。
(2)①稀释浓硫酸时要将浓硫酸沿烧杯壁(或玻璃棒)缓慢地注入水中,并用玻璃
棒不断搅动。
②从图像的走向分析。
(3)①对比实验,根据实验步骤比较得出实验Ⅱ的优点。
②取两片相同的铁片,一片放入浓硫酸中一段时间,取出,与另一片同时放入稀
硫酸溶液中。
③加热产生了刺激性气味的气体说明铁和浓硫酸发生了反应,铁表面的保护膜
被破坏。
答案:(1)脱水 吸水
(2)①浓硫酸 水
②浓硫酸和一定浓度以上的稀硫酸都具有吸水性 浓硫酸吸水能力比稀硫酸
强(吸水速率快、吸水量大) 硫酸浓度越稀吸水性越弱,到一定浓度后就失去
吸水性 硫酸吸水能力可能会受环境温度、湿度、气压、酸的用量、表面积等因
素的影响(任写两点,合理即可)
(3)①
实验现象与结论
浸过浓硫酸的铁片表面无明显变化,另一铁片表面产生红色固体
采用了对比实验的方法,更科学
②取两片相同的铁片,一片放入浓硫酸中一段时间,取出,与另一片同时放入稀
硫酸溶液中(其他合理答案均可)
9③加热条件下,氧化膜被破坏(被浓硫酸溶解),铁继续与浓硫酸反应(或热的浓
硫酸能与铁反应产生刺激性气体;或热的浓硫酸不能使铁钝化;或铁的钝化随条
件的改变而改变;或铁与浓硫酸的作用与温度有关)(其他合理答案均可)
10