文档内容
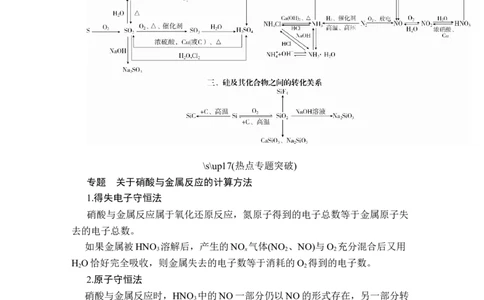
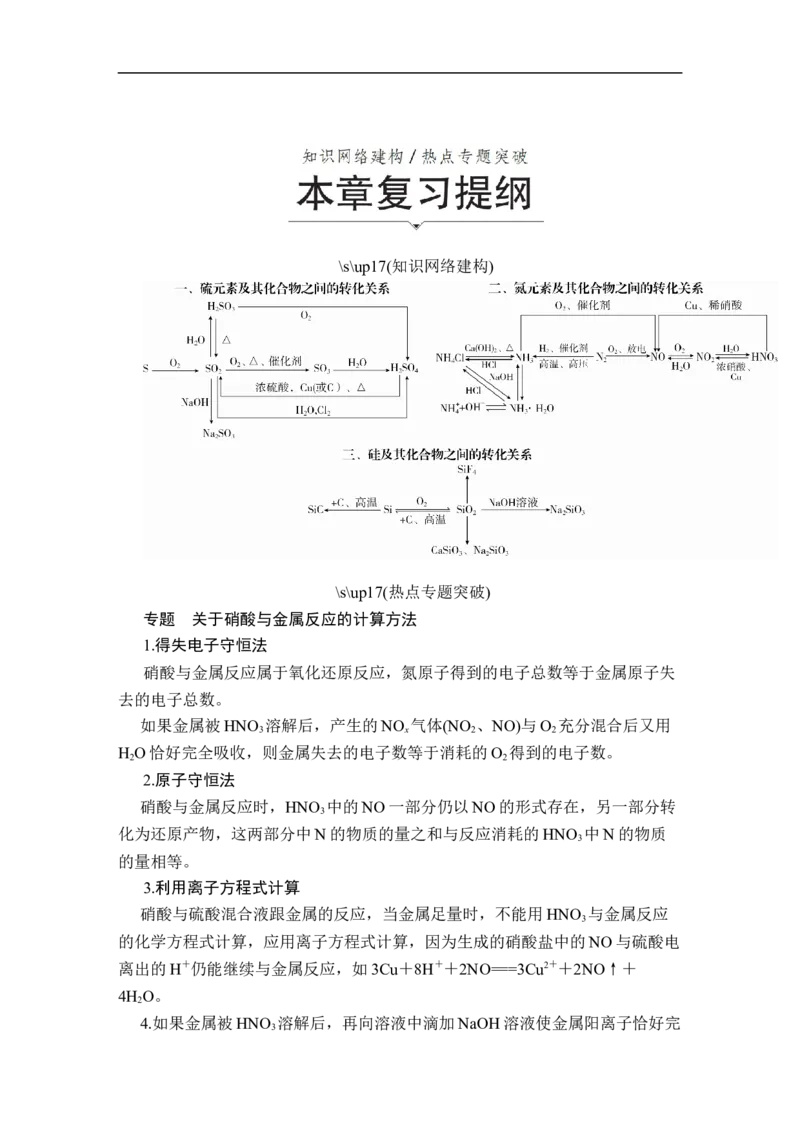
\s\up17(知识网络建构)
\s\up17(热点专题突破)
专题 关于硝酸与金属反应的计算方法
1.得失电子守恒法
硝酸与金属反应属于氧化还原反应,氮原子得到的电子总数等于金属原子失
去的电子总数。
如果金属被HNO 溶解后,产生的NO 气体(NO 、NO)与O 充分混合后又用
3 x 2 2
H O恰好完全吸收,则金属失去的电子数等于消耗的O 得到的电子数。
2 2
2.原子守恒法
硝酸与金属反应时,HNO 中的NO一部分仍以NO的形式存在,另一部分转
3
化为还原产物,这两部分中N的物质的量之和与反应消耗的HNO 中N的物质
3
的量相等。
3.利用离子方程式计算
硝酸与硫酸混合液跟金属的反应,当金属足量时,不能用HNO 与金属反应
3
的化学方程式计算,应用离子方程式计算,因为生成的硝酸盐中的NO与硫酸电
离出的H+仍能继续与金属反应,如3Cu+8H++2NO===3Cu2++2NO↑+
4H O。
2
4.如果金属被HNO 溶解后,再向溶液中滴加NaOH溶液使金属阳离子恰好完
3全沉淀,则金属失去电子的物质的量等于HNO 得到电子的物质的量,也等于生
3
成氢氧化物时消耗的OH-的物质的量,因此,m(沉淀)=m(金属)+m(OH-)=
m(金属)+n(e-)×17 g·mol-1[因为M――→Mn+,Mn+――→M(OH) ]。
n
38.4 g Cu与适量的浓硝酸反应,Cu全部反应后,共收集到1 mol气体。
反应消耗的HNO 的物质的量是( )
3
A.1.0 mol B.1.6 mol C.2.2 mol D.2.4 mol
[批注点拨]
[解析] Cu跟浓硝酸反应的化学方程式为Cu+
4HNO (浓)===Cu(NO ) +2NO ↑+2H O。随着反应的进行,浓硝酸会逐渐变
3 3 2 2 2
成稀硝酸,反应则变为3Cu+8HNO (稀)===3Cu(NO ) +2NO↑+4H O。
3 3 2 2
方法一:极端假设法
n(Cu)==0.6 mol
若38.4 g Cu全部与浓硝酸反应,则可求得参加反应的硝酸的物质的量为0.6
mol×4 =2.4 mol,产生的NO 的物质的量为0.6 mol×2=1.2 mol;若38.4 g Cu
2
全部与稀硝酸反应,则可求得参加反应的硝酸的物质的量为0.6 mol×=1.6
mol,产生的NO的物质的量为0.6 mol×=0.4 mol。事实上Cu应先与浓硝酸反
应,浓硝酸变稀后,又与稀硝酸反应,所以消耗的硝酸的物质的量应在1.6 mol
和2.4 mol之间。观察选项可知应选C。方法二:物料守恒法
参加反应的硝酸一部分作酸,一部分作氧化剂被还原(其中一部分被还原为
NO ,另一部分被还原为NO),故n(HNO )=n[HNO (作酸)]+n[HNO (作氧化
2 3 3 3
剂)]=2n[Cu(NO ) ]+n(NO )+n(NO)=2×+1 mol=2.2 mol。
3 2 2
[答案] C