文档内容
第二课时 硫酸
[明确学习目标] 1.通过浓硫酸分别与不活泼金属、非金属反应,认识浓硫
酸的强氧化性。2.通过比较浓硫酸和稀硫酸性质的差异,认识浓度、反应条件对
反应产物的影响。3.了解SO的检验方法。
学生自主学习
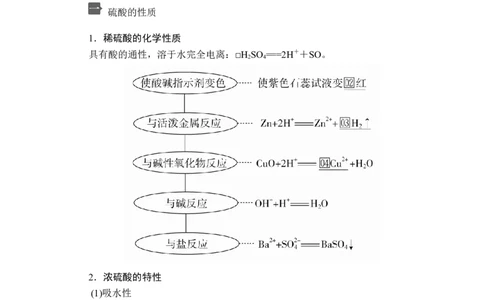
硫酸的性质
1.稀硫酸的化学性质
具有酸的通性,溶于水完全电离:□H SO ===2H++SO。
2 4
2.浓硫酸的特性
(1)吸水性
浓硫酸能够吸收气体、液体中的水分子及固体中的结晶水,故常用作干燥剂。
(2)脱水性
浓硫酸能按水的组成比脱去纸、棉布、木条等有机物中的 □ 氢、氧 元素。
向蔗糖中加入浓硫酸时,观察到的现象有:
①蔗糖变 □ 黑 ;
②蔗糖体积 □ 膨胀 ,变成疏松多孔的海绵状的炭;
③放出有刺激性气味的气体。
(3)强氧化性①与金属的反应:除金、铂以外的绝大多数金属都能与浓硫酸作用。
与铜反应的实验探究
②与非金属的反应
浓硫酸与木炭的反应:□2H SO (浓)+C=====CO ↑+2SO ↑+2H O。
2 4 2 2 2
3.硫酸的用途
(1)重要的化工原料,实验室必备的重要试剂。
(2)工业上可用于制化肥、农药、炸药、染料、盐类等。
(3)用于金属加工前的酸洗除锈及制取各种挥发性酸,作干燥剂等。
硫酸盐、SO的检验
1.\o(□ \o(□
2. □ BaSO 在医疗上被用作“钡餐”,自然界中以 □ 重晶石 (BaSO )形式存在。
4 4
3.硫酸铜是白色粉末,结合水后会变成蓝色晶体,俗称 □ 胆矾 ,化学式为
□ CuSO ·5H O。
4 2
4.硫酸根离子的检验
试剂: □ 稀盐酸、 BaCl 溶液。
2通常将溶液先用 □ 稀盐酸 酸化,以 □ 排除 CO 等可能造成的干扰 ,然后加入
□ BaCl 溶液来检验SO的存在。
2
粗盐中SO检验的流程如下
――→――→――→
1.上述实验,利用SO的什么性质?
提示:SO能与Ba2+反应生成BaSO 白色沉淀。
4
2.实验中,试剂①、试剂②分别是什么?为什么加入试剂①?
提示:盐酸、BaCl 溶液。加盐酸可以排除CO等的干扰。
2
课堂互动探究
知识点一 浓硫酸的性质
1.浓硫酸吸水性、脱水性的区别
由此看出:二者的根本区别在于物质本身是否存在水分子。
2.浓硫酸的强氧化性
(1)本质
浓硫酸具有强氧化性,是因为H SO 分子中+6价的硫元素具有很强的得电
2 4
子能力。
(2)反应规律
①常温下与活泼金属反应(铁、铝除外)表现强氧化性和酸性,生成硫酸盐和
SO ,硫酸浓度变小后,生成的气体为H 。
2 2
②与较不活泼金属反应
金属+浓硫酸――→高价态硫酸盐+SO ↑+H O
2 2a.反应需要加热(否则不反应);
b.浓硫酸的还原产物是SO 。
2
③与非金属反应
非金属单质+浓硫酸――→高价态氧化物+SO ↑+H O
2 2
④与还原性物质反应
浓硫酸具有强氧化性,能将还原性物质(如H S、HI、HBr)氧化。
2
1 向50 mL 18 mol·L-1的浓H SO 中加入过量的铜片并加热。充分反应后,
2 4
被还原的H SO 的物质的量是( )
2 4
A.小于0.45 mol B.等于0.45 mol
C.在0.45~0.90 mol之间 D.大于0.45 mol
[批注点拨]
[解析] 浓硫酸与铜可发生氧化还原反应,而稀硫酸与铜不发生反应。随着
反应的进行,浓硫酸变稀到一定程度时反应就会停止。因此,参加反应的硫酸实
际量要比理论计算量小。由反应 Cu+2H SO (浓)=====CuSO +SO ↑+2H O知,
2 4 4 2 2
硫酸被还原的理论值为 n(H SO )=×18 mol·L-1×0.05 L=0.45 mol,故实际被还
2 4
原的H SO 的物质的量必小于0.45 mol。
2 4
[答案] A
[练1] 将蔗糖放在小烧杯中,一边搅拌一边慢慢加入浓硫酸,可以看到蔗糖颜色逐渐变黑,体积不断膨胀,最终变成疏松多孔的海绵状固体,且伴有刺激
性气味。上述过程中主要体现出浓硫酸( )
A.有强氧化性、酸性 B.有脱水性、酸性
C.有吸水性、脱水性 D.有脱水性、强氧化性
答案 D
解析 在此过程中,浓 H SO 先将蔗糖脱水,然后与 C 反应 C+
2 4
2H SO (浓)=====CO ↑+2SO ↑+2H O,故选D。
2 4 2 2 2
[练2] 下列物质的转化中,浓H SO 既表现了氧化性,又表现了酸性的是(
2 4
)
A.Cu―→CuSO B.C―→CO
4 2
C.CuO―→CuSO D.Fe O ―→Fe (SO )
4 2 3 2 4 3
答案 A
解析 H SO 中所含元素化合价降低,则 H SO 作氧化剂,表现氧化性;生
2 4 2 4
成物中有硫酸盐生成,则可说明硫酸在反应中表现酸性,故选A。
规律方法
解有关浓硫酸的氧化性类型题的注意事项
一是理解题意,明确题目要求。如例 1中求“被还原的H SO 的物质的量”。
2 4
二是硫酸的浓度对反应的影响。类似问题还有 MnO 与浓盐酸在加热条件下产生
2
氯气,而稀盐酸不与MnO 反应。因此,一切因浓度不同而产生不同产物(或不
2
发生反应)的反应都会遇到上述问题,计算时要考虑反应的实际情况。
知识点二 硫酸盐、SO的检验
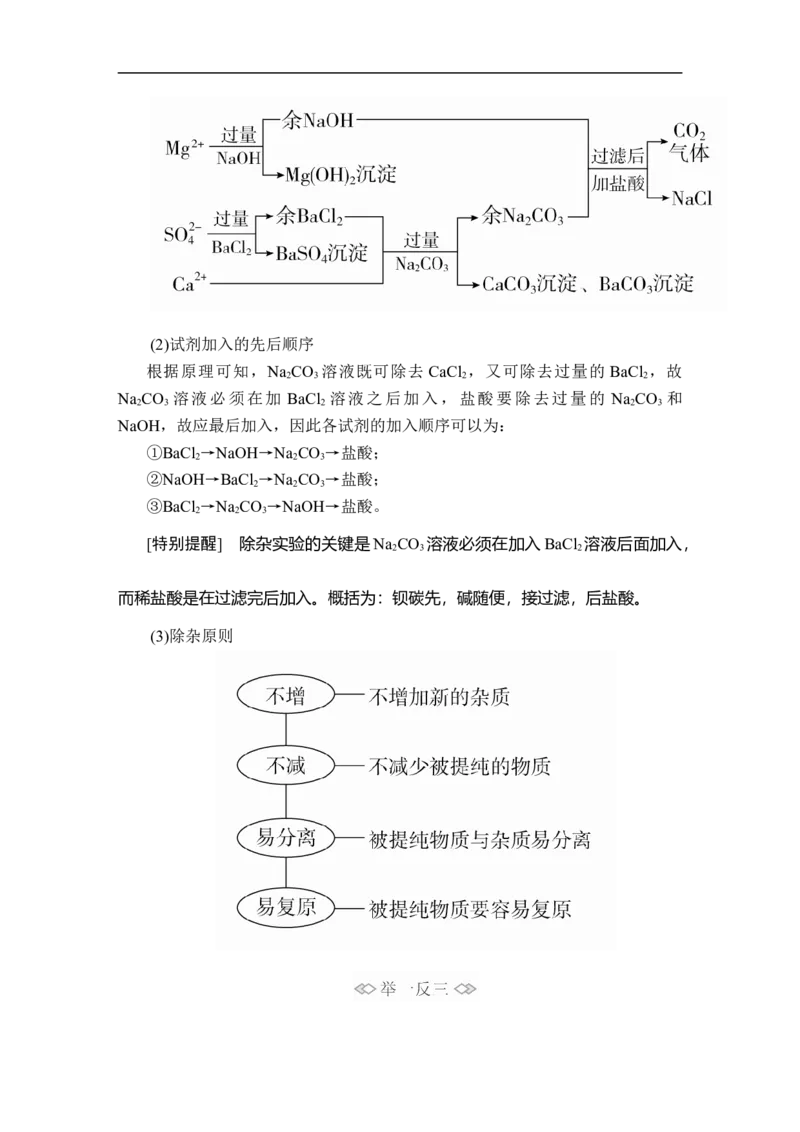
除去粗盐中少量可溶性杂质
(1)除去粗盐中可溶性杂质的原理(2)试剂加入的先后顺序
根据原理可知,Na CO 溶液既可除去 CaCl ,又可除去过量的 BaCl ,故
2 3 2 2
Na CO 溶液必须在加 BaCl 溶液之后加入,盐酸要除去过量的 Na CO 和
2 3 2 2 3
NaOH,故应最后加入,因此各试剂的加入顺序可以为:
①BaCl →NaOH→Na CO →盐酸;
2 2 3
②NaOH→BaCl →Na CO →盐酸;
2 2 3
③BaCl →Na CO →NaOH→盐酸。
2 2 3
[特别提醒] 除杂实验的关键是Na CO 溶液必须在加入BaCl 溶液后面加入,
2 3 2
而稀盐酸是在过滤完后加入。概括为:钡碳先,碱随便,接过滤,后盐酸。
(3)除杂原则2 为了除去KCl固体中少量的MgCl 、MgSO ,可选用Ba(OH) 、HCl和
2 4 2
K CO 三种试剂,按下列步骤操作:
2 3
――→――→――→――→――→――→
(1)写出三种试剂的化学式:
A________,B________,C________。
(2)根据题意,回答下列问题:
①加入过量A的目的是______________________;
②加入过量B的目的是______________________;
③加热煮沸的目的是__________________________。
(3)操作Ⅰ是________,操作Ⅱ是________。
[批注点拨]
[解析] 要使杂质一一除去,必须考虑到所加试剂是过量的,而且过量的试
剂在后面步骤中必须能除去,要除去 Mg2+,可用含OH-的试剂,除SO可用含
Ba2+的试剂,故先加入Ba(OH) 。加入的过量Ba(OH) 中的Ba2+可用K CO 除去,
2 2 2 3
过量Ba(OH) 中的OH-以及过量K CO 中的CO,可用稀盐酸除去,最后加热煮
2 2 3
沸可除去HCl。
[答案] (1)Ba(OH) K CO HCl
2 2 3
(2)①除尽Mg2+和SO ②除尽过量的Ba2+ ③使HCl挥发
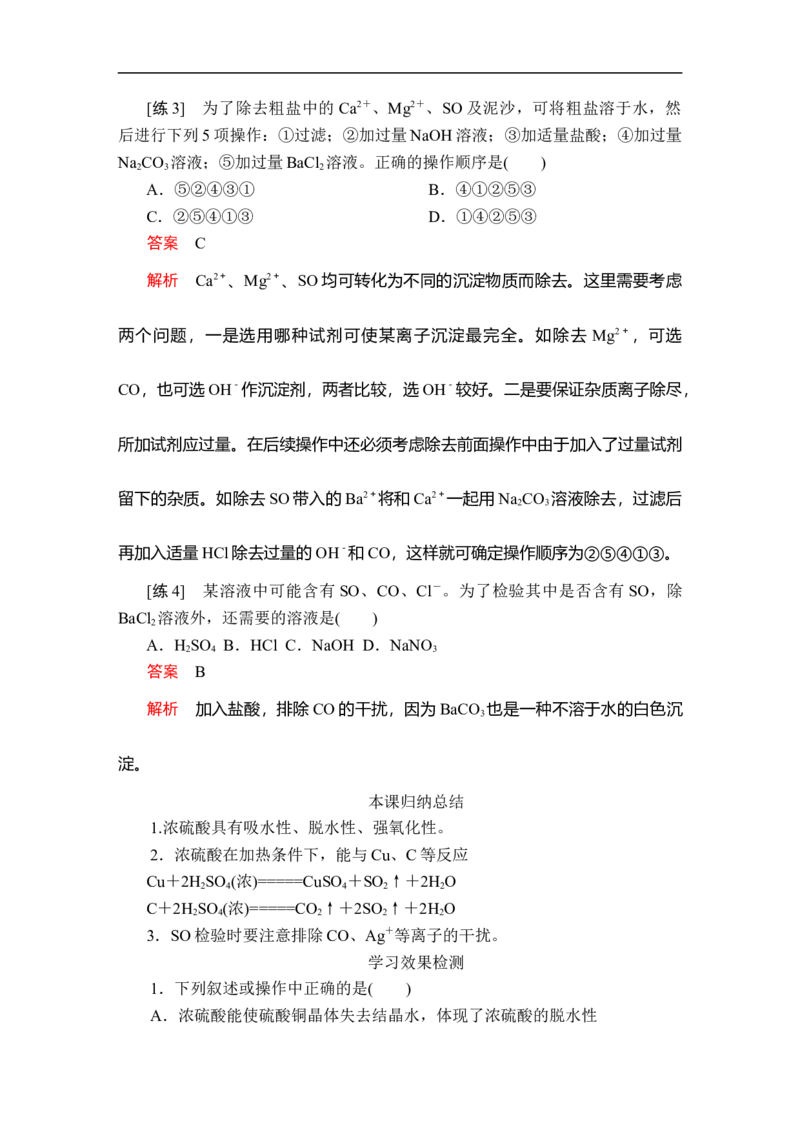
(3)过滤 蒸发[练3] 为了除去粗盐中的 Ca2+、Mg2+、SO及泥沙,可将粗盐溶于水,然
后进行下列5项操作:①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量
Na CO 溶液;⑤加过量BaCl 溶液。正确的操作顺序是( )
2 3 2
A.⑤②④③① B.④①②⑤③
C.②⑤④①③ D.①④②⑤③
答案 C
解析 Ca2+、Mg2+、SO均可转化为不同的沉淀物质而除去。这里需要考虑
两个问题,一是选用哪种试剂可使某离子沉淀最完全。如除去 Mg2+,可选
CO,也可选OH-作沉淀剂,两者比较,选OH-较好。二是要保证杂质离子除尽,
所加试剂应过量。在后续操作中还必须考虑除去前面操作中由于加入了过量试剂
留下的杂质。如除去SO带入的Ba2+将和Ca2+一起用Na CO 溶液除去,过滤后
2 3
再加入适量HCl除去过量的OH-和CO,这样就可确定操作顺序为②⑤④①③。
[练4] 某溶液中可能含有SO、CO、Cl-。为了检验其中是否含有SO,除
BaCl 溶液外,还需要的溶液是( )
2
A.H SO B.HCl C.NaOH D.NaNO
2 4 3
答案 B
解析 加入盐酸,排除CO的干扰,因为BaCO 也是一种不溶于水的白色沉
3
淀。
本课归纳总结
1.浓硫酸具有吸水性、脱水性、强氧化性。
2.浓硫酸在加热条件下,能与Cu、C等反应
Cu+2H SO (浓)=====CuSO +SO ↑+2H O
2 4 4 2 2
C+2H SO (浓)=====CO ↑+2SO ↑+2H O
2 4 2 2 2
3.SO检验时要注意排除CO、Ag+等离子的干扰。
学习效果检测
1.下列叙述或操作中正确的是( )
A.浓硫酸能使硫酸铜晶体失去结晶水,体现了浓硫酸的脱水性B.浓硫酸对有机物的腐蚀性是浓硫酸脱水性和强氧化性的综合体现
C.浓硫酸具有氧化性,稀硫酸无氧化性
D.浓硫酸不慎沾到皮肤上,应立即用布拭去,再涂上稀NaOH溶液
答案 B
解析 浓硫酸使硫酸铜晶体失去结晶水体现浓硫酸的吸水性,A错误;稀硫
酸中的H+具有较弱的氧化性,C错误;NaOH本身具有强腐蚀性,不能涂在皮
肤上中和浓硫酸的腐蚀作用,D错误。
2.下列现象和用途中,浓硫酸表现脱水性的是( )
A.实验室制取氯气时浓硫酸作干燥剂
B.浓硫酸使火柴梗变黑
C.浓硫酸加热时与炭反应
D.浓硫酸加热与铁反应
答案 B
解析 区别浓硫酸的脱水性和吸水性,要看原物质中是否有水分子。一般来
说,脱水性是对有机物质而言,其中的氢、氧两种元素按原子个数比 2∶1即以
H O的形式脱去。A选项中浓硫酸表现吸水性;C选项中浓硫酸表现强氧化性;
2
D选项中浓硫酸表现强氧化性和酸性;只有B选项中浓硫酸表现脱水性。
3.在下图所示的实验装置中,实验开始一段时间后,对看到的现象叙述不
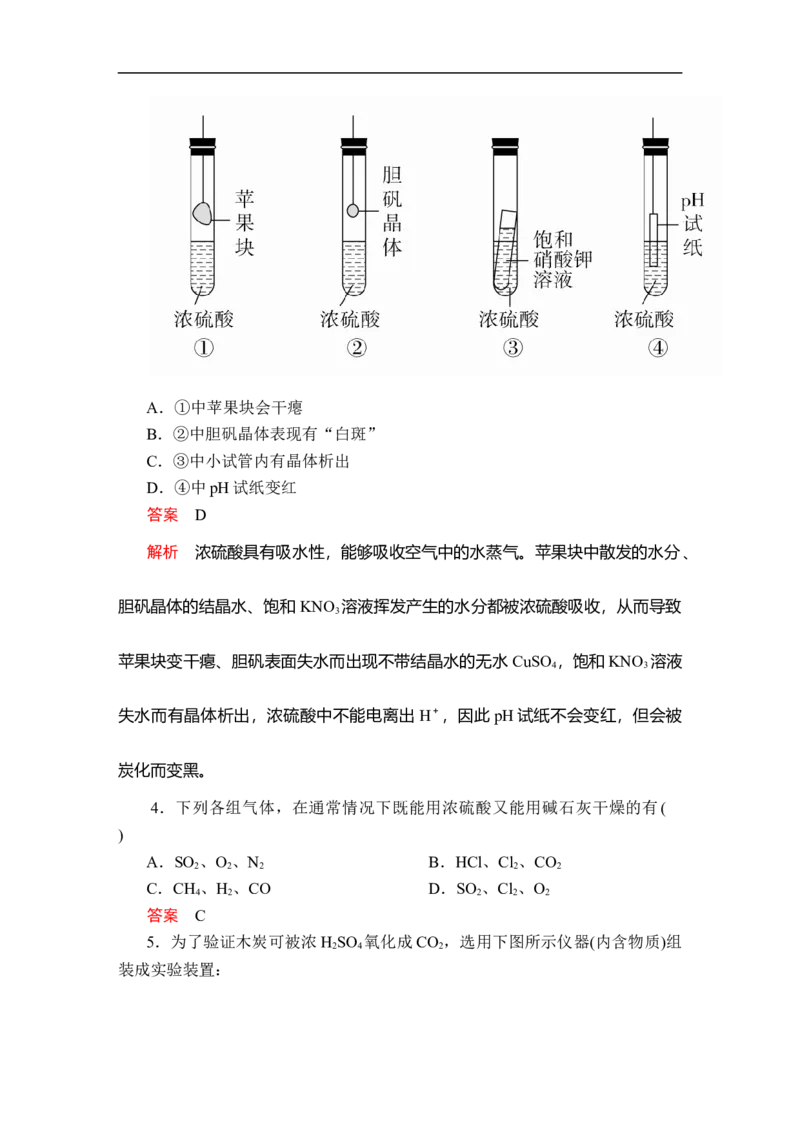
正确的是( )A.①中苹果块会干瘪
B.②中胆矾晶体表现有“白斑”
C.③中小试管内有晶体析出
D.④中pH试纸变红
答案 D
解析 浓硫酸具有吸水性,能够吸收空气中的水蒸气。苹果块中散发的水分、
胆矾晶体的结晶水、饱和KNO 溶液挥发产生的水分都被浓硫酸吸收,从而导致
3
苹果块变干瘪、胆矾表面失水而出现不带结晶水的无水 CuSO ,饱和KNO 溶液
4 3
失水而有晶体析出,浓硫酸中不能电离出 H+,因此pH试纸不会变红,但会被
炭化而变黑。
4.下列各组气体,在通常情况下既能用浓硫酸又能用碱石灰干燥的有(
)
A.SO 、O 、N B.HCl、Cl 、CO
2 2 2 2 2
C.CH 、H 、CO D.SO 、Cl 、O
4 2 2 2 2
答案 C
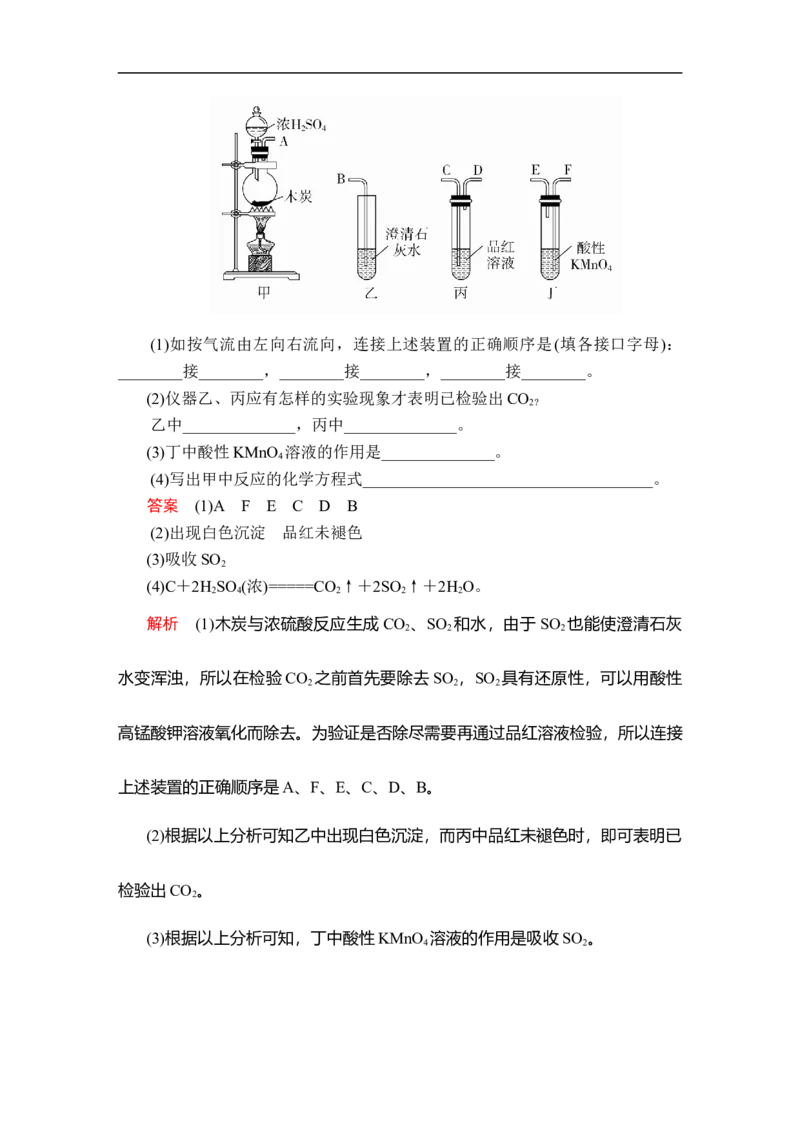
5.为了验证木炭可被浓H SO 氧化成CO ,选用下图所示仪器(内含物质)组
2 4 2
装成实验装置:(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
________接________,________接________,________接________。
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO
2?
乙中______________,丙中______________。
(3)丁中酸性KMnO 溶液的作用是______________。
4
(4)写出甲中反应的化学方程式____________________________________。
答案 (1)A F E C D B
(2)出现白色沉淀 品红未褪色
(3)吸收SO
2
(4)C+2H SO (浓)=====CO ↑+2SO ↑+2H O。
2 4 2 2 2
解析 (1)木炭与浓硫酸反应生成CO 、SO 和水,由于SO 也能使澄清石灰
2 2 2
水变浑浊,所以在检验CO 之前首先要除去SO ,SO 具有还原性,可以用酸性
2 2 2
高锰酸钾溶液氧化而除去。为验证是否除尽需要再通过品红溶液检验,所以连接
上述装置的正确顺序是A、F、E、C、D、B。
(2)根据以上分析可知乙中出现白色沉淀,而丙中品红未褪色时,即可表明已
检验出CO 。
2
(3)根据以上分析可知,丁中酸性KMnO 溶液的作用是吸收SO 。
4 2