文档内容
第六章 章末测试(提升)
一、单选题(本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小题
给出的四个选项中,只有一项是符合题目要求的。)
1.(2021·广东梅县 )下列说法错误的是
A.水的生成与电解是可逆反应
B.温度升高,正、逆反应速率都增大
C.化学反应的速率和限度均可通过改变化学反应条件来改变
D.化学反应达到平衡状态时,正反应速率与逆反应速率相等
2.(2021·黑龙江·大兴安岭实验中学)在一定条件下,对于在密闭容器中进行的反应:P(g)+Q(g)
R(g)+S(g),下列情况已经达到化学平衡状态是
A.P、Q、R、S的浓度相等
B.P、Q、R、S在密闭容器中共存
C.P、Q、R、S的浓度不再变化
D.容器内的压强不再变化
3.(2021·湖北武汉·)科学家提出有关甲醇(CHOH)的碳循环如图所示。下列说法正确的是
3
A.图中能量转化方式只有2种
B.CO、CHOH均属于有机物
2 3
C.CO 和H 合成CHOH原子利用率为100%
2 2 3
D.CO 合成CHOH燃料有利于促进“碳中和”(“碳中和”是指CO 的排放总量和减少总量相当)
2 3 2
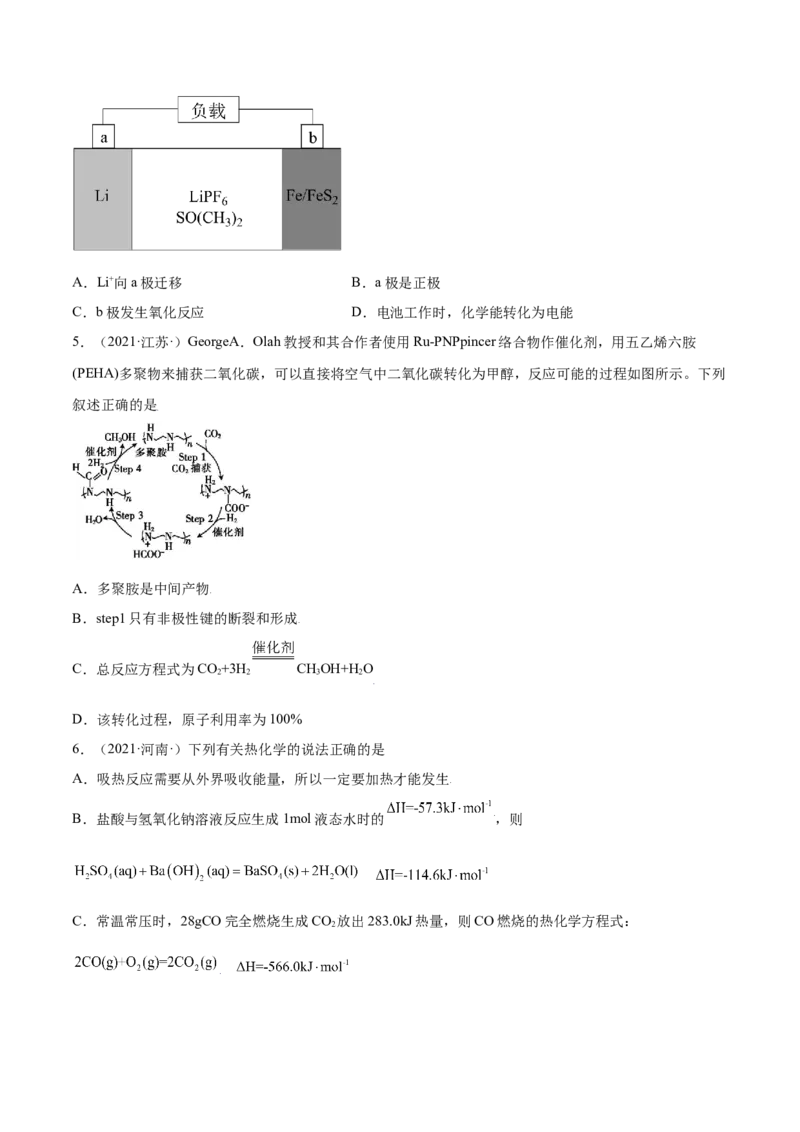
4.(2021·江苏盐城·)下图是一种锂电池放电的装置图,其中LiPF 是电解质、SO(CH ) 是溶剂,电池反
6 3 2
应为4Li+FeS=Fe+2Li S。下列说法正确的是
2 2A.Li+向a极迁移 B.a极是正极
C.b极发生氧化反应 D.电池工作时,化学能转化为电能
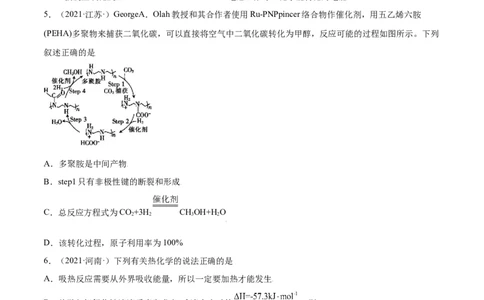
5.(2021·江苏·)GeorgeA.Olah教授和其合作者使用Ru-PNPpincer络合物作催化剂,用五乙烯六胺
(PEHA)多聚物来捕获二氧化碳,可以直接将空气中二氧化碳转化为甲醇,反应可能的过程如图所示。下列
叙述正确的是
A.多聚胺是中间产物
B.step1只有非极性键的断裂和形成
C.总反应方程式为CO+3H CHOH+H O
2 2 3 2
D.该转化过程,原子利用率为100%
6.(2021·河南·)下列有关热化学的说法正确的是
A.吸热反应需要从外界吸收能量,所以一定要加热才能发生
B.盐酸与氢氧化钠溶液反应生成1mol液态水时的 ,则
C.常温常压时,28gCO完全燃烧生成CO 放出283.0kJ热量,则CO燃烧的热化学方程式:
2D.一定条件下,将 (g)和 (g)充入密闭容器中充分反应生成气态 放出x kJ热量,则
热化学方程式:
7.(2021·四川达州·)反应 在四种不同条件下的反应速率为:①
② ③ ④ ,则上述表
示的化学反应速率最快的是
A.① B.② C.③ D.④
8.(2021·江苏·)东南大学王金兰课题组提出合成氨的“表面氢化机理”如图,在较低的电压下实现氮气还
原合成氨。
已知:第一步:*+H+e-=H(快)(吸附在催化剂表面的物种用*表示);
第二步:N+2*H=中间体(吸附在催化剂表面)(慢);
2
第三步:(快)。
下列说法不正确的是
A.上述三步中的决定速率步骤为第二步
B.第三步可表示为2*NH+4H++4e-=2NH
3
C.该法在合成氨的过程中能量的转化形式是电能转化为化学能
D.该法较传统工业合成氨法,具有能耗小、环境友好的优点
9.(2021·四川·成都七中)N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.常温下,45 g CHCH(OH)COOH(乳酸)和CHCOOH(醋酸)的混合物中含有的原子数为6N
3 3 A
B.将含1 mol FeCl 的饱和溶液制成胶体,所含胶粒数目小于1N
3 A
C.14.4 g 28Si 15N 中含质子的数目为7N
3 4 A
D.常温下,在密闭容器中将2 mol NO与1 mol O 充分混合,反应后容器中的分数为2N
2 A
10.(2021·全国·)一定温度下,在一密闭容器中充入一定量的H(g)和I(g)发生如下反应H(g)+I (g)
2 2 2 2
2HI(g),并达到平衡状态,此时H 的转化率为x%,向平衡混合体系中充入一定量的I(g),重新达到平衡
2 2后H 的转化率将
2
A.增大 B.减小 C.不变 D.无法确定
11.(2022·四川南充·)一定温度下,向一恒容密闭容器中充入 和 ,在催化剂作用下发
生反比应: ,下列有关说法错误的是
A.温度升高,可以加快反应速率
B.使用催化剂是为了加快反应速率,提高生产效率
C.达到化学平衡时,生成 的物质的量为
D.若单位时间内消耗 ,同时生成 ,则反应达到平衡状态
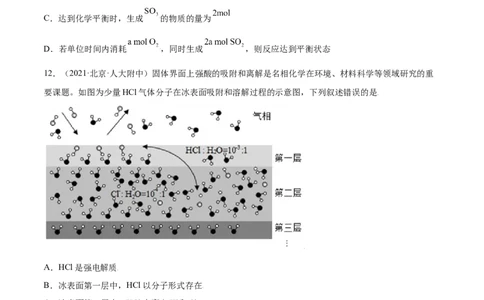
12.(2021·北京·人大附中)固体界面上强酸的吸附和离解是名相化学在环境、材料科学等领域研究的重
要课题。如图为少量HCl气体分子在冰表面吸附和溶解过程的示意图,下列叙述错误的是
A.HCl是强电解质
B.冰表面第一层中,HCl以分子形式存在
C.冰表面第二层中,HCl电离出H+和Cl-
D.冰表面各层中均存在HCl
13.(2021·江苏徐州·)硫酸的工业用途非常广泛,可用于制造化肥、除铁锈、作电解液等。工业制硫酸
的关键一步是将SO 氧化为SO ,该反应为2SO +O 2SO 。但该反应速率小,无法投入工业
2 3 2 2 3
化生产。后来化学家们不断地改进反应条件,找到了理想的催化剂及反应的适宜温度,成功开发出了制造
硫酸的生产工艺。材料中的反应为放热反应,下列说法正确的是A.断开化学键放出能量
B.放热反应都不需要加热
C.及时移走部分产物能加快反应速率
D.该反应的反应物总能量大于生成物的总能量
14.(2022·北京海淀·)在一定条件下发生反应:2A(g)=2B(g)+C(g),将2molA通入2L容积恒定的密闭容
器中,若维持容器内温度不变,5min末测得A的物质的量为0.8mol。用B的浓度变化来表示该反应的速
率[mol·(L·min)-1]为
A.0.24 B.0.08 C.0.06 D.0.12
15.(2022·云南·)一定条件下,在密闭容器中发生反应: 3X(g)+Y(g) 2Z(g)。开始时加入一定量的
X与Y,在2 min末测得Z的物质的量浓度为4 mol/L,以Z表示该反应在2 min内的平均反应速率为
A.8 mol/(L·min) B.4 mol(L·min)
C.2 mol(L·min) D.1 mol(L·min)
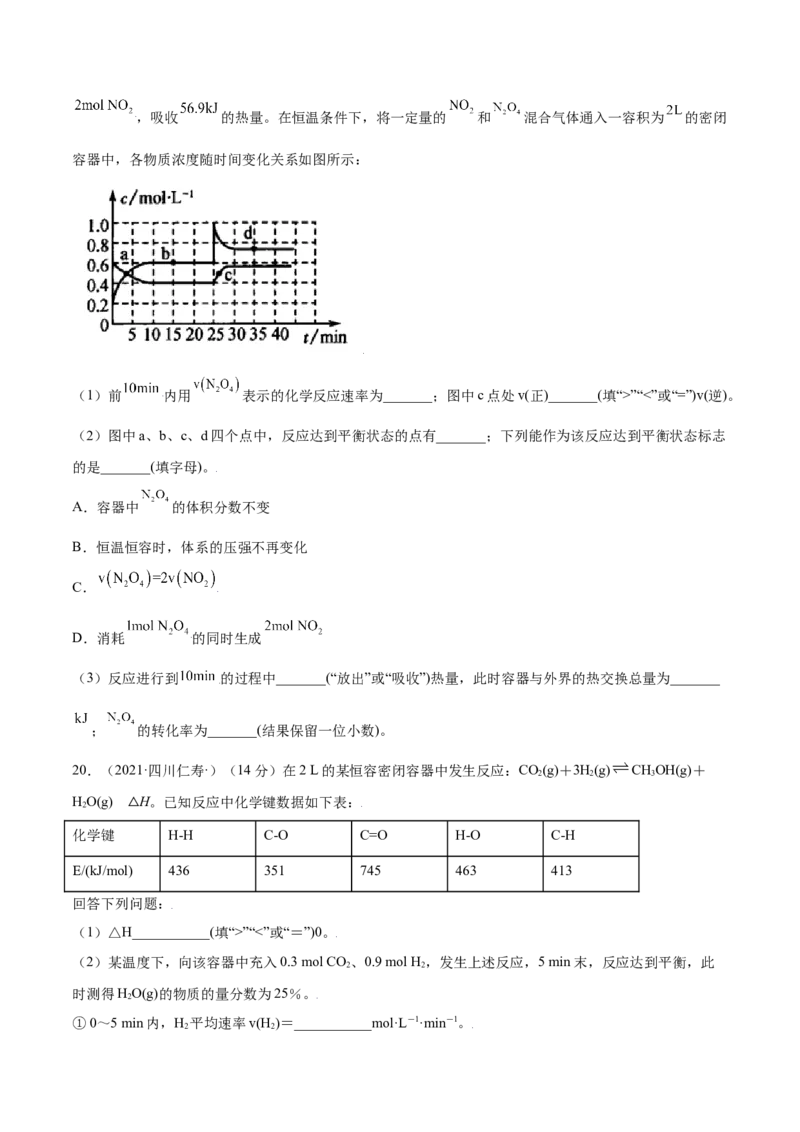
16.(2022·湖南·长郡中学)电絮凝的反应原理是以金属铁为阳极,在直流电的作用下,阳极被溶蚀,产
生金属离子;在经一系列水解、聚合及氧化过程,使废水中的胶态杂质、悬浮杂质凝聚沉淀而分离。下列
说法不正确的是
A.阳极电极方程式为Fe-3e-=Fe3+和2HO-4e-=O ↑+4H+
2 2
B.阴极电极反应式为2HO+2e-=H ↑+2OH-
2 2
C.每产生1molO ,整个电解池中理论上转移电子大于4mol
2
D.选择铝做阳极也可起到相似的絮凝效果
二、非选择题(共5题,共56分)
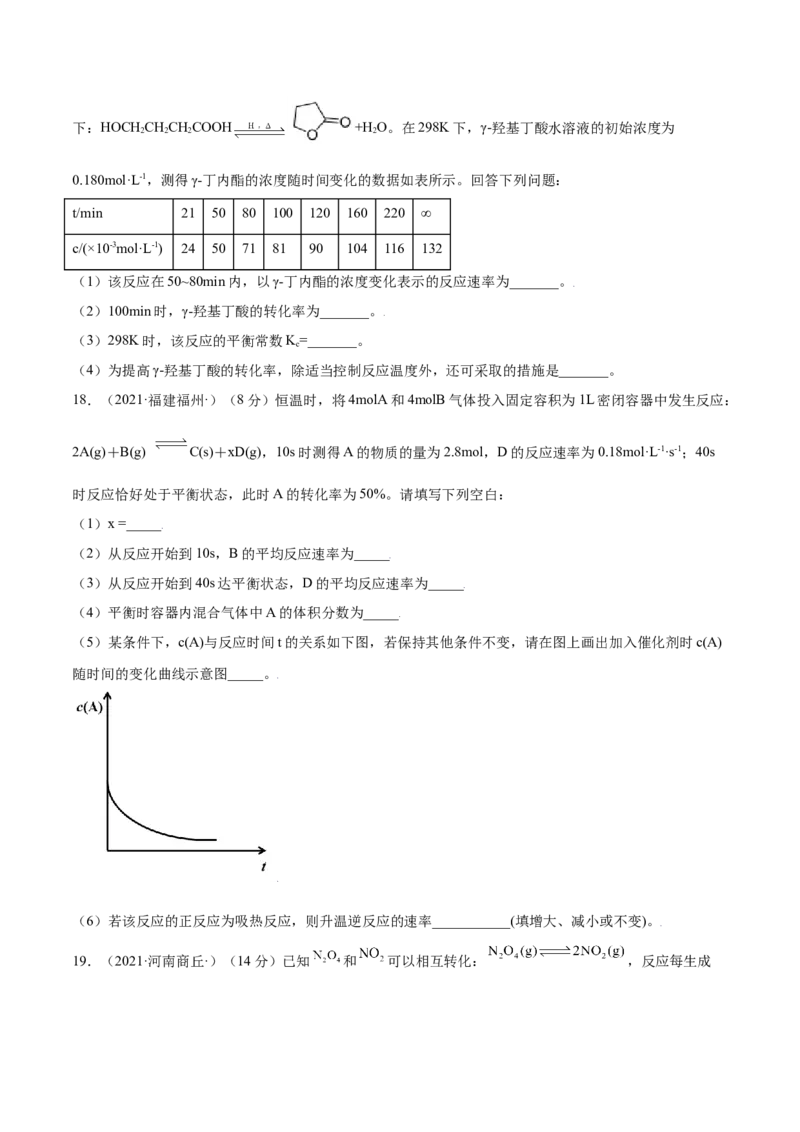
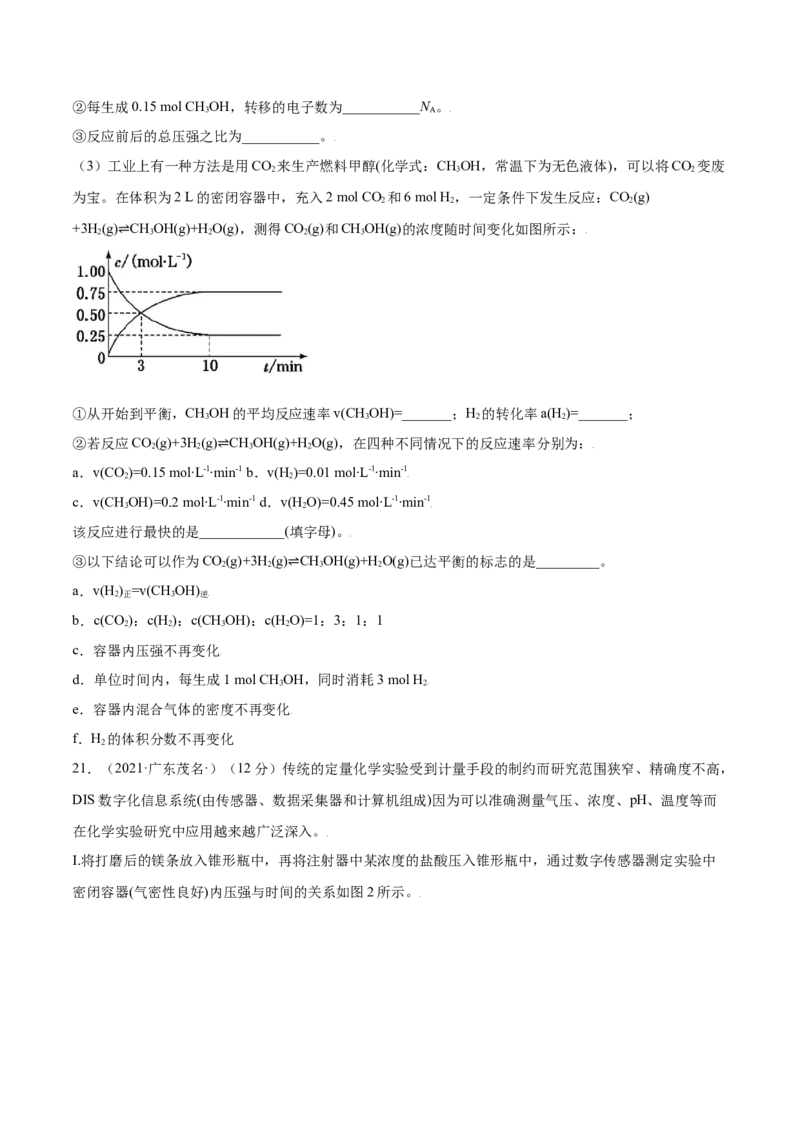
17.(2021·四川成都·)(8分)由γ-羟基丁酸(HOCHCHCHCOOH)生成γ-丁内酯( )的反应如
2 2 2下:HOCH CHCHCOOH +H O。在298K下,γ-羟基丁酸水溶液的初始浓度为
2 2 2 2
0.180mol·L-1,测得γ-丁内酯的浓度随时间变化的数据如表所示。回答下列问题:
t/min 21 50 80 100 120 160 220 ∞
c/(×10-3mol·L-1) 24 50 71 81 90 104 116 132
(1)该反应在50~80min内,以γ-丁内酯的浓度变化表示的反应速率为_______。
(2)100min时,γ-羟基丁酸的转化率为_______。
(3)298K时,该反应的平衡常数K=_______。
c
(4)为提高γ-羟基丁酸的转化率,除适当控制反应温度外,还可采取的措施是_______。
18.(2021·福建福州·)(8分)恒温时,将4molA和4molB气体投入固定容积为1L密闭容器中发生反应:
2A(g)+B(g) C(s)+xD(g),10s时测得A的物质的量为2.8mol,D的反应速率为0.18mol·L-1·s-1;40s
时反应恰好处于平衡状态,此时A的转化率为50%。请填写下列空白:
(1)x =_____
(2)从反应开始到10s,B的平均反应速率为_____
(3)从反应开始到40s达平衡状态,D的平均反应速率为_____
(4)平衡时容器内混合气体中A的体积分数为_____
(5)某条件下,c(A)与反应时间t的关系如下图,若保持其他条件不变,请在图上画出加入催化剂时c(A)
随时间的变化曲线示意图_____。
(6)若该反应的正反应为吸热反应,则升温逆反应的速率___________(填增大、减小或不变)。
19.(2021·河南商丘·)(14分)已知 和 可以相互转化: ,反应每生成,吸收 的热量。在恒温条件下,将一定量的 和 混合气体通入一容积为 的密闭
容器中,各物质浓度随时间变化关系如图所示:
(1)前 内用 表示的化学反应速率为_______;图中c点处v(正)_______(填“>”“<”或“=”)v(逆)。
(2)图中a、b、c、d四个点中,反应达到平衡状态的点有_______;下列能作为该反应达到平衡状态标志
的是_______(填字母)。
A.容器中 的体积分数不变
B.恒温恒容时,体系的压强不再变化
C.
D.消耗 的同时生成
(3)反应进行到 的过程中_______(“放出”或“吸收”)热量,此时容器与外界的热交换总量为_______
; 的转化率为_______(结果保留一位小数)。
20.(2021·四川仁寿·)(14分)在2 L的某恒容密闭容器中发生反应:CO(g)+3H(g) CHOH(g)+
2 2 3
HO(g) H。已知反应中化学键数据如下表:
2
化学键 △ H-H C-O C=O H-O C-H
E/(kJ/mol) 436 351 745 463 413
回答下列问题:
(1)△H___________(填“>”“<”或“=”)0。
(2)某温度下,向该容器中充入0.3 mol CO 、0.9 mol H,发生上述反应,5 min末,反应达到平衡,此
2 2
时测得HO(g)的物质的量分数为25%。
2
①0~5 min内,H 平均速率v(H )=___________mol·L-1·min-1。
2 2②每生成0.15 mol CH OH,转移的电子数为___________N 。
3 A
③反应前后的总压强之比为___________。
(3)工业上有一种方法是用CO 来生产燃料甲醇(化学式:CHOH,常温下为无色液体),可以将CO 变废
2 3 2
为宝。在体积为2 L的密闭容器中,充入2 mol CO 和6 mol H ,一定条件下发生反应:CO(g)
2 2 2
+3H (g) CHOH(g)+H O(g),测得CO(g)和CHOH(g)的浓度随时间变化如图所示:
2 3 2 2 3
⇌
①从开始到平衡,CHOH的平均反应速率v(CHOH)=_______;H 的转化率a(H)=_______;
3 3 2 2
②若反应CO(g)+3H(g) CHOH(g)+H O(g),在四种不同情况下的反应速率分别为:
2 2 3 2
a.v(CO
2
)=0.15 mol∙L-1∙m⇌in-1 b.v(H
2
)=0.01 mol∙L-1∙min-1
c.v(CHOH)=0.2 mol∙L-1∙min-1 d.v(H O)=0.45 mol∙L-1∙min-1
3 2
该反应进行最快的是____________(填字母)。
③以下结论可以作为CO(g)+3H(g) CHOH(g)+H O(g)已达平衡的标志的是_________。
2 2 3 2
a.v(H 2 ) 正 =v(CH 3 OH) 逆 ⇌
b.c(CO):c(H):c(CHOH):c(HO)=1:3:1:1
2 2 3 2
c.容器内压强不再变化
d.单位时间内,每生成1 mol CH OH,同时消耗3 mol H
3 2
e.容器内混合气体的密度不再变化
f.H 的体积分数不再变化
2
21.(2021·广东茂名·)(12分)传统的定量化学实验受到计量手段的制约而研究范围狭窄、精确度不高,
DIS数字化信息系统(由传感器、数据采集器和计算机组成)因为可以准确测量气压、浓度、pH、温度等而
在化学实验研究中应用越来越广泛深入。
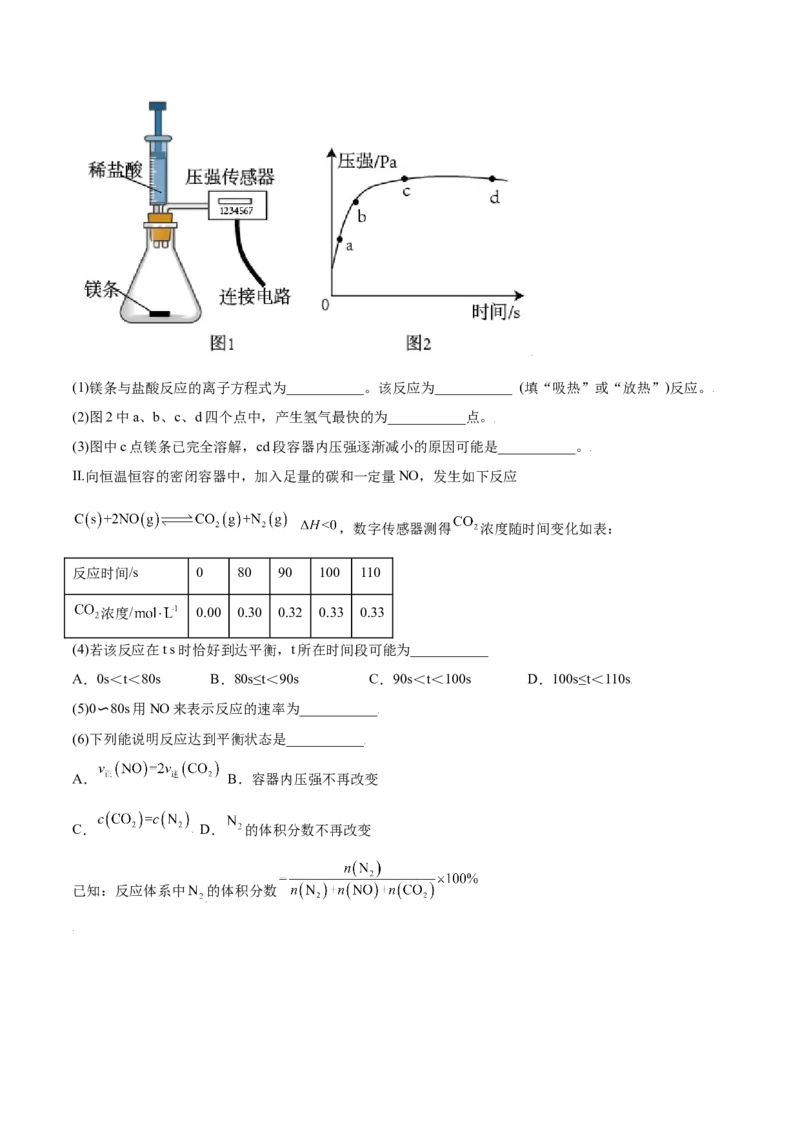
Ⅰ.将打磨后的镁条放入锥形瓶中,再将注射器中某浓度的盐酸压入锥形瓶中,通过数字传感器测定实验中
密闭容器(气密性良好)内压强与时间的关系如图2所示。(1)镁条与盐酸反应的离子方程式为___________。该反应为___________ (填“吸热”或“放热”)反应。
(2)图2中a、b、c、d四个点中,产生氢气最快的为___________点。
(3)图中c点镁条已完全溶解,cd段容器内压强逐渐减小的原因可能是___________。
Ⅱ.向恒温恒容的密闭容器中,加入足量的碳和一定量NO,发生如下反应
,数字传感器测得 浓度随时间变化如表:
反应时间/s 0 80 90 100 110
浓度/ 0.00 0.30 0.32 0.33 0.33
(4)若该反应在t s时恰好到达平衡,t所在时间段可能为___________
A.0s<t<80s B.80s≤t<90s C.90s<t<100s D.100s≤t<110s
(5)0〜80s用NO来表示反应的速率为___________
(6)下列能说明反应达到平衡状态是___________
A. B.容器内压强不再改变
C. D. 的体积分数不再改变
已知:反应体系中 的体积分数倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育