文档内容
第二章 总结与检测 练习(原卷版)
一.选择题(共20小题,每题3分,共60分)
1.下列说法中正确的是( )
A.垃圾是污染物,一定条件下还可能产生二次污染
B.堆肥法处理垃圾是最理想的垃圾处理方法
C.废旧金属、玻璃等不属于垃圾
D.没有绝对的垃圾,垃圾也可回收利用
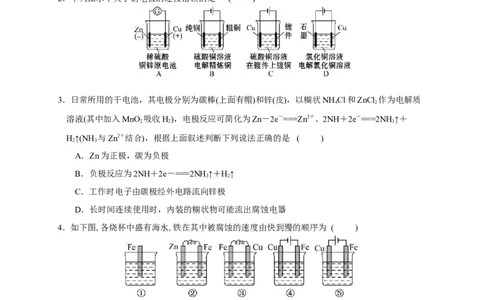
2.下列图示中关于铜电极的连接错误的是 ( )
3.日常所用的干电池,其电极分别为碳棒(上面有帽)和锌(皮),以糊状NH Cl和ZnCl 作为电解质
4 2
溶液(其中加入MnO 吸收H),电极反应可简化为Zn-2e-===Zn2+、2NH+2e-===2NH ↑+
2 2 3
H↑(NH 与Zn2+结合),根据上面叙述判断下列说法正确的是 ( )
2 3
A.Zn为正极,碳为负极
B.负极反应为2NH+2e-===2NH ↑+H↑
3 2
C.工作时电子由碳极经外电路流向锌极
D.长时间连续使用时,内装的糊状物可能流出腐蚀电器
4.如下图,各烧杯中盛有海水,铁在其中被腐蚀的速度由快到慢的顺序为 ( )
5.2011年12月江西铜业排污祸及下游,据测定废水中重金属污染物和有毒非金属污染物达二十余
种,当地民众重金属中毒病症和奇异怪病时有发生. 废水中的重金属指的是( )
A.金属单质 B.金属元素 C.金属铜 D.金属氧化物
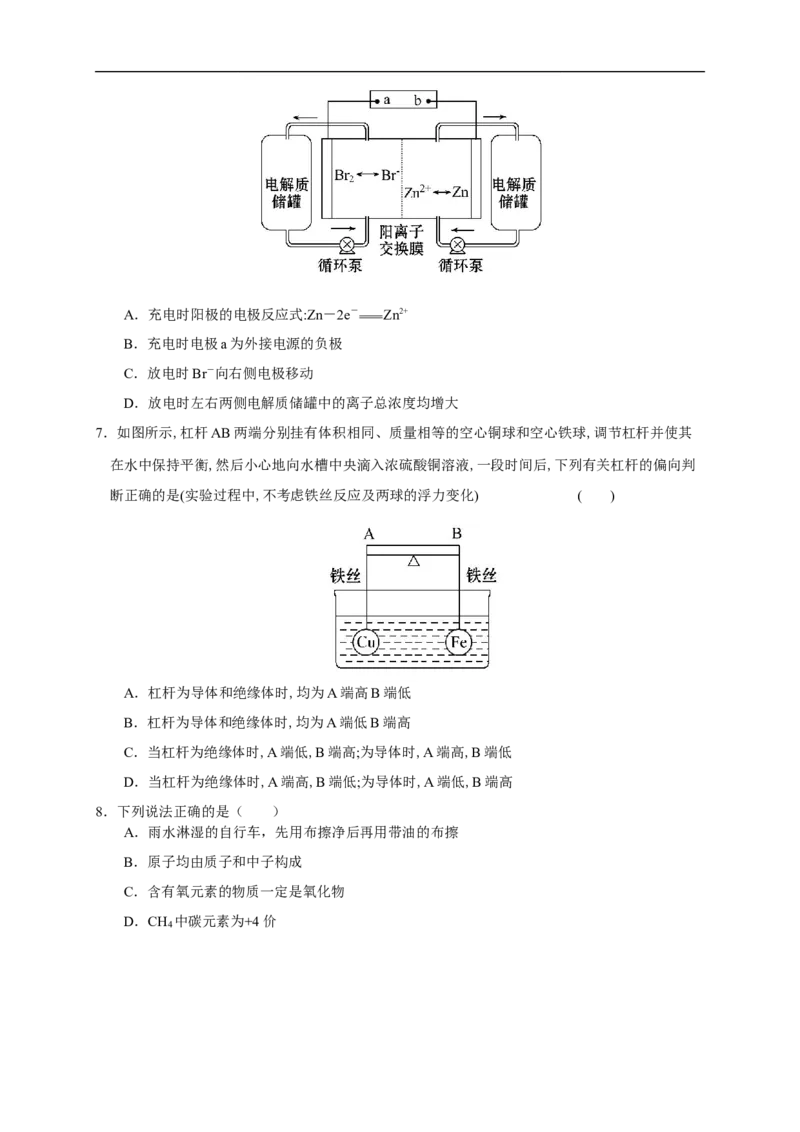
6.液流电池是一种新的蓄电池,是利用正负极电解液分开,各自循环的一种高性能蓄电池,具有容量
高、使用领域(环境)广、循环使用寿命长的特点。如图是一种锌溴液流电池,电解液为溴化锌的水
溶液。下列说法正确的是 ( )A.充电时阳极的电极反应式:Zn-2e- Zn2+
B.充电时电极a为外接电源的负极
C.放电时Br-向右侧电极移动
D.放电时左右两侧电解质储罐中的离子总浓度均增大
7.如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其
在水中保持平衡,然后小心地向水槽中央滴入浓硫酸铜溶液,一段时间后,下列有关杠杆的偏向判
断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化) ( )
A.杠杆为导体和绝缘体时,均为A端高B端低
B.杠杆为导体和绝缘体时,均为A端低B端高
C.当杠杆为绝缘体时,A端低,B端高;为导体时,A端高,B端低
D.当杠杆为绝缘体时,A端高,B端低;为导体时,A端低,B端高
8.下列说法正确的是( )
A.雨水淋湿的自行车,先用布擦净后再用带油的布擦
B.原子均由质子和中子构成
C.含有氧元素的物质一定是氧化物
D.CH 中碳元素为+4价
49. 镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,使镁原电池越
来越成为人们研制绿色原电池的关注焦点。其中一种镁原电池的反应为:xMg+Mo S
3 4
Mg Mo S 下列说法错误的是( )
x 3 4
A.放电时,负极反应为Mg﹣2e﹣═Mg2+
B.放电时,正极反应为Mo S +2xe﹣+xMg2+═Mg Mo S
3 4 x 3 4
C.放电过程中Mg2+向正极迁移
D.放电时,Mo S 发生氧化反应
3 4
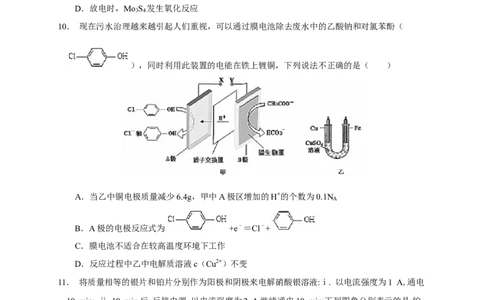
10. 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
),同时利用此装置的电能在铁上镀铜,下列说法不正确的是( )
A.当乙中铜电极质量减少6.4g,甲中A极区增加的H+的个数为0.1N
A
B.A极的电极反应式为 +e﹣=Cl﹣+
C.膜电池不适合在较高温度环境下工作
D.反应过程中乙中电解质溶液c(Cu2+)不变
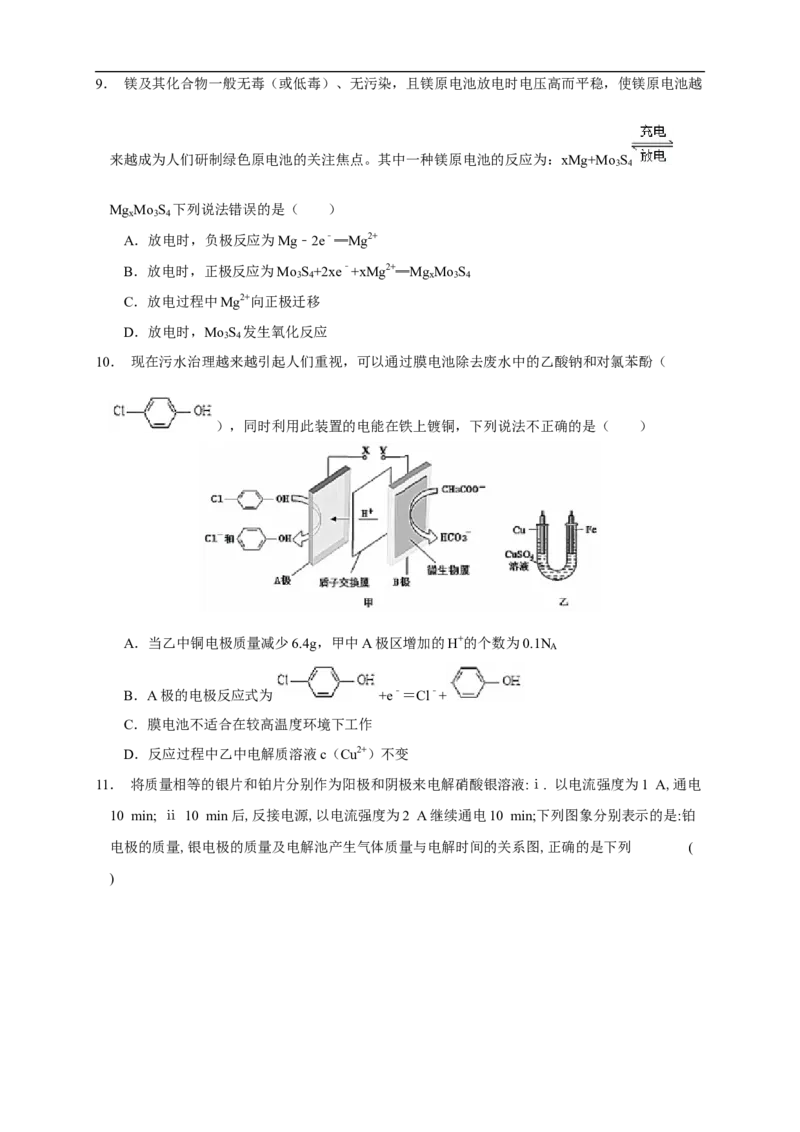
11. 将质量相等的银片和铂片分别作为阳极和阴极来电解硝酸银溶液:ⅰ. 以电流强度为1 A,通电
10 min; ⅱ 10 min后,反接电源,以电流强度为2 A继续通电10 min;下列图象分别表示的是:铂
电极的质量,银电极的质量及电解池产生气体质量与电解时间的关系图,正确的是下列 (
)A.①③ B.①②
C.②③④ D.①②③④
12. 一种热激活电池可用作导弹、火箭的工作电源。热激活电池中作为电解质的固体LiCl﹣KCl
混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO +2LiCl+Ca=
4
CaCl +Li SO +Pb,下列有关说法正确的是( )
2 2 4
A.负极反应式:PbSO +2e+2Li+=Li SO +Pb
4 2 4
B.放电过程中,电流由钙电极流向硫酸铅电极
C.室温下,电池工作每转移0.1mol电子,理论上生成10.35gPb
D.放电过程中,Cl﹣向负极移动
13. 500 mL NaNO 和Cu(NO ) 的混合溶液中c(NO)=6 mol/L,用石墨作电极电解此溶液,当通电
3 3 2
一段时间后,两极均收集到气体22.4 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说
法正确的是( )
A.原混合溶液中c(Na+)=6 mol
B.电解后溶液中c(H+)=4 mol/L
C.上述电解过程中共转移8 mol电子
D.电解后得到的Cu的物质的量为2 mol
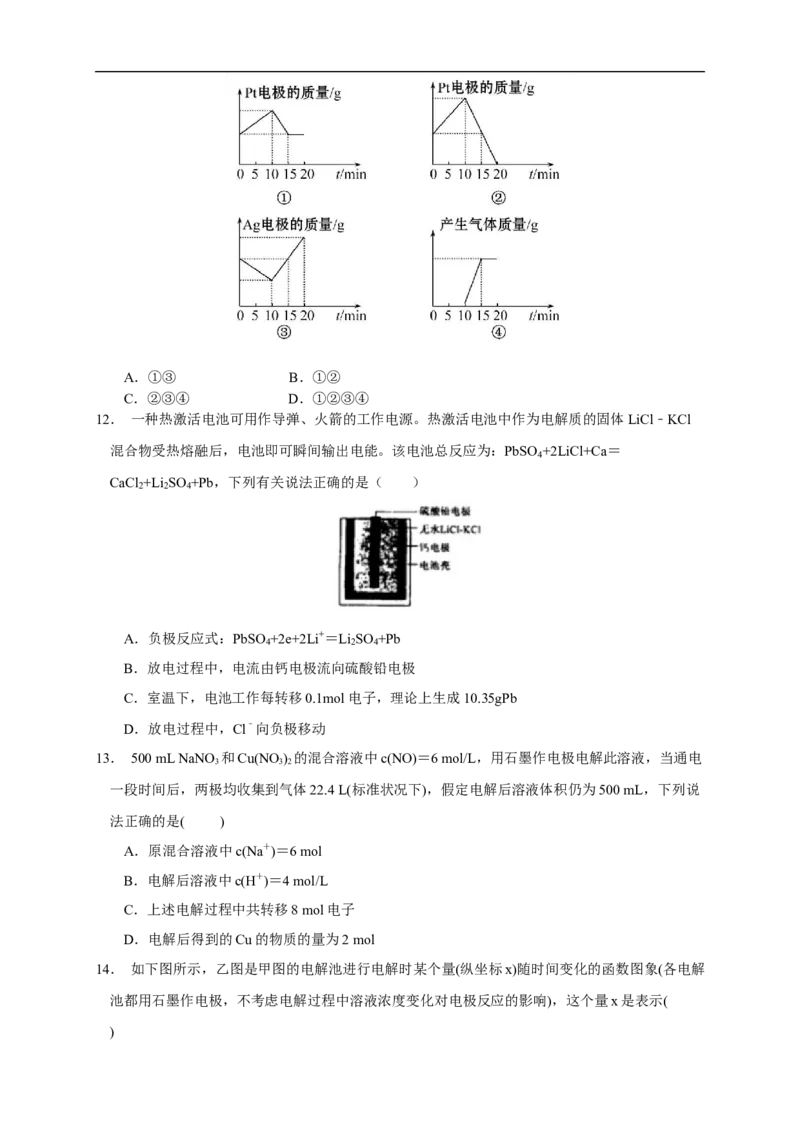
14. 如下图所示,乙图是甲图的电解池进行电解时某个量(纵坐标x)随时间变化的函数图象(各电解
池都用石墨作电极,不考虑电解过程中溶液浓度变化对电极反应的影响),这个量x是表示(
)A.各电解池析出气体的体积
B.各电解池阳极质量的增加量
C.各电解池阴极质量的增加量
D.各电极上放电的离子总数
15. (双选)观察下列几个装置示意图,有关叙述正确的是 ( )
A.装置①中阴极上析出红色固体
B.装置②的待镀铁制品应与电源正极相连
C.装置③闭合开关后,外电路电子由a极流向b 极
D.装置④的X电极是外接电源的正极
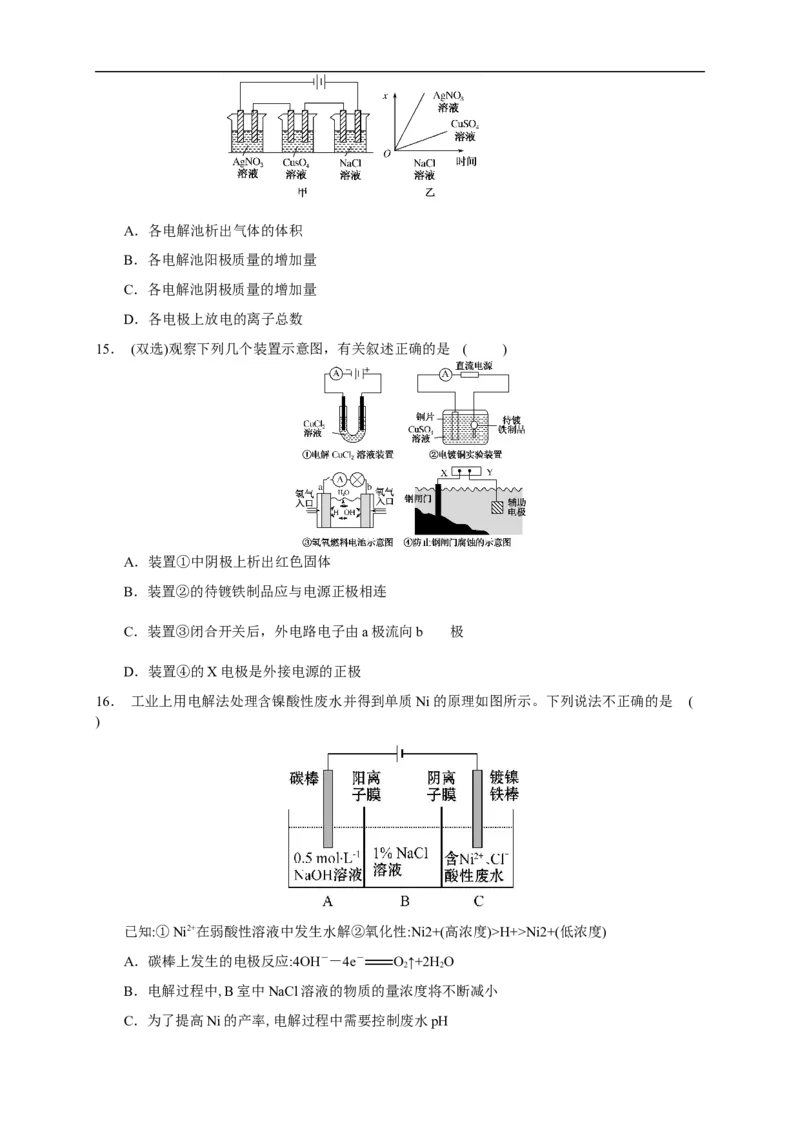
16. 工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是 (
)
已知:①Ni2+在弱酸性溶液中发生水解②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A.碳棒上发生的电极反应:4OH--4e- O↑+2H O
2 2
B.电解过程中,B室中NaCl溶液的物质的量浓度将不断减小
C.为了提高Ni的产率,电解过程中需要控制废水pHD.若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
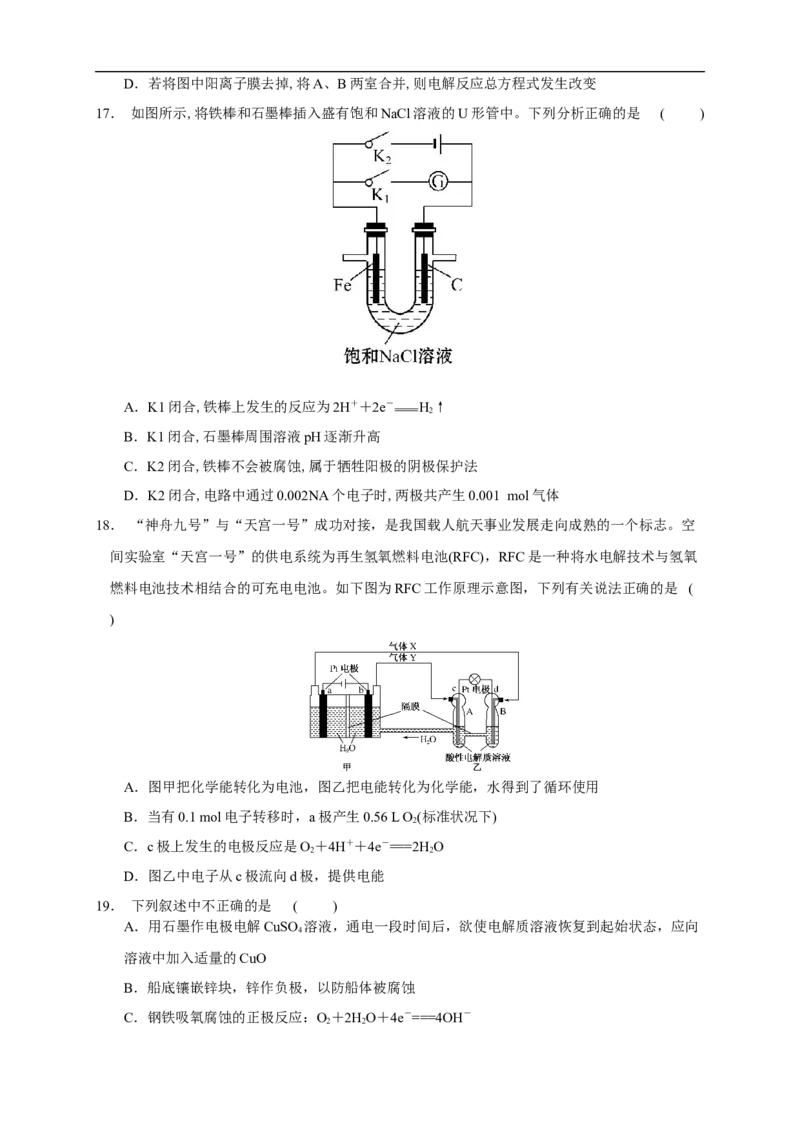
17. 如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U形管中。下列分析正确的是 ( )
A.K1闭合,铁棒上发生的反应为2H++2e- H↑
2
B.K1闭合,石墨棒周围溶液pH逐渐升高
C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
D.K2闭合,电路中通过0.002NA个电子时,两极共产生0.001 mol气体
18. “神舟九号”与“天宫一号”成功对接,是我国载人航天事业发展走向成熟的一个标志。空
间实验室“天宫一号”的供电系统为再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧
燃料电池技术相结合的可充电电池。如下图为RFC工作原理示意图,下列有关说法正确的是 (
)
A.图甲把化学能转化为电池,图乙把电能转化为化学能,水得到了循环使用
B.当有0.1 mol电子转移时,a极产生0.56 L O (标准状况下)
2
C.c极上发生的电极反应是O+4H++4e-===2H O
2 2
D.图乙中电子从c极流向d极,提供电能
19. 下列叙述中不正确的是 ( )
A.用石墨作电极电解CuSO 溶液,通电一段时间后,欲使电解质溶液恢复到起始状态,应向
4
溶液中加入适量的CuO
B.船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁吸氧腐蚀的正极反应:O+2HO+4e-===4OH-
2 2D.电解池中的阳极和原电池中的负极上都发生还原反应
20. 下列有关金属腐蚀与防护的说法不正确的是 ( )
A.纯银器表面在空气中因化学腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C.海轮外壳连接锌块以保护外壳不受腐蚀
D.可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
二、非选择题(共40分)
21. (8分)Ⅰ.某化学活动小组利用如图甲装置对原电池进行研究,请回答下列问题:(其中盐桥为含
有饱和KCl溶液的琼脂)
(1)在甲图装置中,当电流计中指针发生偏转时,盐桥中 K+移向________(填“A”或“B”)烧
杯。
(2)锌电极为电池的________极,发生的电极反应式为________;铜电极上发生的电极反应式为
________。
Ⅱ.该小组同学提出设想:如果将实验中的盐桥换为导线(铜制),电流表是否也发生偏转呢?带
着疑问,该小组利用图乙装置进行了实验,发现电流计指针同样发生偏转。回答下列问题:
(3)对于实验中产生电流的原因,该小组进行了深入探讨,后经老师提醒注意到使用的是铜导线,
烧杯A实际为原电池,B成了用电器。对于图乙,烧杯A实际是原电池的问题上,该小组成员
发生了很大分歧。
①一部分同学认为是由于ZnSO 溶液水解显酸性,此时原电池实际是由 Zn、Cu作电极,
4
HSO 溶液作为电解质溶液而构成的原电池。如果这个观点正确,那么原电池的正极反应为
2 4
________________________________________________________________________。
②另一部分同学认为是溶液酸性较弱,由于溶解在溶液中的氧气的作用,使得 Zn、Cu之间形
成 原 电 池 。 如 果 这 个 观 点 正 确 , 那 么 原 电 池 的 正 极 反 应 为
________________________________________________________________________。
(4)若第(3)问中②观点正确,则可以利用此原理设计电池为在偏远海岛工作的灯塔供电。其具
体装置为以金属铝和石墨为电极,以海水为电解质溶液,最终铝变成氢氧化铝。请写出该电池工作时总反应的化学方程式:
________________________________________________________________________。
22.(7分)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图1
所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH 和空气,其中固体电解质是掺
4
杂了YO 的ZrO 固体,它在高温下能传导阳极生成的O2-(O +4e-===2O2-)。
2 3 2 2
(1)c电极的名称为________,d电极上的电极反应式为
________________________________________________________________________。
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1 CuSO 溶液,a电极上的电极反应式为
4
_______________________________________________________________________,若 a 电极
产生56 mL(标准状况)气体,则所得溶液的pH=________(不考虑溶液体积变化),若要使电解
质溶液恢复到电解前的状态,可加入________(填序号)。
a.CuO b.Cu(OH)
2
c.CuCO d.Cu (OH) CO
3 2 2 3
23. (8分)观察下列装置,回答下列问题:
(1)装置B中PbO 上发生的电极反应方程式为
2
________________________________________________________________________。
(2)装置A中总反应的离子方程式为
_________________________________________________________________________。
(3)若装置E中的目的是在Cu材料上镀银,则溶液X为________,极板N的材料为________。
极板M处的电极反应式为__________________________________。
(4)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为________ L(标准状况下,
不考虑气体的溶解)。
24.(8分) 铁、铜及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)黄铁矿(FeS ,其中S为-1价)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS+
2 2
8O=====6SO +Fe O,氧化产物为________,若有3 mol FeS 参加反应,转移电子的物质的
2 2 3 4 2
量为________。
(2)①钢铁的电化学腐蚀简单示意图如下,将该图稍作修改即可成为钢铁电化学防护的简单示意
图,请在下图虚线框内作出修改,并用箭头标出电子流动方向。②写出修改前的钢铁吸氧腐蚀时石墨电极的电极反应式:_______________________。
(3)高铁酸钾(K FeO)可作净水剂,也可用于制造高铁电池。高铁电池是一种新型可充电电池,
2 4
与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为3Zn+
2KFeO+8HO3Zn(OH) +2Fe(OH) +4KOH,该电池放电时正极反应式为
2 4 2 2 3
________________。用该电池电解100 mL 1 mol·L-1的AgNO 溶液,当电路中通过0.1 mol电
3
子时,被电解溶液的pH为________(溶液体积变化忽略不计)。
25.(9分) 肼(N H)又称联氨,是一种可燃性液体,可用作火箭燃料。
2 4
(1)已知在101 kPa时,32.0 g N H 在氧气中完全燃烧生成氮气和水,放出热量624 kJ(25 ℃时),
2 4
NH 完全燃烧的热化学方程式是___________________________________________。
2 4
(2)肼空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼空气燃料
电池放电时,正极的反应式是________;负极的反应式是___________________。
(3)右图是一个电化学过程示意图。
①锌片上发生的电极反应式是_________________________________。
②假设使用肼空气燃料电池作为本过程中的电源,铜片的质量变化128 g,则肼空气燃料电池
理论上消耗标准状况下的空气______L(假设空气中氧气体积分数为20%)。