文档内容
专题四 溶液及溶解度曲线
命题点分类集训
命题点1 溶液的判断及组成 溶解时的吸、放热现象 乳化
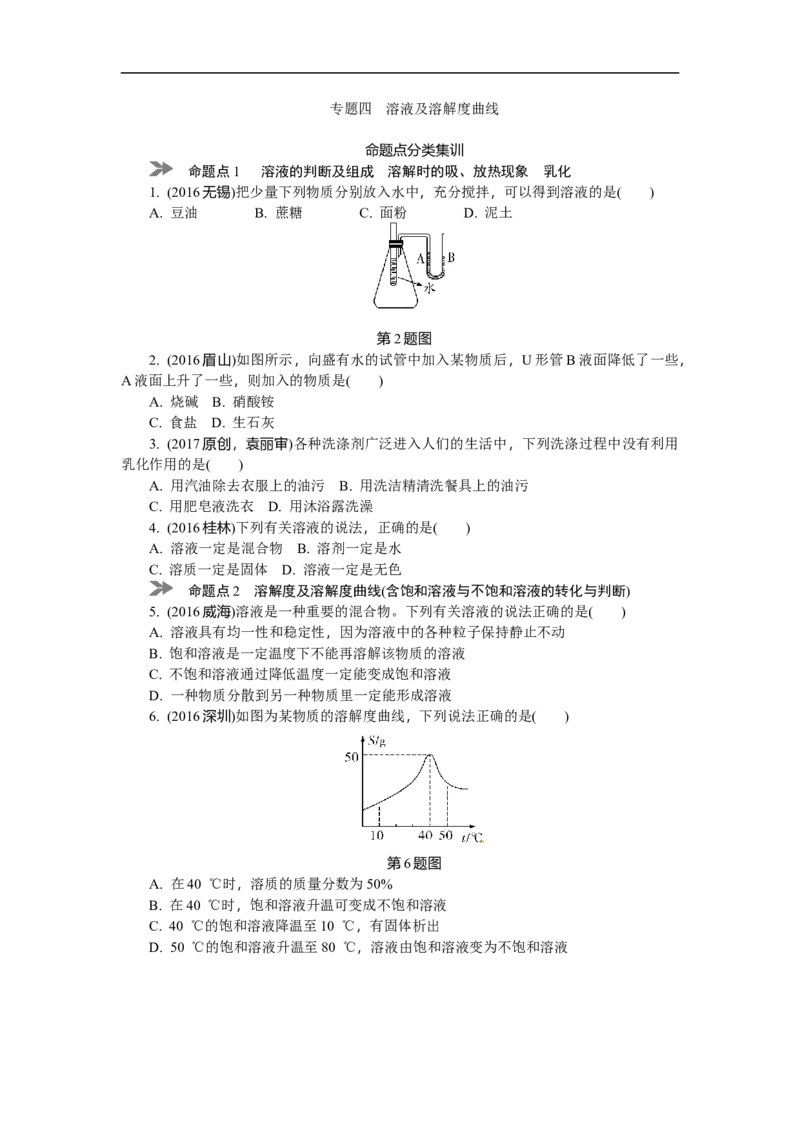
1. (2016无锡)把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A. 豆油 B. 蔗糖 C. 面粉 D. 泥土
第2题图
[来源:Zxxk.Com]
2. (2016眉山)如图所示,向盛有水的试管中加入某物质后,U形管B液面降低了一些,
A液面上升了一些,则加入的物质是( )
A. 烧碱 B. 硝酸铵
C. 食盐 D. 生石灰
3. (2017原创,袁丽审)各种洗涤剂广泛进入人们的生活中,下列洗涤过程中没有利用
乳化作用的是( )
A. 用汽油除去衣服上的油污 B. 用洗洁精清洗餐具上的油污
C. 用肥皂液洗衣 D. 用沐浴露洗澡
4. (2016桂林)下列有关溶液的说法,正确的是( )
A. 溶液一定是混合物 B. 溶剂一定是水
C. 溶质一定是固体 D. 溶液一定是无色
命题点2 溶解度及溶解度曲线(含饱和溶液与不饱和溶液的转化与判断)
5. (2016威海)溶液是一种重要的混合物。下列有关溶液的说法正确的是( )
A. 溶液具有均一性和稳定性,因为溶液中的各种粒子保持静止不动
B. 饱和溶液是一定温度下不能再溶解该物质的溶液
C. 不饱和溶液通过降低温度一定能变成饱和溶液
D. 一种物质分散到另一种物质里一定能形成溶液
6. (2016深圳)如图为某物质的溶解度曲线,下列说法正确的是( )
第6题图
A. 在40 ℃时,溶质的质量分数为50%
B. 在40 ℃时,饱和溶液升温可变成不饱和溶液
C. 40 ℃的饱和溶液降温至10 ℃,有固体析出
D. 50 ℃的饱和溶液升温至80 ℃,溶液由饱和溶液变为不饱和溶液第7题图
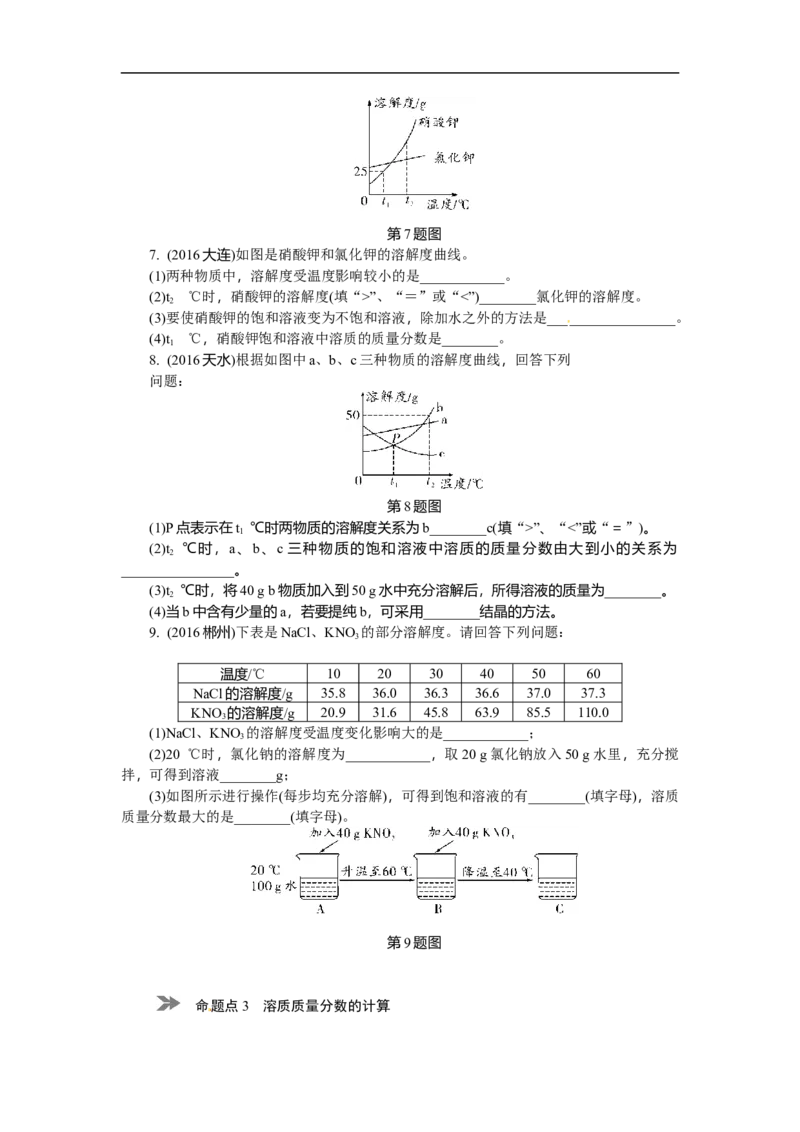
7. (2016大连)如图是硝酸钾和氯化钾的溶解度曲线。
(1)两种物质中,溶解度受温度影响较小的是____________。
(2)t ℃时,硝酸钾的溶解度(填“>”、“=”或“<”)________氯化钾的溶解度。
2
(3)要使硝酸钾的饱和溶液变为不饱和溶液,除加水之外的方法是__________________。
(4)t ℃,硝酸钾饱和溶液中溶质的质量分数是________。
1
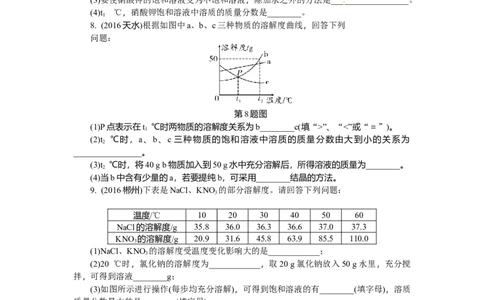
8. (2016天水)根据如图中a、b、c三种物质的溶解度曲线,回答下列
问题:
第8题图
(1)P点表示在t ℃时两物质的溶解度关系为b________c(填“>”、“<”或“=”)。
1
(2)t ℃时,a、b、c 三种物质的饱和溶液中溶质的质量分数由大到小的关系为
2
________________。
(3)t ℃时,将40 g b物质加入到50 g水中充分溶解后,所得溶液的质量为________。
2
(4)当b中含有少量的a,若要提纯b,可采用________结晶的方法。
9. (2016郴州)下表是NaCl、KNO 的部分溶解度。请回答下列问题:
3
温度/℃ 10 20 30 40 50 60
NaCl的溶解度/g 35.8 36.0 36.3 36.6 37.0 37.3
KNO 的溶解度/g 20.9 31.6 45.8 63.9 85.5 110.0
3
(1)NaCl、KNO 的溶解度受温度变化影响大的是____________;
3
(2)20 ℃时,氯化钠的溶解度为____________,取20 g氯化钠放入50 g水里,充分搅
拌,可得到溶液________g;
(3)如图所示进行操作(每步均充分溶解),可得到饱和溶液的有________(填字母),溶质
质量分数最大的是________(填字母)。
第9题图
命题点3 溶质质量分数的计算10. (2016常德)将100 g 98%的浓硫酸注入900 g水中,所得稀硫酸中溶质的质量分数
为( )
A. 9.8% B. 10.0% C. 10.9% D. 11.1%
11. (2016广州)某温度下,在100 g质量分数为20%的KNO 不饱和溶液甲中加入10 g
3
KNO 固体,恰好得到饱和溶液乙,下列说法正确的是( )
3
A. 该温度下,KNO 的溶解度为30 g
3
B. 乙溶液的质量分数为30%
C. 降低温度,可以使甲溶液变成饱和溶液
D. 升高温度,甲、乙两溶液的质量分数都增大
命题点4 一定溶质质量分数溶液的配制
12. (2016茂名)用氯化钠配制50 g质量分数为6%的氯化钠溶液,不需要用到的实验步
骤是( )
A. 计算 B. 量取 C. 溶解 D. 蒸发
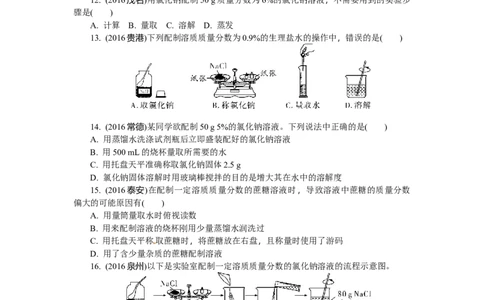
13. (2016贵港)下列配制溶质质量分数为0.9%的生理盐水的操作中,错误的是( )
14. (2016常德)某同学欲配制50 g 5%的氯化钠溶液。下列说法中正确的是( )
A. 用蒸馏水洗涤试剂瓶后立即盛装配好的氯化钠溶液
B. 用500 mL的烧杯量取所需要的水
C. 用托盘天平准确称取氯化钠固体2.5 g
D. 氯化钠固体溶解时用玻璃棒搅拌的目的是增大其在水中的溶解度
15. (2016泰安)在配制一定溶质质量分数的蔗糖溶液时,导致溶液中蔗糖的质量分数
偏大的可能原因有( )
A. 用量筒量取水时俯视读数
B. 用来配制溶液的烧杯刚用少量蒸馏水润洗过
C. 用托盘天平称取蔗糖时,将蔗糖放在右盘,且称量时使用了游码
D. 用了含少量杂质的蔗糖配制溶液
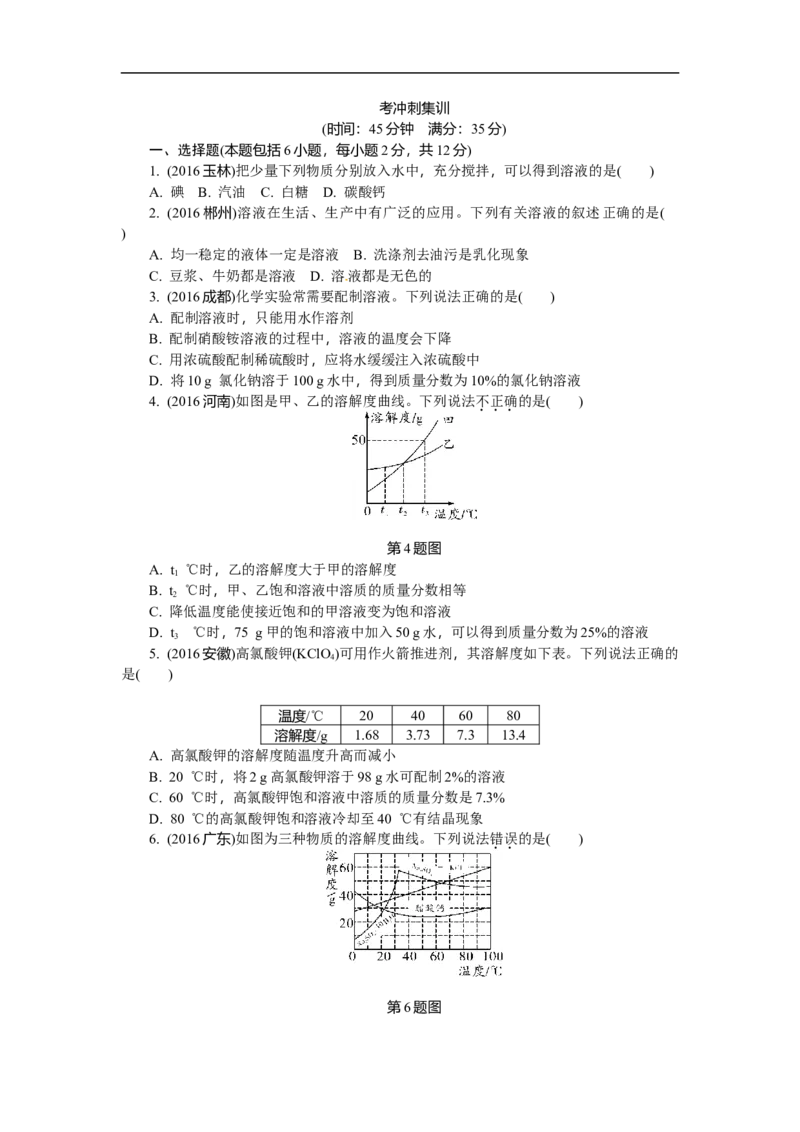
16. (2016泉州)以下是实验室配制一定溶质质量分数的氯化钠溶液的流程示意图。
第16题图
请根据示意图回答:
(1)托盘天平左盘中固体氯化钠的质量为________g,量筒中水的体积为______mL;
(2)上述溶液取10 g加水40 g进行稀释,所得氯化钠溶液的溶质质量分数是________。
中考冲刺集训
(时间:45分钟 满分:35分)
一、选择题(本题包括6小题,每小题2分,共12分)
1. (2016玉林)把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A. 碘 B. 汽油 C. 白糖 D. 碳酸钙
2. (2016郴州)溶液在生活、生产中有广泛的应用。下列有关溶液的叙述正确的是(
)
A. 均一稳定的液体一定是溶液 B. 洗涤剂去油污是乳化现象
C. 豆浆、牛奶都是溶液 D. 溶液都是无色的
3. (2016成都)化学实验常需要配制溶液。下列说法正确的是( )
A. 配制溶液时,只能用水作溶剂
B. 配制硝酸铵溶液的过程中,溶液的温度会下降
C. 用浓硫酸配制稀硫酸时,应将水缓缓注入浓硫酸中
D. 将10 g 氯化钠溶于100 g水中,得到质量分数为10%的氯化钠溶液
4. (2016河南)如图是甲、乙的溶解度曲线。下列说法不正确的是( )
第4题图
A. t ℃时,乙的溶解度大于甲的溶解度
1
B. t ℃时,甲、乙饱和溶液中溶质的质量分数相等
2
C. 降低温度能使接近饱和的甲溶液变为饱和溶液
D. t ℃时,75 g甲的饱和溶液中加入50 g水,可以得到质量分数为25%的溶液
3
5. (2016安徽)高氯酸钾(KClO)可用作火箭推进剂,其溶解度如下表。下列说法正确的
4
是( )
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A. 高氯酸钾的溶解度随温度升高而减小
B. 20 ℃时,将2 g高氯酸钾溶于98 g水可配制2%的溶液
C. 60 ℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D. 80 ℃的高氯酸钾饱和溶液冷却至40 ℃有结晶现象
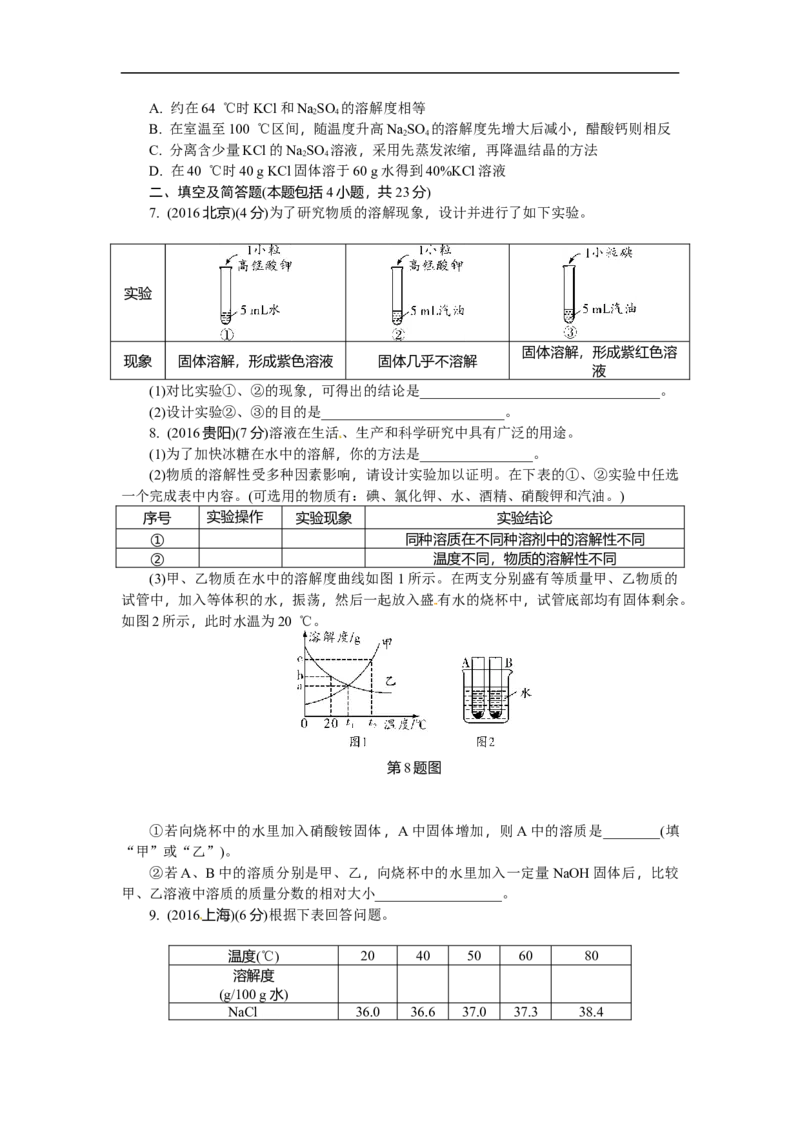
6. (2016广东)如图为三种物质的溶解度曲线。下列说法错误的是( )
第6题图A. 约在64 ℃时KCl和NaSO 的溶解度相等
2 4
B. 在室温至100 ℃区间,随温度升高NaSO 的溶解度先增大后减小,醋酸钙则相反
2 4
C. 分离含少量KCl的NaSO 溶液,采用先蒸发浓缩,再降温结晶的方法
2 4
D. 在40 ℃时40 g KCl固体溶于60 g水得到40%KCl溶液
二、填空及简答题(本题包括4小题,共23分)
7. (2016北京)(4分)为了研究物质的溶解现象,设计并进行了如下实验。
实验
固体溶解,形成紫红色溶
现象 固体溶解,形成紫色溶液 固体几乎不溶解
液
(1)对比实验①、②的现象,可得出的结论是__________________________________。
(2)设计实验②、③的目的是__________________________。
8. (2016贵阳)(7分)溶液在生活、生产和科学研究中具有广泛的用途。
(1)为了加快冰糖在水中的溶解,你的方法是________________。
(2)物质的溶解性受多种因素影响,请设计实验加以证明。在下表的①、②实验中任选
一个完成表中内容。(可选用的物质有:碘、氯化钾、水、酒精、硝酸钾和汽油。)
序号 实验操作 实验现象 实验结论
[来源:学&
科&网Z&X&X&K]
① 同种溶质在不同种溶剂中的溶解性不同
② [来源:学科网] 温度不同,物质的溶解性不同
(3)甲、乙物质在水中的溶解度曲线如图1所示。在两支分别盛有等质量甲、乙物质的
试管中,加入等体积的水,振荡,然后一起放入盛有水的烧杯中,试管底部均有固体剩余。
如图2所示,此时水温为20 ℃。
第8题图
①若向烧杯中的水里加入硝酸铵固体,A中固体增加,则A中的溶质是________(填
“甲”或“乙”)。
②若A、B中的溶质分别是甲、乙,向烧杯中的水里加入一定量NaOH固体后,比较
甲、乙溶液中溶质的质量分数的相对大小__________________。
9. (2016上海)(6分)根据下表回答问题。
温度(℃) 20 40 50 60 80
溶解度
(g/100 g水)
NaCl 36.0 36.6 37.0 37.3 38.4
[来源:Z*xx*k.Com]NH Cl 37.2 45.8 50.4 55.2 65.6
4
KNO 31.6 63.9 85.5 110 169
3
① 20 ℃时,溶解度最大的物质是________。
第9题图1
② 50 ℃时,100 g水中最多溶解NaCl________g。
③量筒的局部示意见图1,量取水时应沿________视线(选填“a”或“b”)进行读数;
________视线(选填“a”或“b”)对应的读数较大。
④A是80 ℃含有120 g水的KNO 溶液。经过如图2操作,得到102 g KNO 固体。
3 3
第9题图2
Ⅰ.A溶液为________(选填“饱和”或“不饱和”)溶液。
Ⅱ.对以上过程的分析,正确的是________(选填编号)。
a.A到B的过程中,溶质质量没有改变
b.B中溶质与溶剂的质量比为169∶100
c.开始析出KNO 固体的温度在60 ℃至80 ℃之间
3
d.A溶液的质量等于222 g
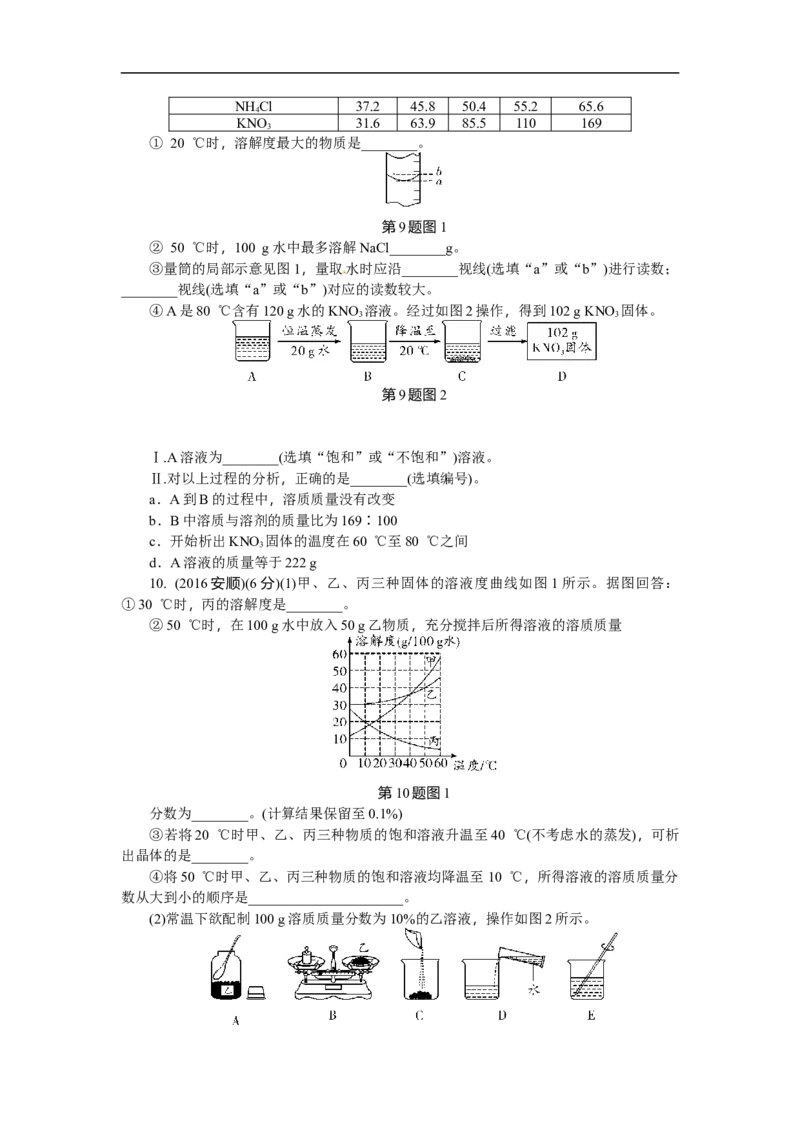
10. (2016安顺)(6分)(1)甲、乙、丙三种固体的溶液度曲线如图1所示。据图回答:
①30 ℃时,丙的溶解度是________。
②50 ℃时,在100 g水中放入50 g乙物质,充分搅拌后所得溶液的溶质质量
第10题图1
分数为________。(计算结果保留至0.1%)
③若将20 ℃时甲、乙、丙三种物质的饱和溶液升温至40 ℃(不考虑水的蒸发),可析
出晶体的是________。
④将50 ℃时甲、乙、丙三种物质的饱和溶液均降温至10 ℃,所得溶液的溶质质量分
数从大到小的顺序是______________________。
(2)常温下欲配制100 g溶质质量分数为10%的乙溶液,操作如图2所示。第10题图2
请回答下列问题:
①上图中操作有错误的是________(填对应字母)。
②量取水时,若采用仰视的方法读数,会导致所配溶液的溶质质量分数________(填
“偏大”、“偏小”或“无影响”)。阶段测评集训二 水与常见的溶液
(时间:60分钟 满分:45分)
一、选择题(本题包括4小题,每小题2分,共8分)
1. (2016云南)下列溶液中,溶剂不是水的是( )
A. 蔗糖溶液 B. 生理盐水 C. 碘的酒精溶液 D. 稀盐酸
2. (2016新疆自治区、兵团)3月22日是“世界水日”,有关水的认识正确的是( )
A. 生活中用活性炭降低水的硬度
B. 将FeCl 、蔗糖、汽油分别加入一定量的水中都能形成溶液
3
C. 自来水厂净水的过程有静置沉淀、过滤、吸附、消毒
D. 从电解水得到H 和O,可知水是由氢原子和氧原子组成的
2 2
3. (2016呼和浩特)小朋要配制50 g质量分数为14%的氢氧化钠溶液来制作“叶脉书
签”。下列关于配制该溶液的说法不正确的是( )
①若用氢氧化钠固体配制,需称取氢氧化钠固体7.0 g
②用托盘天平称氢氧化钠固体时,在两盘各放一张质量相等的纸
③选用200 mL量筒量取所需水的体积
④实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和试剂瓶
⑤用量筒量取水时,俯视读数,配得溶液的溶质质量分数偏小
A. ①③ B. ②③⑤ C. ③⑤ D. ②④⑤
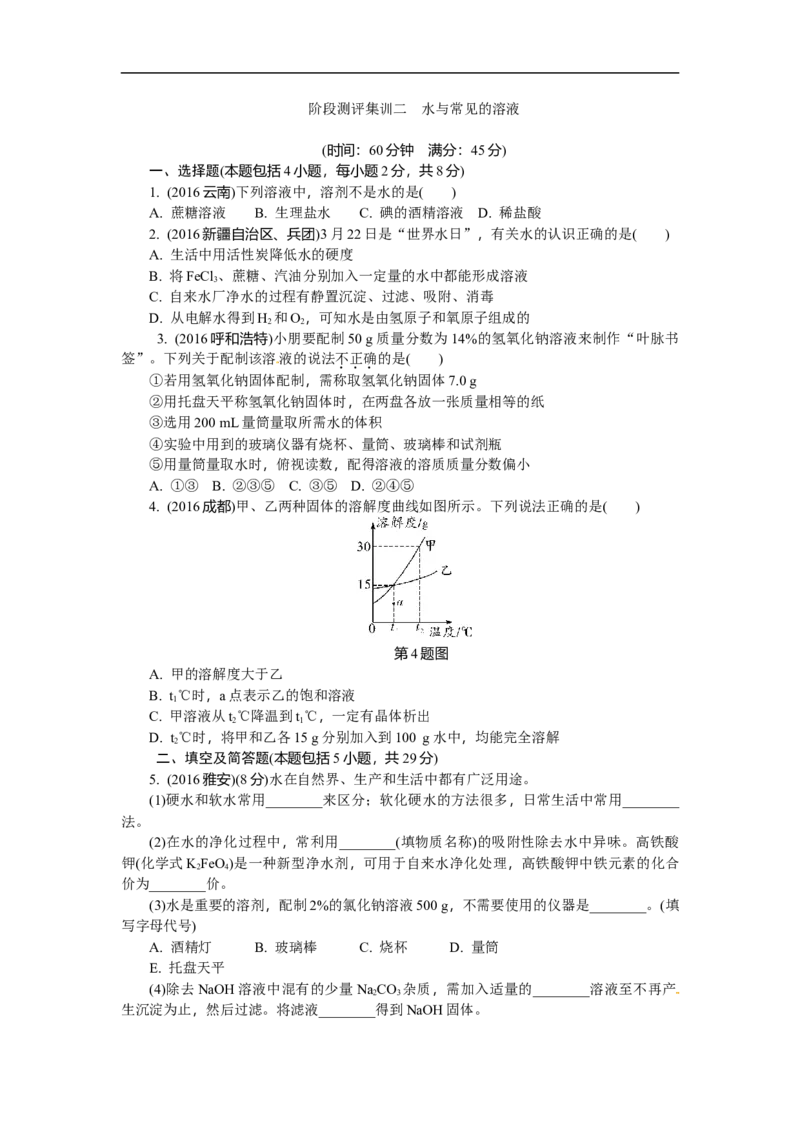
4. (2016成都)甲、乙两种固体的溶解度曲线如图所示。下列说法正确的是( )
第4题图
A. 甲的溶解度大于乙
B. t℃时,a点表示乙的饱和溶液
1
C. 甲溶液从t℃降温到t℃,一定有晶体析出
2 1
D. t℃时,将甲和乙各15 g分别加入到100 g水中,均能完全溶解
2
二、填空及简答题(本题包括5小题,共29分)
5. (2016雅安)(8分)水在自然界、生产和生活中都有广泛用途。
(1)硬水和软水常用________来区分;软化硬水的方法很多,日常生活中常用________
法。
(2)在水的净化过程中,常利用________(填物质名称)的吸附性除去水中异味。高铁酸
钾(化学式KFeO)是一种新型净水剂,可用于自来水净化处理,高铁酸钾中铁元素的化合
2 4
价为________价。
[来源:学科网]
(3)水是重要的溶剂,配制2%的氯化钠溶液500 g,不需要使用的仪器是________。(填
写字母代号)
A. 酒精灯 B. 玻璃棒 C. 烧杯 D. 量筒
E. 托盘天平
(4)除去NaOH溶液中混有的少量NaCO 杂质,需加入适量的________溶液至不再产
2 3
生沉淀为止,然后过滤。将滤液________得到NaOH固体。(5)现有20 ℃时Ca(OH) 的饱和溶液甲,向其中加入一定量CaO,一段时间后得到同
2
温度的溶液乙;甲、乙溶液中溶质质量甲________乙(填“>”、“<”或“=”)。
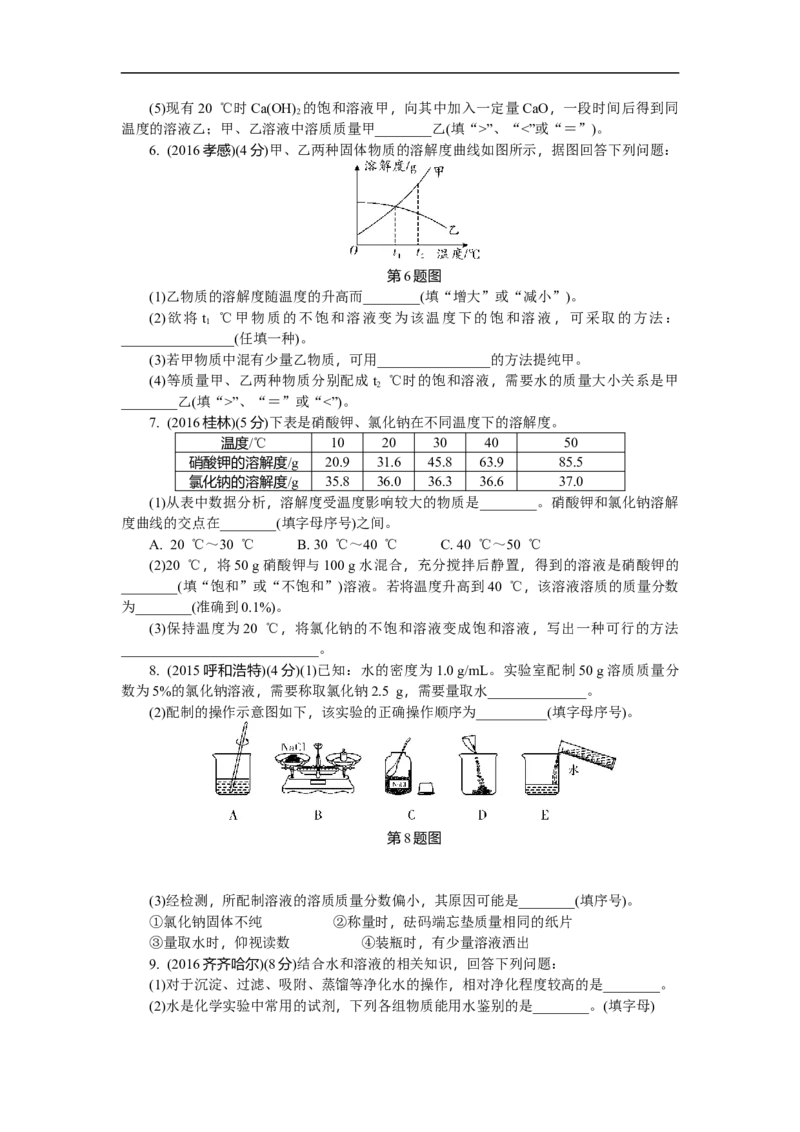
6. (2016孝感)(4分)甲、乙两种固体物质的溶解度曲线如图所示,据图回答下列问题:
第6题图
(1)乙物质的溶解度随温度的升高而________(填“增大”或“减小”)。
(2)欲将 t ℃甲物质的不饱和溶液变为该温度下的饱和溶液,可采取的方法:
1
________________(任填一种)。
(3)若甲物质中混有少量乙物质,可用________________的方法提纯甲。
(4)等质量甲、乙两种物质分别配成 t ℃时的饱和溶液,需要水的质量大小关系是甲
2
________乙(填“>”、“=”或“<”)。
7. (2016桂林)(5分)下表是硝酸钾、氯化钠在不同温度下的溶解度。
温度/℃ 10 20 30 40 50
硝酸钾的溶解度/g 20.9 31.6 45.8 63.9 85.5
氯化钠的溶解度/g 35.8 36.0 36.3 36.6 37.0
(1)从表中数据分析,溶解度受温度影响较大的物质是________。硝酸钾和氯化钠溶解
度曲线的交点在________(填字母序号)之间。
A. 20 ℃~30 ℃ B. 30 ℃~40 ℃ C. 40 ℃~50 ℃
(2)20 ℃,将50 g硝酸钾与100 g水混合,充分搅拌后静置,得到的溶液是硝酸钾的
________(填“饱和”或“不饱和”)溶液。若将温度升高到40 ℃,该溶液溶质的质量分数
为________(准确到0.1%)。
(3)保持温度为20 ℃,将氯化钠的不饱和溶液变成饱和溶液,写出一种可行的方法
____________________________。
8. (2015呼和浩特)(4分)(1)已知:水的密度为1.0 g/mL。实验室配制50 g溶质质量分
数为5%的氯化钠溶液,需要称取氯化钠2.5 g,需要量取水______________。
(2)配制的操作示意图如下,该实验的正确操作顺序为__________(填字母序号)。
第8题图
(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是________(填序号)。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片
③量取水时,仰视读数 ④装瓶时,有少量溶液洒出
9. (2016齐齐哈尔)(8分)结合水和溶液的相关知识,回答下列问题:
(1)对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是________。
(2)水是化学实验中常用的试剂,下列各组物质能用水鉴别的是________。(填字母)第9题图
A. 氢氧化钠和硝酸铵
B. 食盐和蔗糖
C. 高锰酸钾和碘
(3)欲配制100 g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是
____________。
①溶解 ②把配好的溶液装入细口瓶
③称量 ④计算 ⑤量取
(4)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
①P点的含义是______________________________。
②在t ℃时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是________
2
克。
③将t ℃时a、b、c三种物质的饱和溶液升温至t ℃,所得溶液中溶质的质量分数大
1 2
小关系是________。
④a物质中含有少量c物质,可用____________方法提纯a物质。(填“降温结晶”或
“蒸发结晶”)
三、计算题(本题包括1小题,共8分)
10. (2016天津)(8分)取硫酸钠和氯化钠的混合物15 g,加入180 g水使其完全溶解,
再加入100 g 氯化钡溶液恰好完全反应,过滤,得271.7 g滤液(不考虑实验过程中质量损
失)。计算:
(1)该混合物中硫酸钠的质量分数(计算结果精确到0.1%)。
(2)反应后所得滤液中溶质的质量分数(计算结果精确到0.1%)。
专题四 溶液及溶解度曲线
命题点分类集训
命题点1 溶液的判断及组成 溶解时的吸、放热现象 乳化
1. B 2. B 3. A 4. A
命题点2 溶解度及溶解度曲线(含饱和溶液与不饱和溶液的转化与判断)
5. B 6. C
7. (1)氯化钾(或KCl ) (2)>
(3)升高温度
(4)20%
8. (1)= (2)b>a>c (3)75 g
(4)降温(或冷却热饱和溶液)
9. (1) KNO (2)36.0 g 68 (3)AC B
3命题点3 溶质质量分数的计算
10. A 11. C
命题点4 一定溶质质量分数溶液的配制
12. D 13. C 14. C 15.A
16. (1)12 68 (2)3%
中考冲刺集训
1. C 2. B 3. B 4. D 5. D 6. D
7. (4分)(1)同种溶质在不同溶剂中的溶解特性不同(2分) (2)探究溶质种类对溶解特性
的影响(2分)
8. (7分)(1)用玻璃棒搅拌(合理即可)(1分)
(2)①将碘分别加入水和酒精中(1分) 水中的碘不溶解,酒精中的碘溶解,且溶液呈
棕黄色(合理即可)(1分)
②将硝酸钾(或氯化钾)分别加入同体积的冷水和热水中,边加固体边搅拌,比较溶解
的物质的量(1分) 热水中能溶解更多的硝酸钾(或氯化钾)(1分)
(3)①甲(1分) ②甲>乙(1分)
9. (6分)①氯化铵(或NH Cl)(1分) ②37.0(1分)
4
③a(1分) b(1分) ④Ⅰ.不饱和(1分) Ⅱ.a、c(1分)
10. (6分)(1)①10 g(1分) ②28.6%(1分) ③丙(1分)
④乙、甲、丙(1分)
(2)①B(1分) ②偏小(1分)
阶段测评集训二 水与常见的溶液
1. C 2. C 3. B 4. D
5. (8分)(1)肥皂水(1分) 煮沸(1分)
(2)活性炭(1分) +6(1分) (3)A(1分)
(4)氢氧化钙[或Ca(OH) ](1分) 蒸发结晶(1分)
2
(5)>(1分)
6. (4分)(1)减少(1分) (2)增加溶质(或恒温蒸发溶剂)(1分) (3)降温结晶(或冷却热饱
和溶液)(1分)
(4)<(1分)
7. (5分)(1)硝酸钾(1分) A(1分)
(2)饱和(1分) 33.3%(1分)
(3)加溶质氯化钠(或恒温蒸发溶剂)(1分)
8. (4分)(1)47.5 mL(1分) (2)CBDEA(1分)
(3)①②③(2分)
9. (8分)(1)蒸馏(1分)
(2)AC(只选一个不给分)(2分) (3)④③⑤①②(1分)
(4)①t ℃时,a与c的溶解度都是 20 g(或在 t ℃时,a与c的溶解度相等)(1分)
1 1
②75(1分) ③b>a>c(或c