文档内容
专题十四 基本反应类型 化学方程式及其计算
命题点分类集训
命题点1 基本反应类型
1. (2016北京)海水提镁的反应之一:MgCl +Ca(OH) === CaCl +Mg(OH) ↓,该反应
2 2 2 2
属于( )
A. 化合反应 B. 复分解反应 C. 置换反应 D. 分解反应
2.(2016钦州)某反应的微观示意图如图所示,该反应属于( )
[来源:学科网]
第2题图
A. 分解反应
B. 化合反应
C. 置换反应
D. 复分解反应
3. (2016自贡)在下列类型的化学反应中,各元素的化合价一定不会发生变化的是(
)
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
4. (2016毕节)下面是张丽同学写的四个化学反应方程式及注明的反应类型,其中对应
不正确的是( )
A. C+O===== CO 化合反应
2 2
B. 2HO===== 2HO+O↑ 分解反应
2 2 2 2
C. KCl+AgNO=== AgCl↓+KNO 复分解反应
3 3
D. 3CO+Fe O===== 2Fe+3CO 置换反应
2 3 2
命题点2 化学方程式的意义、书写及判断
5. (2016白银改编)化学方程式是重要的化学语言。下列化学方程式书写正确的是(
)
A. 2KClO===== 2KCl+3O↑
3 2
B. Cu+2HCl=== CuCl +H↑
2 2
C. NaOH+KCl=== NaCl+KOH
D. 3HSO +Fe O=== Fe (SO )+3HO
2 4 2 3 2 4 3 2
6. (2016北京)下列关于S+O===== SO 的说法不正确的是( )
2 2
A. 表示硫与氧气在点燃条件下反应生成二氧化硫
B. 参加反应的硫与氧气的质量比为2∶1
C. 反应前后硫原子、氧原子的个数均不变
D. 参加反应的氧气与生成的二氧化硫的分子个数比为1∶1
7. (2016河南)下列化学方程式中符合题意且书写正确的是( )
A. 正常雨水偏弱酸性原因:SO +HO=== HSO
2 2 2 4
B. 生活中用天然气作燃料:C HOH+3O===== 2CO+3HO
2 5 2 2 2
C. 用小苏打治疗胃酸过多症:NaHCO +HCl=== NaCl+CO↑+HO
3 2 2
D. 工业上用熟石灰制取烧碱:Ca(OH) +2NaNO === Ca(NO )+2NaOH
2 3 3 28. (2016淄博)请对下表中的化学方程式进行评价(填写评价序号),并注明化学反应类
型。
化学方程式 评价 化学反应类型
MgCl===== Mg+Cl↑
2 2
Al+O===== Al O
2 2 3
HCl+NaOH=== NaCl+HO
2
2Fe+6HCl=== 2FeCl +3H↑
3 2
评价序号:①完全正确 ②反应条件不正确 ③没有配平 ④违背客观事实
9. (2016荆州)用适当的化学方程式说明或解释下列问题:
(1)铜的金属活动性比铁弱:________________________。
(2)工业上煅烧石灰石制生石灰:________________________。
(3)用石灰浆粉刷墙面,干燥后变得坚硬:__________________________________。
(4)服用含Al(OH) 的药丸治疗胃酸过多症:__________________________________。
3
10. (2016天门)现有过氧化氢溶液、碳、碳酸钠溶液、二氧化锰、铁、硫酸铜溶液、
氢氧化钙溶液、氧气等八种物质,请按要求选择适当的物质书写化学方程式(每种物质不能
复重使用)。
(1)有氧气生成的反应________________________________。
(2)由两种单质参加的反应____________________________。
(3)生成红色固体的反应______________________________。
(4)生成白色沉淀的反应______________________________。
11. (2016柳州)过氧化氢俗称双氧水,在实验室中可用来制取氧气,其反应的化学方
程式为:______________________________________________。过氧化钠是一种淡黄色固
体,由单质钠与氧气在加热条件下反应得到,它的组成与过氧化氢类似。在潜水艇中它被
用作供氧剂。当它与人体呼出的二氧化碳气体反应后,生成氧气和一种盐,这个反应的化
学方程式为__________________________________________。
命题点3 结合化学方程式的计算
12. (2016南京)在催化剂的作用下,用O 将HCl转化为Cl,可提高效益,减少污染。
2 2
第12题图
(1)写出反应Ⅰ的化学方程式________________________。
(2)反应Ⅱ所属基本反应类型为________________。
(3)钠在氯气中燃烧生成氯化钠。若 4.6 g钠完全转化为氯化钠,至少需要氯气的质量
是多少?
13. (2016安徽)早在西汉时期的《淮南万毕术》中就记载“曾青得铁则化为铜”,成为现代湿法冶金的先驱。现有含1.6 kg硫酸铜的工业废液,加入铁粉回收铜,请计算:
(1)硫酸铜中铜元素的质量分数。
(2)理论上与硫酸铜反应消耗铁粉的质量。
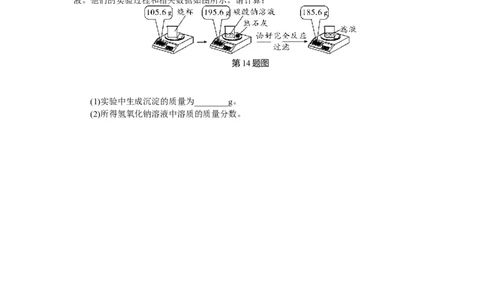
14. (2016河北)某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶
液。他们的实验过程和相关数据如图所示。请计算:
第14题图
(1)实验中生成沉淀的质量为________g。
(2)所得氢氧化钠溶液中溶质的质量分数。全国中考高频化学方程式集训(“四线三格”式))
一、实验室制取气体
1. 用氯酸钾和二氧化锰制氧气
2. 用高锰酸钾制氧气
3. 用过氧化氢制氧气
4. 碳酸钙(或石灰石、大理石)和稀盐酸反应制二氧化碳
二、物质在氧气中燃烧
1. 镁在氧气中燃烧(发出耀眼的白光,放出热量,有白色固体生成)
2. 铁在氧气中燃烧(剧烈燃烧,火星四射,放出热量,生成黑色固体)
3. 氢气在空气中燃烧(发出淡蓝色火焰,放出热量,干冷的烧杯内壁出现水雾)
4. 红(白)磷在空气中燃烧(放出热量,产生大量白烟)
5. 硫粉燃烧(在空气中发出微弱的淡蓝色火焰,在氧气中发出明亮的蓝紫色火焰,均
放出热量,生成有刺激性气味的气体)
6. 碳在氧气中充分燃烧(发出白光,放出热量,产生能使澄清石灰水变浑浊的气体)
7. 碳在氧气中不充分燃烧
8. 一氧化碳在氧气中燃烧(发出蓝色火焰,放出热量,产生能使澄清石灰水变浑浊的
气体)
9. 甲烷(天然气的主要成分)在空气中燃烧三、有CO 参与的反应
2
1. 二氧化碳通过灼热的炭层
2. 二氧化碳和水反应
3. 二氧化碳通入澄清石灰水(实验室检验CO 的常用方法)(澄清石灰水变浑浊)
2
4. 二氧化碳和氢氧化钠反应(除去二氧化碳常用的方法)
四、金属与酸、盐的反应
1. 锌和稀硫酸反应
2. 镁和稀硫酸反应
3. 铁和稀硫酸反应(产生气泡,溶液由无色变为浅绿色)
4. 镁和稀盐酸反应
5. 铝和稀盐酸反应
6. 铁和稀盐酸反应(产生气泡,溶液由无色变为浅绿色)
7. 铁和硫酸铜反应(有红色固体析出,溶液由蓝色变为浅绿色)
8. 铜片放入硝酸银溶液中(有银白色固体析出,溶液由无色变成蓝色)
五、金属氧化物与酸的反应
1. 氧化铁(铁锈的主要成分)和稀硫酸反应(溶液由无色变黄色)2. 氧化铁和稀盐酸反应(溶液由无色变黄色)
3. 氧化铜和稀盐酸反应(溶液由无色变蓝色)
4. 氧化铜和稀硫酸反应(溶液由无色变蓝色)
六、金属的冶炼
1. 焦炭还原氧化铁(红色粉末变黑色)
2. 木炭还原氧化铜(黑色粉末变成红色)
3. 氢气还原氧化铜(黑色粉末变成红色)
4. 氢气还原氧化铁(红色粉末变黑色)
5. 一氧化碳还原氧化铜(黑色粉末变成红色)
6. 一氧化碳还原氧化铁(红色粉末变黑色)
七、酸、碱、盐之间的反应
1. 氢氧化钠和稀硫酸反应
2. 氢氧化钠和稀盐酸反应
3. 氢氧化钙和稀盐酸反应
4. 氢氧化铝和稀盐酸反应(氢氧化铝治疗胃酸过多症)
5. 氢氧化钡和稀硫酸反应(有白色沉淀生成)1. 稀盐酸和碳酸钠(纯碱或苏打)反应(有气泡产生)
2. 稀盐酸和硝酸银反应(有白色沉淀产生)
3. 稀硫酸和氯化钡反应(有白色沉淀产生)
1. 氢氧化钙和碳酸钠反应(有白色沉淀产生)
2. 氢氧化钠和硫酸铜反应(有蓝色沉淀生成,溶液由蓝色变无色)
3. 氢氧化钠和氯化镁反应(有白色沉淀产生)
4. 氢氧化钠和氯化铁反应(有红褐色沉淀生成,溶液由黄色变无色)
5. 氢氧化钡和硫酸铜反应
1. 碳酸钠和氯化钡反应(有白色沉淀产生)
2. 碳酸钠和氯化钙反应(有白色沉淀产生)
3. 氯化钠和硝酸银反应(有白色沉淀产生)
4. 硫酸钠和氯化钡反应(有白色沉淀产生)
5. 硝酸钡和硫酸钠反应(有白色沉淀产生)八、其他反应
1. 生石灰溶于水(放热反应)
2. 水在直流电的作用下分解
3. 高温煅烧石灰石(二氧化碳的工业制法)
4. 碳酸分解
,
阶段测评集训六 物质的化学变化
(时间:40分钟 满分:45分)
一、选择题(本题包括7小题,每小题2分,共14分)
1. (2016安顺)双氧水分解生成水和氧气的反应前后,发生改变的是( )
A. 元素种类 B. 原子种类 C. 分子种类 D. 原子数目
2. (2016广州)下列事实中,属于物质化学性质的是( )
A. 普通玻璃属于易碎品
B. 二氧化碳能使澄清石灰水变浑浊
C. 金刚石硬度大
D. 盛有水和植物油的试管振荡得到乳状浑浊液体
3. (2016广安)下列关于物质的性质或变化叙述正确的是( )
A. 活性炭净水——化学性质
B. 盐酸遇石蕊试液变红——物理性质
C. 冰川融化——物理变化
D. 工业上分离液态空气制取氧气、氮气——化学变化
4. (2016天水)在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学
反应,反应前后各物质的质量变化如图。下列说法中正确的是( )
[来源:Z*xx*k.Com]
第4题图A. 该反应为化合反应
B. 丙一定为该反应的催化剂
C. 此反应中乙物质和丁物质的质量比为3∶2
D. 丁的相对分子质量是甲的2倍
5. (2016来宾)根据微观粒子反应示意图,下列说法正确的是( )
第5题图
A. 反应①的化学方程式:C+O===== CO
2
B. 反应②的化学方程式:CO+O ===== CO
2 2
C. 反应②为复分解反应
D. 反应①为化合反应
6. (2016武汉)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O 2=====
CO+2HO。下列关于X的说法正确的是( )
2 2
A. X由碳、氢、氧三种元素组成 B. X的相对分子质量为10
C. X中碳、氢元素的质量比为1∶4 D. X属于有机化合物
7. (2016黄冈)已知M、N在一定条件下,能发生反应:M+2N=== P+2Q,则下列说
法中不正确的是( )
A. 若M、N、P、Q都是由分子构成的物质,则该反应前后分子的数目一定不变
B. M、N、P、Q可能含有同一种元素
C. 若P、Q都是化合物,则该反应一定是复分解反应
D. 若16 g M和64 g N能恰好完全反应,则M、N的相对分子质量之比为1∶2
二、填空及简答题(本题包括3小题,共18分)
8. (2016大连)(9分)写出下列反应的化学方程式,并注明反应的基本类型。
(1)加热高锰酸钾制氧气:____________________、______________________。
(2)常温下铝与氧气反应:________________________、________________。
(3) 碳 酸 钠 溶 液 与 氢 氧 化 钙 溶 液 反 应 : ______________________________ 、
________________。
9. (2016重庆A)(4分)我国煤炭工业“十三五”科技发展指导意见中指出,煤炭工业应
重点关注煤炭安全绿色开采、智能矿山建设、煤炭清洁利用和高效转化。
(1)煤是一种________(填“可再生”或“不可再生”)能源。
(2)煤的气化是使煤变成清洁能源的有效途径,煤气化的主要反应有:① 2C+O===
2
2CO ② C+HO=== CO+H ③ CO+HO=== H+CO
2 2 2 2 2
反应①的基本反应类型是________反应。
反应②和反应③的相同点是________(填序号)。
A. 都是置换反应 B. 水都发生了还原反应
C. 生成物都是可燃性气体 D. 反应后碳元素的化合价都升高
10. (2016湘潭)(5分)根据原子结构示意图和微观示意图填空。
(1)如图1,A、B是两种微粒的结构示意图,回答下列问题:
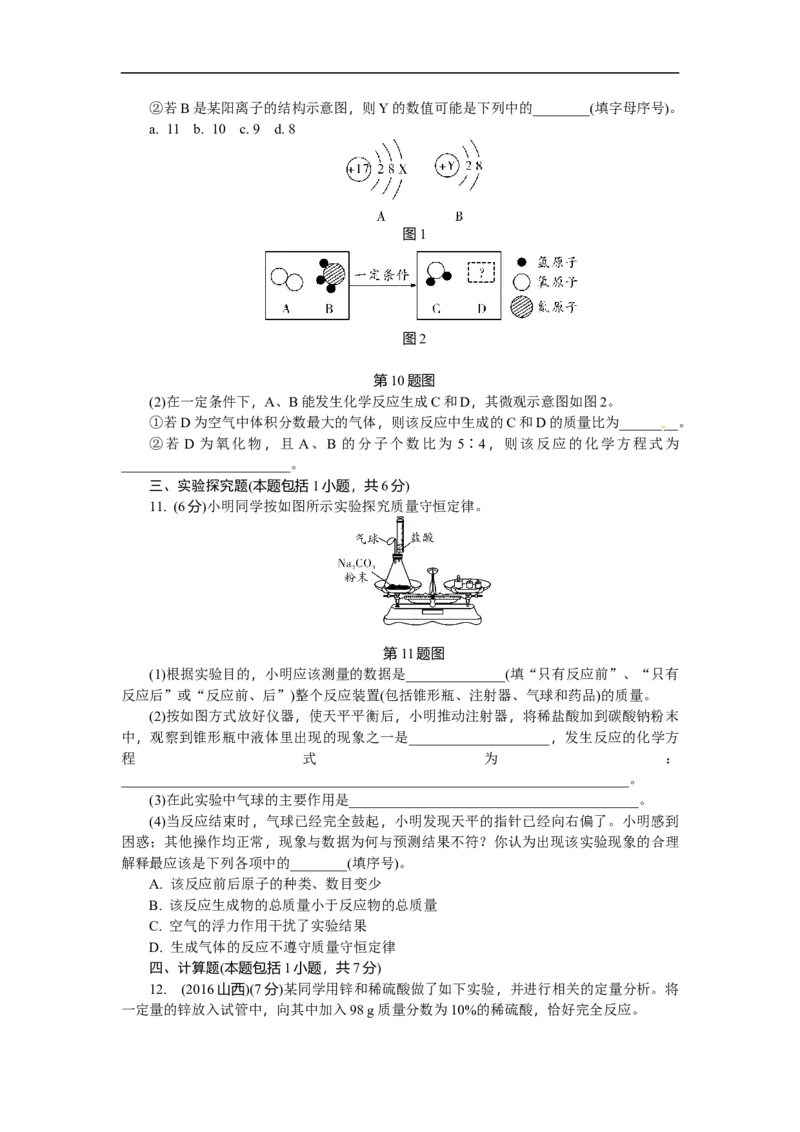
①若A表示某元素的原子,则X=________。②若B是某阳离子的结构示意图,则Y的数值可能是下列中的________(填字母序号)。
a. 11 b. 10 c. 9 d. 8
图1
图2
第10题图
[来源:Zxxk.Com]
(2)在一定条件下,A、B能发生化学反应生成C和D,其微观示意图如图2。
①若D为空气中体积分数最大的气体,则该反应中生成的C和D的质量比为________。
②若 D 为氧化物,且 A、B 的分子个数比为 5∶4,则该反应的化学方程式为
________________________。
三、实验探究题(本题包括1小题,共6分)
11. (6分)小明同学按如图所示实验探究质量守恒定律。
第11题图
(1)根据实验目的,小明应该测量的数据是______________(填“只有反应前”、“只有
反应后”或“反应前、后”)整个反应装置(包括锥形瓶、注射器、气球和药品)的质量。
(2)按如图方式放好仪器,使天平平衡后,小明推动注射器,将稀盐酸加到碳酸钠粉末
中,观察到锥形瓶中液体里出现的现象之一是____________________,发生反应的化学方
程 式 为 :
________________________________________________________________________。
(3)在此实验中气球的主要作用是_________________________________________。
(4)当反应结束时,气球已经完全鼓起,小明发现天平的指针已经向右偏了。小明感到
困惑;其他操作均正常,现象与数据为何与预测结果不符?你认为出现该实验现象的合理
解释最应该是下列各项中的________(填序号)。
A. 该反应前后原子的种类、数目变少
B. 该反应生成物的总质量小于反应物的总质量
C. 空气的浮力作用干扰了实验结果
D. 生成气体的反应不遵守质量守恒定律
四、计算题(本题包括1小题,共7分)
12. (2016山西)(7分)某同学用锌和稀硫酸做了如下实验,并进行相关的定量分析。将
一定量的锌放入试管中,向其中加入98 g质量分数为10%的稀硫酸,恰好完全反应。(1)请计算生成氢气的质量(写出计算过程)。
(2)通过已知数据还能求出的量有________(填字母,符合题意的选项都选)。
a. 参加反应锌的质量 b. 生成硫酸锌的质量
c. 稀硫酸中水的质量 d. 反应后溶液中溶质质量分数
专题十四 基本反应类型 化
学方程式及其计算
命题点分类集训
命题点1 基本反应类型
1. B 2. C 3. D 4. D
命题点2 化学方程式的意义、书写及判断
5. D 6. B 7. C
8.
化学方程式 评价 化学反应类型
MgCl ===== Mg+Cl↑ ② 分解反应
2 2
Al+O===== Al O ③ 化合反应
2 2 3
HCl+NaOH=== NaCl+HO ① 复分解反应
2 [来源:Zxxk.Com]
2Fe+6HCl=== 2FeCl +3H↑ ④ 置换反应
3 2
9. (1)Fe+CuSO === FeSO +Cu
4 4
(2)CaCO===== CaO+CO↑
3 2
(3)Ca(OH) +CO=== CaCO ↓+HO
2 2 3 2
(4)Al(OH) +3HCl=== AlCl +3HO
3 3 2
10. (1)2H O===== 2HO+O↑
2 2 2 2
(2)C+ O===== CO
2 2
(3)Fe +CuSO === FeSO +Cu
4 4
(4)Ca(OH) +NaCO === CaCO ↓+2NaOH
2 2 3 3
11. 2HO===== 2HO+O↑
2 2 2 2
2NaO+2CO=== 2NaCO+O
2 2 2 2 3 2
命题点3 结合化学方程式的计算
12.(1)2HCl+CuO===== CuCl +HO
2 2
(2)置换反应
(3)解:设至少需要氯气的质量为x
2Na + Cl===== 2NaCl
2
46 71
4.6 g x
=
x=7.1 g
答:至少需要氯气的质量为7.1 g。13. 解:(1)CuSO 中铜元素的质量分数为×100%=40%。
4
(2)设理论上与硫酸铜反应消耗铁粉的质量为x
Fe+CuSO === FeSO +Cu
4 4
56 160
x 1.6 kg
=
x=0.56 kg
答:(1)硫酸铜中铜元素的质量分数为40%。(2)理论上与硫酸铜反应消耗铁粉的质量为
0.56 kg。
14. (1)10
(2)解:设反应生成氢氧化钠的质量为x
Ca(OH) +NaCO=== CaCO ↓+2NaOH
2 2 3 3
100
80
10 g
x
=
x=8 g
所得溶液中溶质的质量分数为×100%=10%
答:所得氢氧化钠溶液中溶质质量分数为10%。
全国中考高频化学方程式
集训(“四线三格”式)
一、实验室制取气体
1.
2.
3.
4.
二、物质在氧气中燃烧
1.
2.
3.
4.
5.6.
7.
8.
9.
三、有CO 参与的反应
2
1.
2.
3.
4.
四、金属与酸、盐的反应
1.
2.
3.
4.
[来源:Zxxk.Com]
5.
6.
7.
8.
五、金属氧化物与酸的反应
1.
2.
3.
4.
六、金属的冶炼1.
2.
3.
4.
5.
6.
七、酸、碱、盐之间的反应
1.
2.
3.
4.
5.
1.
2.
3.
1.
2.
3.
4.
5.
1.2.
3.
4.
5.
八、其他反应
1.
2.
3.
4.
阶段测评集训六 物质的化学变化
1. C 2. B 3. C 4. C 5. D 6. D 7. C
8. (9分)(1)2KMnO===== KMnO +MnO +O↑(2分)
4 2 4 2 2
分解反应(1分)
(2)4Al+3O=== 2Al O(2分) 化合反应(1分)
2 2 3
(3)Ca(OH) +Na CO=== CaCO ↓+2NaOH(2分)
2 2 3 3
复分解反应(1分)
9. (3分)(1)不可再生(1分)
(2)化合(1分) BD(1分)
10. (5分)(1)①7(1分) ②a(1分)
(2)①14∶27(1分)
②5O+4NH ===== 6HO+4NO(2分)
2 3 2
11. (6分)(1)反应前、后(1分)
(2)有气泡产生(1分)
NaCO+2HCl=== 2NaCl+HO+CO↑(2分)
2 3 2 2
(3)调节密闭空间的压强、起密封作用(1分)
(4)C(1分)
12. (7分)(1)解:参与反应的HSO 质量为98 g×10%=9.8 g(1分)
2 4
设生成氢气的质量为x
Zn+HSO === ZnSO+H↑(1分)
2 4 4 2
98 2
9.8 g x
=(1分) x=0.2 g(1分)
答:生成氢气的质量为0.2 g。(1分)
(2)abcd(2分)