文档内容
第四章 章末测试(基础)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
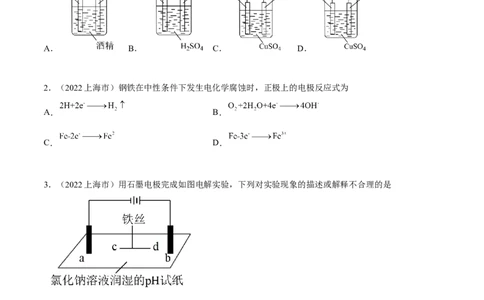
1.(2022上海市)下列装置能够组成原电池的是
A. B. C. D.
2.(2022上海市)钢铁在中性条件下发生电化学腐蚀时,正极上的电极反应式为
A. B.
C. D.
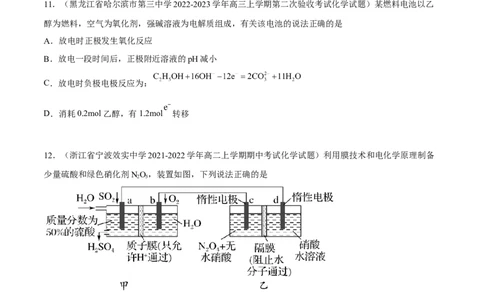
3.(2022上海市)用石墨电极完成如图电解实验,下列对实验现象的描述或解释不合理的是
A.a处试纸变蓝
B.b处变红
C.c处:Fe-2e-=Fe2+
D.d处:2HO+2e-=H ↑+2OH-
2 2
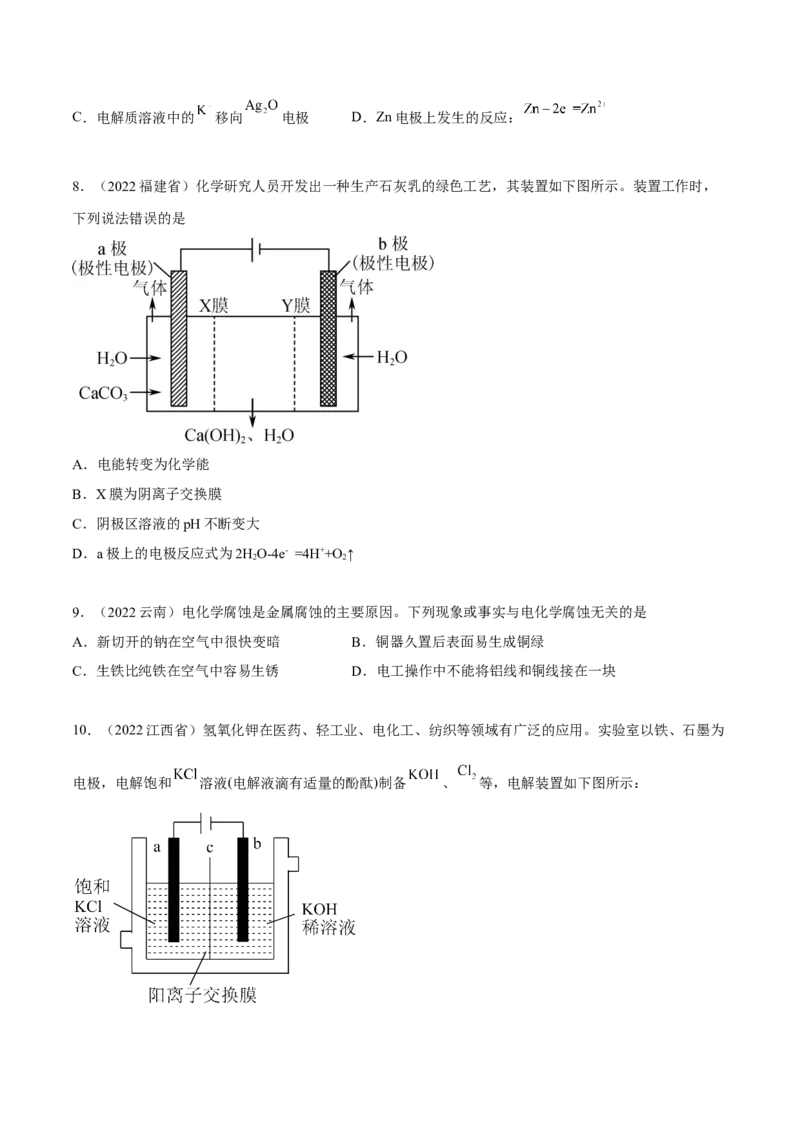
4.(2022浙江省)铅蓄电池是汽车常用的蓄电池Pb+PbO+2H SO =2PbSO+2H O,其构造如图所示。下
2 2 4 4 2
列说法不正确的是A.电池充电时,Pb接电源的负极
B.电池充电时,c(H+)增大
C.电池放电时,负极质量减轻
D.电池放电时,电子从铅电极经导线流向二氧化铅电极
5.(上海市洋泾中学2022-2023学年高一上学期期中考试化学试题)氯碱工业的基本原理就是电解饱和食
盐水。下列关于实验室电解饱和食盐水的说法中错误的是
A.可以选用石墨棒作为阴、阳极材料
B.用湿润的淀粉KI试纸靠近阳极区域,试纸变蓝
C.阴极产生气体具有可燃性
D.实验结束后,将溶液搅拌,然后用pH试纸检验,溶液呈中性
6.(2022广东)电解饱和食盐水时,阳极生成的气体是
A.H B.Cl C.HCl D.O
2 2 2
7.(福建省宁德市2022-2023学年高二上学期期中质量检测化学试题)银锌电池是一种常见化学电源,其
反应原理: ,其工作示意图如下。下列说法不正确的是
A.Zn电极是电源的负极 B.电池工作一段时间后, 电极质量减轻C.电解质溶液中的 移向 电极 D.Zn电极上发生的反应:
8.(2022福建省)化学研究人员开发出一种生产石灰乳的绿色工艺,其装置如下图所示。装置工作时,
下列说法错误的是
A.电能转变为化学能
B.X膜为阴离子交换膜
C.阴极区溶液的pH不断变大
D.a极上的电极反应式为2HO-4e- =4H++O ↑
2 2
9.(2022云南)电化学腐蚀是金属腐蚀的主要原因。下列现象或事实与电化学腐蚀无关的是
A.新切开的钠在空气中很快变暗 B.铜器久置后表面易生成铜绿
C.生铁比纯铁在空气中容易生锈 D.电工操作中不能将铝线和铜线接在一块
10.(2022江西省)氢氧化钾在医药、轻工业、电化工、纺织等领域有广泛的应用。实验室以铁、石墨为
电极,电解饱和 溶液(电解液滴有适量的酚酞)制备 、 等,电解装置如下图所示:下列说法正确的是
A.a电极材料是铁
B.阴极区电极反应:
C.当电路中有 电子转移时,就有 通过膜进入正极区
D.一段时间后整个电解池均变成红色
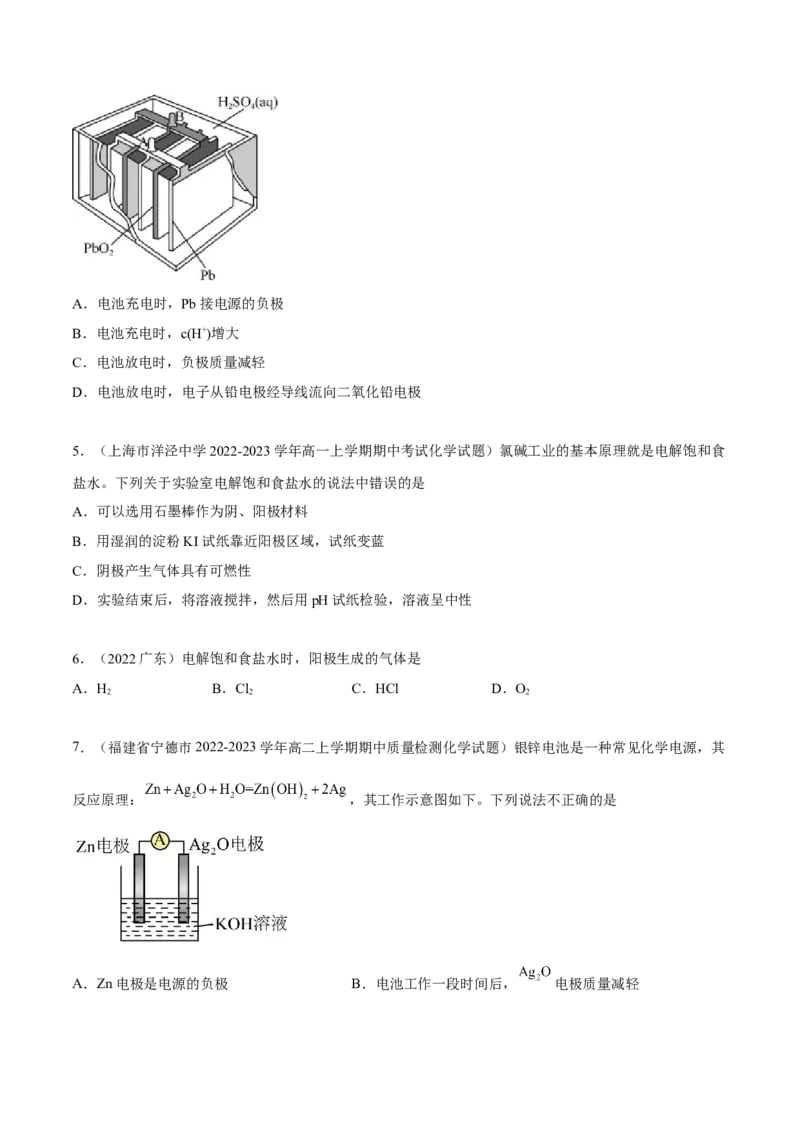
11.(黑龙江省哈尔滨市第三中学2022-2023学年高三上学期第二次验收考试化学试题)某燃料电池以乙
醇为㜣料,空气为氧化剂,强碱溶液为电解质组成,有关该电池的说法正确的是
A.放电时正极发生氧化反应
B.放电一段时间后,正极附近溶液的pH减小
C.放电时负极电极反应为:
D.消耗0.2mol乙醇,有1.2mol 转移
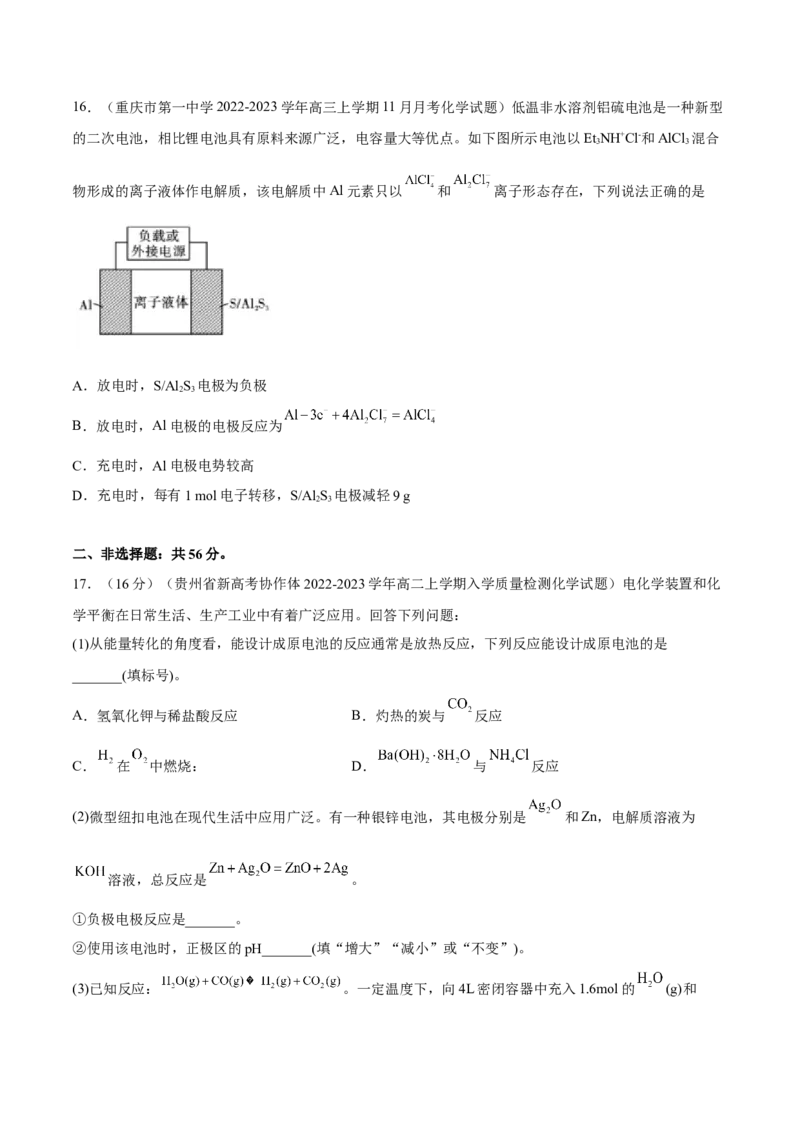
12.(浙江省宁波效实中学2021-2022学年高二上学期期中考试化学试题)利用膜技术和电化学原理制备
少量硫酸和绿色硝化剂NO,装置如图,下列说法正确的是
2 5
A.甲装置将电能转化为化学能
B.每转移2mol电子,生成2mol NO 和1mol HSO
2 5 2 4
C.乙中电极d上发生氧化反应
D.c电极反应式为: NO – 2e- + H O = NO + 2H+
2 4 2 2 5
13.(山东省青岛第五十八中学2022-2023学年高二上学期期中考试化学试题)下列叙述中,正确的个数
为①电解池是将化学能转变为电能的装置;
②金属导电和电解质溶液导电均为物理变化;
③通过电解原理只能实现不能自发进行的氧化还原反应;
④电镀过程相当于金属的“迁移”,可视为物理变化;
⑤纯银质物品久置表面变暗,是由于发生了电化学腐蚀;
⑥为了防止钢铁锈蚀,在排放海水的钢铁阀门上用导线连接一块石墨一同浸入海水中;
⑦一般来说,带有盐桥的原电池比不带盐桥的原电池效率高。
A.1个 B.2个 C.3个 D.4个
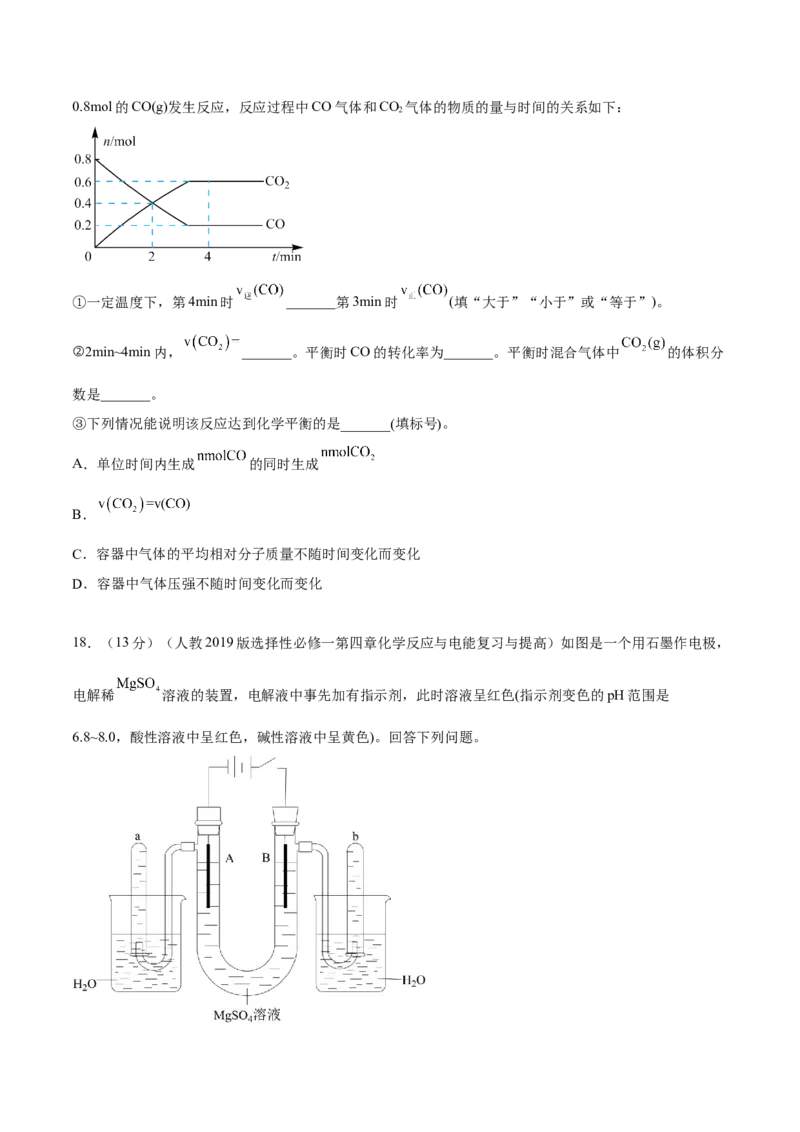
14.(山东省济南市章丘区第四中学2022-2023学年高二上学期期中考试化学试题)电化学降解 的原
理如图所示,下列说法正确的是
A.N为电源的正极
B.电池工作时, 通过质子交换膜从左侧移向右侧
C.Pt电极上的反应式为
D.每生成 ,左右两侧溶液质量变化差为18g
15.(山东省济南市章丘区第四中学2022-2023学年高二上学期期中考试化学试题)下列说法正确的是
A.放电时,铅酸蓄电池的负极质量减轻
B.工业上常采用电解NaCl的水溶液的方法来制取金属单质钠
C.粗铜精炼时,粗铜应与电源的负极相连
D.马口铁(表面镀锡薄钢板)的表面破损时,马口铁会较纯铁腐蚀更严重16.(重庆市第一中学2022-2023学年高三上学期11月月考化学试题)低温非水溶剂铝硫电池是一种新型
的二次电池,相比锂电池具有原料来源广泛,电容量大等优点。如下图所示电池以EtNH+Cl-和AlCl 混合
3 3
物形成的离子液体作电解质,该电解质中Al元素只以 和 离子形态存在,下列说法正确的是
A.放电时,S/Al S 电极为负极
2 3
B.放电时,Al电极的电极反应为
C.充电时,Al电极电势较高
D.充电时,每有1 mol电子转移,S/Al S 电极减轻9 g
2 3
二、非选择题:共56分。
17.(16分)(贵州省新高考协作体2022-2023学年高二上学期入学质量检测化学试题)电化学装置和化
学平衡在日常生活、生产工业中有着广泛应用。回答下列问题:
(1)从能量转化的角度看,能设计成原电池的反应通常是放热反应,下列反应能设计成原电池的是
_______(填标号)。
A.氢氧化钾与稀盐酸反应 B.灼热的炭与 反应
C. 在 中燃烧: D. 与 反应
(2)微型纽扣电池在现代生活中应用广泛。有一种银锌电池,其电极分别是 和Zn,电解质溶液为
溶液,总反应是 。
①负极电极反应是_______。
②使用该电池时,正极区的pH_______(填“增大”“减小”或“不变”)。
(3)已知反应: 。一定温度下,向4L密闭容器中充入1.6mol的 (g)和0.8mol的CO(g)发生反应,反应过程中CO气体和CO 气体的物质的量与时间的关系如下:
2
①一定温度下,第4min时 _______第3min时 (填“大于”“小于”或“等于”)。
②2min~4min内, _______。平衡时CO的转化率为_______。平衡时混合气体中 的体积分
数是_______。
③下列情况能说明该反应达到化学平衡的是_______(填标号)。
A.单位时间内生成 的同时生成
B.
C.容器中气体的平均相对分子质量不随时间变化而变化
D.容器中气体压强不随时间变化而变化
18.(13分)(人教2019版选择性必修一第四章化学反应与电能复习与提高)如图是一个用石墨作电极,
电解稀 溶液的装置,电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是
6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。回答下列问题。(1)在电解过程中,有关电极附近溶液颜色变化的叙述中正确的是___________(填序号)。
①A管溶液由红色变为黄色;
②B管溶液由红色变为黄色;
③A管溶液不变色;
④B管溶液不变色。
(2)写出A管中发生的电极反应:___________。
(3)写出B管中发生的电极反应:___________。
(4)检验a管中气体的方法是___________。
(5)检验b管中气体的方法是___________。
19.(15分)(人教版(2019)高二化学选择性必修1第四章化学反应与电能过模拟2年模拟精编精练)
化学电源在日常生活和工业生产中有着重要的应用。
Ⅰ.如图1所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳
离子交换膜。请按要求回答相关问题:
(1)甲烷燃料电池负极的电极反应式为________________________________。
(2)C极的电极反应式为________________________________________。
(3)若有2.24 L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为________L(标准状况
下);丙装置中阴极析出铜的质量为________g。
Ⅱ.“长征”火箭发射使用的燃料是液态偏二甲肼(C HN),并使用四氧化二氮作为氧化剂,这种组合的优点
2 8 2
是能在短时间内产生巨大能量将火箭送2上太空,且产物不污染空气(产物都是空气的成分)。某校外研
究性学习小组拟将此原理设计为原电池,如图2所示,结合学习过的电化学原理分析其设计方案,回答相
关问题:(4)从a口加入________(填名称)。 的移动方向是________(填“由A到B”或“由B到A”)。
(5)A极发生的电极反应为__________________________________________________________。
(6)若以该电池为电源,用石墨作电极电解200 mL0.5 mol/L的CuSO 溶液,电解一段时间后,两极收集到
4
相同体积(相同条件下)的气体,则整个电解过程转移电子________mol。
20.(12分)(吉林省通化县综合高级中学2020-2021学年高一下学期期末考试化学试题)原电池是将化
学能转化为电能的装置。
I.a为铜片,b为铁片,烧杯中是稀硫酸溶液,当开关K断开时产生的现象为___________;当开关K闭合
时,产生的现象为___________。
A.a不断溶解 B.b不断溶解 C.a上产生气泡 D.b上产生气泡 E.溶液逐渐变蓝
(2)闭合开关K,反应一段时间后断开开关K,经过一段时间后,下列叙述不正确的是___________。
A.溶液中 浓度减小 B.正极附近 浓度逐渐增大
C.溶液中含有 D.溶液中 浓度基本不变
Ⅱ.某同学为了探究锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法
收集反应放出的氢气(气体体积已折算为标准状况下的体积),实验记录如下(累计值):时间/min 1 2 3 4 5
氢气体积/
50 120 232 290 310
mL
(3)反应速率最大的时间段是___________(填“0~1min”“1~2min”“2~3min”“3~4min”或“4~5min”);反应速率
最小的时间段是___________(填“0~1min”“1~2min”“2~3min”“ 3~4min”或“4~5min”),
(4)如果反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在盐酸中分别加入等体积的下列
液体,你认为可行的是___________(填序号)。
A.蒸馏水 B.NaCl溶液 C. 溶液 D. 溶液倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育