文档内容
专题十三 质量守恒定律及其应用
命题点分类集训
命题点1 质量守恒定律的理解
1. (2016嘉兴)科研人员研发出一种能将二氧化碳转化为甲烷的新技术。该技术以纳米
镍粒子为催化剂,将二氧化碳和氢气混合加热发生发应,生成甲烷等物质,从而减少碳排
放。该反应前后发生变化的是( )
A. 元素的种类 B. 碳原子的数目
C. 氢元素的化合价 D. 纳米镍粒子的化学性质
2. (2015六盘水)关于质量守恒定律的理解,错误的是( )
A. 宏观:实际参加反应的反应物总质量等于生成物总质量
B. 微观:反应前后原子种类和个数不变
C. X+3HO=== 2HPO 中的X为PO
2 3 4 2 5
D. 煤燃烧后灰渣质量小于煤,不能用质量守恒定律解释
命题点2 质量守恒定律的应用
考向1 化学式或化学计量数的推断
3. (2016河北)“气体烙铁”是一种以气体X为燃料的加热仪器,加热温度可达1 300
℃,反应的化学方程式为2X+13O===== 8CO+10HO。燃料X的化学式为( )
2 2 2
A. C H B. C H C. CHOH D. C HOH
3 8 4 10 3 2 5
4. (2016铜仁)某物质在空气中燃烧的化学方程式为:C HOH+______O===== 2CO
2 5 2 2
+3HO,在“______”中填上的数字是( )
2
A. 1 B. 2 C. 3 D. 4
5. (2016襄阳)AgNO 固体见光或受热易分解,故保存在棕色瓶中。AgNO 见光分解时
3 3
会产生一种有刺激性气味的气体,该气体可能是( )
A. SO B. NH C. N D. NO
2 3 2 2
6. (2016河南)偏二甲肼(C HN)与NO 反应放出的能量能把火箭送入太空,该化学方
2 8 2 2 4
程式为:C HN+2NO=== 2X↑+3N↑+4HO↑。下列说法正确的是( )
2 8 2 2 4 2 2
A. X的化学式为CO
B. 偏二甲肼中碳的质量分数为40%
C. 该反应属于分解反应
D. 生成N 和HO的质量比为14∶9
2 2
7. (2016绵阳)程浩同学查阅资料得知:Cu与稀硫酸不反应,但Cu可与浓硫酸在加热
的条件下反应,化学方程式为:Cu+2HSO (浓) ===== CuSO +SO ↑+2R,下列说法中
2 4 4 2
不正确的是( )
A. 该反应中涉及了3种类型的化合物
B. R为相对分子质量最小的氧化物
C. 反应前后,HSO 中硫的化合价全部发生了改变
2 4
D. 该反应不属于四种基本反应类型中的任何一种
考向2 物质元素组成的推断
8.(2016邵阳)某化学反应可表示为:二氧化碳+水―→M+氧气。根据以上信息,下
列关于M组成的说法中正确的是( )
A. 一定含有C、H元素,可能含有O元素
B. 只含有C、H元素
C. 含有C、H、O三种元素D. 无法确定
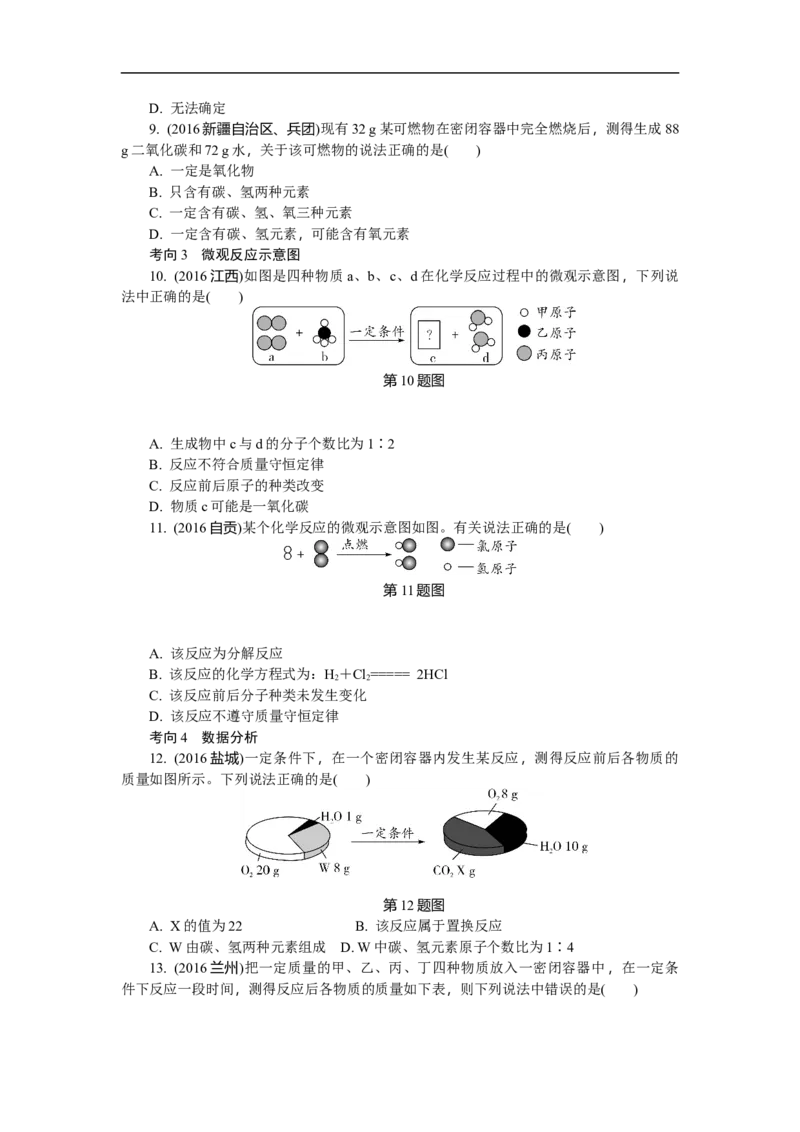
9. (2016新疆自治区、兵团)现有32 g某可燃物在密闭容器中完全燃烧后,测得生成88
g二氧化碳和72 g水,关于该可燃物的说法正确的是( )
A. 一定是氧化物
B. 只含有碳、氢两种元素
C. 一定含有碳、氢、氧三种元素
D. 一定含有碳、氢元素,可能含有氧元素
考向3 微观反应示意图
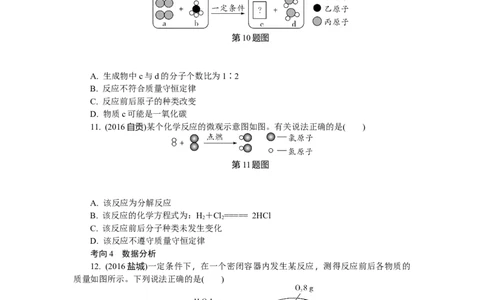
10. (2016江西)如图是四种物质a、b、c、d在化学反应过程中的微观示意图,下列说
法中正确的是( )
第10题图
A. 生成物中c与d的分子个数比为1∶2
B. 反应不符合质量守恒定律
C. 反应前后原子的种类改变
D. 物质c可能是一氧化碳
11. (2016自贡)某个化学反应的微观示意图如图。有关说法正确的是( )
[来源:学.科.网Z.X.X.K]
第11题图
A. 该反应为分解反应
B. 该反应的化学方程式为:H+Cl===== 2HCl
2 2
C. 该反应前后分子种类未发生变化
D. 该反应不遵守质量守恒定律
考向4 数据分析
12. (2016盐城)一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的
质量如图所示。下列说法正确的是( )
第12题图
A. X的值为22 B. 该反应属于置换反应
C. W由碳、氢两种元素组成 D. W中碳、氢元素原子个数比为1∶4
13. (2016兰州)把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条
件下反应一段时间,测得反应后各物质的质量如下表,则下列说法中错误的是( )物质 甲 乙 丙 丁
反应前的质量(g) 7.6 2.0 0.2 0
反应后的质量(g) 3.2 X 5.8 0.4
A. X=0.4
B. 丁一定是单质
[来源:Z#xx#k.Com]
C. 甲和乙是反应物
D. 反应中的甲、丙发生改变的质量比是11∶14
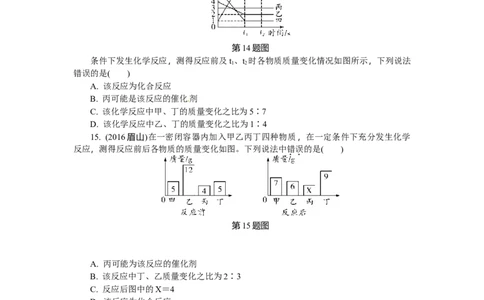
14. (2016湘潭)在一密闭容器中加入甲、乙、丙、丁四种物质,在一定
第14题图
条件下发生化学反应,测得反应前及t、t 时各物质质量变化情况如图所示,下列说法
1 2
错误的是( )
A. 该反应为化合反应
B. 丙可能是该反应的催化剂
C. 该化学反应中甲、丁的质量变化之比为5∶7
D. 该化学反应中乙、丁的质量变化之比为1∶4
15. (2016眉山)在一密闭容器内加入甲乙丙丁四种物质,在一定条件下充分发生化学
反应,测得反应前后各物质的质量变化如图。下列说法中错误的是( )
第15题图
A. 丙可能为该反应的催化剂
B. 该反应中丁、乙质量变化之比为2∶3
C. 反应后图中的X=4
D. 该反应为化合反应
命题点3 质量守恒定律的验证
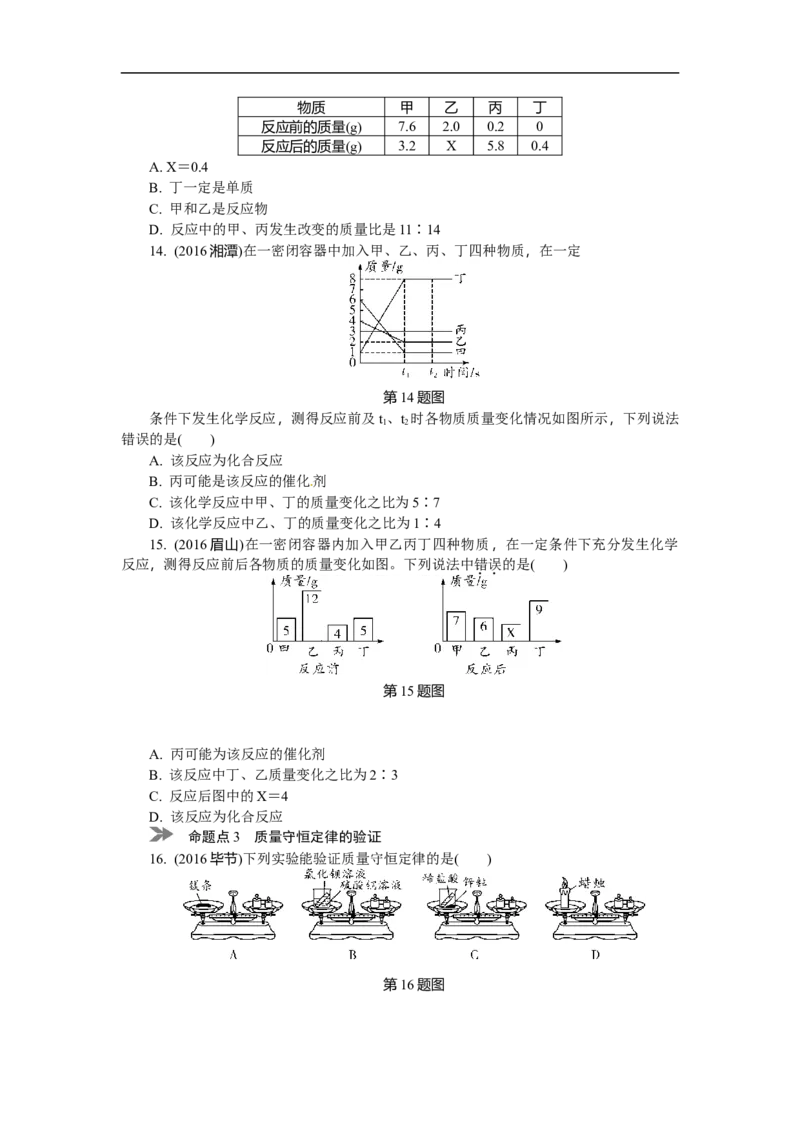
16. (2016毕节)下列实验能验证质量守恒定律的是( )
第16题图A. 镁条在空气中燃烧前后质量的测定
B. 氯化钡溶液与硫酸铜溶液反应前后质量的测定
C. 锌粒和稀盐酸反应前后质量的测定
D. 蜡烛燃烧前后质量的测定中考冲刺集训
[来源:学科网ZXXK]
(时间:40分钟 满分:40分)
一、选择题(本题包括8小题,每小题2分,共16分)
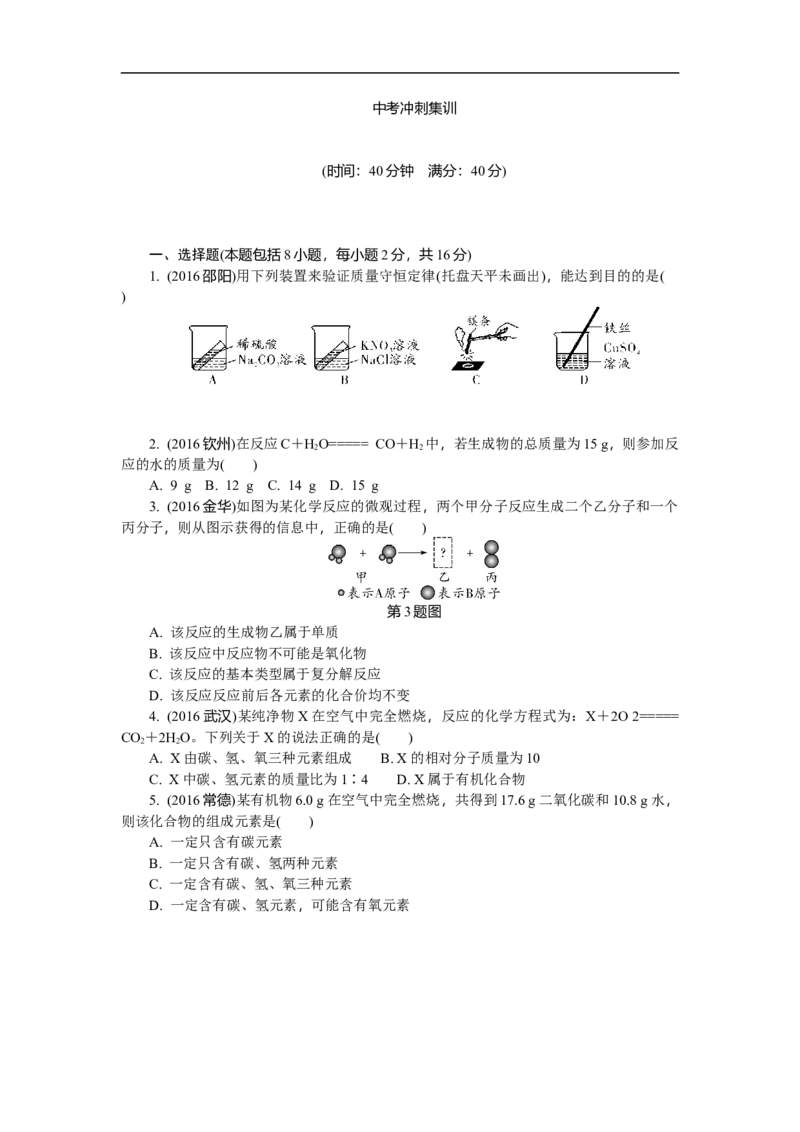
1. (2016邵阳)用下列装置来验证质量守恒定律(托盘天平未画出),能达到目的的是(
)
2. (2016钦州)在反应C+HO===== CO+H 中,若生成物的总质量为15 g,则参加反
2 2
应的水的质量为( )
A. 9 g B. 12 g C. 14 g D. 15 g
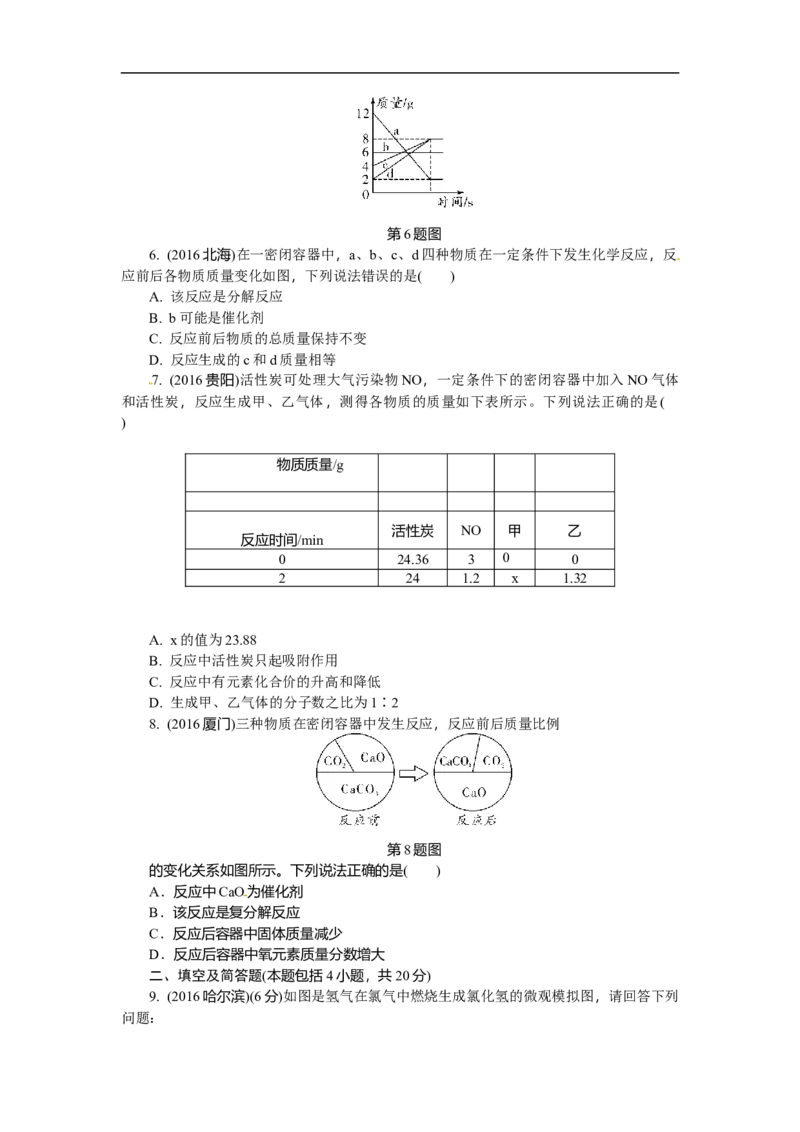
3. (2016金华)如图为某化学反应的微观过程,两个甲分子反应生成二个乙分子和一个
丙分子,则从图示获得的信息中,正确的是( )
第3题图
A. 该反应的生成物乙属于单质
B. 该反应中反应物不可能是氧化物
C. 该反应的基本类型属于复分解反应
D. 该反应反应前后各元素的化合价均不变
4. (2016武汉)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+2O 2=====
CO+2HO。下列关于X的说法正确的是( )
2 2
A. X由碳、氢、氧三种元素组成 B. X的相对分子质量为10
C. X中碳、氢元素的质量比为1∶4 D. X属于有机化合物
5. (2016常德)某有机物6.0 g在空气中完全燃烧,共得到17.6 g二氧化碳和10.8 g水,
则该化合物的组成元素是( )
A. 一定只含有碳元素
B. 一定只含有碳、氢两种元素
C. 一定含有碳、氢、氧三种元素
D. 一定含有碳、氢元素,可能含有氧元素第6题图
6. (2016北海)在一密闭容器中,a、b、c、d四种物质在一定条件下发生化学反应,反
应前后各物质质量变化如图,下列说法错误的是( )
A. 该反应是分解反应
B. b可能是催化剂
C. 反应前后物质的总质量保持不变
D. 反应生成的c和d质量相等
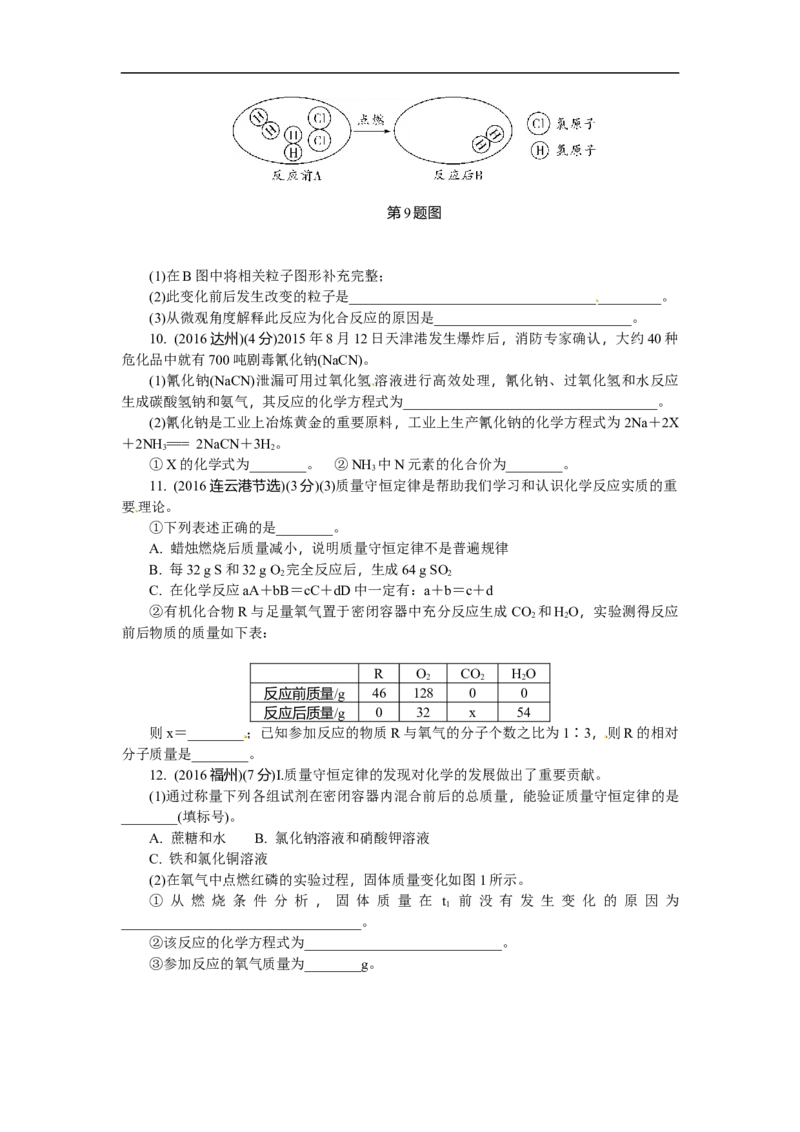
7. (2016贵阳)活性炭可处理大气污染物NO,一定条件下的密闭容器中加入NO气体
和活性炭,反应生成甲、乙气体,测得各物质的质量如下表所示。下列说法正确的是(
)
物质质量/g
活性炭 NO 甲 乙
反应时间/min
0 24.36 3 0 0
[来源:学。科。
网Z。X。X。K]
2 24 1.2 x 1.32
A. x的值为23.88
B. 反应中活性炭只起吸附作用
C. 反应中有元素化合价的升高和降低
D. 生成甲、乙气体的分子数之比为1∶2
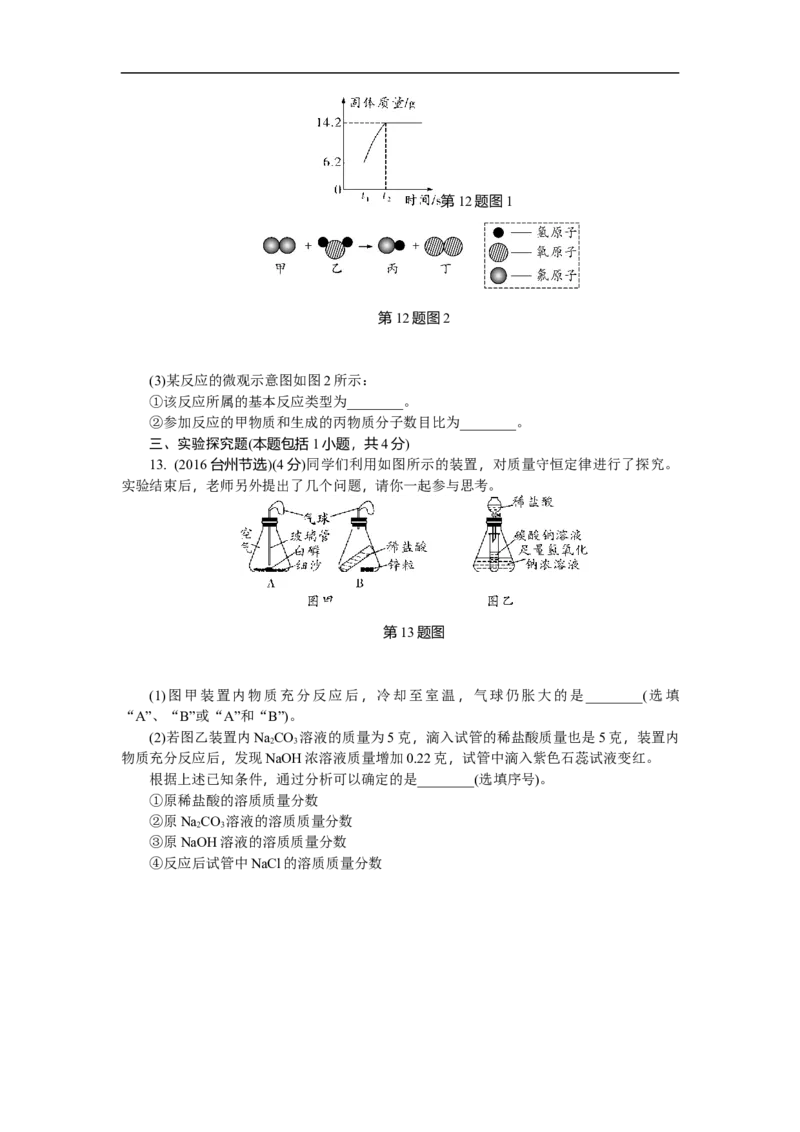
8. (2016厦门)三种物质在密闭容器中发生反应,反应前后质量比例
第8题图
的变化关系如图所示。下列说法正确的是( )
A.反应中CaO为催化剂
B.该反应是复分解反应
C.反应后容器中固体质量减少
D.反应后容器中氧元素质量分数增大
二、填空及简答题(本题包括4小题,共20分)
9. (2016哈尔滨)(6分)如图是氢气在氯气中燃烧生成氯化氢的微观模拟图,请回答下列
问题:第9题图
(1)在B图中将相关粒子图形补充完整;
(2)此变化前后发生改变的粒子是____________________________________________。
(3)从微观角度解释此反应为化合反应的原因是____________________________。
10. (2016达州)(4分)2015年8月12日天津港发生爆炸后,消防专家确认,大约40种
危化品中就有700吨剧毒氰化钠(NaCN)。
(1)氰化钠(NaCN)泄漏可用过氧化氢溶液进行高效处理,氰化钠、过氧化氢和水反应
生成碳酸氢钠和氨气,其反应的化学方程式为____________________________________。
(2)氰化钠是工业上冶炼黄金的重要原料,工业上生产氰化钠的化学方程式为2Na+2X
+2NH === 2NaCN+3H。
3 2
①X的化学式为________。 ②NH 中N元素的化合价为________。
3
11. (2016连云港节选)(3分)(3)质量守恒定律是帮助我们学习和认识化学反应实质的重
要理论。
①下列表述正确的是________。
A. 蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B. 每32 g S和32 g O 完全反应后,生成64 g SO
2 2
C. 在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO 和HO,实验测得反应
2 2
前后物质的质量如下表:
R O CO HO
2 2 2
反应前质量/g 46 128 0 0
反应后质量/g 0 32 x 54
则x=________;已知参加反应的物质R与氧气的分子个数之比为1∶3,则R的相对
分子质量是________。
12. (2016福州)(7分)I.质量守恒定律的发现对化学的发展做出了重要贡献。
(1)通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是
________(填标号)。
A. 蔗糖和水 B. 氯化钠溶液和硝酸钾溶液
C. 铁和氯化铜溶液
(2)在氧气中点燃红磷的实验过程,固体质量变化如图1所示。
① 从 燃 烧 条 件 分 析 , 固 体 质 量 在 t 前 没 有 发 生 变 化 的 原 因 为
1
__________________________________。
②该反应的化学方程式为____________________________。
③参加反应的氧气质量为________g。第12题图1
第12题图2
(3)某反应的微观示意图如图2所示:
①该反应所属的基本反应类型为________。
②参加反应的甲物质和生成的丙物质分子数目比为________。
三、实验探究题(本题包括1小题,共4分)
13. (2016台州节选)(4分)同学们利用如图所示的装置,对质量守恒定律进行了探究。
实验结束后,老师另外提出了几个问题,请你一起参与思考。
第13题图
(1)图甲装置内物质充分反应后,冷却至室温,气球仍胀大的是________(选填
“A”、“B”或“A”和“B”)。
(2)若图乙装置内NaCO 溶液的质量为5克,滴入试管的稀盐酸质量也是5克,装置内
2 3
物质充分反应后,发现NaOH浓溶液质量增加0.22克,试管中滴入紫色石蕊试液变红。
根据上述已知条件,通过分析可以确定的是________(选填序号)。
①原稀盐酸的溶质质量分数
②原NaCO 溶液的溶质质量分数
2 3
③原NaOH溶液的溶质质量分数
④反应后试管中NaCl的溶质质量分数专题十三 质量守恒定律及其应用
命题点分类集训
命题点1 质量守恒定律的理解
1. C 2. D
命题点2 质量守恒定律的应用
3. B 4. C 5. D 6. B 7. C 8. A 9. B 10. A
11. B 12. D 13. B 14. D 15. D
命题点3 质量守恒定律的验证
16. B
中考冲刺集训
1. D 2. A 3. A 4. D 5. B 6. D 7. C 8. C
9. (6分)(1) (2分)
(2)氯分子和参加反应的氢分子(2分)
(3)两种分子反应生成另一种分子(2分)
10. (4分)(1)NaCN+HO+HO=== NaHCO +NH ↑(2分)
2 2 2 3 3
(2)①C(1分) ②-3(1分)
[来源:Zxxk.Com]
11. (3分)(3)①B(1分) ②88(1分) 46(1分)
12. (7分)Ⅰ.(1)C(1分)
(2)①温度未达到红磷的着火点(1分)
②4P+5O===== 2PO(2分)
2 2 5
③ 8.0(1分)
(3)①置换反应(1分) ②1∶2(1分)
13. (4分)(1)B(2分) (2)②④(2分)