文档内容
化学的魅力-原子、离子知识精讲
一、原子 (既讲种类,又讲个数) 一、原子 (既讲种类,又讲个数)
1、定义:化学变化中最小的粒子 (化学变化中原子不可再分) 1、定义:化学变化中最小的粒子 (化学变化中原子不可再分)
(大学) (中学) 2、由原子直接构成的物质
原子和分子可以比大小吗?
物质 分子
(1)金属:Mg、Al、Zn、Fe、Ag、Hg
(2)稀有气体:He、Ne、Ar、Kr、Xe
原子 (3)某些固态非金属:C、S、P
(小学)
【例1】化学变化中的最小粒子是( )
A.分子 B.原子 C.质子 D.电子 1803年,道尔顿、“实心球模型”
1897年,汤姆生、“葡萄干枣糕模型”
11910年,卢瑟福 1912年,波尔(丹麦)
量子
【例2】3月,地震引发了日本核电站的核泄漏,为中国核电站
3、原子的结构
的快速扩张和核安全敲响了警钟,应该思考如何安全
质子 (+) 利用原子能.下列有关原子的说法正确的是( )
原子核 A. 原子中的质子数与中子数一定相等
中子 (不带电) (H无中子)
结构 (+) B. 原子核内的质子数等于核电荷数
C. 原子是不能再分的最小粒子
核外电子: 绕核做高速运动
D. 原子不显电性是因为在原子中不存在带电荷的粒子
(-)
相对原子质量≈ 质子数 + 中子数
核电荷数= 质子数 = 核外电子数
2【例3】原子核( ) 【例5】下列关于原子的说法不正确的是( )
A.由电子和质子构成 B.由质子和中子构成 A.原子是化学变化中的最小粒子,但原子可以再分
C.由电子和中子构成 D.由质子、中子和电子构成 B.核外电子在原子核外的空间里做高速运动
C.原子核是由质子和电子构成的,呈电中性
D.原子可以构成分子,也可以构成物质
【例4】下列叙述错误的是( )
①原子是化学变化中的最小粒子;②原子是不能
再分的粒子;③一切物质都是由原子直接构成的;
④一切原子核都是由质子和中子构成的;⑤原子
不显电性;⑥原子之间有间隔。
A.①② B.②③④
C.③⑤ D.③⑥
4、元素周期表
1860年、门捷列夫
3【例6】我国著名科学家张青莲教授主持测定了铕等9中元素的相对原子
3、原子的结构
质量新值,已知原子质量为152,核电荷数为63,则铕原子的核
质子 (+) 外电子为( )
原子核 A.63 B.89 C.152 D.215
中子 (不带电) (H无中子)
结构 (+)
核外电子: 绕核做高速运动
(-)
相对原子质量≈ 质子数 + 中子数
核电荷数= 质子数 = 核外电子数
原子序数
5、原子结构示意图 二、离子
氢氧根 硝酸根 碳酸根 硫酸根 铵根
定义:带电的原子或原子团(OH-、NO -、CO 2-、SO 2-、NH+)
3 3 4 4
+11 2 8 1 +17 2 8 7 阳离子:带正电的原子或原子团:(Na+、Mg2+、Al3+)
(由金属失电子形成)
分类
Na Cl
阴离子:带负电的原子或原子团 (Cl-、O2-、F-)
(由非金属得电子形成)
+11 2 8 +17 2 8 8
Na+ Cl-
4【例7】根据下列原子结构示意图判断,化学性质最稳定的是( )
三、相对原子质量
一个H O分子的质量?
2
A B C D L 头发 = km m 头发 = t
一个原子的实际质量
【例8】下列关于Na、Na+两种粒子的判断中,正确的是( )
相对原子质量 = 单位:1
①核电荷数相同 ②核外电子数相等 m × 1/12
C
③Na+比Na稳定 ④最外层电子数相等
⑤质子数相等.
A. ①③⑤ B. ②④ C. ①③④⑤ D. 全部
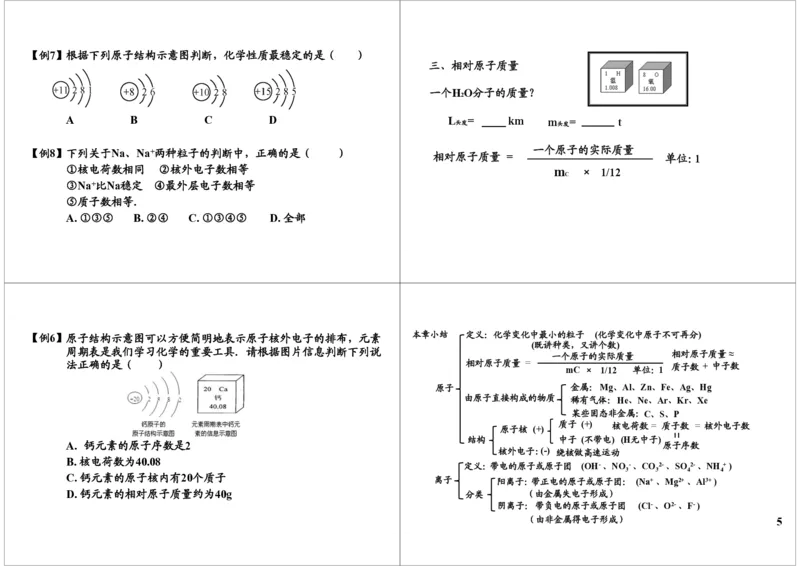
【例6】原子结构示意图可以方便简明地表示原子核外电子的排布,元素 本章小结 定义:化学变化中最小的粒子 (化学变化中原子不可再分)
(既讲种类,又讲个数)
周期表是我们学习化学的重要工具.请根据图片信息判断下列说
一个原子的实际质量 相对原子质量≈
法正确的是( ) 相对原子质量 = 质子数 + 中子数
mC × 1/12 单位:1
原子 金属:Mg、Al、Zn、Fe、Ag、Hg
由原子直接构成的物质 稀有气体:He、Ne、Ar、Kr、Xe
某些固态非金属:C、S、P
原子核 (+) 质子 (+) 核电荷数= 质子数 = 核外电子数
结构 中子 (不带电) (H无中子)
A. 钙元素的原子序数是2 原子序数
核外电子:(-) 绕核做高速运动
B. 核电荷数为40.08
定义:带电的原子或原子团 (OH-、NO -、CO 2-、SO 2-、NH +)
3 3 4 4
C. 钙元素的原子核内有20个质子 离子 阳离子:带正电的原子或原子团: (Na+、Mg2+、Al3+)
D. 钙元素的相对原子质量约为40g 分类 (由金属失电子形成)
阴离子:带负电的原子或原子团 (Cl-、O2-、F-)
(由非金属得电子形成) 5