文档内容
第17讲 物质的分离、除杂与转换
第1课时 物质的除杂、提纯
一、选择题
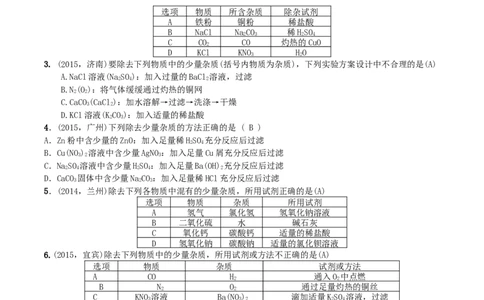
1.(2014,临沂)除去下列物质中含有的少量杂质(括号内的物质),所选试剂不合理的是(A)
A.CaO(CaCO) 稀盐酸
3
B.NaOH溶液[Ca(OH) 溶液] 碳酸钠溶液
2
C.Cu(Fe) 硫酸铜溶液
D.CO(CO) 氢氧化钠溶液
2
2.(2014,益阳)下列除杂所选用的试剂中,正确的是(C)
选项 物质 所含杂质 除杂试剂
A 铁粉 铜粉 稀盐酸
B NaCl NaCO 稀HSO
2 3 2 4
C CO CO 灼热的CuO
2
D KCl KNO HO
3 2
3. (2015,济南)要除去下列物质中的少量杂质(括号内物质为杂质),下列实验方案设计中不合理的是(A)
A.NaCl溶液(NaSO):加入过量的BaCl 溶液,过滤
2 4 2
B.N(O):将气体缓缓通过灼热的铜网
2 2
C.CaCO(CaCl):加水溶解→过滤→洗涤→干燥
3 2
D.KCl溶液(KCO):加入适量的稀盐酸
2 3
4.(2015,广州)下列除去少量杂质的方法正确的是 ( B )
A.Zn粉中含少量的ZnO:加入足量稀HSO 充分反应后过滤
2 4
B.Cu(NO) 溶液中含少量AgNO:加入足量Cu屑充分反应后过滤
3 2 3
C.NaSO 溶液中含少量HSO:加入足量Ba(OH) 充分反应后过滤
2 4 2 4 2
D.CaCO 固体中含少量NaCO:加入足量稀HCl充分反应后过滤
3 2 3
5.(2014,兰州)除去下列各物质中混有的少量杂质,所用试剂正确的是(A)
选项 物质 杂质 所用试剂
A 氢气 氯化氢 氢氧化钠溶液
B 二氧化硫 水 碱石灰
C 氧化钙 碳酸钙 适量的稀盐酸
D 氢氧化钠 碳酸钠 适量的氯化钡溶液
6.(2015,宜宾)除去下列物质中的少量杂质,所用试剂或方法不正确的是(A)
选项 物质 杂质 试剂或方法
A CO H 通入O 中点燃
2 2
B N O 通过足量灼热的铜丝
2 2
C KNO 溶液 Ba(NO) 滴加适量KSO 溶液,过滤
3 3 2 2 4
D NaCl溶液 NaCO 滴加稀盐酸至不再产生气泡
2 3
7.(2014,哈尔滨)除去下列物质中的少量杂质,所选用的试剂和操作方法都正确的是(A)
选项 物质 杂质 试剂 操作方法
A CuO C 足量空气 在空气中
灼烧
B CO HCl 足量氢氧化钠溶
2
液和浓硫酸 依次通过
两种试剂
C KCl KSO 蒸馏水和过量
2 4
BaCl 溶液 溶解、蒸发
2
D FeCl 溶液 CuCl 过量铁粉 过滤
3 2
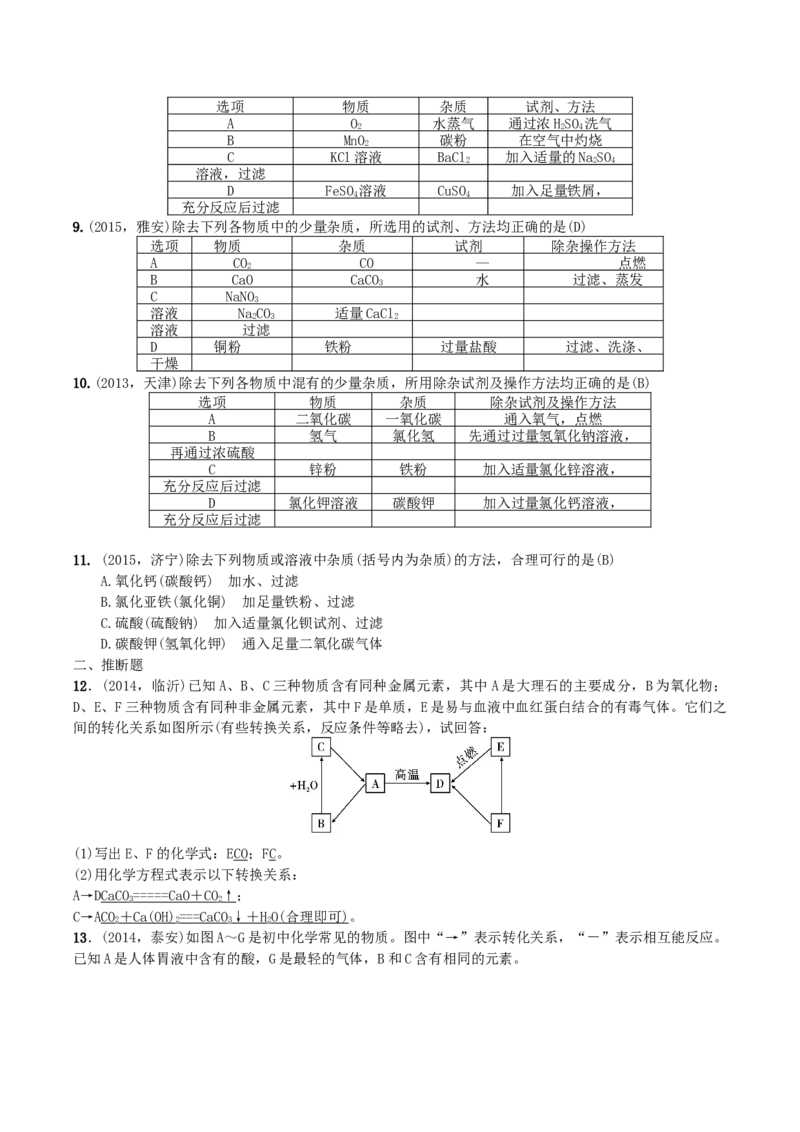
8.(2013,盐城)要除去下列各组物质中的少量杂质,所选试剂和方法不可行的是(C)选项 物质 杂质 试剂、方法
A O 水蒸气 通过浓HSO 洗气
2 2 4
B MnO 碳粉 在空气中灼烧
2
C KCl溶液 BaCl 加入适量的NaSO
2 2 4
溶液,过滤
D FeSO 溶液 CuSO 加入足量铁屑,
4 4
充分反应后过滤
9.(2015,雅安)除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是(D)
选项 物质 杂质 试剂 除杂操作方法
A CO CO — 点燃
2
B CaO CaCO 水 过滤、蒸发
3
C NaNO
3
溶液 NaCO 适量CaCl
2 3 2
溶液 过滤
D 铜粉 铁粉 过量盐酸 过滤、洗涤、
干燥
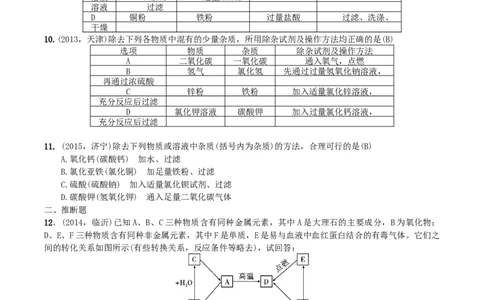
10.(2013,天津)除去下列各物质中混有的少量杂质,所用除杂试剂及操作方法均正确的是(B)
选项 物质 杂质 除杂试剂及操作方法
A 二氧化碳 一氧化碳 通入氧气,点燃
B 氢气 氯化氢 先通过过量氢氧化钠溶液,
再通过浓硫酸
C 锌粉 铁粉 加入适量氯化锌溶液,
充分反应后过滤
D 氯化钾溶液 碳酸钾 加入过量氯化钙溶液,
充分反应后过滤
11. (2015,济宁)除去下列物质或溶液中杂质(括号内为杂质)的方法,合理可行的是(B)
A.氧化钙(碳酸钙) 加水、过滤
B.氯化亚铁(氯化铜) 加足量铁粉、过滤
C.硫酸(硫酸钠) 加入适量氯化钡试剂、过滤
D.碳酸钾(氢氧化钾) 通入足量二氧化碳气体
二、推断题
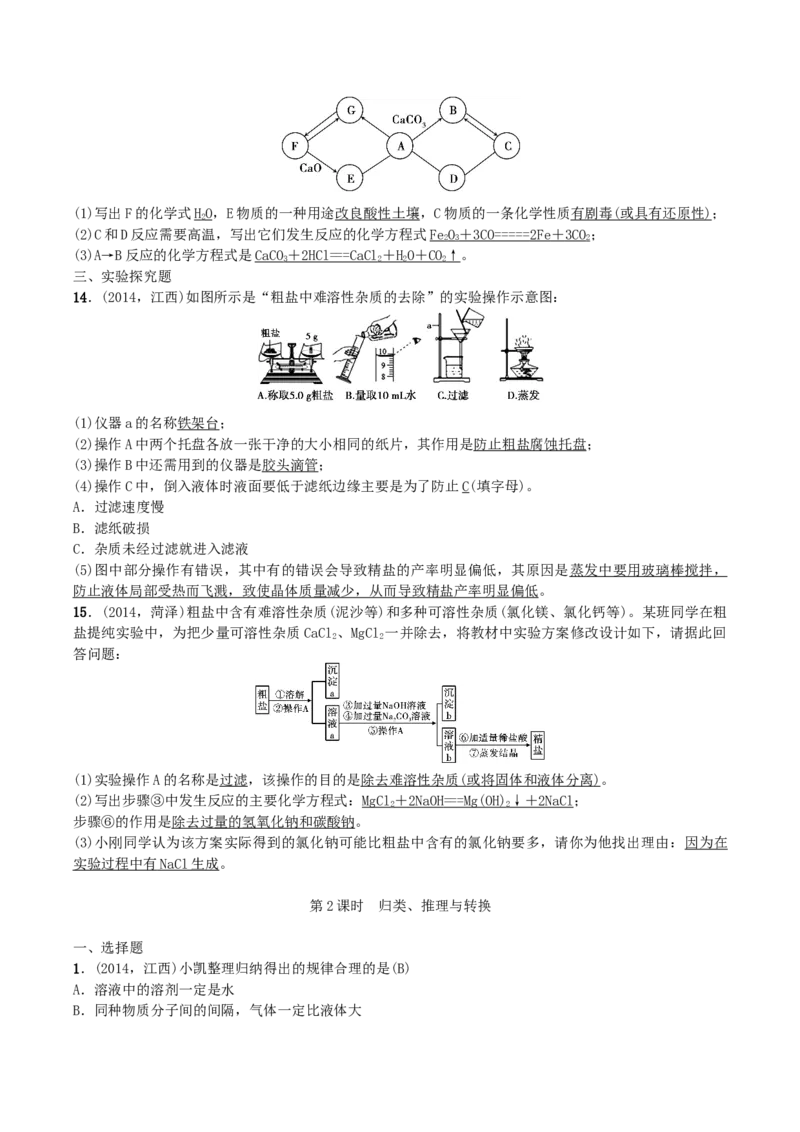
12.(2014,临沂)已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;
D、E、F三种物质含有同种非金属元素,其中F是单质,E是易与血液中血红蛋白结合的有毒气体。它们之
间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:
(1)写出E、F的化学式:ECO;FC。
(2)用化学方程式表示以下转换关系:
A→DCaCO ==== = Ca O + C O↑;
3 2
C→ACO + Ca(OH ) = = =CaC O ↓+ H O ( 合理即可 )。
2 2 3 2
13.(2014,泰安)如图A~G是初中化学常见的物质。图中“→”表示转化关系,“-”表示相互能反应。
已知A是人体胃液中含有的酸,G是最轻的气体,B和C含有相同的元素。(1)写出F的化学式HO,E物质的一种用途改良酸性土壤,C物质的一条化学性质 有剧毒 ( 或具有还原性 );
2
(2)C和D反应需要高温,写出它们发生反应的化学方程式FeO + 3C O ==== = 2F e + 3C O;
2 3 2
(3)A→B反应的化学方程式是CaCO + 2HC l = = =CaC l + H O + C O↑。
3 2 2 2
三、实验探究题
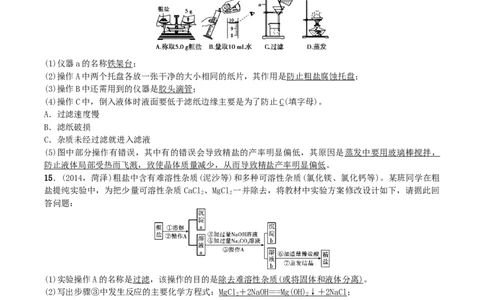
14.(2014,江西)如图所示是“粗盐中难溶性杂质的去除”的实验操作示意图:
(1)仪器a的名称铁架台;
(2)操作A中两个托盘各放一张干净的大小相同的纸片,其作用是防止粗盐腐蚀托盘;
(3)操作B中还需用到的仪器是胶头滴管;
(4)操作C中,倒入液体时液面要低于滤纸边缘主要是为了防止C(填字母)。
A.过滤速度慢
B.滤纸破损
C.杂质未经过滤就进入滤液
(5)图中部分操作有错误,其中有的错误会导致精盐的产率明显偏低,其原因是蒸发中要用玻璃棒搅拌,
防止液体局部受热而飞溅,致使晶体质量减少,从而导致精盐产率明显偏低。
15.(2014,菏泽)粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗
盐提纯实验中,为把少量可溶性杂质CaCl 、MgCl 一并除去,将教材中实验方案修改设计如下,请据此回
2 2
答问题:
(1)实验操作A的名称是过滤,该操作的目的是 除去难溶性杂质 ( 或将固体和液体分离 )。
(2)写出步骤③中发生反应的主要化学方程式:MgCl + 2NaO H = = =Mg(OH ) ↓+ 2NaC l;
2 2
步骤⑥的作用是除去过量的氢氧化钠和碳酸钠。
(3)小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由:因为在
实验过程中有 NaC l 生成 。
第2课时 归类、推理与转换
一、选择题
1.(2014,江西)小凯整理归纳得出的规律合理的是(B)
A.溶液中的溶剂一定是水
B.同种物质分子间的间隔,气体一定比液体大C.酸、碱中一定含有氧元素
D.不能使酚酞试液变红的溶液一定是酸溶液
2.(2014,黄冈)推理是一种重要的学习方法。下列推理正确的是(B)
A.任何化学反应都遵循质量守恒定律,因此任何物质发生化学反应都没有质量变化
B.化合物是由多种元素组成的纯净物,则由多种元素组成的纯净物一定是化合物
C.离子是带电的原子或原子团,则带电的粒子是离子
D.碱能使酚酞试液变红,因此能使酚酞试液变红的物质一定是碱
3.(2014,江苏)逻辑推理是一种重要的化学思维方法,以下推理合理的是(C)
A.CO和CO 组成元素相同,所以具有相似的化学性质
2
B.因为某物质燃烧生成了CO 和HO,所以该物质中含有C、H、O三种元素
2 2
C.质子数决定元素的种类,所以质子数相同的原子属于同种元素
D.酚酞是酸碱指示剂之一,碳酸钠属于盐,所以碳酸钠溶液不能使酚酞变色
4.(2014,德州)逻辑推理是一种重要的化学思维方法。以下推理合理的是(C)
A.离子是带电荷的微粒,所以带电荷的微粒一定是离子
B.酸中一定含有氢元素,所以含有氢元素的物质一定是酸
C.某物质在氧气中燃烧后生成二氧化碳和水,所以该物质中一定含有碳、氢元素
D.碱溶液都能使无色酚酞溶液变红,所以能使无色酚酞溶液变红的一定是碱溶液
5.(2014,聊城)推理是一种重要的化学思维方法,以下推理合理的是(A)
A.单质中只含有一种元素,但是只含有一种元素的物质不一定是单质
B.中和反应一定有盐生成,所以有盐生成的反应一定是中和反应
C.HO和HO 的组成元素相同,所以它们的化学性质相同
2 2 2
D.氧化物一定含氧元素,含氧元素的物质一定是氧化物
6.(2015,广安)分析推理是化学学习常用的方法,下列分析推理正确的是(D)
A.浓盐酸具有挥发性,所以浓硫酸也具有挥发性
B.金刚石和石墨都是由碳原子构成,所以它们的性质相同
C.离子是带电荷的粒子,所以带电荷的粒子一定是离子
D.点燃氢气前需要检验纯度,所以点燃甲烷前也需要检验纯度
7.(2015,江西)逻辑推理是学习化学常用的思维方法,下列推理正确的是(A)
A.物质的分子结构不同则性质不同,所以氧气和臭氧(O)的性质不同
3
B.由同种分子构成的物质一定是纯净物,所以纯净物一定是由同种分子构成
C.氧、硫、氯原子最外层电子数均多于四个,所以非金属元素原子最外层电子数都多于四个
D.单质碳能夺取氧化铜中的氧具有还原性,二氧化碳能夺取氧化铜中的氧所以也具有还原性
8.(2014,甘肃)逻辑推理是一种重要的化学思维方法。下列推理合理的是(D)
A.因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液
B.因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物
C.因为HO和HO 的组成元素相同,所以它们的化学性质相同
2 2 2
D.因为蜡烛燃烧生成CO 和HO,所以蜡烛组成里一定含有碳元素和氢元素
2 2
9.(2014,陕西)运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是(D)
A.铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B.水和过氧化氢的组成元素相同,则两者的化学性质相同
C.Na+、Mg2+、Cl-的最外层电子数均为8,由此得出离子的最外层电子数均为8
D.同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
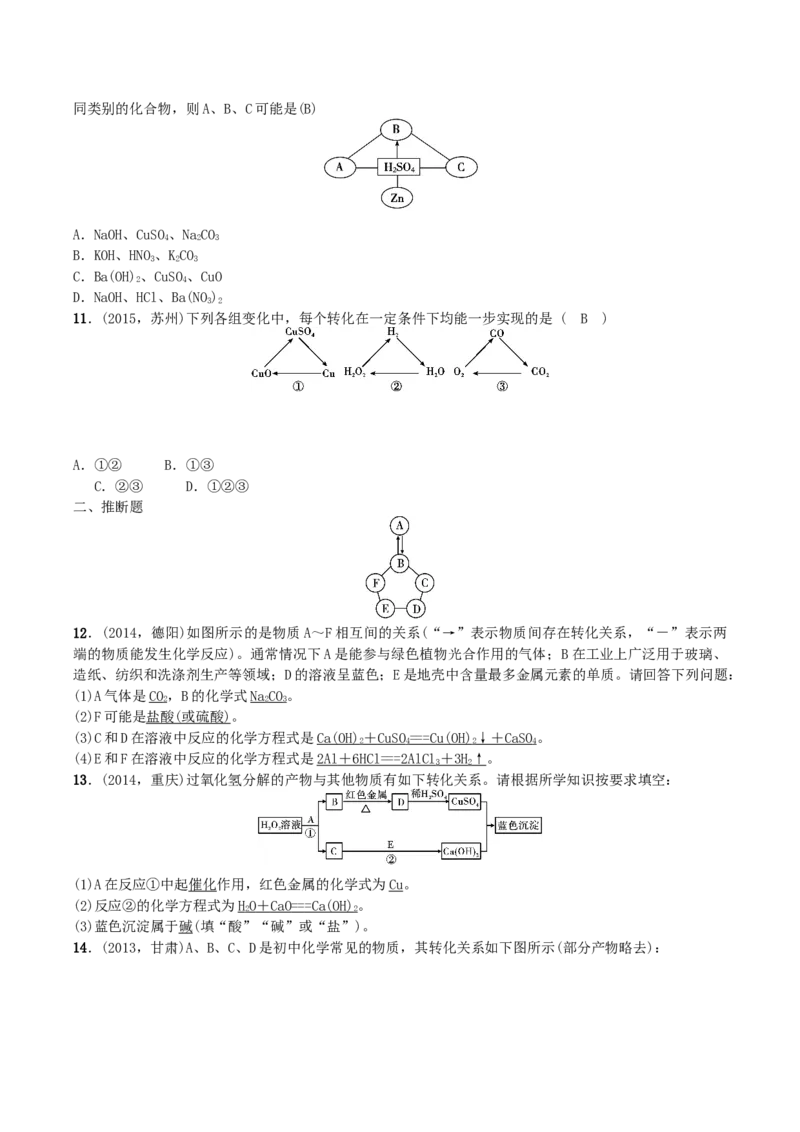
10.(2013,乌鲁木齐)构建知识网络是一种重要的学习方法。如图是关于硫酸化学性质的知识网络:
“—”表示相连的两种物质能发生反应。“→”表示一种物质能转化为另一种物质,A、B、C分别属于不同类别的化合物,则A、B、C可能是(B)
A.NaOH、CuSO、NaCO
4 2 3
B.KOH、HNO、KCO
3 2 3
C.Ba(OH)、CuSO、CuO
2 4
D.NaOH、HCl、Ba(NO)
3 2
11.(2015,苏州)下列各组变化中,每个转化在一定条件下均能一步实现的是 ( B )
A.①② B.①③
C.②③ D.①②③
二、推断题
12.(2014,德阳)如图所示的是物质A~F相互间的关系(“→”表示物质间存在转化关系,“-”表示两
端的物质能发生化学反应)。通常情况下A是能参与绿色植物光合作用的气体;B在工业上广泛用于玻璃、
造纸、纺织和洗涤剂生产等领域;D的溶液呈蓝色;E是地壳中含量最多金属元素的单质。请回答下列问题:
(1)A气体是CO,B的化学式NaCO。
2 2 3
(2)F可能是 盐酸 ( 或硫酸 )。
(3)C和D在溶液中反应的化学方程式是Ca(OH) + CuS O = = =Cu(OH ) ↓+ CaS O。
2 4 2 4
(4)E和F在溶液中反应的化学方程式是 2A l + 6HC l = = =2AlC l + 3 H↑。
3 2
13.(2014,重庆)过氧化氢分解的产物与其他物质有如下转化关系。请根据所学知识按要求填空:
(1)A在反应①中起催化作用,红色金属的化学式为Cu。
(2)反应②的化学方程式为H O + Ca O = = =Ca(OH )。
2 2
(3)蓝色沉淀属于碱(填“酸”“碱”或“盐”)。
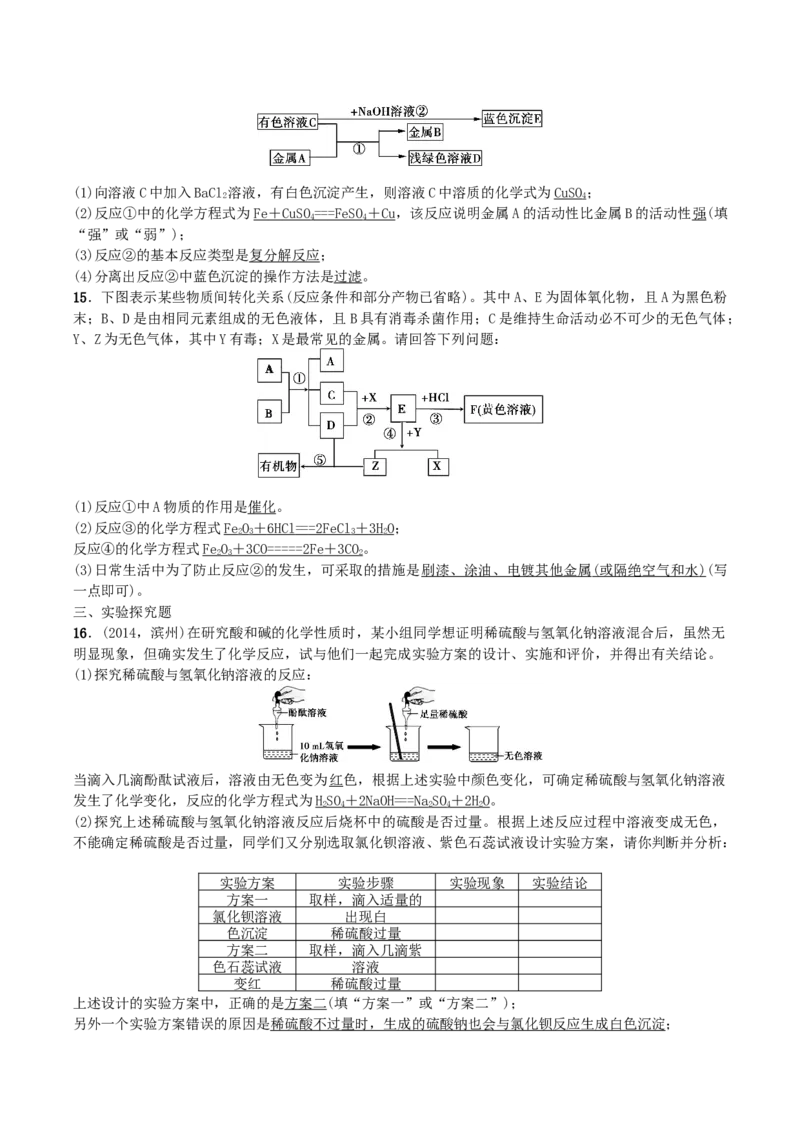
14.(2013,甘肃)A、B、C、D是初中化学常见的物质,其转化关系如下图所示(部分产物略去):(1)向溶液C中加入BaCl 溶液,有白色沉淀产生,则溶液C中溶质的化学式为CuSO;
2 4
(2)反应①中的化学方程式为 F e + CuS O = = =FeS O + C u,该反应说明金属A的活动性比金属B的活动性强(填
4 4
“强”或“弱”);
(3)反应②的基本反应类型是复分解反应;
(4)分离出反应②中蓝色沉淀的操作方法是过滤。
15.下图表示某些物质间转化关系(反应条件和部分产物已省略)。其中A、E为固体氧化物,且A为黑色粉
末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C是维持生命活动必不可少的无色气体;
Y、Z为无色气体,其中Y有毒;X是最常见的金属。请回答下列问题:
(1)反应①中A物质的作用是催化。
(2)反应③的化学方程式FeO + 6HC l = = =2FeC l + 3 HO;
2 3 3 2
反应④的化学方程式FeO + 3C O ==== = 2F e + 3C O。
2 3 2
(3)日常生活中为了防止反应②的发生,可采取的措施是 刷漆、涂油、电镀其他金属 ( 或隔绝空气和水 )(写
一点即可)。
三、实验探究题
16.(2014,滨州)在研究酸和碱的化学性质时,某小组同学想证明稀硫酸与氢氧化钠溶液混合后,虽然无
明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计、实施和评价,并得出有关结论。
(1)探究稀硫酸与氢氧化钠溶液的反应:
当滴入几滴酚酞试液后,溶液由无色变为红色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液
发生了化学变化,反应的化学方程式为HSO + 2NaO H = = =N aSO + 2 HO。
2 4 2 4 2
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量。根据上述反应过程中溶液变成无色,
不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
实验方案 实验步骤 实验现象 实验结论
方案一 取样,滴入适量的
氯化钡溶液 出现白
色沉淀 稀硫酸过量
方案二 取样,滴入几滴紫
色石蕊试液 溶液
变红 稀硫酸过量
上述设计的实验方案中,正确的是方案二(填“方案一”或“方案二”);
另外一个实验方案错误的原因是稀硫酸不过量时,生成的硫酸钠也会与氯化钡反应生成白色沉淀;请你再设计一个确定稀硫酸是否过量的实验方案,你选用的药品是 镁条 ( 或碳酸钠等 ),实验现象及结论是
若有气体放出,证明稀硫酸过量,反之稀硫酸不过量 ( 答案合理即可 )。