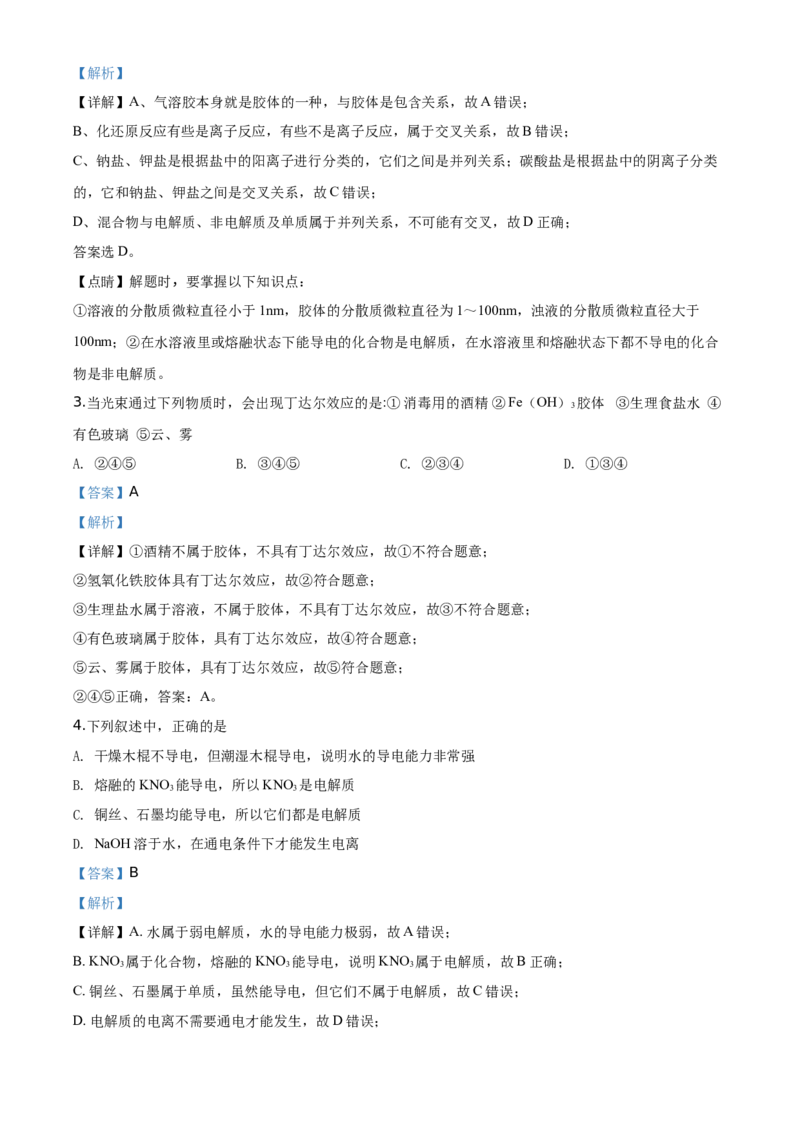文档内容
化学试卷
注意事项:
1.本试卷分第Ⅰ卷和第Ⅱ卷两部分,满分100分。考试时间60分钟。
2.答题前,请务必将班级、姓名、考场号、座号和准考证号填写(或涂)在答题卡和答题纸
的规定位置。
可能用到的相对原子质量:H :1 C:12 N:14 O:16 Na:23 Mg:24 Al:27 Cl:35.5 S:32 Fe:
56 Cu:64 Zn:65 I:127 Ba:137
第I 卷(选择题 共50分)
一、选择题(每题只有一个正确选项,每小题2分,共50分)
1.化学科学的形成、发展与应用过程中,下列科学家与其成就不相对应的是
A. 1961年英国科学家波义尔提出化学元素的概念
B. 1774年法国科学家拉瓦锡提出燃烧的氧化学说
C. 1811年意大利科学家阿伏加德罗提出原子学说
D. 1943年,科学家侯德榜发明联合制碱法
【答案】C
【解析】
【详解】A. 波义尔提出化学元素的概念,故A说法正确;
B. 拉瓦锡提出燃烧作用的氧化学说,故B说法正确;
C. 道尔顿提出原子学说,阿伏加德罗提出阿伏加德罗常数、阿伏加德罗定律,故C说法错误;
D. 候德榜发明联合制碱法,故D说法正确;
答案:C。
2.下列逻辑关系图示中正确的是( )
A. B.
C. D.
【答案】D【解析】
【详解】A、气溶胶本身就是胶体的一种,与胶体是包含关系,故A错误;
B、化还原反应有些是离子反应,有些不是离子反应,属于交叉关系,故B错误;
C、钠盐、钾盐是根据盐中的阳离子进行分类的,它们之间是并列关系;碳酸盐是根据盐中的阴离子分类
的,它和钠盐、钾盐之间是交叉关系,故C错误;
D、混合物与电解质、非电解质及单质属于并列关系,不可能有交叉,故D正确;
答案选D。
【点睛】解题时,要掌握以下知识点:
①溶液的分散质微粒直径小于1nm,胶体的分散质微粒直径为1~100nm,浊液的分散质微粒直径大于
100nm;②在水溶液里或熔融状态下能导电的化合物是电解质,在水溶液里和熔融状态下都不导电的化合
物是非电解质。
3.当光束通过下列物质时,会出现丁达尔效应的是:①消毒用的酒精 ②Fe(OH) 胶体 ③生理食盐水 ④
3
有色玻璃 ⑤云、雾
A. ②④⑤ B. ③④⑤ C. ②③④ D. ①③④
【答案】A
【解析】
【详解】①酒精不属于胶体,不具有丁达尔效应,故①不符合题意;
②氢氧化铁胶体具有丁达尔效应,故②符合题意;
③生理盐水属于溶液,不属于胶体,不具有丁达尔效应,故③不符合题意;
④有色玻璃属于胶体,具有丁达尔效应,故④符合题意;
⑤云、雾属于胶体,具有丁达尔效应,故⑤符合题意;
②④⑤正确,答案:A。
4.下列叙述中,正确的是
A. 干燥木棍不导电,但潮湿木棍导电,说明水的导电能力非常强
B. 熔融的KNO 能导电,所以KNO 是电解质
3 3
C. 铜丝、石墨均能导电,所以它们都是电解质
D. NaOH溶于水,在通电条件下才能发生电离
【答案】B
【解析】
【详解】A. 水属于弱电解质,水的导电能力极弱,故A错误;
B. KNO 属于化合物,熔融的KNO 能导电,说明KNO 属于电解质,故B正确;
3 3 3
C. 铜丝、石墨属于单质,虽然能导电,但它们不属于电解质,故C错误;
D. 电解质的电离不需要通电才能发生,故D错误;答案:B。
【点睛】电解质是在熔融状态下或水溶液中能够电离的化合物,研究的对象是化合物,导电的离子必须是
本身电离产生。
5.下列离子能大量共存的是
A. 使酚酞溶液呈红色的溶液中:NH +、K+、SO 2-、CO2-
4 4 3
B. 无色透明的溶液中:Mg2+、K+、SO 2-、NO -
4 3
C. 含有大量Ba2+的溶液中:Na+、Cu2+、SO 2-、Cl-
4
D. 使石蕊溶液呈红色的溶液中:NH +、K+、CO2-、NO -
4 3 3
【答案】B
【解析】
【详解】A. 使酚酞溶液呈红色,说明溶液显碱性,NH +与OH-反应生成NH ·HO,不能大量共存,故A
4 3 2
不符合题意;
B. 这些离子都没有颜色,且在溶液中不发生任何反应,能够大量共存,故B符合题意;
C.溶液中 Ba2+能与SO 2-生成BaSO 沉淀,不能大量共存,故C不符合题意;
4 4
D. 石蕊溶液呈红色,说明溶液显酸性,CO2-能与H+反应生成CO,不能大量共存,故D不符合题意;
3 2
答案:B。
【点睛】离子是否共存:①注意“色”,题干中溶液是“无色溶液”还是“溶液”,如果是无色溶液,则
有颜色离子不能存在,Fe2+浅绿色、Fe3+棕黄色、Cu2+蓝色、MnO -(紫)红色;②注意“性”,判断溶液显
4
酸性还是碱性;③注意“特殊”,NO -在酸性条件下具有强氧化性,不能与还原性离子大量共存;④注意
3
“反应”,发生复分解反应、氧化还原反应、络合反应等。
6.下列离子反应中,属于氧化还原反应的是
A. Cu2++2OH-= Cu(OH)↓ B. H++OH- =H O
2 2
C. 2H++CO 2-=H O+CO↑ D. Cu2++Fe=Fe2++ Cu
3 2 2
【答案】D
【解析】
【分析】
发生氧化还原反应,反应前后元素化合价一定发生变化。
【详解】A. 反应中没有化合价发生变化,该反应不属于氧化还原反应,故A不符合题意;
B. 反应中没有化合价发生变化,该反应不属于氧化还原反应,故B不符合题意;
C. 反应中没有化合价发生变化,该反应不属于氧化还原反应,故C不符合题意;
D. 反应中Fe元素的化合价由0价→+2价,Cu元素的化合价由+2价→0价,存在化合价的变化,该反应
属于氧化还原反应,故D符合题意;答案:D。
7.在下列反应中,HCl作氧化剂的是
A.
B.
C.
D.
【答案】B
【解析】
【详解】A. 中各元素的化合价没有变化,不属于氧化还原反应,故A不符合
题意;
B. 中,HCl中H元素的化合价由 降低为0,则作氧化剂,故B符合题意;
C. 中,Mn元素的化合价降低,HCl中Cl元素的化合价升高,
则HCl作还原剂,故C不符合题意;
D. 中各元素的化合价没有变化,不属于氧化还原反应,故D不符合题意;
故选B。
8.氢化钠(NaH)可在野外用作生氢剂,其中氢元素为-1价。NaH用作生氢剂时的化学反应原理
为:NaH+HO=NaOH+H ↑。下列有关该反应的说法中,正确的是
2 2
A. 该反应属于置换反应 B. 该反应属于复分解反应
C. NaH被氧化,作还原剂 D. HO中的氢元素都被还原
2
【答案】C
【解析】
【分析】
NaH中H元素显-1价,HO中H元素显+1价,H 中H元素的化合价为0,根据氧化还原反应的归中规
2 2
律分析。
【详解】A. 置换反应是单质+化合物→单质+化合物,根据该反应的特点,该反应不属于置换反应,故A
错误;
B. 所有复分解反应不属于氧化还原反应,故B错误;C. NaH中H元素显-1价,在反应中转化成0价,化合价升高被氧化,NaH为还原剂,故C正确;
D. H O中部分H元素由+1价→0价,化合价降低被还原,HO中部分H被还原,故D错误;
2 2
答案:C。
9.2019年10月1日晚,国庆70周年联欢活动在北京天安门广场隆重举行,晚会通过高空、中空、低空烟
花燃放和特殊烟花装置表演,分波次、多新意地展现烟花艺术的魅力,并配合联欢活动,形成地空一体的
绚丽场景。焰火与高中化学中“焰色试验”知识有关。下列有关“焰色试验”说法中正确的是
A. 烟花呈现的艳丽色彩是由锂、钠、钾、锶、钡等金属单质的燃烧呈现出来的
B. 做焰色试验只能用铂丝蘸取溶液在外焰上灼烧
C. 碳酸钾在酒精灯上灼烧时能直接观察到紫色火焰
D. NaCl与NaSO 灼烧时火焰颜色均为黄色
2 4
【答案】D
【解析】
【详解】A. 烟花呈现的艳丽色彩是由锂、钠、钾、锶、钡等金属元素呈现出来,故A错误;
B. 可以用铂丝,也可以用光亮的铁丝作焰色反应,故B错误;
C. 钾元素需要通过蓝色钴玻璃观察火焰颜色,故C错误;
D. 钠元素的焰色反应中呈现黄色,NaCl和NaSO 都含有钠元素,灼烧时火焰颜色均为黄色,故D正确;
2 4
答案:D。
【点睛】焰色反应是电子的跃迁,不符合化学反应研究范畴,焰色反应只能检验某种元素的存在,该元素
具体形式无法判断,可能是单质也可能是化合物。
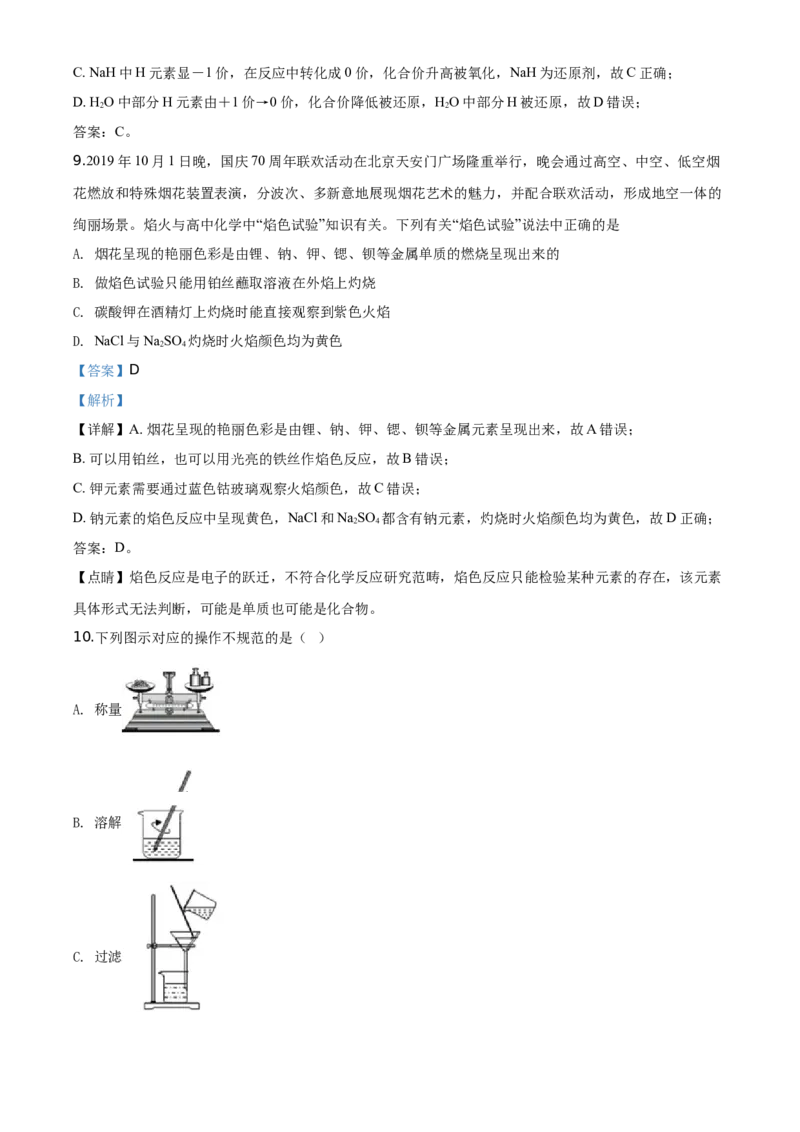
10.下列图示对应的操作不规范的是( )
A. 称量
B. 溶解
C. 过滤D. 转移溶液
【答案】D
【解析】
【详解】A. 称量 时左物右码,操作正确,选项A正确;
B. 溶解 时用玻璃棒搅拌,加速溶解,选项B正确;
C. 过滤 时,遵守“一贴二低三靠”,操作正确,选项C正确;
D. 转移溶液 时必须用玻璃棒引流,选项D不规范;
答案选D。
11.某同学将金属钠露置于空气中,观察到下列现象:银白色→变灰暗→变白色→出现液滴→白色固体。
其变质过程中不可能产生 的物质是
A. NaO B. NaOH
2
C. NaCO D. NaHCO
2 3 3
【答案】D
【解析】
【详解】钠变质过程是:钠→氧化钠→氢氧化钠→氢氧化钠溶液→碳酸钠晶体。所以在变质的过程中不能
出现的是NaHCO 。答案选D。
312.如图所示,在A处通入未经干燥的氯气。当关闭B阀时C处的红布条看不到明显现象;当打开B阀后,
C处的红布条逐渐褪色。则D瓶中盛放的溶液可能是( )
①饱和NaCl溶液②NaOH溶液③HO④浓硫酸
2
A. ① B. ①③ C. ②④ D. ③④
【答案】C
【解析】
【分析】
干燥的氯气不能使有色布条褪色,湿润的氯气能使有色布条褪色,关闭B阀,C处红布条看不到明显现象,
氯气可能被吸收也可能被干燥。
【详解】干燥 的氯气不能使有色布条褪色,湿润的氯气能使有色布条褪色,关闭B阀,C处红布条看不到
明显现象,氯气可能被吸收也可能被干燥,打开 B阀后,C处红布条逐渐褪色,未经干燥的氯气通过B进
入C,①饱和NaCl溶液不能吸收氯气,即从饱和氯化钠溶液出来的氯气中含有水蒸气,能使有色布条褪色,
故①不符合题意;
②NaOH溶液:氯气能与NaOH溶液反应,氯气被吸收,故②符合题意;
③HO:氯气能溶于水,但不能被水完全吸收,通过水后,湿润的氯气能使有色布条褪色,故③不符合题
2
意;
④浓硫酸:浓硫酸能干燥氯气,干燥的氯气不能使有色布条褪色,故④符合题意;
②④符合题意,答案:C。
13.下列反应中,其产物的颜色按红、红褐、淡黄、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧 ②FeSO 溶液中滴入NaOH溶液,并在空气中放置一段时间 ③FeCl 溶液中滴
4 3
入KSCN溶液 ④无水硫酸铜放入医用酒精中
A. ②③①④ B. ③②①④
C. ③①②④ D. ①②③④
【答案】B
【解析】
【详解】①金属钠在纯氧中燃烧生成淡黄色的过氧化钠;②FeSO 溶液中滴入NaOH溶液先生成白色沉淀
4
氢氧化亚铁,但很快转化为灰绿色,最终转化为红褐色的氢氧化铁;③FeCl 溶液中滴入KSCN溶液,发
3
生络合反应,溶液呈红色;④无水硫酸铜放入医用酒精中,医用酒精中含有水,无水硫酸铜遇水变蓝,故溶液变蓝,故其产物的颜色按按红、红褐、淡黄、蓝色顺序排列的是③②①④,B项正确;
答案选B。
14.将30mL0.5mol/ L NaOH溶液加水稀释到 0.03 mol/L ,则选用的容量瓶规格为
A. 100 mL B. 250 mL C. 500 mL D. 1000 mL
【答案】C
【解析】
【分析】
利用稀释前后溶质的质量或物质的量不变进行分析。
【详解】稀释前后溶质的物质的量保持不变,因此有 30×10-3L×0.5mol·L-1=V(NaOH)×10-
3L×0.03mol·L-1,解得V(NaOH)=500mL,故C正确;
答案:C。
15.对于 、 、 和三种粒子,下列叙述正确的是
A. 质子数一定相同,质量数和中子数一定不同
B. 化学性质几乎相同
C. 一定都由质子、中子、电子构成
D. 核电荷数、核外电子数一定相同
【答案】A
【解析】
【详解】A. 三种微粒的质子数都为1,质量数分别是1、3、2,中子数分别为0、2、1,故A正确;
B. 是阳离子,核外无电子, 、 属于原子,核外有1个电子,三种微粒的化学性质不相同,故B
错误;
C. 不含有中子数,故C错误;
D. 质子数等于核电荷数,对于原子来说,质子数等于核外电子数,故D错误;
答案:A。
【点睛】易错点是选项D,质子数等于核电荷数=原子序数,对原子:质子数=核外电子数;阴离子:核外
电子数=质子数+所带电荷数;阳离子:核外电子数=质子数-所带电荷数。
16.2016年 IUPAC将第117号元素命名为Ts(中文名 ,音tian),T 是第七周期第ⅦA族元素。下列
S
说法中,不正确的是
A. Ts的最外层电子数是7
B. Ts原子原子半径比At原子大
C. Ts在同族元素中非金属性最弱D. 中子数为176的Ts,其核素符号是
【答案】D
【解析】
【详解】A. 主族元素最外层电子数等于所在的族序数,Ts原子序数为117,位于第七周期ⅦA族,Ts的最
外层电子数是7,故A说法正确;
B. At位于第六周期ⅦA族,同主族从上到下,原子半径增大,即Ts的原子半径大于At的原子,故B说法
正确;
C. 同主族从上到下非金属性减弱,Ts在同族元素中非金属性最弱,故C说法正确;
D. 质量数=质子数+中子数=117+176=293,因此该核素的符号是 ,故D说法错误;
答案:D。
17.下列说法正确的是 ( )
A. 含氧的化合物就是氧化物
B. 1 mol H O中含有2 mol氢和1 mol氧
2
C. 氧化剂的氧化性的相对强弱取决于得到电子数目的多少
D. 等质量的铝分别与足量的盐酸和氢氧化钠溶液反应时逸出气体的量相等
【答案】D
【解析】
【详解】A.氧化物中含有两种元素,其中一种元素为氧元素,所以含有氧元素的化合物不一定为氧化物,
如硫酸、氯酸钾等都含有氧元素,二者不属于氧化物,选项A错误;
B.1 mol HO中含有2mol氢原子和1mol氧原子,必须指明具体的粒子名称,选项B错误;
2
C.氧化剂的氧化性的相对强弱与得到电子数目的多少无关,与得到电子能力的强弱有关,选项C错误;
D.等量的铝失去的电子固定,无论与酸反应还是与碱溶液反应,则反应生成氢气的量相等,选项D正确;
答案选D。
18.下列离子方程式中,正确的是
A. 氧化亚铁与稀盐酸反应:FeO+2H+=Fe3++H O
2
B. 向氯化铜溶液中加入氢氧化钠溶液:Cu2++OH-=Cu(OH)↓
2
C. 氯化铁溶液与铜反应:Fe3++Cu=Fe2++Cu2+
D. 向氯化亚铁溶液中通入氯气:2Fe2++Cl=2Fe3++2Cl-
2
【答案】D
【解析】
【详解】A. 氧化亚铁中铁显+2价,即正确的离子方程式为FeO+2H+=Fe2++HO,故A错误;
2B. 反应中原子不守恒,正确的离子方程式是Cu2++2OH-=Cu(OH) ↓,故B错误;
2
C. 反应中电荷不守恒,正确的离子方程式是2Fe3++Cu=2Fe2++Cu2+,故C错误;
D. 氯气能将Fe2+氧化成Fe3+,反应的离子方程式为2Fe2++Cl=2Fe3++2Cl-,故D正确;
2
答案:D。
【点睛】离子方程式正误判断:①是否符合客观事实,如2Fe+6H+=2Fe3++3H↑;②原子、电荷是否守
2
恒,如本题的选项B和C;③拆写是否正确,如醋酸与NaOH反应:H++OH-=H O,醋酸是弱酸,不能
2
拆写成离子;④是否漏写离子方程式,如Ba(OH) 与HSO 反应,书写成H++OH-=H O,漏写了Ba2++
2 2 4 2
SO -=BaSO ↓;⑤“量”是否正确,如NaHCO 溶液加入少量Ca(OH) ,写成HCO -+Ca2++OH-
4 4 3 2 3
=CaCO ↓+HO,应注意Ca(OH) 是少量,正确的是2HCO -+Ca2++2OH-=CaCO ↓+2HO+CO2-。
3 2 2 3 3 2 3
19.下列物质含有共价键的是
A. HCl B. MgO C. CaCl D. KBr
2
【答案】A
【解析】
【分析】
一般金属元素与非金属元素形成离子键,非金属元素之间形成共价键,以此来解答。
【详解】A. HCl属于共价化合物,只存在共价键,故A可选;
B.MgO属于离子化合物,只存在离子键,故B不选;
C. CaCl 属于离子化合物,只存在离子键,故C不选;
2
D. KBr属于离子化合物,只存在离子键,故D不选;
故答案选A。
【点睛】共价化合物中一定含有共价键,一定没有离子键;离子化合物中一定含有离子键,可能含有共价
键。
20.下列关于物质性质变化的比较,不正确的是( )
A. 酸性强弱:HIO >HBrO>HClO B. 原子半径大小:Na>S>O
4 4 4
C. 碱性强弱:KOH>NaOH>LiOH D. 金属性强弱:Na>Mg>Al
【答案】A
【解析】
【详解】A.非金属性:Cl>Br>I,元素 的非金属性越强,对应的最高价氧化物的水化物酸性越强,则有
酸性强弱:HIO>HBrO>HClO,故A错误;
4 4 4
B.同周期元素从左到右原子半径逐渐减小,则Na>S,原子核外电子层数越多,半径越大,O的原子核外
有2个电子层,半径最小,则原子半径:Na>S>O,故B不选;
C.金属性:K>Na>Li,元素的金属性越强,对应最高价氧化物的水化物的碱性越强,则有碱性强弱:KOH>NaOH>LiOH,故C不选;
D.同周期元素从左到右金属性逐渐减弱,则有金属性强弱:Na>Mg>Al,故D不选。
故答案选A。
21.实验室利用下图所示的装置制备干燥、纯净的氯气。下列有关叙述不正确的是( )
A. 本实验操作顺序为:检验装置气密性→添加固体药品→添加液体药品→加热
B. 装置Ⅱ、Ⅲ中的试剂依次为浓硫酸、饱和NaCl溶液
C. 氯气密度比空气大,故装置Ⅳ中长导管进气,短导管出气
D. 装置Ⅴ中反应的离子方程式为:Cl+2OH﹣=Cl﹣+ClO﹣+ H O
2 2
【答案】B
【解析】
【详解】A. 本实验操作顺序为:检验装置气密性→在圆底烧瓶中添加固体药品二氧化锰→通过分液漏斗添
加液体药品浓盐酸→加热制取氯气,净化干燥后收集,且注意尾气处理,选项A正确;
B. 装置Ⅱ、Ⅲ中的试剂依次为饱和NaCl溶液、浓硫酸,以除去氯气中的氯化氢气体和干燥氯气,选项B
不正确;
C. 氯气密度比空气大,故装置Ⅳ中长导管进气,短导管出气,利用排空气法收集且有尾气吸收,选项C正
确;
D. 装置Ⅴ中多余的氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:Cl+2OH
2
﹣=Cl﹣+ClO﹣+ H O,选项D正确。
2
答案选B。
【点睛】本题考查氯气的制备及收集,利用二氧化锰和浓盐酸共热制取氯气,制得的氯气中含有氯化氢,
进行净化和干燥,最后收集和尾气处理,得到纯净、干燥的氯气。
22.质量都为4.2g的A气体和B气体,在标准状况下的体积分别为3.36L和2.94L,则这两种气体的摩尔质
量之比为( )
A. 7:8 B. 8∶7 C. 1∶1 D. 15∶13【答案】A
【解析】
【分析】
利用 进行分析;
【详解】A气体: ,解得M=28g/mol;同理气体B的摩尔质量为32g/mol,因此两种气
体的摩尔质量之比为28g·mol-1∶32g·mol-1=7∶8;
答案为A。
23.下列关于铝的说法中,正确的是
A. 铝的化学性质不活泼
B. 铝不与酸、碱反应
C. 常温下铝不与氧气反应
D. 铝表面容易生成一层致密的氧化铝保护膜
【答案】D
【解析】
【详解】A. 铝是活泼性金属,化学性质活泼,故A错误;
B. 铝是活泼金属,能与酸反应,Al能与碱反应,如与NaOH溶液反应:2Al+2OH-+2HO=2AlO-+
2 2
3H↑,故B错误;
2
C. 铝是活泼金属,常温下氧气能与Al反应生成氧化铝,故C错误;
D. 铝是活泼金属,铝表面能被氧气氧化生成一层致密氧化薄膜,能够阻碍内部铝被氧化,故D正确;
答案:D。
24.下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素原子的核电荷数为X元素的2倍。
下列说法正确的是
X
Y Z W
T
A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次增大
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次增强C. YX 晶体熔化、液态WX 汽化均需克服分子间作用力
2 3
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,TX 具有氧化性
2 3
【答案】D
【解析】
【分析】
X、Y、Z、W为短周期元素,令X的核电荷数为a,X和W属于同主族,且属于短周期元素,即W的核
电荷数为a+8,W的核电荷数为X元素的2倍,即a+8=2a,则a=8,即X为O,W为S,Z为P,T为
As,Y为Si。
【详解】X、Y、Z、W为短周期元素,令X的核电荷数为a,X和W属于同主族,且属于短周期元素,即
W的核电荷数为a+8,W的核电荷数为X元素的2倍,即a+8=2a,则a=8,即X为O,W为S,Z为P,
T为As,Y为Si,
A. O、S、P原子半径大小顺序是P>S>O,同主族从上到下非金属性减弱,同周期从左向右非金属性增强,
因此它们气态氢化物的热稳定性大小顺序是HO>HS>PH,故A错误;
2 2 3
B. 硫元素在自然界中既有游离态也有化合态,故B错误;
C. SiO 熔化时破坏的是共价键,SO 汽化时破坏的是分子间作用力,故C错误;
2 2
D. As位于元素周期表中的金属与非金属分界处,其单质具有半导体特性,As O 中+3价As既有氧化性又
2 3
有还原性,故D正确;
答案:D。
25.下列说法正确的是
A. 同温同压下甲烷和氧气的密度之比为2∶1
B. 1 g甲烷和1 g氧气的原子数之比为5∶1
C. 等物质的量的甲烷和氧气的质量之比为2∶1
D. 在标准状况下等质量的甲烷和氧气的体积之比为1∶2
【答案】B
【解析】
【分析】
A.同温同压下气体的密度之比等于摩尔质量之比;
B.根据N=nN =N m/M来计算;
A A
C.根据m=nM来计算;
D.根据公式V=nV =mVm/M来计算。
m
【详解】A.同温同压下,甲烷和氧气的密度之比等于摩尔质量之比即等于16:32=1:2,故A错误;
B.根据N=nN =mN /M可知,1g甲烷和1g氧气的原子数之比为(1/16×5N ):(1/32×2)=5:1,故B正确;
A A AC.根据m=nM可知,等物质的量的甲烷和氧气的质量之比为16:32=1:2,故C错误;
D.根据公式V=nV =mV /M可知,在标准状况下等质量的甲烷和氧气的体积之比=(mV /16):(mV /
m m m m
32)=2:1,故D错误;
故答案选B。
【点睛】根据气态方程:PV==nRT及n=m/M、m=ρV可知,P×M==m/VRT= P×M=ρRT ,当P、T一定时,
M与ρ成正比。
第II卷(非选择题 共50分)
二、填空题
26.有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子
层数,且A的L层电子数是K层电子数的两倍,C在空气中燃烧时呈现黄色火焰,C的单质在加热下与B
的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)写出下列元素的名称:A_____,B_____,C_____,D_____。
(2)D元素位于周期表中____周期_____族。D2-的结构示意图是____。
(3)AB 是___(填“共价”或“离子”)化合物,C B 所含化学键的类型是___、___。写出AB 与C B 反应
2 2 2 2 2 2
的化学方程式:___________________。
(4)用电子式表示化合物C D的形成过程:________。
2
【答案】 (1). 碳 (2). 氧 (3). 钠 (4). 硫 (5). 三 (6). ⅥA (7). (8). 共
价 (9). 离子键 (10). 非极性共价键 (11). 2CO +2NaO=2Na CO +O (12).
2 2 2 2 3 2
【解析】
【分析】
A和B具有相同的电子层数,即A和B位于同周期,A的L层电子数是K层电子数的两倍,即A为C,C
在空气中燃烧时呈现黄色火焰,即C为Na,Na在加热条件下与B的单质充分反应,可以得到与D单质颜
色相同的淡黄色固态化合物,即B为O,D为S。
【详解】(1) A和B具有相同的电子层数,即A和B位于同周期,A的L层电子数是K层电子数的两倍,
即A为C,C在空气中燃烧时呈现黄色火焰,即C为Na,Na在加热条件下与B的单质充分反应,可以得
到与D单质颜色相同的淡黄色固态化合物,即B为O,D为S;
(2)D为S,位于第三周期VIA族;S2-的结构示意图为 ;(3)AB 化学式为CO,CO 属于共价化合物;C B 的化学式为NaO,其电子式为 ,含有
2 2 2 2 2 2 2
离子键、(非极性)共价键;CO 与NaO 反应:2NaO+2CO=2Na CO+O;
2 2 2 2 2 2 2 3 2
(4)C D的化学式为NaS,属于离子化合物,即用电子式表示化合物形成过程:
2 2
。
27.某校化学兴趣小组同学猜想自来水中可能含有大量Cu2+、Ca2+、Mg2+和某些阴离子,从而进行了三组
实验:
①取适量自来水于试管中,滴加足量的NaOH溶液,产生白色沉淀;
②过滤后取滤液于试管中,滴加足量的NaCO 溶液,又有白色沉淀生成;
2 3
③另取适量自来水于试管中,滴加足量稀硝酸后再滴加AgNO 溶液,也产生白色沉淀。
3
请回答以下问题:
(1)不用做实验就可排除的离子是_____。
(2)通过实验可初步确定自来水中_____(填“含有”或“不含有”)大量Ca2+、Mg2+;判断依据的离子反应方
程式有__________。
(3)自来水中所含阴离子可以确定有______,理由是_____。
(4)确定实验②中滴加的NaCO 溶液已过量的检验方法是______。
2 3
【答案】 (1). Cu2+ (2). 含有 (3). Mg2++2OH-=Mg(OH) ↓、CO2-+Ca2+=CaCO ↓ (4). Cl-(或氯离
2 3 3
子) (5). Cl-+Ag+=AgCl↓,白色沉淀不溶于稀硝酸 (6). 取实验②反应后的上清液适量于试管中 ,滴加
足量盐酸,若产生无色气泡(或滴加CaCl 溶液,若产生白色沉淀),则证明NaCO 溶液已过量
2 2 3
【解析】
【详解】(1)含Cu2+的溶液显蓝色,而自来水无色,故直接可以排除的离子是Cu2+,故答案为Cu2+;
(2)根据①、②的现象,生成的白色沉淀是碳酸钙和碳酸镁,初步确定自来水中含有Ca2+、Mg2+阳离子;反
应的离子方程式是:CO2-+Ca2+=CaCO ↓、Mg2++2OH-=Mg(OH) ↓,故答案为是:CO2-+Ca2+=CaCO ↓、Mg2+
3 3 2 3 3
+2OH-=Mg(OH) ↓;
2
(3)Cl-+Ag+=AgCl↓,白色沉淀不溶于HNO,滴加足量稀硝酸后再滴加AgNO 溶液,也产生白色沉淀,
3 3
说明自来水中含有Cl-。故答案为Cl-(或氯离子);Cl-+Ag+=AgCl↓,白色沉淀不溶于稀硝酸。
(4)确定实验②中滴加的NaCO 溶液已过量的检验方法是:取②步反应的滤液于试管,滴加足量盐酸,
2 3
如产生无色气泡,(或滴加CaCl 溶液,如产生白色沉淀),证明NaCO 溶液已过量;
2 2 3
故答案为取②步反应的滤液于试管,滴加足量盐酸,如产生无色气泡,(或滴加CaCl 溶液,如产生白色沉
2
淀),证明NaCO 溶液已过量。
2 3
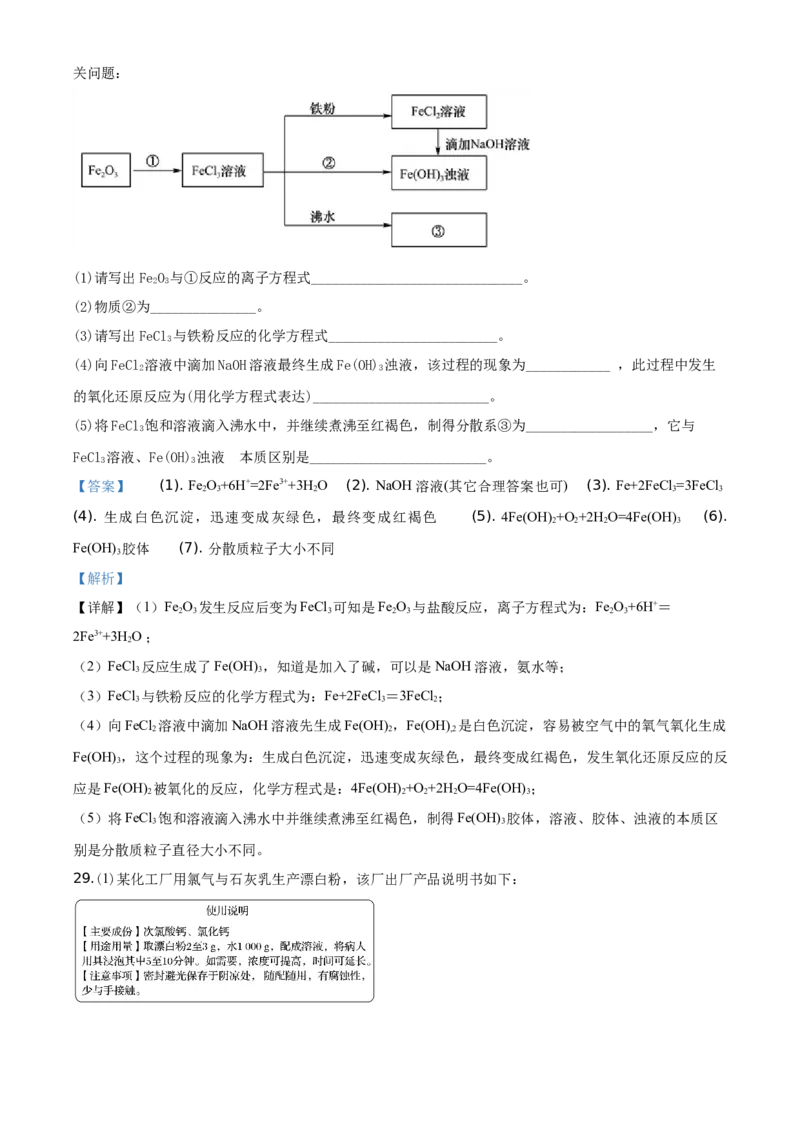
28.某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:
(1)请写出FeO 与①反应的离子方程式______________________________。
2 3
(2)物质②为_______________。
(3)请写出FeCl 与铁粉反应的化学方程式________________________。
3
(4)向FeCl 溶液中滴加NaOH溶液最终生成Fe(OH) 浊液,该过程的现象为____________ ,此过程中发生
2 3
的氧化还原反应为(用化学方程式表达)_________________________。
(5)将FeCl 饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为__________________,它与
3
FeCl 溶液、Fe(OH) 浊液 的本质区别是_________________________。
3 3
【答案】 (1). Fe O+6H+=2Fe3++3H O (2). NaOH溶液(其它合理答案也可) (3). Fe+2FeCl =3FeCl
2 3 2 3 3
(4). 生成白色沉淀,迅速变成灰绿色,最终变成红褐色 (5). 4Fe(OH) +O +2H O=4Fe(OH) (6).
2 2 2 3
Fe(OH) 胶体 (7). 分散质粒子大小不同
3
【解析】
【详解】(1)Fe O 发生反应后变为FeCl 可知是Fe O 与盐酸反应,离子方程式为:Fe O+6H+=
2 3 3 2 3 2 3
2Fe3++3H O ;
2
(2)FeCl 反应生成了Fe(OH) ,知道是加入了碱,可以是NaOH溶液,氨水等;
3 3
(3)FeCl 与铁粉反应的化学方程式为:Fe+2FeCl =3FeCl ;
3 3 2
(4)向FeCl 溶液中滴加NaOH溶液先生成Fe(OH) ,Fe(OH) 是白色沉淀,容易被空气中的氧气氧化生成
2 2 ,2
Fe(OH) ,这个过程的现象为:生成白色沉淀,迅速变成灰绿色,最终变成红褐色,发生氧化还原反应的反
3
应是Fe(OH) 被氧化的反应,化学方程式是:4Fe(OH) +O +2H O=4Fe(OH) ;
2 2 2 2 3
(5)将FeCl 饱和溶液滴入沸水中并继续煮沸至红褐色,制得Fe(OH) 胶体,溶液、胶体、浊液的本质区
3 3
别是分散质粒子直径大小不同。
29.(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:①漂白粉长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式______,____。
②某实验室研究员将完全变质后的漂白粉溶于水,向其中加入足量稀硝酸,收集到标准状况下448 mL气
体,则该漂白粉中所含有效成份的质量为_____________(假设漂白粉中的其它成份不与硝酸反应)。
(2)将14 g NaO和NaO 的混合物加入足量的水中充分反应后,生成标准状况下的气体1.12 L,所得溶
2 2 2
液的体积为400 mL。试计算:原混合物中NaO的质量为______g,所得溶液的物质的量浓度为______
2
mol·L-1。
【答案】 (1). Ca(ClO) +HO+CO =CaCO +2HClO (2). 2HClO 2HCl+O↑ (3). 2.86 g
2 2 2 3 2
(4). 6.2 (5). 1.0
【解析】
【分析】
(1)①漂白粉长期露置在空气中与水、二氧化碳反应生成 HClO,HClO光照分解而变质;②漂白粉中所含
有效成份是次氯酸钙,完全变质后变成碳酸钙,向其中加入足量稀硝酸,生成二氧化碳,根据 Ca(ClO)~
2
CO 计算;
2
(2)根据生成的氧气的体积计算n(O),根据反应方程式2NaO+2HO=4Na++4OH-+O↑计算出过氧化钠的
2 2 2 2 2
物质的量,从而可计算出混合物中过氧化钠、氧化钠的质量;混合物溶于水后都生成NaOH,溶液中的溶
质是NaOH,根据Na原子守恒计算n(NaOH),最后计算c(NaOH)。
【详解】(1)①漂白粉长期置露在空气中会变质,是因为漂白粉与二氧化碳、水的反应生成次氯酸,次氯
酸容易分解,反应分别为Ca(ClO)+CO+HO=CaCO ↓+2HClO、2HClO 2HCl+O↑,故答案为
2 2 2 3 2
Ca(ClO)+CO+HO=CaCO ↓+2HClO;2HClO 2HCl+O↑;
2 2 2 3 2
②漂白粉中所含有效成份是次氯酸钙,完全变质后的漂白粉中含有碳酸钙,向其中加入足量稀硝酸,反应
生成二氧化碳,根据
Ca(ClO)~CaCO ~CO
2 3 2
.
143g 224L
m(Ca(ClO)) 0.448L
2
有m(Ca(ClO))= =2.86g,故答案为2.86g;
2
(2)n(O)= =0.05mol,根据反应2NaO+2HO=4Na++4OH-+O↑可知,混合物中过氧化钠的物
2 2 2 2 2质的量为:n(NaO)=2n(O)=0.05mol×2=0.1mol,则混合物中过氧化钠的质量为:m(NaO)=78g/
2 2 2 2 2
mol×0.1mol=7.8g,氧化钠的质量为:14g-7.8g=6.2g,n(NaO)= =0.1mol,
2
n(NaO)=0.1mol,混合物溶于水后都生成NaOH,溶液中的溶质是NaOH,根据Na原子守恒得所得溶液
2 2
中n(NaOH)=n(Na+)=2n(NaO)+2n(NaO)=2×(0.1+0.1)mol=0.4mol,c(NaOH)= =1.0 mol·L
2 2 2
-1,故答案为6.2;1.0。