文档内容
第五单元测试题
可能用到的相对原子质量:H-1、C-12、O-16 N-14 S-32
一.(32分)选择题(每题只有1个正确答案,将答案填入本题后的表格中。)
1.化学反应遵守质量守恒定律的原因在于反应前后( )
A.物质的种类没有改变 B.分子的种类没有改变
C.原子的种类、数目和质量都没有改变 D.分子的数目没有改变
2.下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中“ ”、“
”、“ ”分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的
化学计量数之比为( )
A.4∶1∶3 B.3∶1∶2 C.4∶1∶2 D.3∶1∶3
3.宣传科学知识,揭露伪科学,是我们的义务。下列各项中属于伪科学的是( )
A.用催化剂将水变为燃油(由碳氢元素组成)
B.使白磷在空气中自燃
C.用液氢发射火箭
D.用扫描隧道显微镜可观察到分子的图像
点燃
4.在2H +O 2HO的反应中,反应前后肯定发生变化的是 ( )
2 2 2
A.元素的种类 B.分子的种类 C.物质的质量总和 D.各种原子的数目
5.下列说法正确的是( )
A.10g酒精和50g水混匀后形成60g酒精溶液,这符合质量守恒定律
B.细铁丝在氧气中燃烧后,生成物质量比细铁丝的质量大,这不符合质量守恒定律
C.2L氢气和1L氧气反应,生成3L水
D.1g氢气和8g氧气恰好完全反应,生成9g水
6.化学方程式:S+O SO 的下列读法中,正确的是( )
2 2A.硫和氧气在点燃的条件下生成二氧化硫 B.硫加氧气点燃等于二氧化硫
C.硫元素和氧元素反应生成二氧化硫 D.硫原子加上氧分子点燃生成二氧化硫分子
7、下列化学方程式书写正确的是( )
点燃
A、Zn + HCl = ZnCl + H B、 4Fe + 3O = 2FeO
2 2 2 2 3
点燃
C、2KMnO KMnO + MnO + O ↑ D、S+O SO↑
4 2 4 2 2 2 2
8.在电解水的化学反应中,HO、H、O 的质量比为( )
2 2 2
A.9:1:16 B.9:1:8 C.9:2:8 D.10:1:9
9.已知化学反应:2A+B = 2C+D,当10g A和8g B刚好完全反应后,生成6g C。如果要得到3g
D,则参加反应的B物质的质量是( )
A.1g B.2g C.3g D.4g
10.已知反应3A+2B=2C+D,A、B两物质完全反应时,质量比为3:4。若生成C和D共140g,则
该反应消耗B的质量为 ( )
A.60g B.80g C.90g D.120g
11.葡萄糖在人体组织中缓慢氧化,放出热量,供给人们所需能量,是人类生命活动所需能量
的重要来源之一。若R代表葡萄糖,所发生的氧化反应为R+6O 6CO+6HO,则葡萄糖的化
2 2 2
学式为 ( )
A.CH B.CH O C.CH O D.CHO
6 12 6 12 6 6 10 5 5 6 2
12.在化学反应xM+yN = mP+nQ中,下列说法正确的是( )
A.若M、P为单质,N、Q为化合物,则该反应不一定是置换反应
B.化学计量数x与y之和一定等于m与n的和
C.若取ag M和ag N反应,生成P和Q的质量总和不一定是2ag
D.反应物M和N的质量比一定等于生成物P和Q的质量比
13.在密闭容器中加热蔗糖可产生碳和水,由此可以说明( )
A.蔗糖是由碳和水组成的纯净物 B.蔗糖是由碳和水组成的混合物
C.蔗糖分子是由碳元素和水分子构成的 D.蔗糖是由碳元素、氢元素和氧元素组成
的
14.镁带在耐高温的密闭容器中(内含空气)加热,则下列图中能正确表示容器内所盛物质总
质量变化的是( )15.将20g H、O、N 的混合气体点燃,完全反应后生成18gHO,则剩余的气体不可能是( )
2 2 2 2
A.H 和N B.O 和N C.H、O 和N D.2g N
2 2 2 2 2 2 2 2
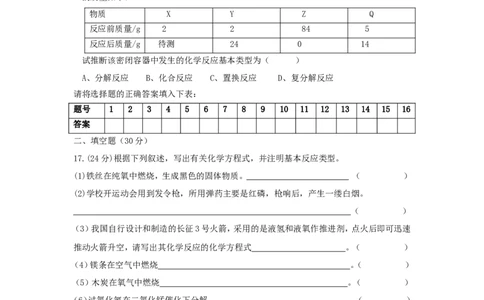
16、在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质
的质量如下:
物质 X Y Z Q
反应前质量/g 2 2 84 5
反应后质量/g 待测 24 0 14
试推断该密闭容器中发生的化学反应基本类型为( )
A、分解反应 B、化合反应 C、置换反应 D、复分解反应
请将选择题的正确答案填入下表:
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
答案
二、填空题(30分)
17.(24分)根据下列叙述,写出有关化学方程式,并注明基本反应类型。
(1)铁丝在纯氧中燃烧,生成黑色的固体物质。 ( )
(2)学校开运动会用到发令枪,所用弹药主要是红磷,枪响后,产生一缕白烟。
( )
(3)我国自行设计和制造的长征3号火箭,采用的是液氢和液氧作推进剂,点火后即可迅速
推动火箭升空,请写出其化学反应的化学方程式 。( )
(4)镁条在空气中燃烧 。( )
(5)木炭在氧气中燃烧 。( )
(6)过氧化氢在二氧化锰催化下分解 。( )
(7)加热高锰酸钾 。( )
(8)加热氯酸钾和二氧化锰的混合物 。( )
18. (6分)一氧化氮是大气的主要污染物之一。近几年来,又发现在生物体内存在少量的一
氧化氮,它有扩张血管和增强记忆力的功能,成为当前生命科学研究的热点。
⑴一氧化氮是工业制硝酸的中间产物,生成一氧化氮反应的化学方程式为:
催化剂
4X+5O 4NO+6HO,根据质量守恒定律推断,X的化学式为 。
2 2
⑵汽车尾气中含有一氧化氮、一氧化碳等有毒气体,治理的方法是在汽车尾气的排风管上装一个催化转换器,在催化剂的作用下,一氧化氮与一氧化碳反应可生成二氧化碳和氮气,该
反应的化学方程式为: 。
⑶市售打火机里装的不是汽油,而是液体丁烷(CH ),丁烷在空气中燃烧后产生二氧化碳和
4 10
水蒸气,写出丁烷完全燃烧的化学方程式 。
三.简答题:(24分)
19、(10分)无色液体A在一定的条件下可分解成B、C两种气体,将点燃的硫放人B中,则燃
烧更旺,发出明亮的蓝紫色火焰,生成一种有刺激性气味的气体D。将C通过加热的氧化铜,
则生成A和E。
(1)由此可推断(填化学式):A是:( )B是:( ) C 是:( ) D 是:( )
(2)写出下列化学方程式:A → B + C ___________________________________
点燃的硫放人B中 ____________________ _______________
C + CuO → A + E _______________________________ ________
20.、(6分)将16g硫在给定质量的氧气中燃烧,某同学记录的实验数据如下表所示:
组别 1 2 3 4 5 6
给定O 的质量/g 10 15 16 20 24 32
2
生成SO 的质量/g 20 30 32 32 48 32
2
⑴观察、分析表中数据,有明显误差的是哪一组? 。
⑵分析正确数据,由此可得出哪些结论?(至少写二条)
21、(4分)早在17世纪,质量守恒定律被发现之前,英国化学家波义耳做过一个实验:在密
闭的玻璃容器中燃烧金属时,得到了金属灰,然后称量金属灰的质量,发现比原金属质量增
加了。
(1)试解释金属灰质量比原金属质量增加的原因。
(2)由于波义耳称量方法上的原因,他错过了发现质量守恒定律的机会。请你改进他的称量
方法,以验证质量守恒定律。
气球
22、(4分)如右图所示,反应前天平平衡,取下此装置
(装置气密性良好)将其倾斜,使稀盐酸与碳酸钠接触, 稀盐酸
大理石
待充分反应后,气球膨胀,再将装置放回天平左盘,
天平的指针向右偏转。这一现象是否遵守质量守恒定律?
为什么?四、我会计算:(14分)
23、(6分)电解5.4g水生成氢气多少克?同时生成氧气多少克?生成的氢气在标准状况下
的体积是多少?(氢气密度为0.09g/L)
24、(8分)现有氯酸钾和二氧化锰的混合物共26.5g,待反应不再有气体生成后,将试管冷却、
称量,得到剩余固体16.9g。求:
⑴制取氧气的质量。
⑵剩余固体中含有哪些物质?各为多少克?参考答案
一.(32分)选择题(每题只有1个正确答案,将答案填入本题后的表格中。)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
答案 C B A B D A C B B B B C D B C A
二、填空题(30分)
17.(1) 3Fe+ 2O FeO(化合反应 )
2 3 4
(2)4P+ 5O 2PO(化合反应)
2 2 5
(3)2H + O 2HO(化合反应)
2 2 2
(4)2Mg+ O 2MgO(化合反应)
2
(5)C+O CO(化合反应)
2 2
(6) 2HO 2HO+O(分解反应)
2 2 2 2
(7)2KMnO KMnO + MnO +O(分解反应)
4 2 4 2 2
(8)2KClO 2KCl+3O (分解反应)
3 2
18. (6分)
催化剂
(1)4X+5O 4NO+6HO, ,X的化学式为 N H 。
2 2 3
⑵
催化剂
2CO+2NO===2CO+N。
2 2
⑶2CH +13O 8CO+10HO
4 10 2 2 2
三.简答题:(24分)
19、(10分)
(1)由此可推断(填化学式):A是:(HO)B是:(O) C 是:(H) D 是:(SO)
2 2 2 2
(2)2HO 2H + O S+O SO CuO+H Cu+HO
2 2 2 2 2 2 2
20.(6分) 第 5 组 。
⑵1、参加反应和各物质质量总和等于反应后生成的各物质质量总和
2、参加反应的硫和氧气及生成的二氧化硫的质量比为1:1:2.21、
( 1 )答:金属燃烧时有空气中氧气参加反应
( 2 )称量反应前各物质的质量总和;反应后称量各物质的质量总和
22、(4分)答:这一现象是遵守质量守恒定律的,参加反应的物质及生成的物质没有遗漏。天
平不衡是因为 N aCO+2HCl=2NaCl+HO+CO↑,其中生成的气体使气球鼓起,因此空气对气球
2 3 2 2
产生了浮力,所以天平的指针向右偏转。
四、我会计算:(14分)
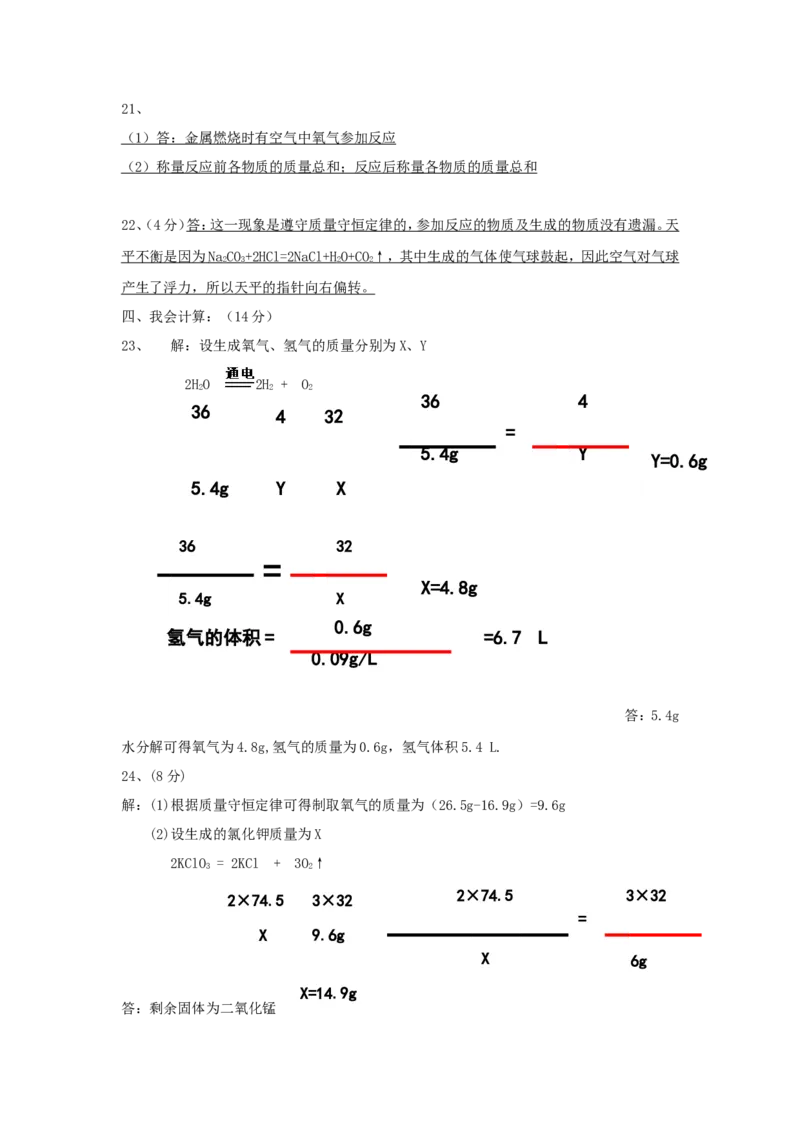
23、 解:设生成氧气、氢气的质量分别为X、Y
2HO 2H + O
2 2 2
36 4
36
4 32
=
5.4g Y
Y=0.6g
5.4g Y X
36 32
=
X=4.8g
5.4g X
0.6g
氢气的体积= =6.7 L
0.09g/L
答:5.4g
水分解可得氧气为4.8g,氢气的质量为0.6g,氢气体积5.4 L.
24、(8分)
解:(1)根据质量守恒定律可得制取氧气的质量为(26.5g-16.9g)=9.6g
(2)设生成的氯化钾质量为X
2KClO = 2KCl + 3O↑
3 2
2×74.5 3×32
2×74.5 3×32
=
X 9.6g
X 9.6g
X=14.9g
答:剩余固体为二氧化锰和氯化钾,其中氯化钾质量为14.9g二氧化锰质量为(16.9g-14.9g)=2g