文档内容
第5讲 溶 液
第1课时 溶液的形成及溶解度
一、选择题
1.(2015,上海)生活中常见的物质属于溶液的是(C)
A.草莓酱 B.蒸馏水
C.蔗糖水 D.玉米糊
2.(2015,眉山)关于溶液的说法正确的是(D)
A.溶液都是无色透明的
B.水可以溶解任何物质
C.均一、稳定的液体都是溶液
D.饱和溶液不一定是浓溶液
3.(2014,莱芜)下列叙述中错误的是(C)
A.食用油溶于汽油,食用油是溶质,汽油是溶剂
B.洗涤剂去除油污是利用了乳化作用
C.稀溶液一定是不饱和溶液
D.硝酸铵溶于水,溶液温度明显降低
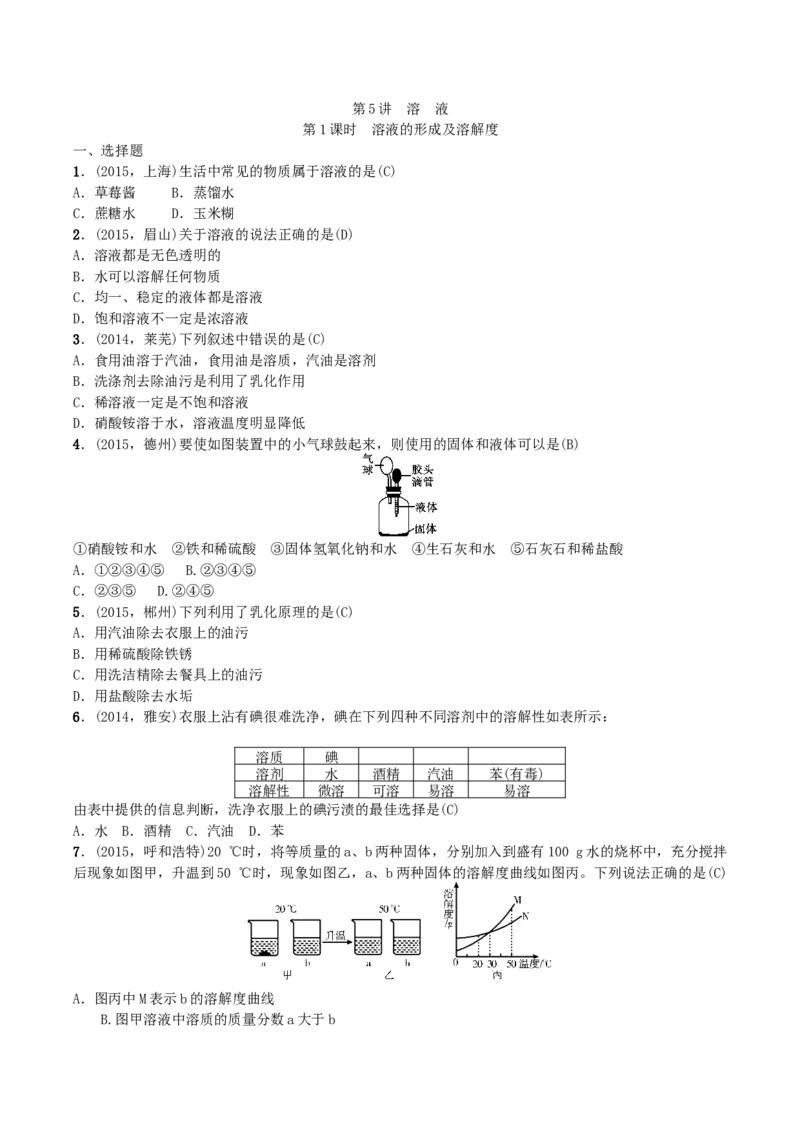
4.(2015,德州)要使如图装置中的小气球鼓起来,则使用的固体和液体可以是(B)
①硝酸铵和水 ②铁和稀硫酸 ③固体氢氧化钠和水 ④生石灰和水 ⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.②③⑤ D.②④⑤
5.(2015,郴州)下列利用了乳化原理的是(C)
A.用汽油除去衣服上的油污
B.用稀硫酸除铁锈
C.用洗洁精除去餐具上的油污
D.用盐酸除去水垢
6.(2014,雅安)衣服上沾有碘很难洗净,碘在下列四种不同溶剂中的溶解性如表所示:
溶质 碘
溶剂 水 酒精 汽油 苯(有毒)
溶解性 微溶 可溶 易溶 易溶
由表中提供的信息判断,洗净衣服上的碘污渍的最佳选择是(C)
A.水 B.酒精 C.汽油 D.苯
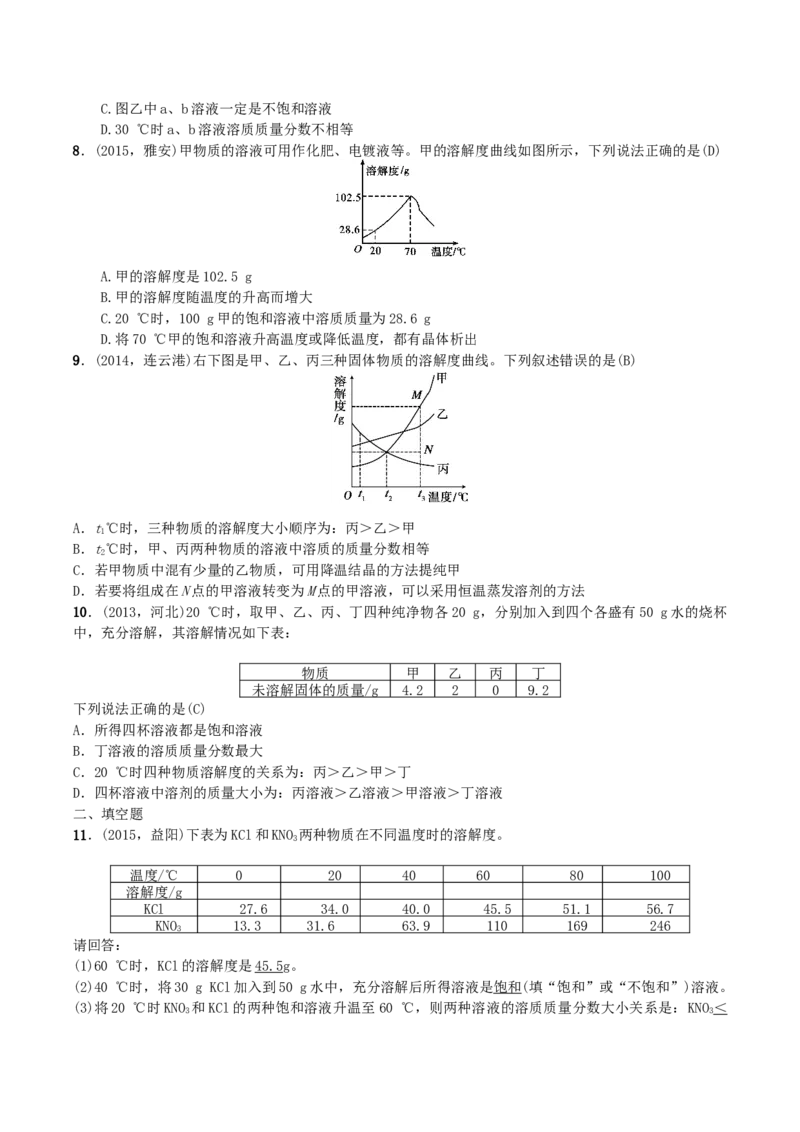
7.(2015,呼和浩特)20 ℃时,将等质量的a、b两种固体,分别加入到盛有100 g水的烧杯中,充分搅拌
后现象如图甲,升温到50 ℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是(C)
A.图丙中M表示b的溶解度曲线
B.图甲溶液中溶质的质量分数a大于bC.图乙中a、b溶液一定是不饱和溶液
D.30 ℃时a、b溶液溶质质量分数不相等
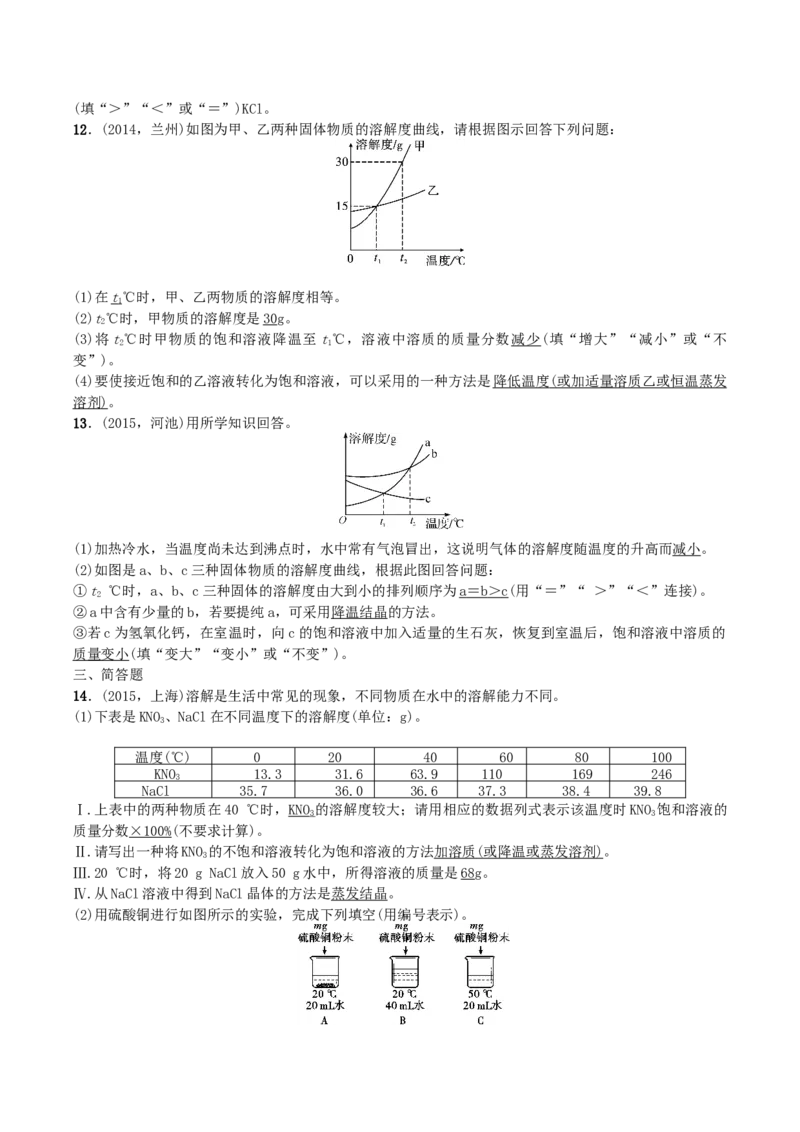
8.(2015,雅安)甲物质的溶液可用作化肥、电镀液等。甲的溶解度曲线如图所示,下列说法正确的是(D)
A.甲的溶解度是102.5 g
B.甲的溶解度随温度的升高而增大
C.20 ℃时,100 g甲的饱和溶液中溶质质量为28.6 g
D.将70 ℃甲的饱和溶液升高温度或降低温度,都有晶体析出
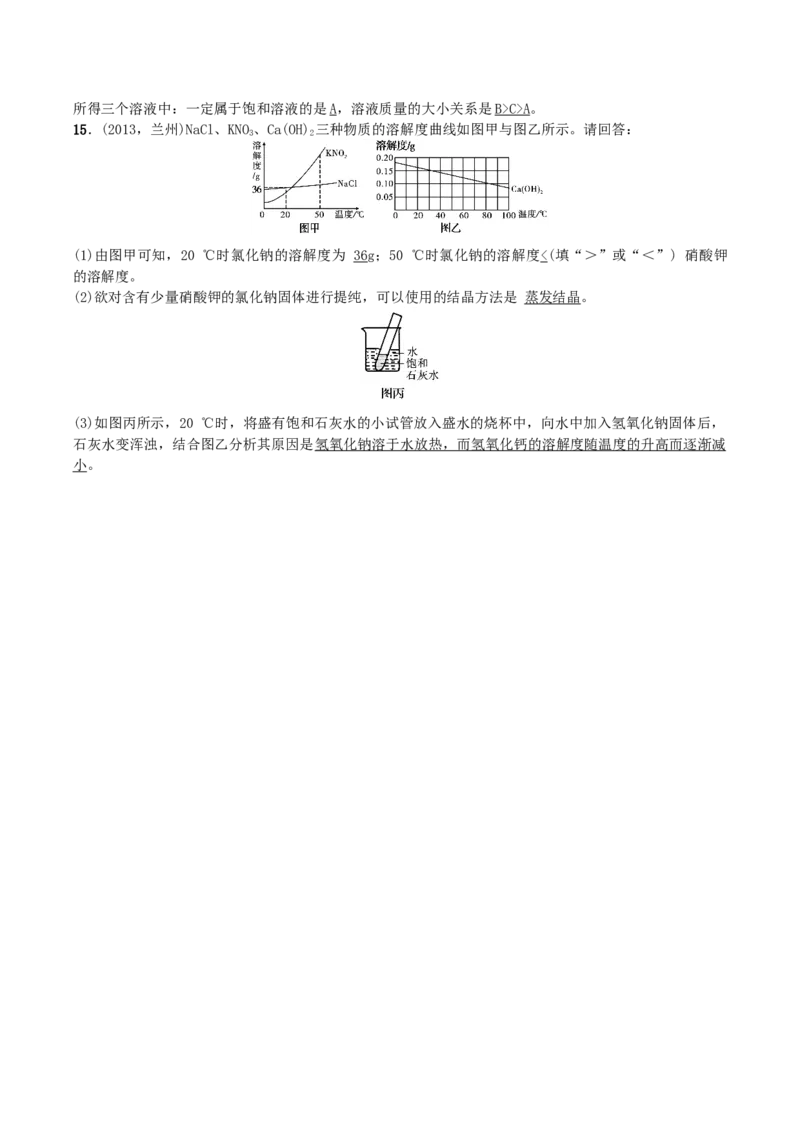
9.(2014,连云港)右下图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述错误的是(B)
A.t℃时,三种物质的溶解度大小顺序为:丙>乙>甲
1
B.t℃时,甲、丙两种物质的溶液中溶质的质量分数相等
2
C.若甲物质中混有少量的乙物质,可用降温结晶的方法提纯甲
D.若要将组成在N点的甲溶液转变为M点的甲溶液,可以采用恒温蒸发溶剂的方法
10.(2013,河北)20 ℃时,取甲、乙、丙、丁四种纯净物各20 g,分别加入到四个各盛有50 g水的烧杯
中,充分溶解,其溶解情况如下表:
物质 甲 乙 丙 丁
未溶解固体的质量/g 4.2 2 0 9.2
下列说法正确的是(C)
A.所得四杯溶液都是饱和溶液
B.丁溶液的溶质质量分数最大
C.20 ℃时四种物质溶解度的关系为:丙>乙>甲>丁
D.四杯溶液中溶剂的质量大小为:丙溶液>乙溶液>甲溶液>丁溶液
二、填空题
11.(2015,益阳)下表为KCl和KNO 两种物质在不同温度时的溶解度。
3
温度/℃ 0 20 40 60 80 100
溶解度/g
KCl 27.6 34.0 40.0 45.5 51.1 56.7
KNO 13.3 31.6 63.9 110 169 246
3
请回答:
(1)60 ℃时,KCl的溶解度是45.5g。
(2)40 ℃时,将30 g KCl加入到50 g水中,充分溶解后所得溶液是饱和(填“饱和”或“不饱和”)溶液。
(3)将20 ℃时KNO 和KCl的两种饱和溶液升温至60 ℃,则两种溶液的溶质质量分数大小关系是:KNO <
3 3(填“>”“<”或“=”)KCl。
12.(2014,兰州)如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:
(1)在t℃时,甲、乙两物质的溶解度相等。
1
(2)t℃时,甲物质的溶解度是30g。
2
(3)将t℃时甲物质的饱和溶液降温至t℃,溶液中溶质的质量分数减少(填“增大”“减小”或“不
2 1
变”)。
(4)要使接近饱和的乙溶液转化为饱和溶液,可以采用的一种方法是 降低温度 ( 或加适量溶质乙或恒温蒸发
溶剂 )。
13.(2015,河池)用所学知识回答。
(1)加热冷水,当温度尚未达到沸点时,水中常有气泡冒出,这说明气体的溶解度随温度的升高而减小。
(2)如图是a、b、c三种固体物质的溶解度曲线,根据此图回答问题:
①t ℃时,a、b、c三种固体的溶解度由大到小的排列顺序为 a = b > c(用“=”“ >”“<”连接)。
2
②a中含有少量的b,若要提纯a,可采用降温结晶的方法。
③若c为氢氧化钙,在室温时,向c的饱和溶液中加入适量的生石灰,恢复到室温后,饱和溶液中溶质的
质量变小(填“变大”“变小”或“不变”)。
三、简答题
14.(2015,上海)溶解是生活中常见的现象,不同物质在水中的溶解能力不同。
(1)下表是KNO、NaCl在不同温度下的溶解度(单位:g)。
3
温度(℃) 0 20 40 60 80 100
KNO 13.3 31.6 63.9 110 169 246
3
NaCl 35.7 36.0 36.6 37.3 38.4 39.8
Ⅰ.上表中的两种物质在40 ℃时,KNO 的溶解度较大;请用相应的数据列式表示该温度时KNO 饱和溶液的
3 3
质量分数×100%(不要求计算)。
Ⅱ.请写出一种将KNO 的不饱和溶液转化为饱和溶液的方法 加溶质 ( 或降温或蒸发溶剂 )。
3
Ⅲ.20 ℃时,将20 g NaCl放入50 g水中,所得溶液的质量是68g。
Ⅳ.从NaCl溶液中得到NaCl晶体的方法是蒸发结晶。
(2)用硫酸铜进行如图所示的实验,完成下列填空(用编号表示)。所得三个溶液中:一定属于饱和溶液的是A,溶液质量的大小关系是B>C>A。
15.(2013,兰州)NaCl、KNO、Ca(OH) 三种物质的溶解度曲线如图甲与图乙所示。请回答:
3 2
(1)由图甲可知,20 ℃时氯化钠的溶解度为 36g;50 ℃时氯化钠的溶解度<(填“>”或“<”) 硝酸钾
的溶解度。
(2)欲对含有少量硝酸钾的氯化钠固体进行提纯,可以使用的结晶方法是 蒸发结晶。
(3)如图丙所示,20 ℃时,将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入氢氧化钠固体后,
石灰水变浑浊,结合图乙分析其原因是氢氧化钠溶于水放热,而氢氧化钙的溶解度随温度的升高而逐渐减
小。第2课时 溶液的浓度
一、选择题
1.(2014,广州)将50 g 98%的浓硫酸溶于450 g水中,所得溶液中溶质的质量分数为(A)
A.9.8% B.10.2% C.10.8% D.19.6%
2.(2015,福州)实验室用硝酸钾固体配制100.0 g溶质质量分数为3.0%的硝酸钾溶液,下列说法正确的
是(D)
A.用50 mL量筒量水
B.将固体放于托盘天平的右盘称取
C.将固体直接投入量筒中溶解
D.将配好的溶液装入贴有标签(如图)的试剂瓶中,塞好瓶塞
3.(2013,庆阳)某同学在实验室配制50 g 6%的氯化钠溶液,下图所示的部分操作其中错误的是(C)
4.(2014,苏州)下列有关“配制50 g溶质质量分数为6%的氯化钠溶液”的操作错误的是(C)
A.使用托盘天平前,要先取下支撑托盘的垫圈,再调节天平平衡
B.称取氯化钠前,要在天平两端的托盘上分别放质量相同的纸片
C.移动游码使其右侧对齐3 g的刻度线,然后将氯化钠加到天平的右盘上
D.取用规格为50 mL的量筒量取47 mL水,快到所需刻度时改用胶头滴管定容
5.配制溶质质量分数为5%的下列溶液,能达到目的是(A)
A.称取5.0 g氯化钾,溶解在95 mL水中,充分搅拌
B.称取5.0 g生石灰,放入95 mL水中,充分搅拌
C.量取5.0 mL浓盐酸,倒入95 mL水中,充分搅拌
D.称取5.0 g碳酸钙,放入95 mL水中,充分搅拌
二、填空题
6.(2014,泉州)“84消毒液”广泛应用于物体表面的消毒,其有效成分是次氯酸钠。
(1)配制50 g溶质质量分数为12%的次氯酸钠溶液中,需要固体次氯酸钠6g,水44mL。
(2)可将上述溶液稀释成溶质质量分数为0.2%的次氯酸钠溶液3_000g。
7.右图为A、B两种固体物质的溶解度曲线。请回答下列问题:
(1)t ℃时,A物质的溶解度=_(填“>”“<”或“=”) B物质的溶解度。
1
(2)将t ℃时A、B两物质的饱和溶液降温到t ℃(其他条件不变),没有晶体析出的是B 物质。
2 1(3)t ℃时,有一接近饱和的B溶液,可采取 升温 ( 或加入 B 溶质或蒸发适量水 )(任写一种)的方法,使它
2
变为饱和溶液。
(4)t ℃时,将30 g A物质投入100 g水中,充分搅拌后,所得溶液中溶质质量分数是20%。
2
8.(2015,天津)利用海水提取粗盐的过程如图所示,回答有关问题。
(1)一定质量的海水,通过贮水池引入到蒸发池,在没有引入结晶池之前的蒸发过程中,蒸发池中氯化钠
的质量会不变(填“增大”“不变”或“减小”)。
(2)粗盐中含有的难溶性杂质,在实验室里可以通过溶解、过滤、蒸发等操作将其去除,这些操作中都会
用到玻璃棒,其中在过滤操作中玻璃棒的作用是引流(填“引流”或“加快溶解”)。
(3)用氯化钠固体配制100 g质量分数为6%的氯化钠溶液。
①配制时,涉及以下实验步骤:A.称量及量取;B.计算;C.溶解;D.装瓶贴标签。其正确的实验步骤顺序
是BACD(填字母)。
②将已配好的100 g质量分数为6%的氯化钠溶液变成质量分数为16%的氯化钠溶液,需要再加NaCl的质量
是11.9g(计算结果精确到0.1)。
9.(2015,滨州)如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图:
(1)用图中序号表示配制溶液的正确操作顺序②⑤①④③。
(2)图②中用来取用NaCl的仪器是药匙。
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示位置见图,则称取的NaCl质量为18.2g。
(4)NaCl称量完毕放回砝码时,发现10 g的砝码有缺损,若其他操作步骤均正确,则所配制溶液的质量分
数小于(填“大于”“小于”或“等于”)10%。
10.(2014,绵阳)如图是甲、乙两种固体物质在水中的溶解度曲线。
(1)t℃时,甲的溶解度<(填“<”“>”或“=”)乙的溶解度。
1
(2)将t℃时甲、乙的饱和溶液分别升温至t ℃,甲溶液中溶质的质量分数将不变,乙溶液中溶质的质量
2 3
分数将减小。(均填“增大”“减小”或“不变”)
(3)t ℃时,甲的饱和溶液中溶质的质量m 与乙的饱和溶液中溶质的质量m 相比较,两者的大小关系是
2 甲 乙
D(填字母)。
A.m >m B.m <m
甲 乙 甲 乙
C.m =m D.不确定
甲 乙
11.(2015,呼和浩特)(1)已知:水的密度为1.0 g/mL。实验室配制50 g溶质质量分数为5%的氯化钠溶液,
需要称取氯化钠2.5 g,需要量取水47.5_mL。
(2)配制的操作示意图如下,该实验的正确操作顺序为CBDEA(填字母)。(3)经检测,所配制溶液的溶质质量分数偏小,其原因可能是①②③(填序号)。
①氯化钠固体不纯 ②称量时,砝码端忘垫质量相同的纸片 ③量取水时,仰视读数 ④装瓶时,有少量
溶液洒出
12.(2015,广州)配制并稀释一定质量分数的NaSO 溶液。
2 4
(1)配制50 g质量分数为6%的NaSO 溶液。
2 4
①计算:需要NaSO 3.0 g,水 47.0 g。
2 4
②称量:用托盘天平称量3.0 g的NaSO 。天平调零后,分别在天平左右托盘放上质量相同的纸片,先移
2 4
动游码到 3. 0_g,然后 慢慢加入 N aSO,至托盘天平恰好平衡。
2 4
③量取:用量筒量取47.0 mL水。请在如图中画出47.0 mL水的液面位置。
④溶解。
(2)稀释溶液。(由于整个配制过程中溶液很稀,其密度可近似看作1 g/mL)
①取1 mL 6%的NaSO 溶液加水稀释至100 mL,得到溶液a;
2 4
②若用3.0 g NaSO 配制与溶液a浓度相同的溶液,其体积是5_000mL。
2 4
三、计算题
13.(2013,孝感)盐水选种是我国古代劳动人民发明的一种巧妙的挑选种子的方法。农业生产上常用质量
分数为15%~20%的氯化钠溶液来选种。
(1)要配制200 kg 18%的氯化钠,计算应称取氯化钠的质量。
(2)选种进行一段时间后,农技员估计溶液和溶质质量分数都有所减少,他取出45 g氯化钠溶液,加入过
量的AgNO 溶液,得到沉淀14.35 g,计算氯化钠溶液中溶质的质量分数。
3
(反应原理:NaCl+AgNO===AgCl↓+NaNO;相对原子质量Na-23 N-14 O-16 Cl-35.5
3 3
Ag-108)
解:(1)200 kg×18%=36 kg
(2)设溶液中氯化钠的质量为x。
NaCl+AgNO===AgCl↓+NaNO
3 3
58.5 143.5
x 14.35 g
= x=5.85 g
氯化钠溶液中溶质质量分数=×100%=13%