文档内容
硝酸及硝酸与金属反应的计算
【学习目标】
1、掌握硝酸的性质和用途,熟悉硝酸的强氧化性
2、掌握硝酸与金属反应计算技巧——电子守恒法、原子守恒法、电荷守恒法
【主干知识梳理】
一、硝酸
1、物理性质
纯硝酸是无色、易挥发(沸点为83℃)、有刺激性气味的液体,常用浓HNO 的质量分数为69%,能跟水以任
3
意比互溶,打开盛浓硝酸的试剂瓶盖,有白雾产生(与浓盐酸相同)。质量分数为98%以上的浓硝酸挥发出来
的HNO 蒸气遇空气中的水蒸气形成极微小的硝酸液滴而产生“发烟现象”。因此,质量分数为98%以上的
3
浓硝酸通常叫做“发烟硝酸”
2、化学性质
(1)酸性:属于强酸,溶于水完全电离:HNO ===H++NO -,具有酸的通性,能与碱、碱性氧化物、某些盐反
3 3
应
CaCO 与HNO 反应:CaCO +2HNO (稀)===Ca(NO ) +CO ↑+HO (若无稀盐酸可用稀硝酸代替室制
3 3 3 3 3 2 2 2
CO)
2
【微点拨】
①稀硝酸使石蕊试液变红色,浓硝酸使紫色石蕊试液先变红后褪色(酸性和强氧化性)
②硝酸具有酸的一些通性,但硝酸与活泼金属反应时无氢气产生
(2)不稳定性:硝酸见光或受热易发生分解,HNO 越浓,越易分解,温度越高分解越快,光照越强分解越快
3
4HNO 4NO ↑+O↑+2HO
3 2 2 2
【微点拨】
①实验室中浓硝酸显黄色的原因:浓硝酸分解生成的NO 又溶于硝酸所致。消除黄色的方法是向浓硝酸中通
2
入空气或O,发生反应为4NO +O+2HO===4HNO
2 2 2 2 3
②硝酸一般保存在棕色试剂瓶中,并放置在阴凉处
(3)强氧化性:HNO 中的+5价氮元素具有很强的得电子能力。硝酸的浓度越大,反应温度越高,其氧化性越强。
3
还原产物一般为:HNO (浓)→NO,HNO (稀)→NO;很稀的硝酸还原产物也可能为NO、N 或NH NO
3 2 3 2 2 4 3
①硝酸与金属的反应:硝酸与金属反应时,硝酸既表现氧化性又表现酸性
金属与硝酸反应规律
a.除Au、Pt等少数金属外,硝酸几乎可以氧化所有的金属
3Ag+4HNO(稀)===3AgNO +NO↑+2HO
3 3 2
b.活泼金属与硝酸反应不生成 H ,硝酸的浓度不同,还原产物不同,可能是NO 、NO、NO、N 、
2 2 2 2
NH NO
4 3
如:4Mg+10HNO (稀)===4Mg (NO)+NH NO +3HO
3 3 2 4 3 2
c.铜与浓、稀硝酸反应
Cu+4HNO (浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
浓硝酸与铜反应 该反应较剧烈,反应过程中有红棕色气体产生,此外,随着反应的进行,
硝酸的浓度渐渐变稀,反应产生的气体是NO 、NO等的混合气体
2
3Cu+8HNO (稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
稀硝酸与铜反应 该反应较缓慢,反应后溶液显蓝色,反应产生的无色气体遇到空气后变为
红棕色(无色的NO被空气氧化为红棕色的NO )
2
d.与Fe、Al反应:常温下,浓硝酸能使Fe、A1发生钝化,这是因为浓硝酸将Fe、A1表面氧化,使Fe、
A1的表面形成一层致密的氧化物薄膜,阻止了反应的进一步进行。常温下,可用铁或铝制容器盛放浓硝酸,但要注意密封,以防止硝酸挥发变稀后与铁、铝反应。当加热时,加热时可以与Fe、Al发生反应
铁在加热时,与过量的浓硝酸反应:Fe+6HNO (浓) Fe(NO)+3NO ↑+3HO
3 3 3 2 2
e.铁与稀硝酸反应:先生成Fe(NO ),若Fe过量,Fe(NO ) 再与Fe反应生成Fe(NO )
3 3 3 3 3 2
Fe(少量)+4HNO(稀===Fe(NO )+NO↑+2HO
3 3 3 2
3Fe(过量)+8HNO(稀)===3Fe(NO )+2NO↑+4HO
3 3 2 2
f.王水是浓硝酸和浓盐酸按体积比1∶3 的混合物,能使一些不溶于硝酸的金属如金、铂等溶解
②硝酸与非金属的反应:硝酸与非金属反应时,硝酸只表现出氧化性
金属与非硝酸反应规律 非金属单质+浓硝酸 最高价氧化物或其含氧酸+NO ↑+HO
2 2
a.木炭与浓硝酸反应:C+4HNO (浓) CO ↑+4NO ↑+2HO
3 2 2 2
b.硫与浓硝酸反应:S + 6HNO (浓) HSO +6 NO ↑+4H O
3 2 4 2 2
c.红磷与浓硝酸反应:P + 5HNO (浓) HPO+5 NO ↑+H O
3 3 4 2 2
d.白磷与浓硝酸反应:P + 20HNO (浓) 4HPO+20 NO ↑+4H O
4 3 3 4 2 2
③硝酸与还原性化合物的反应:硝酸可氧化HS、SO 、NaSO 、HI(I—)、Fe2+、FeO等还原性物质
2 2 2 3
a.稀硝酸与HS反应的离子方程式:3HS+2HNO (稀)===3S↓+2NO↑+4HO
2 2 3 2
b.稀硝酸与SO 反应的离子方程式:3SO +2NO -+2HO===3SO 2-+2NO↑+4H+
2 2 3 2 4
c.稀硝酸与NaSO 反应的离子方程式:3SO 2-+2NO -+2H+===3SO 2-+2NO↑+HO
2 3 3 3 4 2
d.稀硝酸与HI反应的离子方程式:6I-+2NO -+8H+===3I+2NO↑+4HO
3 2 2
e.稀硝酸与Fe2+反应的离子方程式:3Fe2++NO -+4H+===3Fe3++NO↑+2HO
3 2
f.稀硝酸与FeO反应的离子方程式:3FeO+NO -+10H+===3Fe3++NO↑+5HO
3 2
④NO-无氧化性,而当NO -在酸性溶液中时,则具有强氧化性
3 3
a.在Fe(NO ) 溶液中加入盐酸或硫酸,因引入了H+而使Fe2+被氧化为Fe3+
3 2
b.过量的Cu与浓硝酸反应,待反应停止后,再加入稀盐酸或硫酸,此时铜片上有无色气体生成,这是因
为:加入的稀盐酸或硫酸电离出的H+与Cu(NO ) 中的NO -结合具有强氧化性,能使Cu继续溶解
3 2 3
c.铜片与稀硝酸、稀硫酸反应3Cu+2HNO +3HSO ===3CuSO +2NO↑+4HO
3 2 4 4 2
⑤能氧化并腐蚀某些有机物,如皮肤、衣服、纸张、橡胶等。因此在使用硝酸(尤其是浓硝酸)时要特别小心,
万一不慎将浓硝酸弄到皮肤上,应立即用大量水冲洗,再用小苏打或肥皂液洗涤
3、用途:硝酸是一种重要的化工原料,可用于制造炸药、染料、塑料、硝酸盐、氮肥等
4、硝酸的保存方法:硝酸易挥发,见光或受热易分解,具有强氧化性而腐蚀橡胶,因此,实验室保存硝酸时,
应将硝酸保存在棕色、细口、磨口玻璃塞的玻璃试剂瓶中,并放置在黑暗且温度较低的地方
5、硝酸的制法
(1)硝酸的实验室制法
原理:NaNO +HSO (浓) NaHSO +HNO ↑ (利用浓HSO 的高沸点,难挥发性制取挥发性的HNO )
3 2 4 4 3 2 4 3
因HNO 不稳定,加热温度不宜过高;由于硝酸易腐蚀橡胶,因此该反应禁用橡胶塞,所用仪器为曲颈甑
3
(2)硝酸的工业制法
流程示意图
将氨和空气的混合气(氧∶氮≈2∶1)通入灼热(760~840 ℃)的铂铑合金网,在合金网的催
主要流程 化作用下,氨被氧化成一氧化氮(NO),生成的一氧化氮结合反应后残余的氧气继续被
氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸
各步反应的化
4NH +5O=====4NO+6HO,2NO+O===2NO,3NO +HO===2HNO +NO
学方程式 3 2 2 2 2 2 2 3
尾气吸收 NO +NO+2NaOH===2NaNO + H O,2NO + 2NaOH===NaNO + NaNO + H O
2 2 2 2 2 3 2
【对点训练1】
1、下列关于硝酸的叙述正确的是( )
A.常温下,浓硝酸可以使金属镁钝化 B.稀硝酸与活泼金属反应主要放出氢气C.浓硝酸和稀硝酸都是强氧化剂 D.室温下,铜能与浓硝酸反应,不能与稀硝酸反应
2、下列有关浓硝酸的说法中不正确的是( )
A.实验室常用浓硝酸与金属锌反应制备氢气 B.常温下浓硝酸能使金属铝钝化
C.浓硝酸不稳定,见光易分解,需要避光保存 D.浓硝酸易挥发,打开瓶塞,瓶口有白雾产生
3、取三张蓝色石蕊试纸湿润后贴在玻璃片上,然后按顺序分别滴加浓硝酸、98.3%的浓硫酸、新制氯水,三张
试纸最终变成( )
A.白、红、白 B.红、黑、白 C.红、红、红 D.白、黑、白
4、下列实验事实与硝酸性质不相对应的一组是( )
A.稀硝酸使紫色石蕊溶液变红——酸性 B.铁与稀硝酸反应不能放出氢气——强氧化性
C.要用棕色试剂瓶盛装浓硝酸——不稳定性 D.氢氧化亚铁固体与稀硝酸混合——仅强酸性
5、将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是( )
A.反应剧烈程度:两者相同
B.消耗硝酸的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
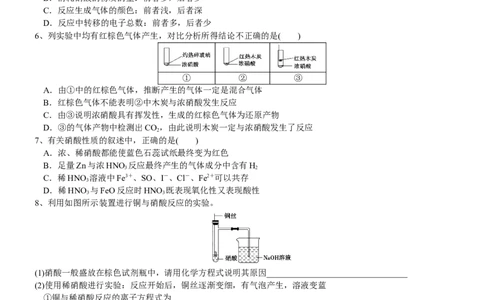
6、列实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
① ② ③
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO,由此说明木炭一定与浓硝酸发生了反应
2
7、有关硝酸性质的叙述中,正确的是( )
A.浓、稀硝酸都能使蓝色石蕊试纸最终变为红色
B.足量Zn与浓HNO 反应最终产生的气体成分中含有H
3 2
C.稀HNO 溶液中Fe3+、SO、I-、Cl-、Fe2+可以共存
3
D.稀HNO 与FeO反应时HNO 既表现氧化性又表现酸性
3 3
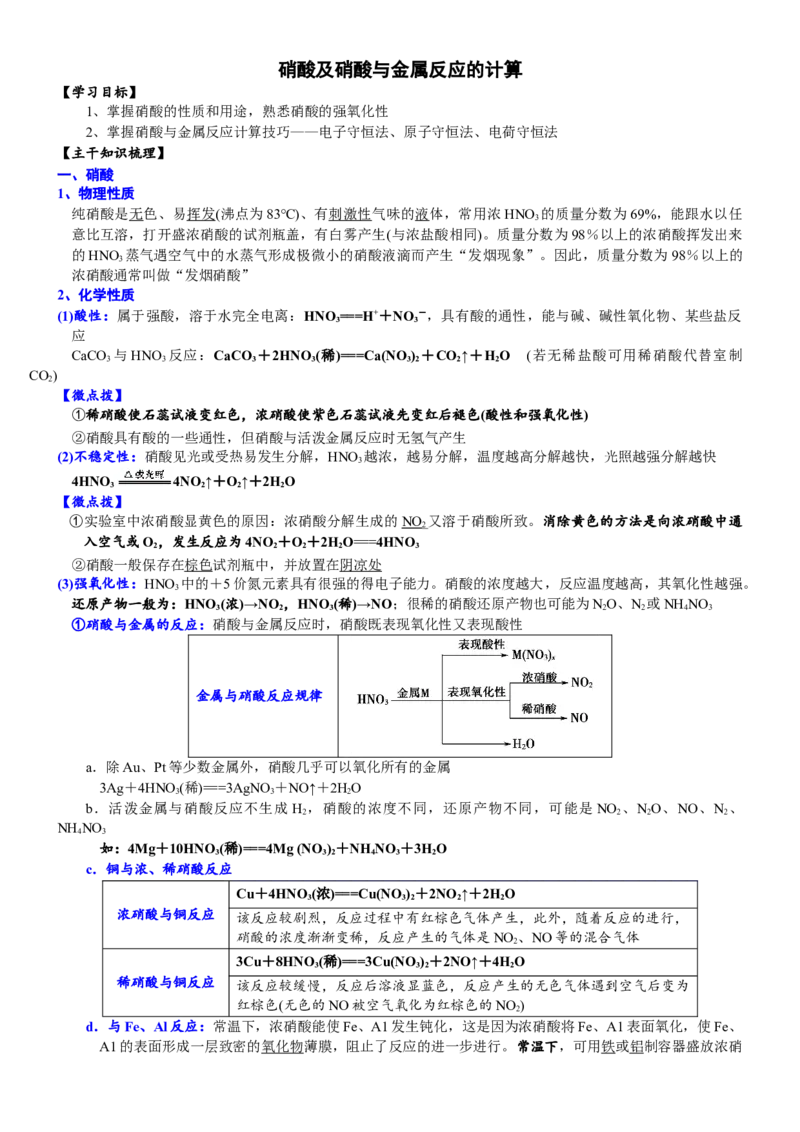
8、利用如图所示装置进行铜与硝酸反应的实验。
(1)硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因_________________________________
(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝
①铜与稀硝酸反应的离子方程式为_________________________________
②实验中观察到试管中的气体略有红棕色,其原因是___________________________(用化学方程式表示)
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体
①铜与浓硝酸反应的化学方程式为___________________________________________________
②某同学推测反应后溶液呈绿色的原因是NO 在溶液中达到饱和,NO 的饱和溶液呈黄色,硝酸铜溶液呈蓝
2 2
色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是
__________________________________(用化学方程式表示)
二、硝酸与金属反应的计算
1、原子守恒法:HNO 与金属反应时,一部分HNO 起酸的作用,以NO的形式存在于溶液中;一部分作为氧
3 3
化剂转化为还原产物,这两部分中氮原子的总物质的量等于反应消耗的HNO 中氮原子的物质的量
3
例1、若将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生 5.6L标准状况下的气体,则所消耗的硝酸的物
质的量是________,所得气体的平均相对分子质量为________
例2、38.4克的Cu与适量的浓HNO 反应,铜全部溶解,共收集到22.4L气体,则反应消耗HNO 的物质的量为
3 3________
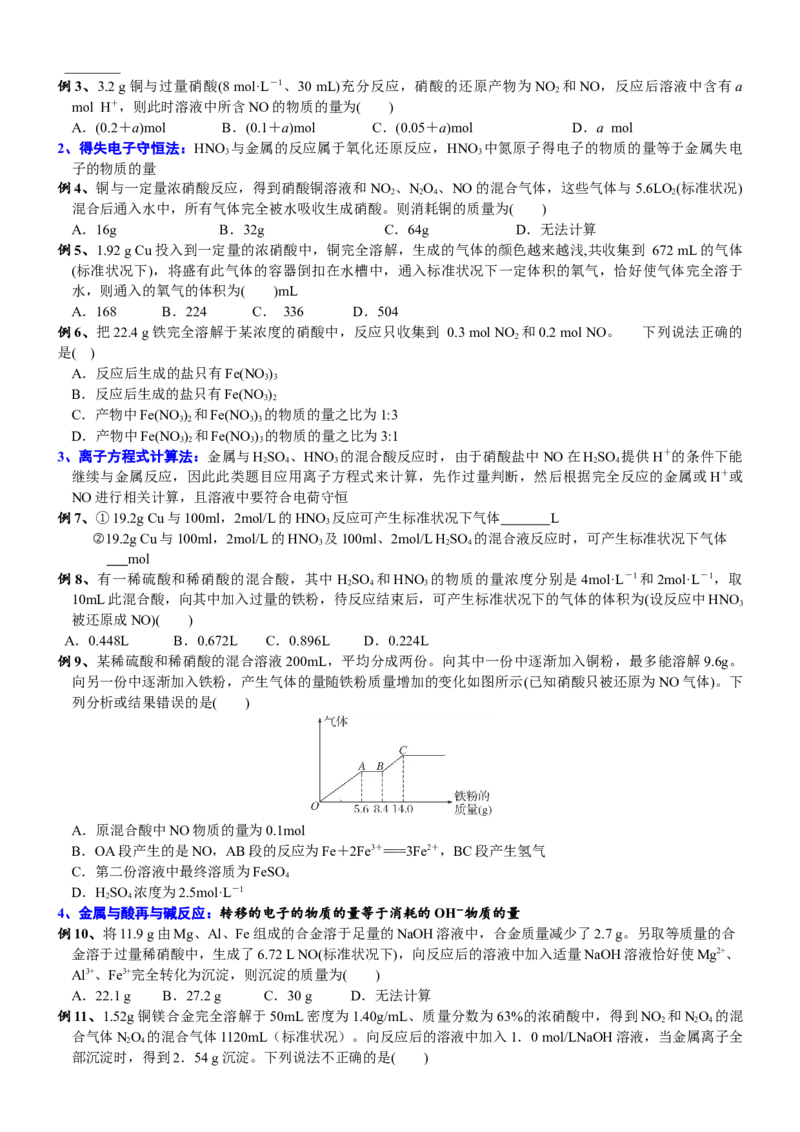
例3、3.2 g铜与过量硝酸(8 mol·L-1、30 mL)充分反应,硝酸的还原产物为NO 和NO,反应后溶液中含有a
2
mol H+,则此时溶液中所含NO的物质的量为( )
A.(0.2+a)mol B.(0.1+a)mol C.(0.05+a)mol D.a mol
2、得失电子守恒法:HNO 与金属的反应属于氧化还原反应,HNO 中氮原子得电子的物质的量等于金属失电
3 3
子的物质的量
例4、铜与一定量浓硝酸反应,得到硝酸铜溶液和 NO 、NO 、NO的混合气体,这些气体与5.6LO (标准状况)
2 2 4 2
混合后通入水中,所有气体完全被水吸收生成硝酸。则消耗铜的质量为( )
A.16g B.32g C.64g D.无法计算
例5、1.92 g Cu投入到一定量的浓硝酸中,铜完全溶解,生成的气体的颜色越来越浅,共收集到 672 mL 的气体
(标准状况下),将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于
水,则通入的氧气的体积为( )mL
A.168 B.224 C. 336 D.504
例6、把22.4 g铁完全溶解于某浓度的硝酸中,反应只收集到 0.3 mol NO 和0.2 mol NO。 下列说法正确的
2
是( )
A.反应后生成的盐只有Fe(NO )
3 3
B.反应后生成的盐只有Fe(NO )
3 2
C.产物中Fe(NO ) 和Fe(NO ) 的物质的量之比为1:3
3 2 3 3
D.产物中Fe(NO ) 和Fe(NO ) 的物质的量之比为3:1
3 2 3 3
3、离子方程式计算法:金属与HSO 、HNO 的混合酸反应时,由于硝酸盐中NO在HSO 提供H+的条件下能
2 4 3 2 4
继续与金属反应,因此此类题目应用离子方程式来计算,先作过量判断,然后根据完全反应的金属或H+或
NO进行相关计算,且溶液中要符合电荷守恒
例7、①19.2g Cu与100ml,2mol/L的HNO 反应可产生标准状况下气体 L
3
②19.2g Cu与100ml,2mol/L的HNO 及100ml、2mol/L H SO 的混合液反应时,可产生标准状况下气体
3 2 4
mol
例8、有一稀硫酸和稀硝酸的混合酸,其中 HSO 和HNO 的物质的量浓度分别是4mol·L-1和2mol·L-1,取
2 4 3
10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反应中HNO
3
被还原成NO)( )
A.0.448L B.0.672L C.0.896L D.0.224L
例9、某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。
向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下
列分析或结果错误的是( )
A.原混合酸中NO物质的量为0.1mol
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+===3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO
4
D.HSO 浓度为2.5mol·L-1
2 4
4、金属与酸再与碱反应:转移的电子的物质的量等于消耗的OH-物质的量
例10、将11.9 g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7 g。另取等质量的合
金溶于过量稀硝酸中,生成了6.72 L NO(标准状况下),向反应后的溶液中加入适量NaOH溶液恰好使Mg2+、
Al3+、Fe3+完全转化为沉淀,则沉淀的质量为( )
A.22.1 g B.27.2 g C.30 g D.无法计算
例11、1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO 和NO 的混
2 2 4
合气体NO 的混合气体1120mL(标准状况)。向反应后的溶液中加入1.0 mol/LNaOH溶液,当金属离子全
2 4
部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )A.该合金中铜与镁的物质的量之比是2:l
B.该浓硝酸中HN0 的物质的量浓度是14.0 mol/L
3
C.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
D.NO 和NO 的混合气体中,NO 的体积分数是80%
2 2 4 2
例12、铜镁合金4.6 g 完全溶于浓硝酸中,若反应中硝酸被还原,只产生 4480 mL NO 气体和 336 mL N O 气
2 2 4
体(标准状况下),反应后的溶液中加足量NaOH溶液,生成沉淀的质量为 g
【课后作业】
1、下列关于硝酸的说法不正确的是( )
A.浓硝酸是一种易挥发的液体混合物
B.浓硝酸在空气中敞口放置,因吸收水蒸气而浓度减小
C.浓硝酸不稳定,易分解生成二氧化氮、氧气和水
D.常温下,浓硝酸常保存在棕色试剂瓶中
2、下列关于硝酸的认识中,正确的是( )
A.浓硝酸和稀硝酸都具有氧化性
B.浓硝酸与金属反应不产生氢气,而稀硝酸与金属反应可置换出氢气
C.因常温下铝和铁不与浓硝酸反应,所以浓硝酸可盛放在铝制或铁制容器中
D.硝酸与金属反应时,只表现出氧化性
3、下列关于硝酸的叙述正确的是( )
A.常温下,浓硝酸可以使金属镁钝化 B.稀硝酸与活泼金属反应主要放出氢气
C.浓硝酸和稀硝酸都是强氧化剂 D.室温下,铜能与浓硝酸反应,不能与稀硝酸反应
4、下列反应中硝酸既表现出酸性又表现出氧化性的是( )
A.使石蕊溶液变红
B.与铜反应放出NO气体,生成Cu(NO )
3 2
C.与NaCO 反应放出CO 气体,生成NaNO
2 3 2 3
D.与S单质混合共热时生成HSO 和NO
2 4 2
5、已知3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO,则下列说法不正确的是( )
3 3 2 2
A.Cu做还原剂,HNO 做氧化剂 B.HNO 在该反应中只有部分表现出了氧化性
3 3
C.每生成22.4 L(标准状况)NO有3 mol电子转移 D.如果有8 mol HNO 被还原,则生成了2 mol NO
3
6、将铜粉置于稀HSO 中,加热后无明显现象,但加入一种盐后,铜粉质量减少,而且溶液变蓝,则此盐可能
2 4
是( )
A.NaCl B.NaSO C.NaNO D.NaCO
2 4 3 2 3
7、用以下三种途径来制取相同质量的硝酸铜:①铜跟浓硝酸反应,②铜跟稀硝酸反应,③铜跟氧气反应生成氧
化铜,氧化铜再跟硝酸反应。以下叙述正确的是( )
A.三种途径所消耗的铜的物质的量不相等
B.三种途径所消耗的硝酸的物质的量相等
C.所消耗铜的物质的量:途径③>途径①>途径②
D.所消耗硝酸的物质的量:途径①>途径②>途径③
8、把二氧化硫通入硝酸铁溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入氯化钡溶液,则会
产生白色沉淀。在上述一系列变化过程中,最终被还原的是( )
A.SO B.NO C.Fe3+ D.Fe2+
2
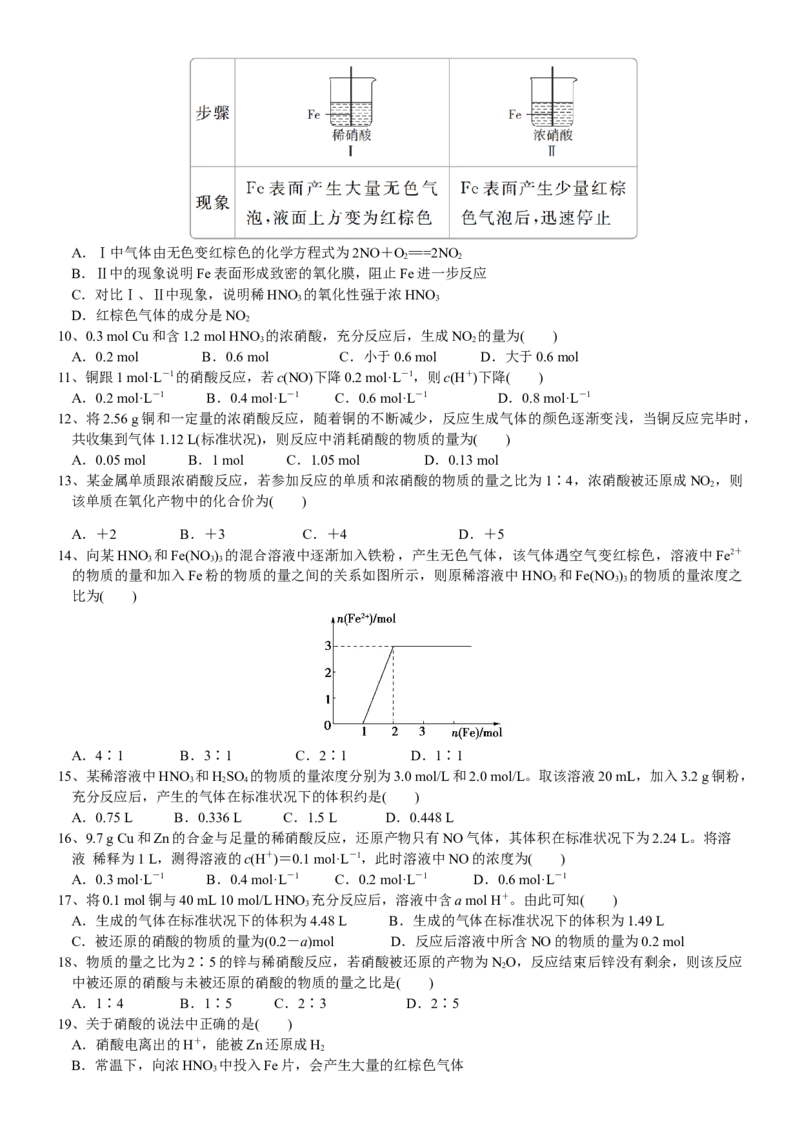
9、在通风橱中进行下列实验,下列说法中不正确的是( )A.Ⅰ中气体由无色变红棕色的化学方程式为2NO+O===2NO
2 2
B.Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应
C.对比Ⅰ、Ⅱ中现象,说明稀HNO 的氧化性强于浓HNO
3 3
D.红棕色气体的成分是NO
2
10、0.3 mol Cu和含1.2 mol HNO 的浓硝酸,充分反应后,生成NO 的量为( )
3 2
A.0.2 mol B.0.6 mol C.小于0.6 mol D.大于0.6 mol
11、铜跟1 mol·L-1的硝酸反应,若c(NO)下降0.2 mol·L-1,则c(H+)下降( )
A.0.2 mol·L-1 B.0.4 mol·L-1 C.0.6 mol·L-1 D.0.8 mol·L-1
12、将2.56 g铜和一定量的浓硝酸反应,随着铜的不断减少,反应生成气体的颜色逐渐变浅,当铜反应完毕时,
共收集到气体1.12 L(标准状况),则反应中消耗硝酸的物质的量为( )
A.0.05 mol B.1 mol C.1.05 mol D.0.13 mol
13、某金属单质跟浓硝酸反应,若参加反应的单质和浓硝酸的物质的量之比为1∶4,浓硝酸被还原成NO ,则
2
该单质在氧化产物中的化合价为( )
A.+2 B.+3 C.+4 D.+5
14、向某HNO 和Fe(NO ) 的混合溶液中逐渐加入铁粉,产生无色气体,该气体遇空气变红棕色,溶液中Fe2+
3 3 3
的物质的量和加入Fe粉的物质的量之间的关系如图所示,则原稀溶液中HNO 和Fe(NO ) 的物质的量浓度之
3 3 3
比为( )
A.4∶1 B.3∶1 C.2∶1 D.1∶1
15、某稀溶液中HNO 和HSO 的物质的量浓度分别为3.0 mol/L和2.0 mol/L。取该溶液20 mL,加入3.2 g铜粉,
3 2 4
充分反应后,产生的气体在标准状况下的体积约是( )
A.0.75 L B.0.336 L C.1.5 L D.0.448 L
16、9.7 g Cu和Zn的合金与足量的稀硝酸反应,还原产物只有NO气体,其体积在标准状况下为2.24 L。将溶
液 稀释为1 L,测得溶液的c(H+)=0.1 mol·L-1,此时溶液中NO的浓度为( )
A.0.3 mol·L-1 B.0.4 mol·L-1 C.0.2 mol·L-1 D.0.6 mol·L-1
17、将0.1 mol铜与40 mL 10 mol/L HNO 充分反应后,溶液中含a mol H+。由此可知( )
3
A.生成的气体在标准状况下的体积为4.48 L B.生成的气体在标准状况下的体积为1.49 L
C.被还原的硝酸的物质的量为(0.2-a)mol D.反应后溶液中所含NO的物质的量为0.2 mol
18、物质的量之比为2∶5的锌与稀硝酸反应,若硝酸被还原的产物为NO,反应结束后锌没有剩余,则该反应
2
中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
A.1∶4 B.1∶5 C.2∶3 D.2∶5
19、关于硝酸的说法中正确的是( )
A.硝酸电离出的H+,能被Zn还原成H
2
B.常温下,向浓HNO 中投入Fe片,会产生大量的红棕色气体
3C.向装有Fe(NO ) 溶液的试管中加入稀HSO ,可在管口观察到红棕色气体
3 2 2 4
D.过量的Fe粉中加入稀HNO,充分反应后,滴入KSCN溶液,溶液呈红色
3
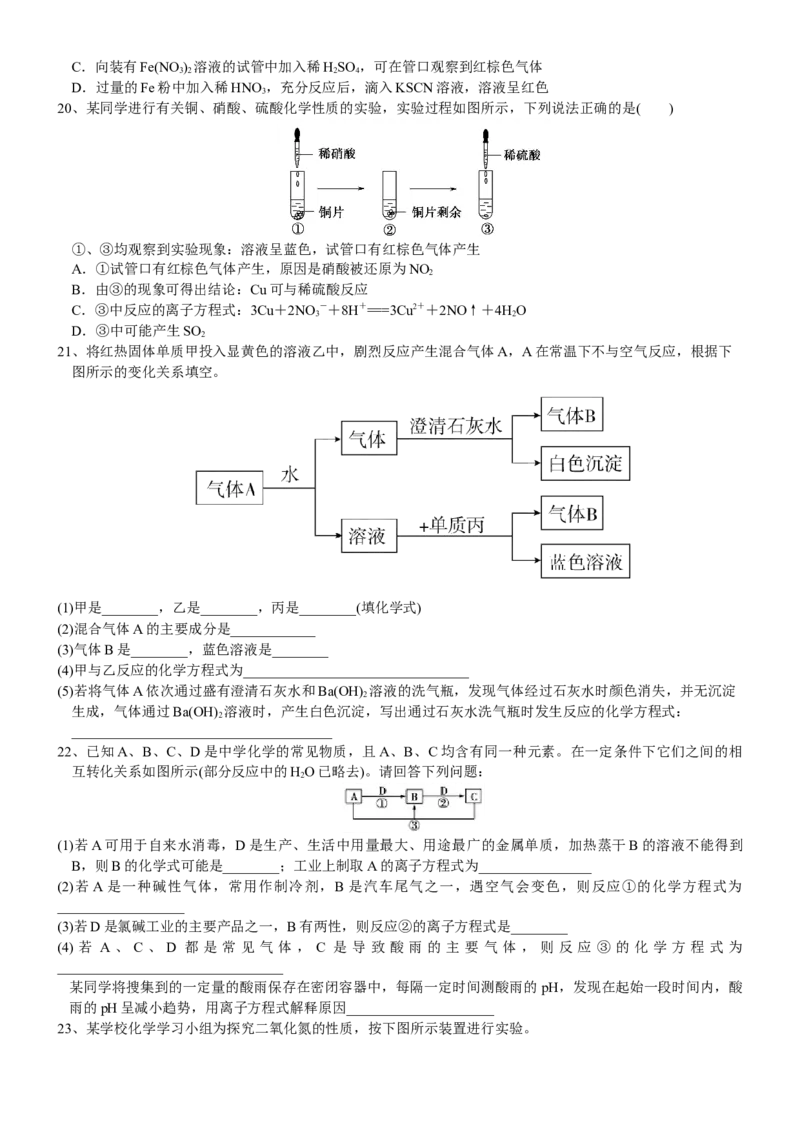
20、某同学进行有关铜、硝酸、硫酸化学性质的实验,实验过程如图所示,下列说法正确的是( )
①、③均观察到实验现象:溶液呈蓝色,试管口有红棕色气体产生
A.①试管口有红棕色气体产生,原因是硝酸被还原为NO
2
B.由③的现象可得出结论:Cu可与稀硫酸反应
C.③中反应的离子方程式:3Cu+2NO -+8H+===3Cu2++2NO↑+4HO
3 2
D.③中可能产生SO
2
21、将红热固体单质甲投入显黄色的溶液乙中,剧烈反应产生混合气体A,A在常温下不与空气反应,根据下
图所示的变化关系填空。
(1)甲是________,乙是________,丙是________(填化学式)
(2)混合气体A的主要成分是____________
(3)气体B是________,蓝色溶液是________
(4)甲与乙反应的化学方程式为________________________________
(5)若将气体A依次通过盛有澄清石灰水和Ba(OH) 溶液的洗气瓶,发现气体经过石灰水时颜色消失,并无沉淀
2
生成,气体通过Ba(OH) 溶液时,产生白色沉淀,写出通过石灰水洗气瓶时发生反应的化学方程式:
2
_____________________________________
22、已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相
互转化关系如图所示(部分反应中的HO已略去)。请回答下列问题:
2
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,加热蒸干B的溶液不能得到
B,则B的化学式可能是________;工业上制取A的离子方程式为________________
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为
__________________
(3)若D是氯碱工业的主要产品之一,B有两性,则反应②的离子方程式是________
(4) 若 A 、 C 、 D 都 是 常 见 气 体 , C 是 导 致 酸 雨 的 主 要 气 体 , 则 反 应 ③ 的 化 学 方 程 式 为
________________________________
某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸
雨的pH呈减小趋势,用离子方程式解释原因_____________________
23、某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。请回答下列问题:
(1)装置甲中盛放浓硝酸的仪器 A 的名称是:________________,该装置中发生反应的化学方程式为
___________
(2)实验过程中,装置乙、丙中出现的现象分别是:_____________________________、____________________
装置丙中的试管内发生反应的离子方程式为:_____________________
(3)为了探究 NO 的还原性,可以在装置丁的导气管 C 中通入一种气体,通入的这种气体的名称是
______________
(4)取下装置丙中的试管D,在其中滴加FeSO 溶液,溶液变为________色,为了证明铁元素在该反应中的产物,
4
可以再在溶液中滴加KSCN溶液,溶液变为________色
24、将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的一氧化氮和二氧化氮混合气体在标准状
况下的体积为11.2 L
(1)一氧化氮的体积为________,二氧化氮的体积为________(结果精确到小数点后一位)
(2)待产生的气体全部释放后,向溶液中加入V mL a mol·L-1的氢氧化钠溶液,恰好使溶液中铜离子全部转化成
沉淀,原硝酸溶液的物质的量浓度为________
25、将7.68 g铜与50 mL一定浓度的硝酸恰好完全反应,收集到标准状况下4.48 L气体。请思考:
(1)反应过程中,失去电子的物质的量为多少?
(2)被还原的HNO 为多少摩尔?未被还原的HNO 为多少摩尔?
3 3
(3)硝酸的物质的量浓度为多少?
(4)4.48 L气体的成分有哪些?各是多少L?
【硝酸及硝酸与金属反应的计算】答案
【对点训练1】
1、C。解析:常温下,浓硝酸可以使铁、铝金属发生钝化,而镁不能钝化,A错误;稀硝酸具有强氧化性,与
活泼金属反应主要还原产物为含氮元素的物质,不能得到氢气,B错误;浓硝酸和稀硝酸都是强氧化剂,C正
确;室温下,铜与浓硝酸、稀硝酸均反应,只是反应的速度及还原产物不同,D错误。
2、A。解析:浓硝酸的氧化性很强,与金属反应时一般不生成氢气而生成氮氧化物,所以实验室中不能使用浓硝酸制备氢气,A错误;常温下铁、铝遇浓硝酸会被迅速氧化,在表面产生一层致密氧化物薄膜,对内层的金
属起到了保护作用,这种现象叫钝化,B正确;浓硝酸不稳定,见光容易分解:4HNO=====4NO ↑+O↑+
3 2 2
2HO,所以应避光保存,C正确;浓硝酸易挥发,打开瓶塞,瓶口有白雾产生,D正确。
2
3、D
4、D。解析:稀硝酸具有酸性,使紫色石蕊溶液变红,但它具有强氧化性,会把红色物质氧化为无色,A正确
稀硝酸具有氧化性,与Fe反应,产生硝酸盐、NO和水,不能产生氢气,这是它的强氧化性,B正确;硝酸不
稳定,光照容易分解产生NO 、O 和水,所以硝酸要放在棕色试剂瓶中避光保存,C正确;稀硝酸具有酸性,
2 2
能与氢氧化亚铁发生中和反应,但硝酸同时具有强氧化性,会把Fe2+氧化为Fe3+,不仅仅表现酸性,D错误。
5、B。解析:同质量的铜分别和过量浓、稀硝酸反应,浓硝酸反应的更剧烈,A错误;铜和浓、稀硝酸反应的
方程式分别为① 4HNO(浓)+Cu===Cu(NO) +2NO ↑+2HO,② 8HNO(稀)+3Cu===3Cu(NO) +2NO↑+
3 3 2 2 2 3 3 2
4HO。①产生红棕色气体,②产生无色气体,C错误;由于参加反应的铜的质量相同,且两反应中还原剂都是
2
铜,反应后铜的价态又相同,所以反应中转移的电子总数相等,D错误;1 mol Cu和浓硝酸反应消耗4 mol硝酸,
1 mol Cu和稀硝酸反应消耗 mol硝酸,同质量的铜和过量浓硝酸、稀硝酸反应时,消耗的浓硝酸多,B正确。
6、D。解析:A对,①中灼热碎玻璃不与浓HNO 反应,仍有红棕色气体NO 生成,说明浓硝酸受热发生了分
3 2
解反应,生成NO 、O 和HO;B对,由于浓硝酸受热分解生成NO ,则②中红棕色气体可能来源于浓硝酸的
2 2 2 2
分解,故不能表明②中木炭与浓硝酸发生反应;C对,③中木炭未与浓硝酸接触,生成的红棕色气体只能是挥
发出的HNO 与红热木炭发生反应,或挥发出的HNO 受热分解生成NO ,说明浓硝酸具有挥发性,NO 是还原
3 3 2 2
产物;D错,由于空气中含有O ,则红热的木条可能与O 反应产生了CO ,且木炭和浓硝酸未接触,故不能说
2 2 2
明木炭与浓硝酸发生了反应。
7、D。解析:A项,浓HNO 具有强氧化性,能使红色褪去;B项,HNO 与金属反应不可能生成H;C项,
3 3 2
SO、I-、Fe2+与HNO 均反应,不能共存;D项,生成Fe(NO ) 表现酸性,生成NO表现氧化性。]
3 3 3
8、(1)硝酸见光易分解:4HNO =====4NO ↑+O↑+2HO
3 2 2 2
(2)①3Cu+8H++2NO===3Cu2++2NO↑+4HO
2
②2NO+O===2NO
2 2
(3)①4HNO (浓)+Cu===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
②3NO+HO===2HNO +NO
2 2 3
二、硝酸与金属反应的计算
例1、0.65mol 41.2
例2、2.2mol
例3、B。解析:3.2 g铜与过量硝酸(8 mol·L-1、30 mL)充分反应生成Cu2+,充分反应后溶液中Cu2+的物质的量
为0.05 mol,含a mol H+,根据电荷守恒,可得硝酸根的物质的量等于铜离子物质的量的2倍和氢离子的物质
的量之和,则此时溶液中所含NO的物质的量为(0.1+a)mol。]
例4、B。解析:该题氮元素变化为硝酸―→氮的氧化物―→硝酸,所以题目中的反应可以看成是铜与氧气的反
应,其中硝酸为“催化剂”,所以铜的物质的量为2×=0.5mol,即32g
例5、C。解析:从反应的始态和最终状态看,铜在反应中失去电子,氧气在反应中得电子,设通入的氧气的体积为
x mL,则:(1.92/64)×2=(x/22400) ×4 解得:x=336
例6、D。解析:用极限法判断:22.4 g铁如完全转化为Fe(NO ) 转移1.2 mol电子; 如完全转化为Fe(NO ) 转移 0.8
3 3 3 2
mol 电子,反应中实际转移0.3×1+0.2×3=0.9 mol 电子,所以产物中既有Fe(NO ) 又有Fe(NO ) 这,分别设Fe(NO )
3 2 3 3 3 2
和Fe(NO ) 的物质的量分别x、y,
3 3
则(据得失电子守恒有) : x+y=0.4① 2×x+3×y=0.9②
解之:x=0.3 y=0.1
例7、①1.12 ②0.15
例8、B。解析:金属和混酸反应通过离子方程式计算比较简便,3Fe+8H++2NO===3Fe2++2NO↑+4HO(铁过
2
量,产物为Fe2+),反应中Fe和H+过量,生成的NO的量以NO为准来计算,共得NO0.448L,若只考虑到这一
步反应,得答案A是错误的,因为过量的铁还可以和溶液中过量的H+反应产生H ,即有Fe+2H+===Fe2++
2
H↑,生成的H 为0.224L,所以气体体积共计0.672L,应选B。
2 2
例 9、A。解析:关键看图,铁粉既能与硝酸反应也能与硫酸反应,从题干图中看出(注意只是第二份
100mL)OA段产生的是NO,AB段的反应为Fe+2Fe3+===3Fe2+,BC段产生氢气,反应为Fe+2H+===Fe2++
H↑,可知NO反应完了,第二份中NO应为×3÷3=0.1mol,溶液中最终溶质为FeSO ,此时反应的铁的质量是
2 414g,即0.25mol,故原混合酸中HSO 浓度为=2.5mol·L-1,NO物质的量为0.2mol。所以选A。
2 4
例10、B
例11、C
例12、8.51。解析:反应中铜镁合金失去电子,最终转化为 Cu(OH) 和 Mg(OH) 沉淀,比较始态和终态,固体增加
2 2
的质量为OH-的质量,而OH-的物质的量等于转移的电子的物质的量,再根据气体计算转移的电子的物质的量:
n=4480 mL /22400 mL·mol-1+(336 mL/22400 mL·mol-)×2=0.23 mol。 所以沉淀的质量为: 4.6+0.23×17=8.51 g
【课后作业】
1、B。解析:浓硝酸是一种易挥发的液体混合物,在空气中敞口放置,其浓度会不断减小;浓硝酸不具有吸水
性,浓硝酸不稳定,见光易分解生成二氧化氮、氧气和水,所以浓硝酸常保存在棕色试剂瓶中。
2、A。解析:浓、稀硝酸都有氧化性,与金属反应均不产生氢气;在与金属反应时,硝酸既表现氧化性又表现
酸性;浓硝酸可盛放在铝制或铁制容器中,因为铝和铁在冷浓硝酸中钝化。
3、C
4、B。解析:A项,HNO 只表现酸性;B项,Cu与稀硝酸反应时,部分起酸的作用生成Cu(NO ) ,部分做氧
3 3 2
化剂被还原为NO;C项,2HNO+NaCO===CO ↑+HO+2NaNO ,HNO 只表现强酸性;D项,HNO 将S氧
3 2 3 2 2 3 3 3
化为HSO ,自身被还原为NO ,在该反应中HNO 只表现强氧化性。
2 4 2 3
5、D。解析:根据反应
知,A正确;HNO 在该反应中既表现酸性又表现氧化性,B正确;根据双线桥分析,该反应每生成2 mol NO
3
转移6 mol电子,C正确;HNO 被还原生成NO,若有8 mol HNO 被还原,则生成8 mol NO,D错误。
3 3
6、C。解析:NO在酸性条件下能将Cu氧化。
7、D
8、B。解析:有关反应的方程式:SO +2Fe3++2HO===2Fe2++4H++SO,3Fe2++4H++NO===3Fe3++NO↑
2 2
+2HO。此时滴入氯化钡溶液,可生成不溶于稀硝酸的硫酸钡白色沉淀。上述反应中 Fe3+先被SO 还原成Fe2
2 2
+,Fe2+又将NO还原为NO。
9、C。解析:Ⅰ中由于稀硝酸有强的氧化性,与铁发生氧化还原反应,硝酸得到电子被还原变为NO,气体为
无色,当遇到空气时,发生反应:2NO+O===2NO,气体变为红棕色的NO ,A、D正确;在Ⅱ中浓硝酸有强
2 2 2
氧化性,在室温下遇铁、铝会使金属表面氧化产生一层氧化物薄膜,对内层金属起保护作用,从而防止金属的
进一步反应,即发生钝化现象,因此不能进一步反应,这恰好说明浓硝酸的氧化性比稀硝酸强,B正确,C错
误。
10、C。解析:因铜与浓硝酸反应:Cu+4HNO(浓)===Cu(NO) +2NO ↑+2HO,随着反应的进行,浓硝酸变
3 3 2 2 2
稀,稀硝酸与铜反应:3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO,所以放出的NO 小于0.6 mol。
3 3 2 2 2
11、D。解析:铜跟1 mol·L-1的硝酸反应的离子方程式为8H++2NO+3Cu===3Cu2++2NO↑+4HO,消耗的H
2
+和NO的物质的量之比为8∶2=4∶1,它们浓度的变化量之比是4∶1。
12、D。解析:有关反应的化学方程式: Cu+4HNO(浓)===Cu(NO) +2NO ↑+2HO;3Cu+
3 3 2 2 2
8HNO(稀)===3Cu(NO)+2NO↑+4HO。被还原硝酸的物质的量=1.12 L÷22.4 L· mol-1=0.05 mol,生成硝酸铜
3 3 2 2
的物质的量=2.56 g÷64 g·mol-1=0.04 mol,反应共消耗硝酸的物质的量=0.05 mol+0.04 mol×2=0.13 mol。
13、A。解析:根据得失电子守恒解题,但要注意硝酸中有和金属元素结合的硝酸根未被还原,所以,设反应
后金属的化合价为x,则列式为1×(x-0)=(4-x)×(5-4),解得x=+2。注意(4-x)代表的是有4 mol硝酸反应,
和金属元素结合的未被还原的硝酸为x mol,所以得电子的硝酸的物质的量为(4-x)mol。
14、A。解析:由图像可知,当加入1 mol Fe时,n(Fe2+)=0,再加入Fe,n(Fe2+)逐渐增大,说明当加入Fe少
于1 mol时,发生反应:Fe+4HNO(稀)===Fe(NO) +NO↑+2HO,所以混合溶液中含有4 mol HNO ,当再加
3 3 3 2 3
入1 mol Fe时,发生反应:Fe+2Fe3+===3Fe2+,得到3 mol Fe2+,由图像和前面分析可知原混合溶液中含有 1
mol Fe(NO )。故原稀溶液中HNO 和Fe(NO ) 的物质的量浓度之比为4∶1。A项正确。
3 3 3 3 3
15、A。解析:20 mL溶液中:n(H+)=0.14 mol,n(NO)=0.06 mol,n(Cu)=0.05 mol。依据离子方程式计算:
3Cu + 8H+ + 2NO===3Cu2++2NO↑+4HO
23 8 2 2×22.4 L
0.05 mol 0.14 mol 0.06 mol V(NO)
三者反应时,H+与NO均过量,依据Cu的物质的量可得V(NO)≈0.75 L。
16、B。解析:n(NO)=0.1 mol,转移电子的物质的量为0.1 mol×3=0.3 mol,n(Cu+Zn)=0.3 mol÷2=0.15
mol,n[Cu(NO )]+n[Zn(NO )]=0.15 mol,其中所含n(NO)=0.3 mol,溶液的c(HNO)=c(H+)=0.1 mol·L-1,
3 2 3 2 3
其中含n(NO)=0.1 mol,溶液中NO的总浓度为0.4 mol·L-1。
17、C。解析:根据题意知剩余HNO 为a mol,Cu(NO ) 的量为0.1 mol,被还原的HNO 为0.04×10 mol-a mol
3 3 2 3
-0.1×2 mol=(0.2-a)mol,生成的NO 为(0.2-a) mol。
x
18、A
19、C。解析:A不正确,硝酸具有强氧化性,与Zn反应生成氮氧化物等,不能生成H;B不正确,Fe被浓硝
2
酸钝化,阻止进一步反应;C正确,稀HSO 电离出H+,NO在酸性条件下具有强氧化性,被Fe2+还原为NO,
2 4
试管口遇O 生成红棕色的NO ;D不正确,过量的Fe粉中加入稀HNO,生成Fe2+,与KSCN溶液不反应。
2 2 3
20、C。解析:稀硝酸和铜片反应的离子方程式为3Cu+2NO -+8H+===3Cu2++2NO↑+4HO,①试管口有红
3 2
棕色气体产生是因为NO被空气中的氧气氧化为NO ,故A错误;③中的现象产生是因为溶液中的NO在酸性
2
环境下具有强氧化性,继续与铜发生反应:3Cu+2NO -+8H+===3Cu2++2NO↑+4HO,故B错误,C正确;
3 2
③中SO 2-没有参与反应,不可能产生SO ,故D错误。
4 2
21、(1)C 浓HNO Cu
3
(2)NO、CO
2 2
(3)NO Cu(NO )
3 2
(4)C+4HNO (浓) 4NO ↑+CO ↑+2HO
3 2 2 2
(5)3NO+HO===2HNO +NO,2HNO +Ca(OH) ===Ca(NO )+2HO
2 2 3 3 2 3 2 2
解析:常温下与丙单质反应生成蓝色溶液,只能是铜与HNO 反应。气体A与水反应生成HNO,A中含有
3 3
NO ,又知A是红热固体单质甲投入显黄色的溶液乙中,剧烈反应产生混合气体,可知甲是木炭,乙是浓
2
HNO,丙是铜,A中含有NO 、CO,B是NO。
3 2 2
22、(1)FeCl 2Cl-+2HO2OH-+Cl ↑+H↑
3 2 2 2
(2)4NH+5O=====4NO+6HO
3 2 2
-
(3) Al(OH) +OH-===AlO2+2HO
3 2
-
2
(4) (4)2H S+SO ===3S↓+2HO 2H SO +O===4H++2SO 4
2 2 2 2 3 2
解析:(1)氯气常用于自来水消毒,则 A为Cl ;铁是使用最广泛的金属单质,D是铁,则B为FeCl 、C是
2 3
FeCl 。(2)碱性气体为NH ,汽车尾气中遇空气变色的气体是NO。(3)常见的两性物质是Al O 和Al(OH) ,D、
2 3 2 3 3
C分别为NaOH和NaAlO ,故B为Al(OH) 。(4)导致酸雨的主要气体是SO ,A与SO 均含有硫元素,且二者
2 3 2 2
反应生成硫单质,故A为HS。酸雨的主要成分是HSO ,在放置过程中被氧化为HSO ,酸性增强。
2 2 3 2 4
23、(1)分液漏斗 Cu+4HNO (浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
-
(2)生成红棕色气体 蒸馏水中有气泡产生,生成无色气体 3NO +HO===2H++2NO3+NO
2 2
(3)氧气
(4)黄 红 (或“血红”)
24、(1)5.8 L 5.4 L
(2) mol·L-1
解析:有关反应的化学方程式:
Cu+4HNO(浓)===Cu(NO)+2NO ↑+2HO,
3 3 2 2 2
3Cu+8HNO(稀)===3Cu(NO)+2NO↑+4HO,
3 3 2 2
Cu(NO )+2NaOH===Cu(OH) ↓+2NaNO 。
3 2 2 3
氮的氧化物的物质的量=11.2 L÷22.4 L· mol-1=0.5 mol,
铜的物质的量=32.64 g÷64 g·mol-1=0.51 mol,
设生成二氧化氮、一氧化氮的物质的量分别为x、y,
x=0.24 mol,y=0.26 mol;二氧化氮的体积=0.24 mol×22.4 L· mol-1≈5.4 L,
一氧化氮的体积=0.26 mol×22.4 L· mol-1≈5.8 L,
原硝酸溶液的物质的量浓度=(0.5 mol+0.001Va mol) ÷0.14 L= mol·L-1。
25、(1)0.24 mol
(2)n(被还原HNO )=0.2 mol,n(未被还原HNO )=0.24 mol
3 3
(3)c(HNO )=8.8 mol·L-1
3
(4)V(NO)=0.448 L,V(NO)=4.032 L
2
解析:(1)n(e-)=n(Cu)×2=×2 mol=0.24 mol。
(2)n(被还原HNO)=n(气体)==0.2 mol,
3
n(未被还原HNO)=n(Cu)×2=0.12 mol×2=0.24 mol。
3
(3)n(HNO)=0.2 mol+0.24 mol=0.44 mol,
3
c(HNO)==8.8 mol·L-1。
3
(4)成分为NO 、NO,根据电子守恒和氮原子守恒可知
2
n(NO)=0.02 mol,n(NO )=0.18 mol,
2
故V(NO)=0.448 L,V(NO )=4.032 L。
2