文档内容
考点 32 沉淀溶解平衡
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 难溶电解质的沉淀溶解平衡及应用............................................................................................2
考法02 溶度积常数及其应用...................................................................................................................5
.............................................................................................................................................8
1.高考真题考点分布
考点内容 考点分布
2024·湖南卷,3分;2024·北京卷,3分;2023·河北卷,3分;2023·北京卷,3分;,3
沉淀溶解平衡 分;,3分;,3分;,3分;,3分;2024·浙江卷,3分;2024·江苏卷,15分;2023
及其应用 浙江卷,3分;2023北京卷,3分;2022·湖南卷,3分;2022·江苏卷,3分;2022全国
乙卷,6分;
2024·江苏卷,3分;2024·湖北卷,3分;2024·浙江卷,3分;2023·湖南卷,3分;2023·
溶度积常数
辽宁卷,3分;,3分;,3分;,3分;,3分;2024·浙江卷,3分;2023·辽宁卷,3
及其应用
分;2023·全国甲卷,6分;2023·全国乙卷,6分;2022山东卷,3分;
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,沉淀的溶解、生成、转化、K 计算仍是高考命题的热点。
sp
【备考策略】【命题预测】
预计2025年高考会以新的情境载体考查沉淀的溶解、生成、转化、K 的相关计算等知识,题目难度一般
sp
较小。
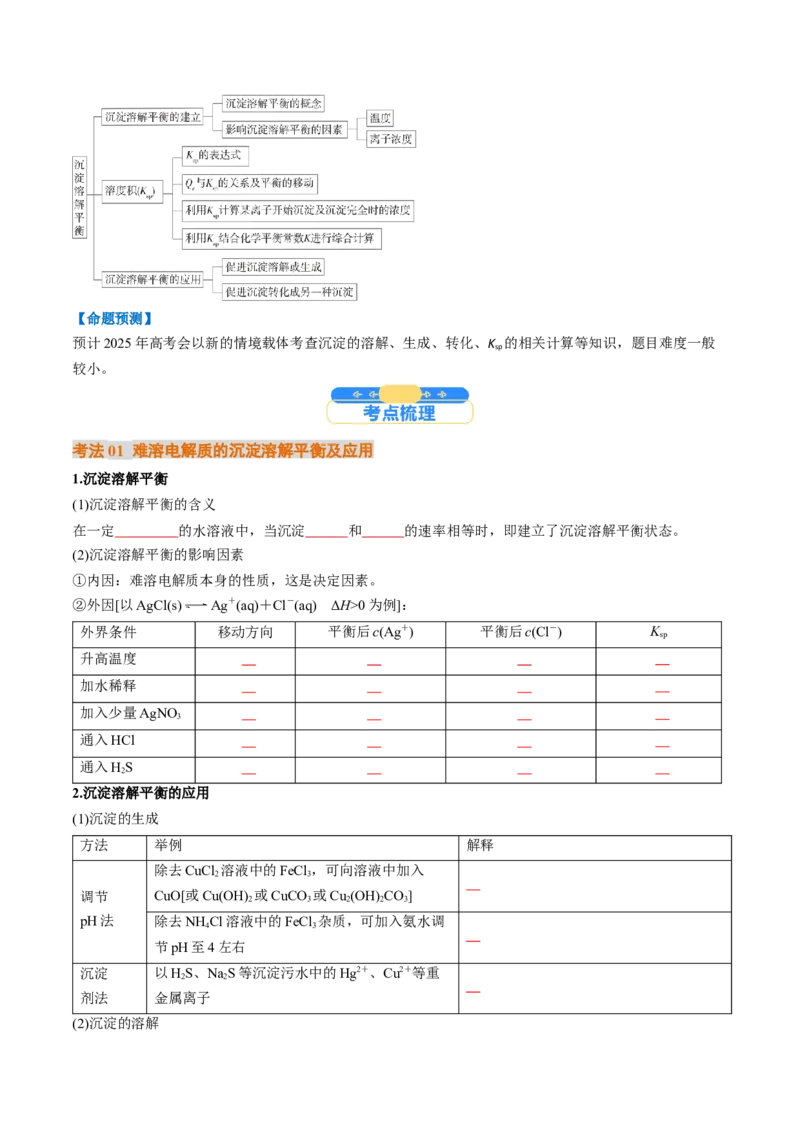
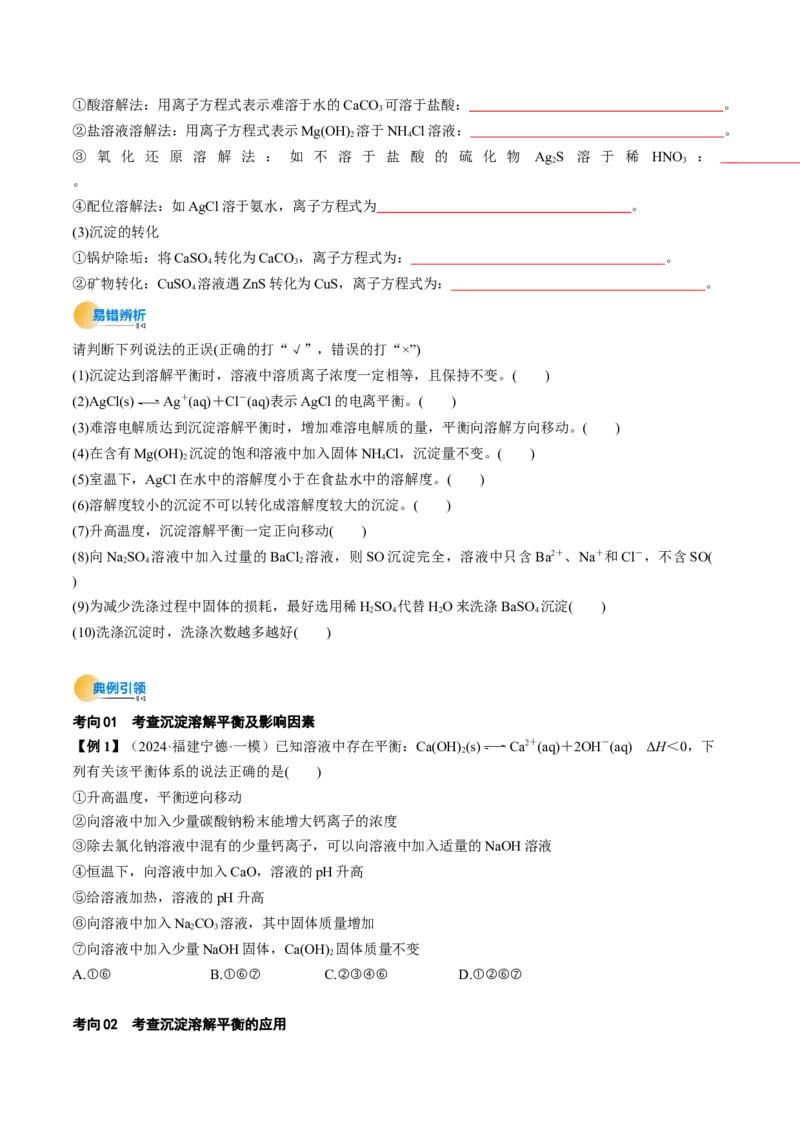
考法01 难溶电解质的沉淀溶解平衡及应用
1.沉淀溶解平衡
(1)沉淀溶解平衡的含义
在一定 的水溶液中,当沉淀 和 的速率相等时,即建立了沉淀溶解平衡状态。
(2)沉淀溶解平衡的影响因素
①内因:难溶电解质本身的性质,这是决定因素。
②外因[以AgCl(s) Ag+(aq)+Cl-(aq) ΔH>0为例]:
外界条件 移动方向 平衡后c(Ag+) 平衡后c(Cl-) K
sp
升高温度
加水稀释
加入少量AgNO
3
通入HCl
通入HS
2
2.沉淀溶解平衡的应用
(1)沉淀的生成
方法 举例 解释
除去CuCl 溶液中的FeCl ,可向溶液中加入
2 3
调节 CuO[或Cu(OH) 或CuCO 或Cu (OH) CO]
2 3 2 2 3
pH法 除去NH Cl溶液中的FeCl 杂质,可加入氨水调
4 3
节pH至4左右
沉淀 以HS、NaS等沉淀污水中的Hg2+、Cu2+等重
2 2
剂法 金属离子
(2)沉淀的溶解①酸溶解法:用离子方程式表示难溶于水的CaCO 可溶于盐酸: 。
3
②盐溶液溶解法:用离子方程式表示Mg(OH) 溶于NH Cl溶液: 。
2 4
③ 氧 化 还 原 溶 解 法 : 如 不 溶 于 盐 酸 的 硫 化 物 Ag S 溶 于 稀 HNO :
2 3
。
④配位溶解法:如AgCl溶于氨水,离子方程式为 。
(3)沉淀的转化
①锅炉除垢:将CaSO 转化为CaCO ,离子方程式为: 。
4 3
②矿物转化:CuSO 溶液遇ZnS转化为CuS,离子方程式为: 。
4
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)沉淀达到溶解平衡时,溶液中溶质离子浓度一定相等,且保持不变。( )
(2)AgCl(s) Ag+(aq)+Cl-(aq)表示AgCl的电离平衡。( )
(3)难溶电解质达到沉淀溶解平衡时,增加难溶电解质的量,平衡向溶解方向移动。( )
(4)在含有Mg(OH) 沉淀的饱和溶液中加入固体NH Cl,沉淀量不变。( )
2 4
(5)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度。( )
(6)溶解度较小的沉淀不可以转化成溶解度较大的沉淀。( )
(7)升高温度,沉淀溶解平衡一定正向移动( )
(8)向NaSO 溶液中加入过量的BaCl 溶液,则SO沉淀完全,溶液中只含Ba2+、Na+和Cl-,不含SO(
2 4 2
)
(9)为减少洗涤过程中固体的损耗,最好选用稀HSO 代替HO来洗涤BaSO 沉淀( )
2 4 2 4
(10)洗涤沉淀时,洗涤次数越多越好( )
考向01 考查沉淀溶解平衡及影响因素
【例1】(2024·福建宁德·一模)已知溶液中存在平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq) ΔH<0,下
2
列有关该平衡体系的说法正确的是( )
①升高温度,平衡逆向移动
②向溶液中加入少量碳酸钠粉末能增大钙离子的浓度
③除去氯化钠溶液中混有的少量钙离子,可以向溶液中加入适量的NaOH溶液
④恒温下,向溶液中加入CaO,溶液的pH升高
⑤给溶液加热,溶液的pH升高
⑥向溶液中加入NaCO 溶液,其中固体质量增加
2 3
⑦向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
A.①⑥ B.①⑥⑦ C.②③④⑥ D.①②⑥⑦
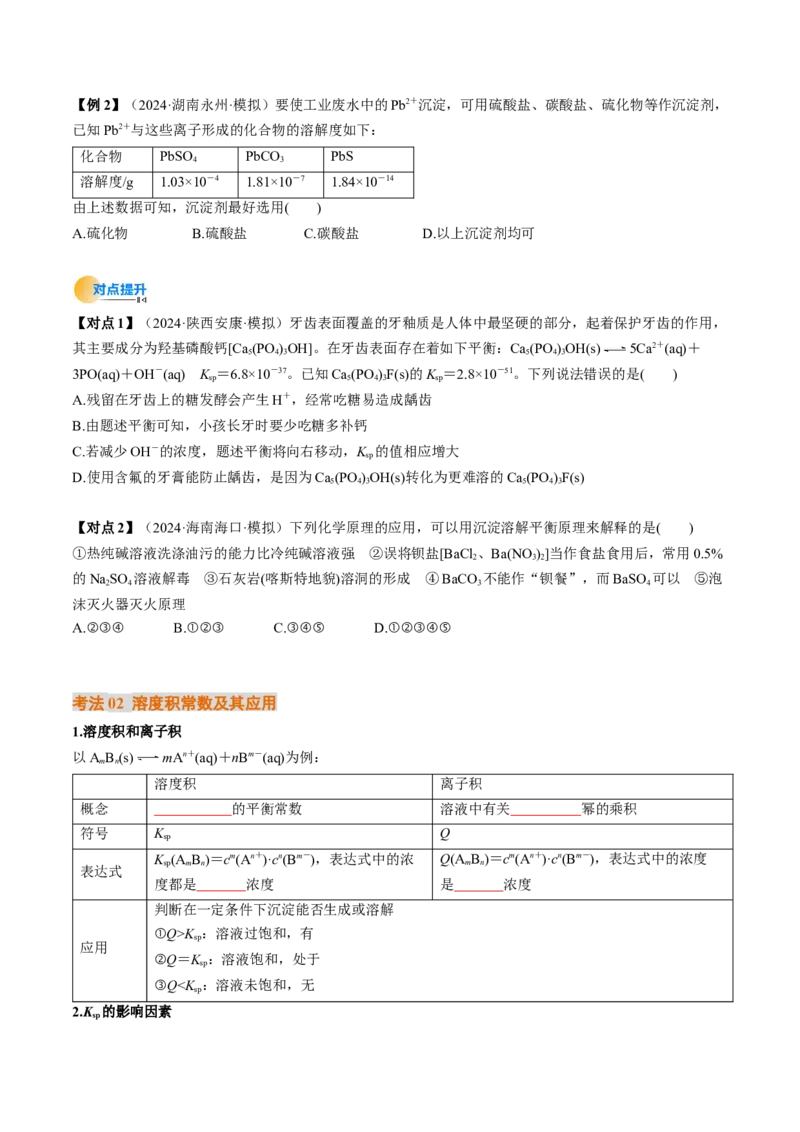
考向02 考查沉淀溶解平衡的应用【例2】(2024·湖南永州·模拟)要使工业废水中的Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,
已知Pb2+与这些离子形成的化合物的溶解度如下:
化合物 PbSO PbCO PbS
4 3
溶解度/g 1.03×10-4 1.81×10-7 1.84×10-14
由上述数据可知,沉淀剂最好选用( )
A.硫化物 B.硫酸盐 C.碳酸盐 D.以上沉淀剂均可
【对点1】(2024·陕西安康·模拟)牙齿表面覆盖的牙釉质是人体中最坚硬的部分,起着保护牙齿的作用,
其主要成分为羟基磷酸钙[Ca (PO )OH]。在牙齿表面存在着如下平衡:Ca (PO )OH(s) 5Ca2+(aq)+
5 4 3 5 4 3
3PO(aq)+OH-(aq) K =6.8×10-37。已知Ca (PO )F(s)的K =2.8×10-51。下列说法错误的是( )
sp 5 4 3 sp
A.残留在牙齿上的糖发酵会产生H+,经常吃糖易造成龋齿
B.由题述平衡可知,小孩长牙时要少吃糖多补钙
C.若减少OH-的浓度,题述平衡将向右移动,K 的值相应增大
sp
D.使用含氟的牙膏能防止龋齿,是因为Ca (PO )OH(s)转化为更难溶的Ca (PO )F(s)
5 4 3 5 4 3
【对点2】(2024·海南海口·模拟)下列化学原理的应用,可以用沉淀溶解平衡原理来解释的是( )
①热纯碱溶液洗涤油污的能力比冷纯碱溶液强 ②误将钡盐[BaCl 、Ba(NO )]当作食盐食用后,常用0.5%
2 3 2
的NaSO 溶液解毒 ③石灰岩(喀斯特地貌)溶洞的形成 ④BaCO 不能作“钡餐”,而BaSO 可以 ⑤泡
2 4 3 4
沫灭火器灭火原理
A.②③④ B.①②③ C.③④⑤ D.①②③④⑤
考法02 溶度积常数及其应用
1.溶度积和离子积
以A B (s) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
概念 的平衡常数 溶液中有关 幂的乘积
符号 K Q
sp
K (A B )=cm(An+)·cn(Bm-),表达式中的浓 Q(A B )=cm(An+)·cn(Bm-),表达式中的浓度
sp m n m n
表达式
度都是 浓度 是 浓度
判断在一定条件下沉淀能否生成或溶解
①Q>K :溶液过饱和,有
sp
应用
②Q=K :溶液饱和,处于
sp
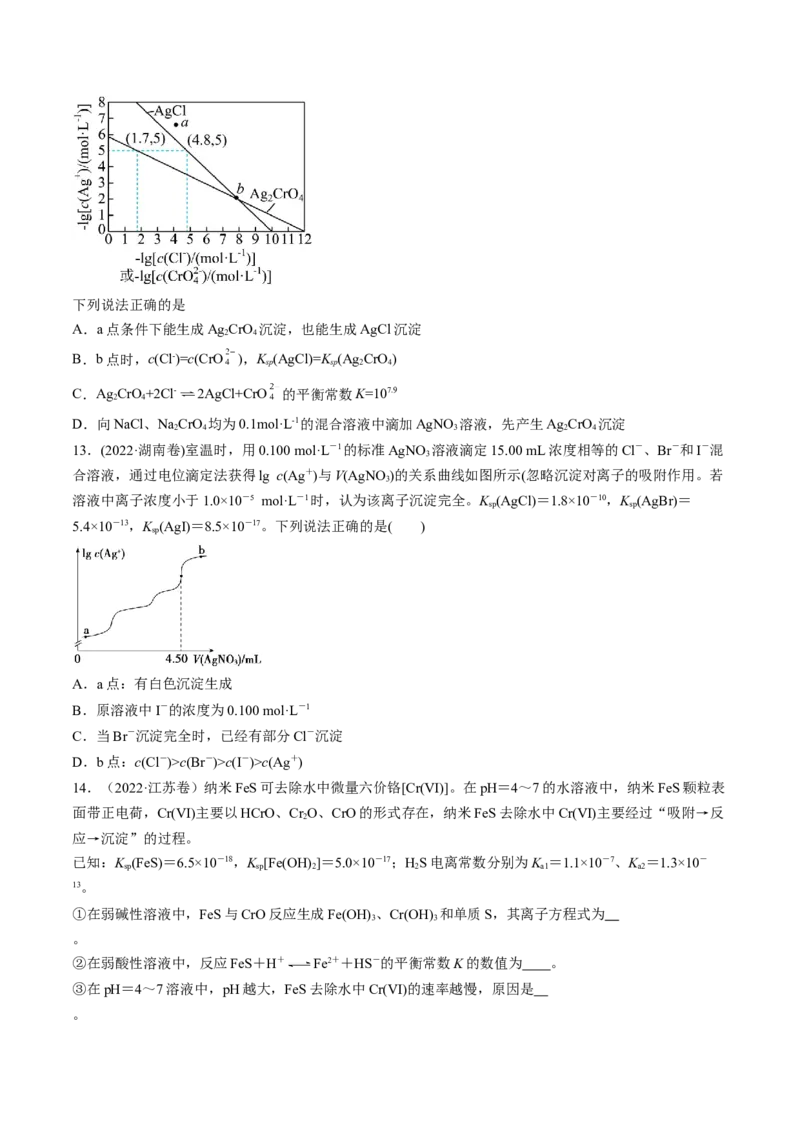
③Qc(Br-)>c(I-)>c(Ag+)
14.(2022·江苏卷)纳米FeS可去除水中微量六价铬[Cr(Ⅵ)]。在pH=4~7的水溶液中,纳米FeS颗粒表
面带正电荷,Cr(Ⅵ)主要以HCrO、Cr O、CrO的形式存在,纳米FeS去除水中Cr(Ⅵ)主要经过“吸附→反
2
应→沉淀”的过程。
已知:K (FeS)=6.5×10-18,K [Fe(OH) ]=5.0×10-17;HS电离常数分别为K =1.1×10-7、K =1.3×10-
sp sp 2 2 a1 a2
13。
①在弱碱性溶液中,FeS与CrO反应生成Fe(OH) 、Cr(OH) 和单质S,其离子方程式为
3 3
。
②在弱酸性溶液中,反应FeS+H+ Fe2++HS-的平衡常数K的数值为 。
③在pH=4~7溶液中,pH越大,FeS去除水中Cr(Ⅵ)的速率越慢,原因是
。