文档内容
南充市二○二五年初中学业水平考试
理科综合试题
注意事项:
1.理科综合试题包括物理、化学两部分,满分200分。其中物理100分(按90
分折合计入总成绩),化学100分(按60分折合计入总成绩)。考试时间共
120分钟。
2. 考生答题前须将姓名、座位号、身份证号、准考证号填在答题卡指定位置。
3. 所有解答内容均须涂、写在答题卡上。
4. 选择题须用2B 铅笔将答题卡相应题号对应选项涂黑,若需改动,须擦净另
涂。
5. 非选择题在答题卡对应题号位置用0.5毫米黑色字迹笔书写。
化学
可能用到的相对原子质量:H—1 C—12 O—16 Ca—40
一、选择题(本大题包括12个小题,每小题3分,共36分)每小题只有一个
选项符合题意。 南充是一座历史悠久的文化名城,这里生活着勤劳的果城人民。
完成1~4题。
1.南充凉粉是享誉全国的美食,下述生产过程中,主要涉及化学变化的是
A.磨粮为粉 B.水溶过滤 C.熬浆成形 D.切块装盘
2.生命健康与安全是幸福生活的保证,下列说法正确的是
A.人体缺铁会引起骨质疏松症
B.用亚硝酸钠代替食盐来腌渍鱼、肉等食品
C.油锅着火时,用大量水扑灭
D.合理用药对保障人体健康有重要作用
3.为保护我们南充美丽的生态环境,下列做法或说法正确的是
A.澄清的工业废水可以直接排放
B.大力植树造林可减少沙尘天气的发生
C.天然气燃烧的产物易形成酸雨
D.保护嘉陵江生态环境,禁止使用农药和化肥
4.下列劳动实践项目与所述化学知识不相符的是
试卷第1页,共3页A.将炉具清洁剂与洁厕灵混在一起使用——两者混合后,去污能力增强
B.用柠檬酸与小苏打自制汽水——两者发生化学反应生成二氧化碳
C.干冰用于易变质食物的短期保鲜——干冰升华吸热
D.用活性炭去除冰箱异味——活性炭具有吸附性
实验是科学探究的重要形式和学习化学的重要途径。完成5~7题。
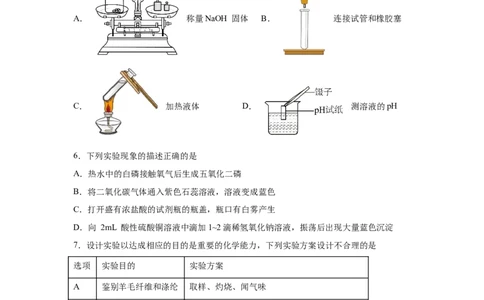
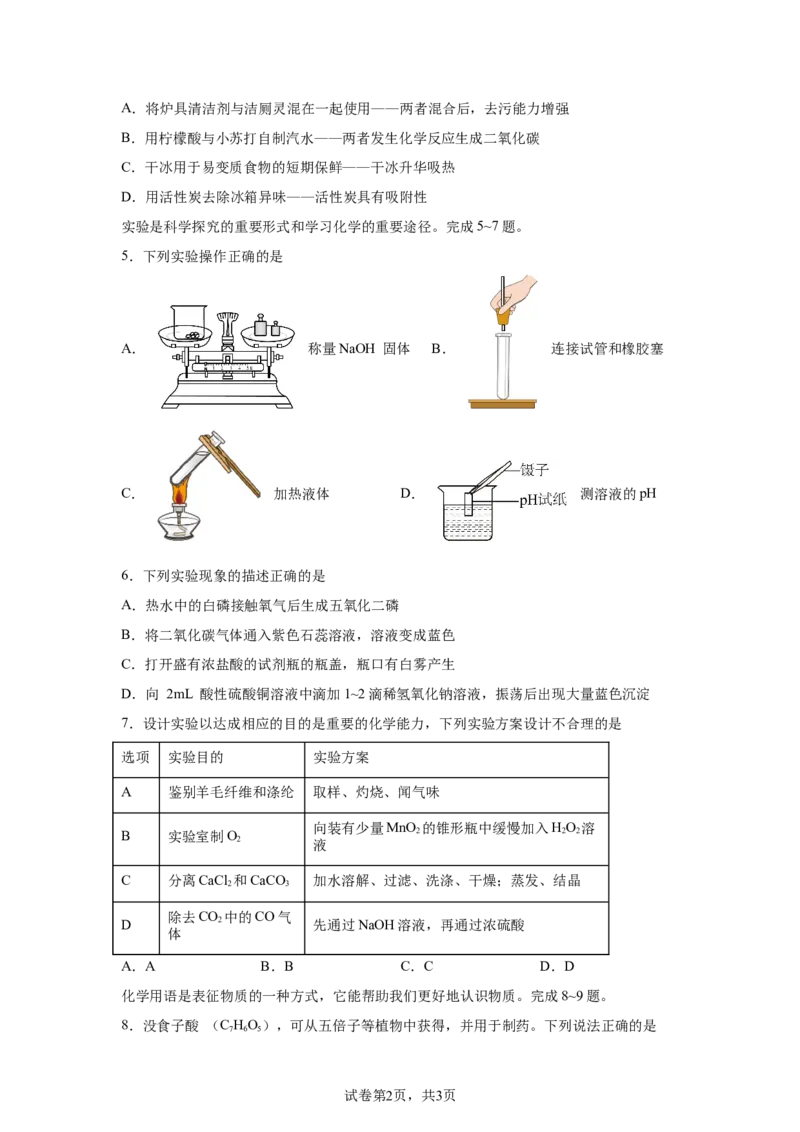
5.下列实验操作正确的是
A. 称量NaOH 固体 B. 连接试管和橡胶塞
C. 加热液体 D. 测溶液的pH
6.下列实验现象的描述正确的是
A.热水中的白磷接触氧气后生成五氧化二磷
B.将二氧化碳气体通入紫色石蕊溶液,溶液变成蓝色
C.打开盛有浓盐酸的试剂瓶的瓶盖,瓶口有白雾产生
D.向 2mL 酸性硫酸铜溶液中滴加1~2滴稀氢氧化钠溶液,振荡后出现大量蓝色沉淀
7.设计实验以达成相应的目的是重要的化学能力,下列实验方案设计不合理的是
选项 实验目的 实验方案
A 鉴别羊毛纤维和涤纶 取样、灼烧、闻气味
向装有少量MnO 的锥形瓶中缓慢加入HO 溶
B 实验室制O 2 2 2
2 液
C 分离CaCl 和CaCO 加水溶解、过滤、洗涤、干燥;蒸发、结晶
2 3
除去CO 中的CO气
D 2 先通过NaOH溶液,再通过浓硫酸
体
A.A B.B C.C D.D
化学用语是表征物质的一种方式,它能帮助我们更好地认识物质。完成8~9题。
8.没食子酸 (C HO),可从五倍子等植物中获得,并用于制药。下列说法正确的是
7 6 5
试卷第2页,共3页A.没食子酸属于氧化物 B.没食子酸中碳元素的质量分数最大
C.没食子酸由18个原子构成 D.没食子酸的相对分子质量是170g
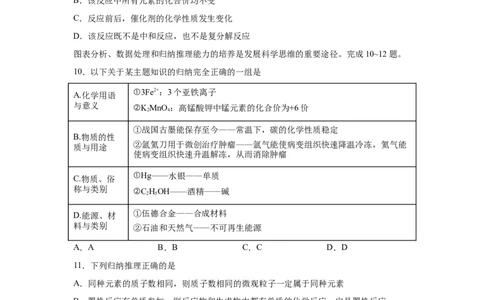
9.竖炉炼铁时,催化反应室中发生的反应的微观示意图如下,下列说法正确的是
A.该反应前后的分子数目不变
B.该反应中所有元素的化合价均不变
C.反应前后,催化剂的化学性质发生变化
D.该反应既不是中和反应,也不是复分解反应
图表分析、数据处理和归纳推理能力的培养是发展科学思维的重要途径。完成10~12题。
10.以下关于某主题知识的归纳完全正确的一组是
A.化学用语
①3Fe2+:3个亚铁离子
与意义
②K MnO :高锰酸钾中锰元素的化合价为+6价
2 4
①战国古墨能保存至今——常温下,碳的化学性质稳定
B.物质的性
②氩氦刀用于微创治疗肿瘤——氩气能使病变组织快速降温冷冻,氦气能
质与用途
使病变组织快速升温解冻,从而消除肿瘤
C.物质、俗
①Hg——水银——单质
称与类别
②C HOH——酒精——碱
2 5
D.能源、材 ①伍德合金——合成材料
料与类别 ②石油和天然气——不可再生能源
A.A B.B C.C D.D
11.下列归纳推理正确的是
A.同种元素的质子数相同,则质子数相同的微观粒子一定属于同种元素
B.置换反应有单质参加,则反应物和生成物中都有单质的化学反应一定是置换反应
C.常温下,碱溶液的pH 大 于 7 , 则pH>7的溶液一定是碱性溶液
D.HCl 、HSO 等酸都含氢元素,则含氢元素的化合物一定属于酸
2 4
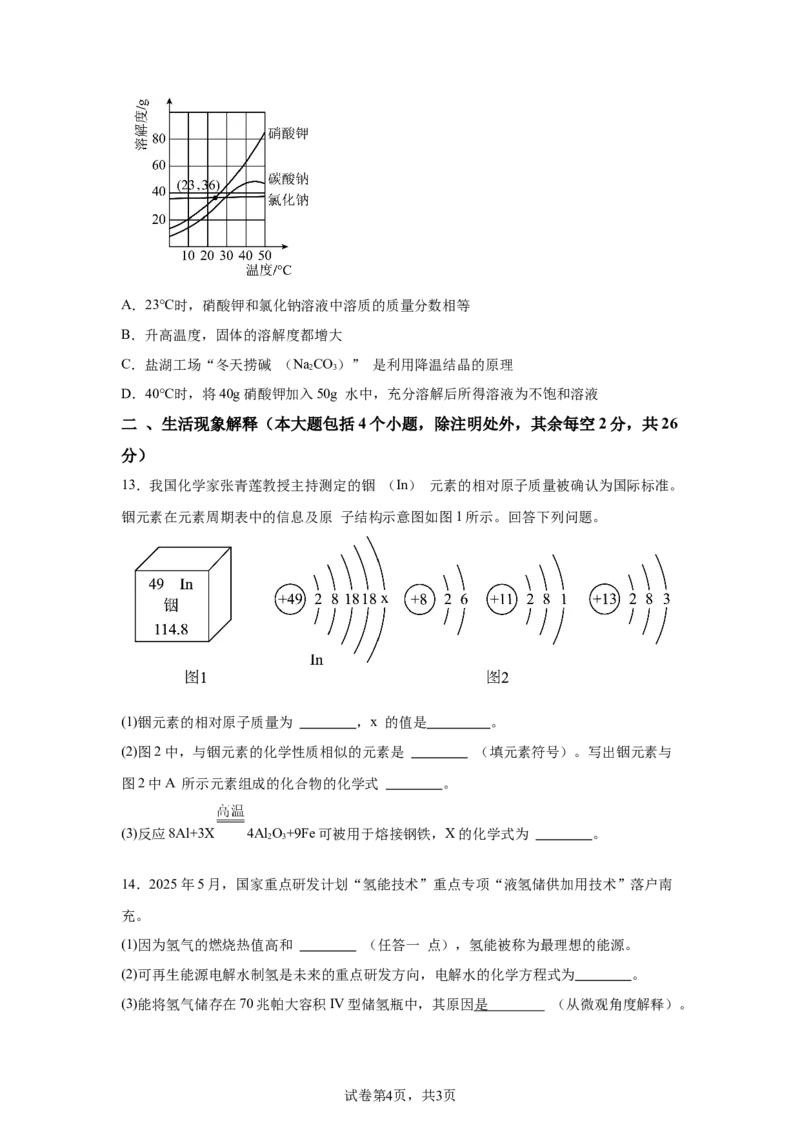
12.几种固体的溶解度曲线如图所示,下列说法正确的是
试卷第3页,共3页A.23℃时,硝酸钾和氯化钠溶液中溶质的质量分数相等
B.升高温度,固体的溶解度都增大
C.盐湖工场“冬天捞碱 (NaCO)” 是利用降温结晶的原理
2 3
D.40℃时,将40g硝酸钾加入50g 水中,充分溶解后所得溶液为不饱和溶液
二 、生活现象解释(本大题包括4个小题,除注明处外,其余每空2分,共26
分)
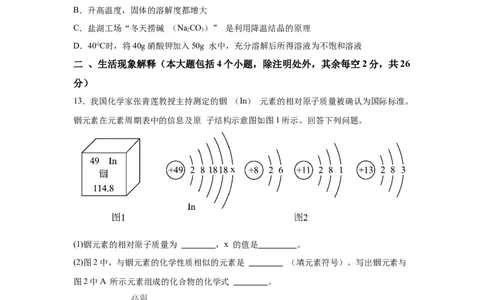
13.我国化学家张青莲教授主持测定的铟 (In) 元素的相对原子质量被确认为国际标准。
铟元素在元素周期表中的信息及原 子结构示意图如图1所示。回答下列问题。
(1)铟元素的相对原子质量为 ,x 的值是 。
(2)图2中,与铟元素的化学性质相似的元素是 (填元素符号)。写出铟元素与
图2中A 所示元素组成的化合物的化学式 。
(3)反应8Al+3X 4Al O+9Fe可被用于熔接钢铁,X的化学式为 。
2 3
14.2025年5月,国家重点研发计划“氢能技术”重点专项“液氢储供加用技术”落户南
充。
(1)因为氢气的燃烧热值高和 (任答一 点),氢能被称为最理想的能源。
(2)可再生能源电解水制氢是未来的重点研发方向,电解水的化学方程式为 。
(3)能将氢气储存在70兆帕大容积IV型储氢瓶中,其原因 是 (从微观角度解释)。
试卷第4页,共3页海洋资源的综合利用,对于促进经济和社会可持续发展具有重要意义。完成下面小题。
15.请回答下列问题。
(1)我们可从海水中获取粗盐。去除粗盐中难溶性杂质的操作,正确的顺序是 (填序号)。
A.过 滤 B.溶 解 C.蒸发
(2)将提纯后的海盐进一步精制,得到的精盐应用广泛。工业上,可用电解饱和NaCl溶液
的方法来制烧碱、氢气和氯气(Cl)。 该反应的化学方程式为 。
2
16.《周礼 ·考工记》中记载,古人取海洋中的贝壳烧成灰(主要成分是CaO),混入到
草木灰( 含 KCO)的水溶液中,利用生成物中能够去污的成分来清洗丝帛。
2 3
(1)草木灰可当作化肥中的 肥施用,促进植物生长、增强抗病虫害和抗倒伏能力。
(2)贝壳灰与水反应会 (填“吸热”或“放热”)。
(3)将贝壳灰与草木灰混入水中,充分反应后过滤,滤液中一定存在的溶质是
( 填 化学式)。可能存在的溶质是 (填一种可能情况),可以用
(填一种 试剂)来检验其是否存在。
三 、科普阅读理解( 本大题包括1个小题,每空2分,共10分)
17.2024年,国家卫生健康委等16个部门联合制定了《“体重管理年”活动实施方案》。
该《方案》的“体重管理指导原则”中提到关于超重肥胖人群的食物构成的建议:①高蛋
白饮食(指每日蛋白质供能比达20%-30%);②低碳水化合物(糖类)饮食(供能比
≤40%); ③生酮饮食,适用于严密医学监督确保安全情况下,单纯性肥胖以及肥胖代谢
综合征人群短期 内快速降低体重。部分营养素完全氧化释放能量及供能比情况如下表所示。
糖类
营养素种类 蛋白质 油脂
(按葡萄糖计)
放出的能量kJ/g 18 16 39
20%
每日供能比 60%-70% -
25%
图1不同年龄的人所需蛋白质的指数
人们对蛋白质的需求量因年龄、体重、健康状况的差异而有所不同,根据年龄,从图1中
试卷第5页,共3页查出指数,乘以体重(kg)可得到一天所需蛋白质的质量(g)。
蛋白质广泛存在于动物和植物体内。常见的动物性食物中的蛋白质大部分是完全蛋白质,
其蛋白质含量在10%-21%,必需氨基酸的种类齐全且利用率高。常见的植物性食物中的蛋
白质也是人类膳食的重要来源.其中:大豆中蛋白质含量高达35%-40%、谷类食物中蛋白质
含量一般为6%-10%,薯类中蛋白质含量只有2%-3%。
根据上文,回答下列问题。
(1)蛋白质属于 (填“有机物”或“无机物”)。
(2)人体内,葡萄糖(C H O)在酶的催化作用下发生氧化反应的化学方程式为 。
6 12 6
(3)某同学令年15岁(0.88g/kg),体重50kg,则他每日需蛋白质的质量为 g。
(4)下列说法正确的是 。
A.每 1 0 0g 营养素完全氧化放出能量最多的是糖类
B.超重肥胖人群可通过提高每日饮食中蛋白质供能比来管理体重
C.单纯性肥胖人群若需短期内快速降低体重,可在严密医学监督确保安全情况下尝 试生
酮饮食
D.植物性食物中的蛋白质含量一定比动物性食物中的蛋白质含量低
(5)除了合理膳食外,我们还能通过 来管理与维持健康体重。(填一种生活方
式)
四、科学探究实验 (本大题包括1个小题,每空2分,共18分)
18.请回答下列问题。
(1)实验室常用下图装置来制取气体。
①在用B 装置制取CO 的实验中,仪器m的作用是 X 。选择正确的 装置制取
2
并收集一瓶干燥的CO 气体,其接口的连接顺序是 (填序号)。
2
②实验室用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,应选择的发生装置是
(填序号)。
(2)小明家铁质水龙头严重锈蚀,在重新购置时,五金店老板建议他选不易生锈的镀铬水
龙头。想到金属活动性顺序表中没有铬这种金属,小明和同学们做了如下探究:
试卷第6页,共3页【探究目的】比较铬与铁、铜的金属活动性强弱。
【提出猜想1】依据铬不易生锈,猜想两种金属的活动性: Cu>Cr。
【进行实验】有以下试剂可供选择:铜片、铬片、FeSO 溶液、稀硫酸、AgNO 溶液。
4 3
操作步骤 实验现象 实验结论
取大小相同的金属铬片和铜片,打磨后
分别放入2支试管中,再分别加入等浓 铬片表面有气泡冒出,溶液变 猜想1错
度等体积的 (选填一种试 成蓝色;铜片无明显现象。 误
剂)。
【提出猜想2】铬不易生锈,铁易生锈,猜想两种金属的活动性:Fe Cr(填“<”
或“>”)。
【进行实验】将打磨后的铁片放入蓝色CrSO 溶液中,未观察到明显现象。
4
【得出结论】猜想2错误。
【探究结果】综合以上信息,三种金属的活动性顺序为Cr>Fe>Cu。
【实验与评价】小乙同学只选用3种试剂进行实验,也得出与小明相同的结论。小乙同学
所选的试剂的组合可能是 。(限选试剂:铁片、铜片、 铬片(银白色)、
FeSO 溶液、CuSO 溶 液 、CrSO 溶液(蓝色)、稀硫酸)
4 4 4
【反思交流】
a. 小明同学疑惑:铬的金属活动性比铁强,为什么镀铬水龙头不易生锈呢?小乙想到了 铝
制品耐腐蚀的原理,认为金属铬不易生锈的原因可能是 。
b. 实验室常用稀盐酸去除铁制品表面的铁锈,该反应的化学方程式为 。
c. 我们应该保持对物质世界的好奇心,养成注重实证、严谨求实的科学态度。
【拓展应用】除考虑美观和成本因素外,根据水龙头的使用特点,铁质水龙头上镀铬主要
是利用了铬的抗腐蚀性好和 。
五 、定量分析应用〔本大题包括1个小题,19题第(1)(2)题各2分,共
10分〕
19.维生素D(C H O)可以促进人体对钙的吸收,常与碳酸钙一起作为补钙剂的成分。
3 27 44
请计算:
(1)维生素D 中氢、氧元素的质量比为 (填最简整数比)。
3
(2) g 维生素D 含 有 8g 氧元素。
3
(3)某补钙剂标签如图所示,小丁同学对标签中标注的含钙量产生质疑。取10片该补钙剂
于锥形瓶中,加入足量稀盐酸(该实验条件下,其 它成分不参与反应),完全反应后收集
到CO 的质 量为3.96g。依据实验数据,计算该补钙剂中钙元 素的质量分数,并根据计算
2
试卷第7页,共3页结果判断此标签标注 的含钙量是否真实。(写出计算过程,计算结果精 确到0.1%)
商品名称 Xx补钙剂
配料表 碳酸钙、维生素D₃……
规格 2g片
含钙量
≥17.5%
(%)
储存条件 遮光、密闭、室温干燥保存
保质期 三年
试卷第8页,共3页1.C
【详解】A、磨粮为粉仅是物理粉碎,未生成新物质,属于物理变化。不符合题意。
B、水溶过滤是溶解和分离过程,未生成新物质,属于物理变化。不符合题意。
C、熬浆成形需加热,淀粉发生糊化,生成新物质(如糊精),属于化学变化。符合题意。
D、切块装盘仅为形状和位置的改变,未生成新物质,属于物理变化。不符合题意。
结论:正确选项为 C。
2.D
【详解】A. 人体缺铁会导致血红蛋白合成减少,引发缺铁性贫血,而非骨质疏松症。骨质
疏松症主要由缺钙引起。错误。
B. 亚硝酸钠有毒,不可替代食盐大量使用,否则会导致中毒。错误。
C. 油锅着火时,用大量水扑灭,水会因密度大沉入油底,高温下迅速汽化引发油滴飞溅,
加剧火势。正确方法是隔绝氧气(如盖锅盖)。错误。
D. 合理用药能有效治疗疾病并减少副作用,对健康至关重要。正确。
故选D。
3.B
【详解】A. 工业废水即使澄清,也可能含有溶解的有害物质(如重金属、有机物),直接
排放会污染水体。错误。
B. 植树造林能防风固沙,减少地表沙尘飞扬,从而降低沙尘天气发生概率。正确。
C. 天然气主要成分是甲烷,燃烧产物为CO 和HO,不会大量生成导致酸雨的SO 或
2 2 2
NO 。错误。
2
D. 完全禁止农药和化肥不现实,应合理使用以减少污染,而非禁止。错误。
故选B。
4.A
【详解】A、炉具清洁剂(强碱性)与洁厕灵(强酸性)混合会发生中和反应,降低去污
效果,甚至可能产生有毒气体。错误。
B、柠檬酸与小苏打(碳酸氢钠)反应生成二氧化碳,符合汽水制作原理。正确。
C、干冰升华吸热降温,同时二氧化碳抑制微生物,可用于保鲜。正确。
D、活性炭依靠吸附性去除异味,符合其物理性质。正确。
故选A。
5.A
【详解】A、托盘天平的使用要遵循“左物右码”的原则,氢氧化钠易潮解具有腐蚀性,
答案第1页,共2页称量氢氧化钠,要放在玻璃器皿(例如烧杯)中,图示操作正确;
B、塞紧胶塞,应该把橡皮塞慢慢转动着塞进试管口,切不可把试管放在桌上再使劲塞进
塞子,以免压破试管,手不能放在导管上,图示操作错误;
C、加热试管中的液体时,用外焰加热,液体不超过试管容积的三分之一,试管夹夹在中
上部,用手拿试管夹的长柄,试管口斜向上,与水平方向大约成45°夹角,图示操作错误;
D、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干
燥的pH试纸上,与标准比色卡对比来确定pH。不能将pH试纸伸入待测液中,以免污染
待测液,图示操作错误;
故选A。
6.C
【详解】A、白磷在热水中接触氧气会燃烧,现象应为产生大量白烟,而非直接描述生成
五氧化二磷(产物非现象)。错误。
B、 二氧化碳溶于水和水反应生成碳酸,紫色石蕊溶液遇碳酸变红。错误。
C、浓盐酸挥发出的HCl气体遇水蒸气形成盐酸小液滴,呈现白雾,描述正确。正确。
D、酸性硫酸铜溶液中H+优先与OH-中和,少量NaOH不足以生成Cu(OH)₂沉淀,氢氧化
钠会先和氢离子反应,故不会立即出现大量蓝色沉淀。错误。
故选C。
7.D
【详解】A、羊毛主要成分是蛋白质,灼烧有烧焦羽毛味,涤纶燃烧有特殊气味,方法正
确;合理。
B、HO 在MnO 催化下分解制O,缓慢加入可控制反应速率;合理。
2 2 2 2
C、CaCl 溶于水,CaCO 不溶,加水溶解、过滤、洗涤、干燥得到碳酸钙;蒸发、结晶得
2 3
到氯化钙;合理。
D、NaOH会吸收CO: ,而非CO,导致原气体被除去;不
2
合理。
故选D。
8.B
【详解】A、氧化物是指由两种元素组成,其中一种是氧元素的化合物,而没食子酸是由
碳、氢、氧三种元素组成的化合物,不属于氧化物,故A错误;
B、没食子酸中碳、氢、氧元素的质量比是(12×7):(1×6):(16×5)=84:6:80,碳元素质量分数最
答案第2页,共2页大,故B正确;
C、没食子酸是分子构成的,1个没食子酸分子由7个碳原子、6个氢原子和5个氧原子构
成,故C错误;
D、没食子酸的相对分子质量=12×7+1×6+16×5=170,单位是“1”,不写出,故D错误;
故选:B。
9.D
【分析】根据描述,微观上,CO、CH 分子在催化剂作用下,转化为CO、H 分子,反应
2 4 2
为 。
【详解】A. 根据方程式,反应前分子数目:共2个分子;反应后: 共4个分子,分子数
目改变,A错误。
B. 碳元素:CO 中为+4价,CH 中为−4价;反应后CO中C为+2价 ,化合价改变;H元
2 4
素:CH 中H为−1价,反应后H 中H为0价,化合价改变;元素化合价有变化,B错误。
4 2
C.根据催化剂定义可知,催化剂反应前后质量和化学性质不变,仅改变化学反应速率;C
错误。
D. 根据方程式,中和反应是酸 + 碱 → 盐 + 水,此反应无酸、碱参与。复分解反应:
两种化合物互相交换成分生成新化合物,此反应是CO 与CH 分解、重组,非交换成分。
2 4
该反应既不是中和反应,也不是复分解反应,D 正确。
故选D。
10.B
【详解】A. ① 3Fe2+:3个亚铁离子,正确;②KMnO 是锰酸钾,锰的化合价为+6;而高
2 4
锰酸钾的化学式为KMnO ,锰的化合价为+7,题目中化学式与名称不匹配,错误。A选项
4
错误。
B. ① 战国古墨保存至今,常温下碳的化学性质稳定,碳在常温下不易发生化学反应,正
确;② 氩氦刀用于微创治疗肿瘤,氩气释放时吸热导致冷冻,氦气释放时升温实现解冻,
符合实际应用,正确。B选项正确。
C. ① Hg俗称水银,汞是金属单质,正确;② C HOH,乙醇(酒精)属于醇类有机物,
2 5
不是碱,错误。C选项错误。
D. ① 伍德合金是金属合金,属于金属材料,而非合成材料(如塑料),错误;② 石油和
天然气,二者为化石燃料,不可在短时期内再生,正确。D选项错误。
答案第3页,共2页故选B。
11.C
【详解】A. 同种元素的质子数相同,但质子数相同的微观粒子不一定是同种元素。例如,
水分子和氨气分子可能质子数相同,但属于不同物质;O2-和F-质子数均为9,但属于不同
元素;不符合题意;
B. 置换反应需满足“单质+化合物→新单质+新化合物”的结构。若反应物和生成物中均有
单质,但不符合此结构(如O→O 的反应),则不是置换反应;不符合题意;
3 2
C. pH>7的溶液一定呈碱性,无论溶质是否为碱。例如,碳酸钠溶液因水解呈碱性,
pH>7;符合题意;
D. 含氢元素的化合物不一定是酸。例如,水、氨气、NaOH(碱)均含氢元素,但属于不
同类别;不符合题意;
故选C。
12.C
【详解】A、23C 时硝酸钾和氯化钠溶解度相等,但未说明是饱和溶液,无法比较溶质质
∘
量分数,错误。
B、碳酸钠溶解度随温度升高先增大后减小(图像趋势),不是所有固体溶解度都随温度
升高而增大,错误。
C、碳酸钠溶解度受温度影响大,冬天温度低,碳酸钠溶解度减小结晶析出,“冬天捞
碱” 利用降温结晶,正确。
D、从溶解度曲线看,40C时硝酸钾溶解度大于 60g,小于80g(即100g水最多溶解硝酸
∘
钾质量>60g,小于80g)。加入40g硝酸钾到50g水中,因50g水可溶解硝酸钾质量大于
30g,小于40g,则硝酸钾不能全部溶解,溶液为饱和溶液,错误。
故选C。
13.(1) 114.8 3
(2) Al In O
2 3
(3)Fe O
3 4
【详解】(1)根据元素周期表的信息可知,元素名称下方的数字表示相对原子质量,铟元
素的相对原子质量为114.8;在原子中,质子数等于核外电子数,则有:
49=2+8+18+18+x,解得x=3;
(2)元素的化学性质与原子的最外层电子数关系密切,最外层电子数相同的元素化学性质
相似。铟原子最外层电子数是3,图2中B(铝原子)最外层电子数也是3,所以与铟元素
答案第4页,共2页的化学性质相似的元素是 铝,元素符号为Al;图2中A所示元素是氧元素,氧元素常见
化合价为−2价,铟原子最外层电子数是3,在化学反应中易失去3个电子,显+3价,书写
化学式时,一般正价的写在左边,负价的写在右边,根据化合物中各元素化合价代数和为
零,铟元素与氧元素组成的化合物化学式为 InO;
2 3
(3)根据化学方程式8Al+3X 4Al O+9Fe可知,反应前:8个铝原子;反应后:8个
2 3
铝原子、12个氧原子、9个铁原子。化学反应前后原子的种类和数目不变,3X中应含有12
个氧原子和9个铁原子,则X的化学式为 Fe O。
3 4
14.(1)燃烧产物只有水,无污染,原料来源广泛
(2)
(3)分子之间有间隔
【详解】(1)氢气燃烧产物是水,无污染,且氢气可通过水电解制取,原料来源广泛,故
氢能被称为最理想的能源;
(2)水通电分解生成氢气和氧气,该反应的化学方程式为: ;
(3)能将氢气储存在70兆帕大容积IV型储氢瓶中,其原因是分子之间存在间隔,受压后,
分子之间的间隔变小。
15.(1)BAC
(2)
【详解】(1)粗盐提纯需先溶解(B),使可溶物与难溶物分离;再过滤(A)去除难溶
杂质;最后蒸发(C)结晶得到精盐。
(2)电解饱和NaCl溶液时,水参与反应,生成NaOH、H 和Cl,方程式配平后各元素原
2 2
子数守恒,气体需标注“↑”,即: 。
16.(1)钾##K
(2)放热
答案第5页,共2页(3) KOH 碳酸钾或氢氧化钙 稀盐酸(或碳酸钠,与上一空对应)
【详解】(1)草木灰的主要成分是碳酸钾,碳酸钾含N、P、K中的钾元素,故草木灰可
作钾肥施用;
(2)贝壳灰的主要成分是氧化钙,氧化钙与水反应生成氢氧化钙,放出大量的热,故反应
会放热;
(3)将贝壳灰与草木灰混入水中,氧化钙和水反应生成氢氧化钙,氢氧化钙和碳酸钾反应
生成碳酸钙和氢氧化钾,氢氧化钾是生成物,故充分反应后过滤,滤液中一定存在的溶质
是:KOH;
氢氧化钙或碳酸钾可能过量,故可能存在的溶质是碳酸钾或氢氧化钙;
如果可能存在的溶质是碳酸钾,碳酸钾能与稀盐酸反应生成氯化钾、二氧化碳和水,可加
入过量的稀盐酸,产生气泡,说明含碳酸钾;
如果可能存在的溶质是氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙和氢氧化钠,故可
加入适量的碳酸钠溶液,产生白色沉淀,说明含氢氧化钙。
17.(1)有机物
(2)C H O+6O 6CO+6H O
6 12 6 2 2 2
(3)44
(4)BC
(5)适量运动、戒烟酒、保持积极的心态和良好的睡眠习惯等(任答一种,合理即可)
【详解】(1)蛋白质含碳元素,属于有机物。
(2)葡萄糖在酶催化下与氧气反应生成二氧化碳和水,方程式是
;
(3)从图 1 “不同年龄的人所需蛋白质的指数” 中,15 岁对应的指数是0.88。根据文中
“根据年龄,从图 1 中查出指数,乘以体重可得到一天所需蛋白质的质量(g)”,该同
学体重50kg,则每日需蛋白质质量为0.88g/kg×50kg=44g 。
(4)A、从表格中可知,蛋白质放出能量为18kJ/g、糖类(按葡萄糖计 )是16kJ/g、油脂
是39kJ/g,所以每100g营养素完全氧化放出能量最多的是油脂,不是糖类,A 错误。
B、文中提到 “体重管理指导原则” 中对超重肥胖人群有 “高蛋白饮食(指每日蛋白质
答案第6页,共2页供能比达20%−30% )” 的建议,说明超重肥胖人群可通过提高每日饮食中蛋白质供能比
来管理体重,B 正确。
C、原文明确说 “生酮饮食,适用于严密医学监督确保安全情况下,单纯性肥胖以及肥胖
代谢综合征人群短期内快速降低体重”,所以单纯性肥胖人群若需短期内快速降低体重,
可在严密医学监督确保安全情况下尝试生酮饮食,C 正确。
D、文中提到 “常见的动物性食物中的蛋白质大部分是完全蛋白质,其蛋白质含量在10%
−21%…… 常见的植物性食物中…… 大豆中蛋白质含量高达35%−40%” ,说明植物性食
物(如大豆 )中蛋白质含量可能比动物性食物高,不是一定低,D 错误。
故选BC。
(5)要管理与维持健康体重,除了合理膳食,还可以通过适量运动,运动能消耗能量,增
加新陈代谢;也可以是戒烟酒,避免因烟酒影响身体代谢;或者保持积极的心态和良好的
睡眠习惯等,这些健康的生活方式都有助于维持健康体重,任答一种合理的即可。
18.(1) 添加液体试剂 bgfd A
(2) 稀硫酸##稀盐酸 > 铜片、铬片和 FeSO 溶液##铁片、CuSO 溶液和
4 4
CrSO 溶液(填名称或化学式均可) 铬与空气中的氧气反应生成了致密的氧化膜,阻
4
止铬进一步被氧化 Fe O+6HCl=2FeCl +3H O 硬度大##耐磨##耐磨性强
2 3 3 2
【详解】(1)①仪器m是长颈漏斗,其在该实验中的作用是添加液体试剂 ;
实验室制取二氧化碳用大理石(或石灰石)和稀盐酸,发生装置选固液不加热型,即B装
置,要收集干燥的二氧化碳,需要先通过浓硫酸干燥(长进短出,从g进f出),再收集,
二氧化碳密度比空气大,能溶于水,用向上排空气法收集,连接顺序为bgfd;
② 实验室用加热无水醋酸钠和碱石灰固体混合物的方法制取甲烷,属于固体加热型,应选
择的发生装置是A;
(2)进行实验:
在金属活动性顺序里,位于氢前面的金属能置换出稀盐酸、稀硫酸中的氢;要比较铬和铜
的金属活动性,根据铬片表面有气泡冒出,溶液变成蓝色;铜片无明显现象,说明选用的
试剂能与铬反应但不与铜反应,可选用稀盐酸或稀硫酸;
提出猜想2:
由于铬不易生锈,铁易生锈,根据金属活动性顺序,活动性较强的金属容易发生反应,猜
想铁的金属活动性比铬强,即 Fe>Cr;
实验与评价:
要得出Cr>Fe>Cu的结论,所选试剂组合可以是铬片、FeSO 溶液、铜片(将铬片放入
4
答案第7页,共2页FeSO 溶液中,铬片表面有黑色物质析出,说明Cr>Fe;再将铜片放入FeSO 溶液中无明显
4 4
现象,说明Fe>Cu,从而得出Cr>Fe>Cu);也可以是铁片、CrSO 溶液、CuSO 溶液(将
4 4
铁片放入CrSO 溶液中无明显现象,说明Cr>Fe;将铁片放入CuSO 溶液中,铁片表面有
4 4
红色物质析出,说明Fe>Cu,从而得出Cr>Fe>Cu);
反思交流:
a.铝制品耐腐蚀的原理是铝在空气中易与氧气反应生成致密的氧化膜,阻止铝进一步被氧
化,金属铬不易生锈的原因可能类似于铝,铬在空气中与氧气反应,其表面生成一层致密
的氧化膜,阻止铬进一步被氧化;
b. 铁锈的主要成分是F O,与稀盐酸反应生成氯化铁和水,化学方程式为
e2 3
Fe O+6HCl=2FeCl +3H O;
2 3 3 2
拓展应用:
在水龙头的使用过程中,手的拧动会对水龙头表面产生摩擦力,如果水龙头表面硬度不够,
就容易被磨损,导致表面光泽度下降、出现划痕等问题,除考虑美观和成本因素外,根据
水龙头的使用特点,铁质水龙头上镀铬主要是利用了铬的抗腐蚀性好和硬度大(或耐磨,
耐磨性强)。
19.(1)11:4
(2)192
(3)解:设10片补钙剂中CaCO 质量为x
3
x=9g
上述CaCO 中钙元素质量为:
3
该补钙剂中含钙元素的质量分数为: 大于17.5%
答:补钙剂中含钙元素的质量分数为18.0%,此标签标注的含钙量真实。
【详解】(1)维生素D 中氢、氧元素的质量比为:(44×1):(1×16)=44:16=11:4;
3
答案第8页,共2页(2)含有 8g 氧元素的维生素D 的质量为: ;
3
(3)见答案。
答案第9页,共2页