文档内容
济宁市二二一年初中学业水平考试
可能用到的相对原子质量:H-1 C-12 O-16 Cl-35.5 Na-23 Ca-40
第Ⅰ卷(选择题 共16分)
一、选择题(下列各题只有一个正确选项。其中,1~4小题各1分,5~10小题各2分,本大题共16分)
1.下列日常生活中的现象,没有发生化学变化的是( )
A.光合作用
B.滴水成冰
C.牛奶酸败
D.食醋酿造
2.下面对于过氧化氢(H O)组成的说法,正确的是( )
2 2
A.过氧化氢由氢气和氧气组成
B.过氧化氢由氢分子和氧分子构成
C.过氧化氢由氢元素和氧元素组成
D.过氧化氢由氢原子和氧原子构成
3.下列各组物质,都属于氧化物的一组是( )
A.MnO 、SO 、PO
2 2 2 5
B.ZnO、CO、HSO
2 2 3
C.Na O、HO、KClO
2 2 3
D.SiO、KOH、CHO
2 4
4.下列化学方程式的书写和对反应类型的判断,都正确的是( )
A.2FeCl +Fe 3FeCl 化合反应
3 2
B.HgO Hg+O↑ 分解反应
2
C.CuO+CO Cu+CO 置换反应
2
D.KCl+HNO KNO+HCl 复分解反应
3 3
5.根据下面实验过程得出的结论,不正确的是( )
实验结论
氧气浓度大,木炭燃烧剧烈
二氧化碳能与水反应生成碳酸氢氧化钠固体有吸水性
溶液中一定含有SO2-
4
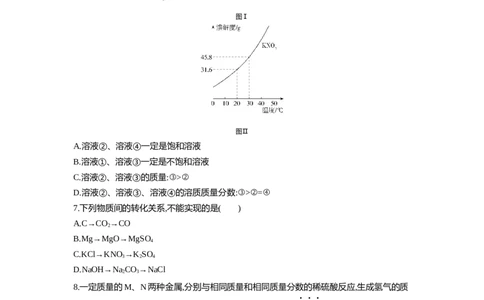
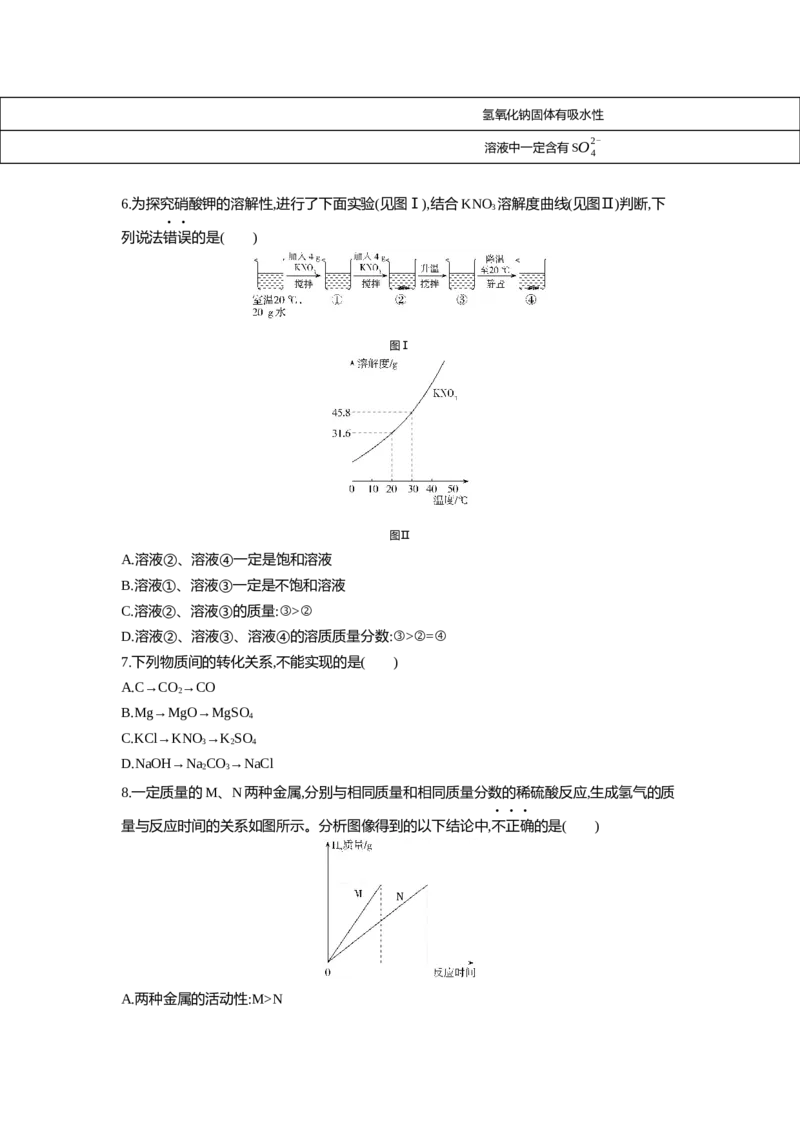
6.为探究硝酸钾的溶解性,进行了下面实验(见图Ⅰ),结合KNO 溶解度曲线(见图Ⅱ)判断,下
3
列说法错误的是( )
图Ⅰ
图Ⅱ
A.溶液②、溶液④一定是饱和溶液
B.溶液①、溶液③一定是不饱和溶液
C.溶液②、溶液③的质量:③>②
D.溶液②、溶液③、溶液④的溶质质量分数:③>②=④
7.下列物质间的转化关系,不能实现的是( )
A.C→CO→CO
2
B.Mg→MgO→MgSO
4
C.KCl→KNO→KSO
3 2 4
D.NaOH→NaCO→NaCl
2 3
8.一定质量的M、N两种金属,分别与相同质量和相同质量分数的稀硫酸反应,生成氢气的质
量与反应时间的关系如图所示。分析图像得到的以下结论中,不正确的是( )
A.两种金属的活动性:M>NB.两种金属生成氢气的质量:M=N
C.两种金属消耗稀硫酸的质量:M=N
D.充分反应后,得到溶液的质量:M=N
9.下列四组物质的溶液,使用一种试剂仅通过一次反应就能将它们鉴别开来的是( )
A.HCl、NaOH、NaCO B.NaCl、NaCO、NaNO
2 3 2 3 3
C.NaCl、BaCl 、KCO D.NaOH、BaCl 、Ba(NO )
2 2 3 2 3 2
10.为确定某溶液中含有以下离子H+、Mg2+、Ba2+、Cl-、C O2-、N O-中的几种,进行了以下
3 3
实验:
①经测定,溶液pH=1;
②取部分未知溶液,加入过量NaOH溶液,有白色沉淀产生;
③取②中部分溶液,加入NaCO 溶液,无明显现象。
2 3
分析上述实验,下面对溶液中含有离子的判断,正确的是 ( )
A.一定含有H+、Mg2+、Ba2+、Cl-、N
O-
3
B.一定含有H+、Mg2+、Cl-,一定不含有C
O2-
3
C.一定含有H+、Ba2+、N
O-
,一定不含有Cl-
3
D.一定含有H+、Mg2+,可能同时含有Cl-、N
O-
3
第Ⅱ卷(非选择题 共34分)
二、填空与简答(共17分)
11.(4分)利用氢、氮、氧三种元素,按要求用符号回答下面问题:
(1)具有可燃性的气体单质 ;
(2)化学性质稳定的气体单质 ;
(3)由氢、氮两种元素组成的化合物 ;
(4)由氢、氮、氧三种元素组成的化合物 。
12.(3分)下表是元素周期表第三周期的元素,请回答:
(1)元素周期表每个方格中都标有元素的基本信息,左上角数字表示该元素的 ;
(2)下图四种粒子结构示意图中,属于同一种元素的是 (填序号),该元素与钠元素形成
化合物的化学式为 。13.(3分)化学肥料对农作物的增产具有十分重要的作用,俗话说:“庄稼一枝花,全靠肥当家”。
下面是农业生产中广泛施用的几种化学肥料:①NHNO ②KNO ③NH Cl
4 3 3 4
④(NH )HPO
4 2 4
请回答:
(1)属于复合肥料的是 (填序号,下同);
(2)属于铵态氮肥的是 ,它们成分中都含有的离子是 (填符号)。
14.(4分)铝在地壳中主要以铝土矿的形式存在,铝土矿的主要成分为Al O(含有少量Fe O、
2 3 2 3
SiO 等杂质)。工业上冶炼铝的工艺流程见下图:
2
(1)铝土矿中的SiO 不溶于水,也不与盐酸反应,操作①的目的是 ;
2
(2)操作③得到的Al(OH) 受热分解生成Al O,该反应的化学方程式为
3 2 3
,铝土矿经过操作①~④的目的是 ;
(3)在冰晶石作助熔剂条件下,高温电解Al O 得到金属铝,该反应的化学方程式为
2 3
。
15.(3分)实验废液中含有AgNO、Cu(NO ) 和Mg(NO),为减少废液对环境的影响,实验小组
3 3 2 3 2
的同学做了下面的实验:
(1)取废液样品,加入少量锌粉,充分反应后,过滤,向滤渣中加入稀盐酸,无明显现象,则滤渣中
一定含有的金属是 (填符号,下同);
(2)另取废液样品,加入过量锌粉,充分反应后,过滤,向滤渣中加入稀盐酸,有气泡产生,则滤液
中含有的溶质是 。实验表明,加入过量锌粉能有效去除废液中的离子是
。
三、实验与探究(共11分)
16.(1)(6分)某兴趣小组为探究甲烷的元素组成,经查询资料,采用下图所示装置,制取并收集一
定量甲烷气体进行实验。
【查询资料】
Ⅰ.甲烷是一种无色无味的气体,密度比空气小、难溶于水、有可燃性
Ⅱ.实验室常用醋酸钠和碱石灰固体共热制取甲烷,有关反应的化学反应方程式:CHCOONa+NaOH NaCO+CH ↑
3 2 3 4
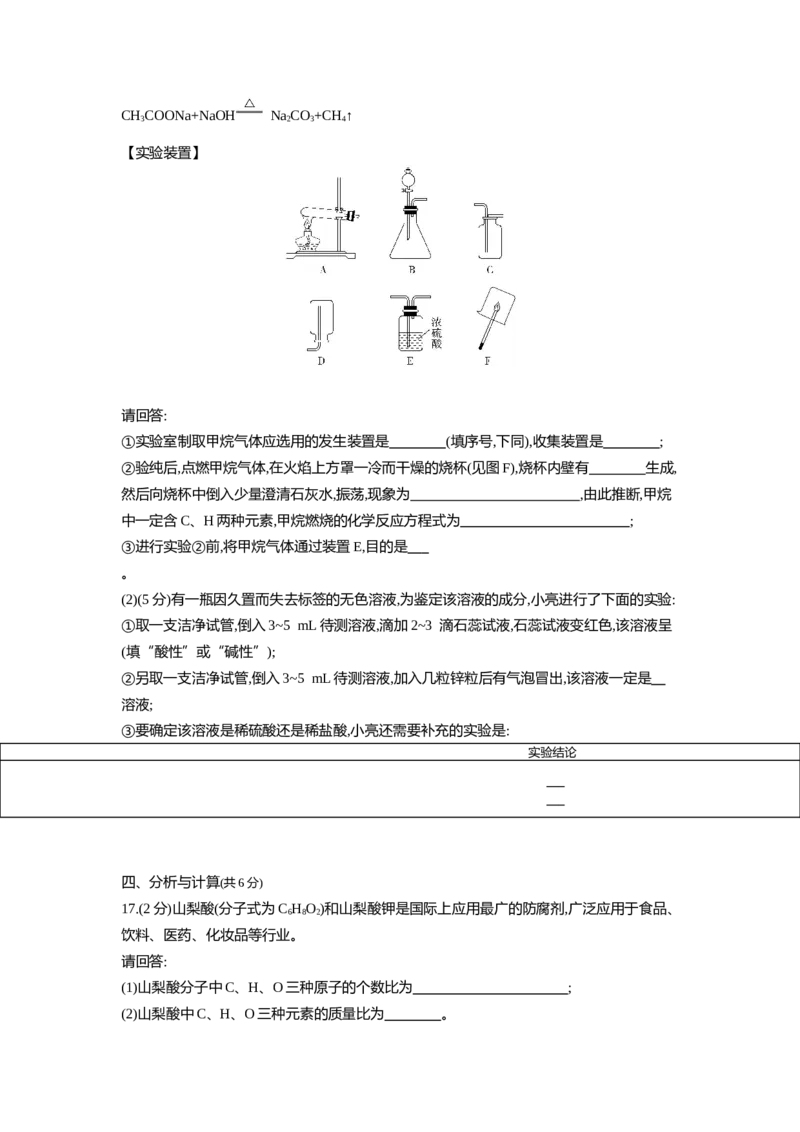
【实验装置】
请回答:
①实验室制取甲烷气体应选用的发生装置是 (填序号,下同),收集装置是 ;
②验纯后,点燃甲烷气体,在火焰上方罩一冷而干燥的烧杯(见图F),烧杯内壁有 生成,
然后向烧杯中倒入少量澄清石灰水,振荡,现象为 ,由此推断,甲烷
中一定含C、H两种元素,甲烷燃烧的化学反应方程式为 ;
③进行实验②前,将甲烷气体通过装置E,目的是
。
(2)(5分)有一瓶因久置而失去标签的无色溶液,为鉴定该溶液的成分,小亮进行了下面的实验:
①取一支洁净试管,倒入3~5 mL待测溶液,滴加2~3 滴石蕊试液,石蕊试液变红色,该溶液呈
(填“酸性”或“碱性”);
②另取一支洁净试管,倒入3~5 mL待测溶液,加入几粒锌粒后有气泡冒出,该溶液一定是
溶液;
③要确定该溶液是稀硫酸还是稀盐酸,小亮还需要补充的实验是:
实验结论
四、分析与计算(共6分)
17.(2分)山梨酸(分子式为C HO)和山梨酸钾是国际上应用最广的防腐剂,广泛应用于食品、
6 8 2
饮料、医药、化妆品等行业。
请回答:
(1)山梨酸分子中C、H、O三种原子的个数比为 ;
(2)山梨酸中C、H、O三种元素的质量比为 。18.(4分)市售的食用纯碱往往含有少量氯化钠,探究小组以某品牌食用纯碱为样品测定其中
NaCO 的质量分数,实验过程如下:
2 3
食用纯碱
名称:食用纯碱
净重:400 g
保质期:十八个月
质检:符合国家食品安全要求
储存方法:阴凉干燥通风处
请分析实验过程,回答:
(1)写出相关反应的化学方程式: ;
(2)实验中加入“过量”CaCl 溶液,目的是
2
;
(3)若取用样品的质量为2.2 g,且实验过程中无质量损失,最终得到沉淀的质量为2 g。则2.2
g纯碱样品中NaCO 的质量为 g,该品牌食用纯碱中NaCO 的质量分数为 。
2 3 2 3
23 济宁市二二一年初中学业水平考试(参考答案)
1 2 3 4 5 6 7 8 9 10
B C A A D B C D C D
一、选择题
1.B 光合作用、牛奶酸败、食醋酿造的过程中都有新物质生成,属于化学变化;滴水成冰只
是水的状态发生改变,没有新物质生成,属于物理变化,故选B。
2.C 过氧化氢是由氢元素和氧元素组成的,故选C。
方法指导 描述物质的组成和构成的正确说法:过氧化氢由氢元素和氧元素组成;过氧化氢分子由氢原子和氧原子构成;
一个过氧化氢分子由2个氢原子和2个氧原子构成。
3.A MnO 、SO 、PO 都是由氧元素和另一种元素组成的化合物,都属于氧化物;H SO 、
2 2 2 5 2 3
KClO、KOH、CHO中虽然都含有氧元素,但它们都是由三种元素组成的,不属于氧化物。
3 4
4.A A中化学方程式书写正确,两种物质生成一种物质的反应,属于化合反应,故A正确;氧化
汞分解的化学方程式没有配平,故B错误;CO还原氧化铜是两种化合物反应生成一种单质和
一种化合物,不属于置换反应,故C错误;KCl和HNO 不反应,故D错误。
35.D 木炭在氧气中剧烈燃烧,是因为氧气的浓度越大,可燃物燃烧越剧烈,故A正确;湿润的
蓝色石蕊试纸放入二氧化碳中,试纸变红是因为二氧化碳和水反应生成了碳酸,故B正确;氢
氧化钠固体有吸水性,放置在空气中,表面变潮湿并且逐渐溶解,故C正确;Ag+或S O2-遇到氯
4
化钡溶液都能产生不溶于稀硝酸的白色沉淀,故D错误。
6.B 溶液②、溶液④的烧杯底部都有固体存在,一定是饱和溶液,故A正确;20 ℃时,硝酸钾
的溶解度为31.6 g,20 g 水中最多能溶解6.32 g硝酸钾,故溶液①一定是不饱和溶液,溶液③
的烧杯底部没有固体存在,可能是不饱和溶液,也可能恰好达到饱和,故B错误;溶液②中有溶
质没有溶解,溶液质量小于28 g,溶液③中的溶质完全溶解,溶液质量等于28 g,故C正确;溶
液②中有溶质没有溶解,溶液③中的溶质完全溶解,溶剂质量相等,故溶质质量分数③>②,溶液
②和溶液④都是20 ℃时硝酸钾的饱和溶液,溶质质量分数相等,故D正确。
7.C 碳在氧气中完全燃烧生成二氧化碳,二氧化碳和碳在高温下反应生成一氧化碳,故A能
实现;镁在氧气中燃烧生成氧化镁,氧化镁和稀硫酸反应生成硫酸镁,故B能实现;氯化钾和硝
酸银反应生成硝酸钾,硝酸钾不能反应生成硫酸钾,故C不能实现;氢氧化钠和二氧化碳反应
生成碳酸钠,碳酸钠和稀盐酸反应生成氯化钠,故D能实现。
方法指导 判断复分解反应能否发生时,反应物中有KNO、NaNO、AgCl、BaSO 中的任意一种,复分解反应不能发生。
3 3 4
8.D 从题图可知,金属的活动性M>N,生成氢气的质量相等,根据质量守恒定律可知,反应消
耗稀硫酸的质量相等,A、B、C正确,故选D。
规律总结 两种足量的活泼金属与等质量、等质量分数的稀硫酸反应,生成等质量的氢气,则消耗稀硫酸的质量一定相等,
消耗金属的质量一定不相等,反应后溶液的质量不相等。
9.C 向NaCl、BaCl 、KCO 的溶液中分别滴加稀硫酸,无明显现象的是NaCl,生成白色沉
2 2 3
淀的是BaCl ,产生气泡的是KCO,能够一次鉴别,故选C。
2 2 3
10.D 溶液的pH=1,显酸性,证明溶液中一定存在H+,一定不存在C
O2-
;加入过量的氢氧化钠
3
溶液,产生白色沉淀,证明一定有Mg2+;加入碳酸钠溶液无明显现象,证明一定没有Ba2+。根据
溶液中阳离子和阴离子的正、负电荷总数相等可知,溶液中可能同时含有Cl-和N
O-
,也可能
3
只含有其中一种,故A、B、C错误,D正确。
二、填空与简答
11.答案 (1)H (2)N (3)NH (4)HNO(或NH NO 或NH ·HO)
2 2 3 3 4 3 3 2
解析 (1)具有可燃性的气体单质是氢气,化学式为H。(2)化学性质稳定的气体单质是氮气,
2
化学式为N。(3)由氢、氮两种元素组成的化合物是氨气,化学式为NH 。(4)由氢、氮、氧
2 3
三种元素组成的化合物的化学式为HNO(或NH NO 或NH ·HO)。
3 4 3 3 2
12.答案 (1)原子序数 (2)C、D NaS
2
解析 (1)元素周期表每个方格的左上角数字表示该元素的原子序数。(2)C、D的质子数相
同,属于同一种元素,该元素是硫元素,其与钠元素形成的化合物是硫化钠,化学式为NaS。
2
13.答案 (1)②④ (2)①③ N
H+
4
解析 (1)②中含有K、N,属于复合肥,④中含有N、P,属于复合肥。(2)①和③属于铵态氮肥。
14.答案 (1)除去SiO
2
(2)2Al(OH) Al O+3H O 得到纯净的Al O
3 2 3 2 2 3
(3)2AlO 4Al+3O ↑
2 3 2
解析 (1)SiO 不溶于水,也不与盐酸反应,AlO、Fe O 和盐酸反应,所以操作①的目的是除
2 2 3 2 3
去SiO。(2)氢氧化铝受热分解生成氧化铝和水,化学方程式为2Al(OH) Al O+3H O;铝
2 3 2 3 2
土矿经过操作①~④,除去SiO、Fe O 等杂质,得到纯净的Al O。(3)在冰晶石作助熔剂条件
2 2 3 2 3
下,高温电解氧化铝生成铝和氧气,化学方程式为2Al O 4Al+3O ↑。
2 3 2
15.答案 (1)Ag (2)Mg(NO)、Zn(NO ) Ag+、Cu2+
3 2 3 2
解析 锌和硝酸镁不反应;锌先和硝酸银反应生成银和硝酸锌,硝酸银反应完全后,锌再和硝
酸铜反应生成铜和硝酸锌。(1)向滤渣中加入稀盐酸,无明显现象,证明滤渣中一定没有Zn,一定有Ag,可能有Cu。(2)向滤渣中加入稀盐酸,产生气泡,证明滤渣中一定有Zn,因为锌是过量
的,所以滤液中一定没有AgNO 和Cu(NO ),一定含有没有反应的Mg(NO) 和反应生成的
3 3 2 3 2
Zn(NO )。实验表明,加入过量的锌粉能够有效去除废液中的Ag+、Cu2+。
3 2
方法技巧 固体混合物中一种金属存在,那么排在它后面的金属的离子一定不存在;溶液中一种金属离子存在,那么排在
它前面的金属一定不存在。
三、实验与探究
16.答案 (1)①A D ②水珠 澄清石灰水变浑浊 CH+2O CO+2H O ③除去甲烷
4 2 2 2
中的水蒸气 (2)①酸性 ②酸 ③取待测液少许倒入试管中,滴加硝酸钡溶液或氯化钡溶液
产生白色沉淀(无明显现象) 该溶液是稀硫酸(稀盐酸)
解析 (1)①实验室制取甲烷应用固固加热型发生装置,故选A;因为甲烷密度小于空气,故收
集装置选D。②甲烷燃烧生成水和二氧化碳,现象是烧杯内壁上出现水珠,倒入烧杯中的澄清
石灰水变浑浊,甲烷燃烧的化学方程式为CH+2O CO+2H O。③进行实验②前,将甲烷
4 2 2 2
气体通过装置E,目的是除去甲烷中的水蒸气。(2)①滴加石蕊试液,石蕊试液变红,证明溶液
显酸性。②活泼金属能和酸反应生成氢气,待测液中加入锌粒产生气泡,证明待测液一定是酸
溶液。③确定待测液是稀硫酸还是稀盐酸,设计实验如下:取待测液少许倒入试管中,滴加硝
酸钡溶液或氯化钡溶液,如果产生白色沉淀,则该溶液是稀硫酸;如果无明显现象,则待测液是
稀盐酸。
易错警示 要鉴别S O2-和Cl-时,一定要加入含Ba2+的盐溶液(硝酸钡溶液或氯化钡溶液),不能加入硝酸银溶液,因为
4
Ag+和Cl-反应生成白色沉淀,Ag+和S O2-反应生成微溶于水的硫酸银,也可能出现白色沉淀。
4
四、分析与计算
17.答案 (1)3∶4∶1 (2)9∶1∶4
解析 (1)根据山梨酸的化学式可知,山梨酸分子中C、H、O三种原子的个数比是
6∶8∶2=3∶4∶1。(2)山梨酸中C、H、O三种元素的质量比是(6×12)∶(8×1)∶(2×16)=9∶1∶4。
18.答案 (1)Na CO+CaCl CaCO ↓+2NaCl
2 3 2 3
(2)使碳酸钠完全反应 (3)2.12 96.4%
解析 (1)碳酸钠和氯化钙反应生成碳酸钙和氯化钠,化学方程式为NaCO+CaCl
2 3 2
CaCO ↓+2NaCl。(2)加入过量氯化钙溶液是为了使碳酸钠完全反应。
3
(3)设2.2 g纯碱样品中碳酸钠的质量为x。
NaCO+CaCl CaCO ↓+2NaCl
2 3 2 3
106 100
x 2 g
106 x
= x=2.12 g
100 2 g
2.12 g
碳酸钠的质量分数为 ×100%≈96.4%。
2.2 g