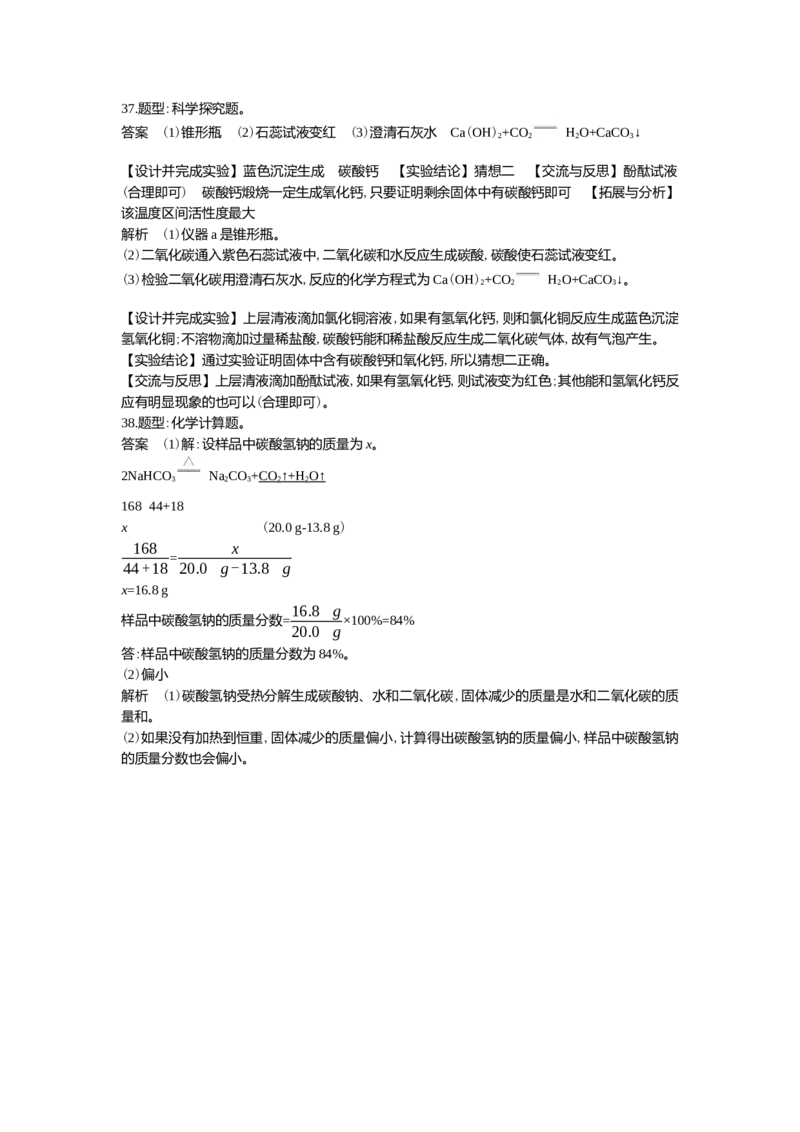文档内容
2022年山东省枣庄市初中学业水平考试
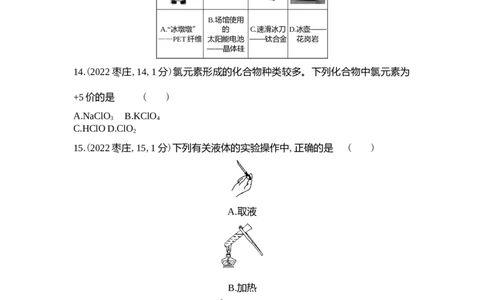
13.(2022枣庄,13,1分)2022年北京冬奥会取得圆满成功。下列冬奥会用品涉及
的材料中,属于金属材料的是 ( )
B.场馆使用
A.“冰墩墩” 的 C.速滑冰刀 D.冰壶——
——PET纤维 太阳能电池 ——钛合金 花岗岩
——晶体硅
14.(2022枣庄,14,1分)氯元素形成的化合物种类较多。下列化合物中氯元素为
+5价的是 ( )
A.NaClO B.KClO
3 4
C.HClOD.ClO
2
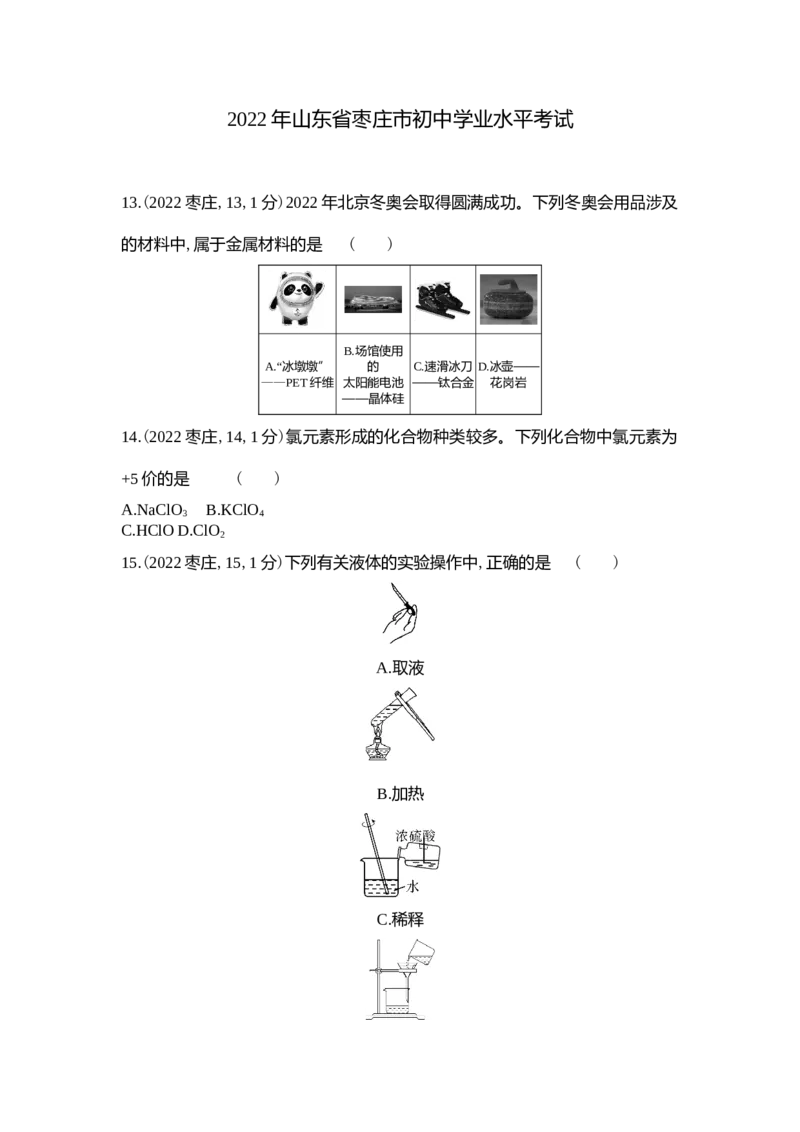
15.(2022枣庄,15,1分)下列有关液体的实验操作中,正确的是 ( )
A.取液
B.加热
C.稀释D.过滤
16.(2022枣庄,16,1分)下列物质的用途主要由其物理性质决定的是 ( )
A.用稀盐酸除铁锈
B.用石墨做电极
C.用生石灰作干燥剂
D.用铁矿石炼铁
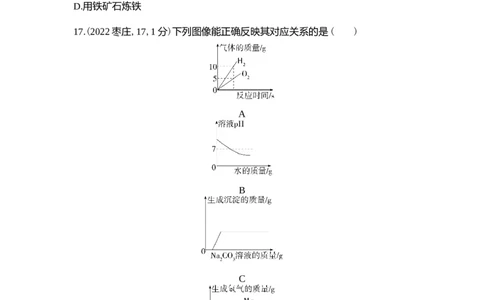
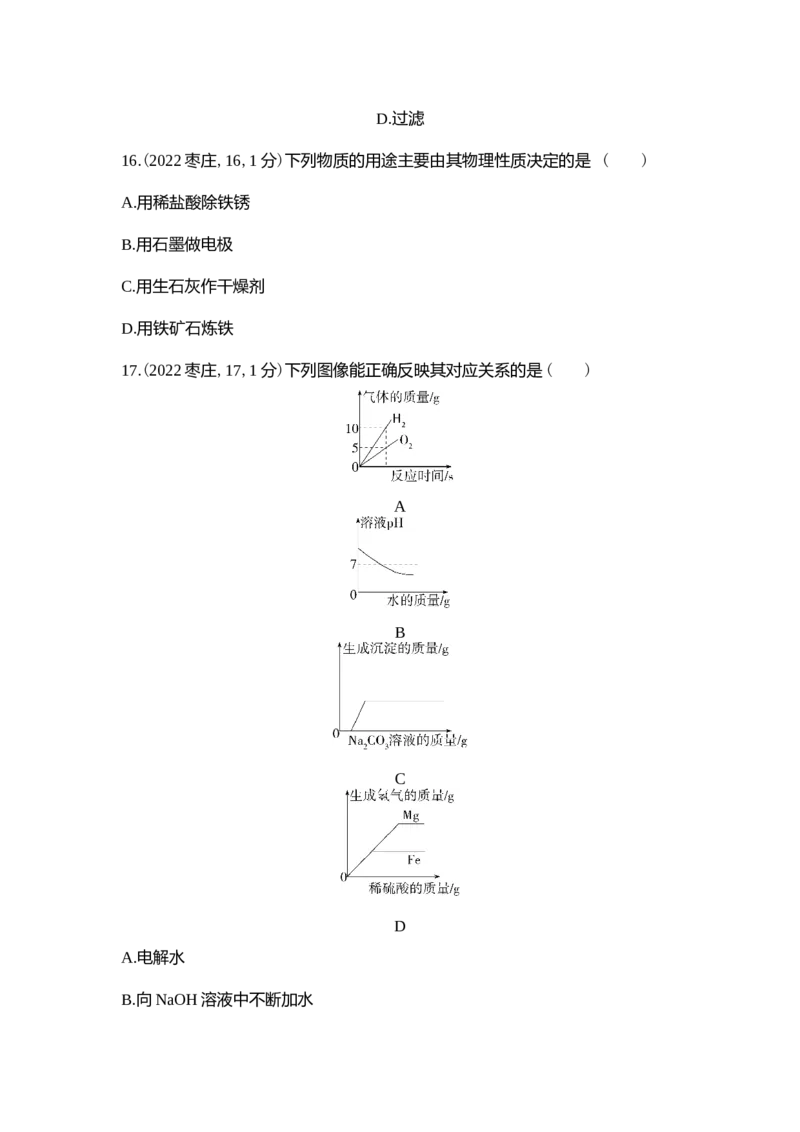
17.(2022枣庄,17,1分)下列图像能正确反映其对应关系的是( )
A
B
C
D
A.电解水
B.向NaOH溶液中不断加水C.向CaCl 溶液中滴加Na CO 溶液至过量
2 2 3
D.向等质量的镁粉和铁粉中分别逐滴加入同浓度的稀硫酸至过量
18.(2022枣庄,18,1分)下列物质中,前者属于氧化物,后者属于混合物的是 (
)
A.熟石灰、海水
B.冰水混合物、食盐水
C.干冰、硫酸钠
D.生铁、二氧化锰
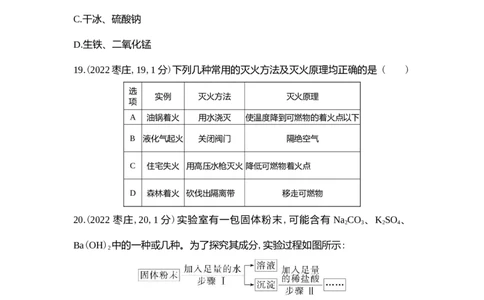
19.(2022枣庄,19,1分)下列几种常用的灭火方法及灭火原理均正确的是 ( )
选
实例 灭火方法 灭火原理
项
A 油锅着火 用水浇灭 使温度降到可燃物的着火点以下
B 液化气起火 关闭阀门 隔绝空气
C 住宅失火 用高压水枪灭火 降低可燃物着火点
D 森林着火 砍伐出隔离带 移走可燃物
20.(2022 枣庄,20,1 分)实验室有一包固体粉末,可能含有 Na CO 、K SO 、
2 3 2 4
Ba(OH) 中的一种或几种。为了探究其成分,实验过程如图所示:
2
下列说法错误的是 ( )
A.步骤Ⅰ中得到的溶液一定显碱性
B.步骤Ⅱ中沉淀若全部溶解,则原固体粉末一定有Ba(OH) 、Na CO ,一定没有
2 2 3
K SO
2 4
C.步骤Ⅱ中沉淀若部分溶解,则原固体粉末一定有 Ba(OH) 、Na CO 、K SO
2 2 3 2 4D.步骤Ⅱ中沉淀若不溶解,则原固体粉末一定有 Ba(OH) ,可能有 Na CO 、
2 2 3
K SO
2 4
一、填空与简答题(本题包括5个小题,共30分)
33.(2022枣庄,33,5分)空气又称大气,是生命、燃烧和工业等所需氧的主要来
源。
(1)空气中,氧气的体积分数约为 ;构成氧气的粒子是 (写化学
式)。
(2)氧原子结构示意图为 ,在化学变化中易 (填“得到”或“失
去”)电子。
(3)在低温、加压条件下,将空气液化,然后将温度升高至-196 ℃~-183 ℃,使液态
氮先蒸发,剩余液态氧储存于钢瓶中。从微观视角分析,空气液化过程中,主要改
变的是 。
34.(2022枣庄,34,5分)溶液与人类的生产生活息息相关。
(1)下列物质分别放入适量水中,充分搅拌,能够得到溶液的是 (填字母
标号)。
A.面粉 B.白糖 C.豆油
(2)配制一定溶质质量分数的溶液的步骤有①溶解 ②计算 ③装瓶并贴标签
④称量(量取)。其正确的顺序为 (填序号)。
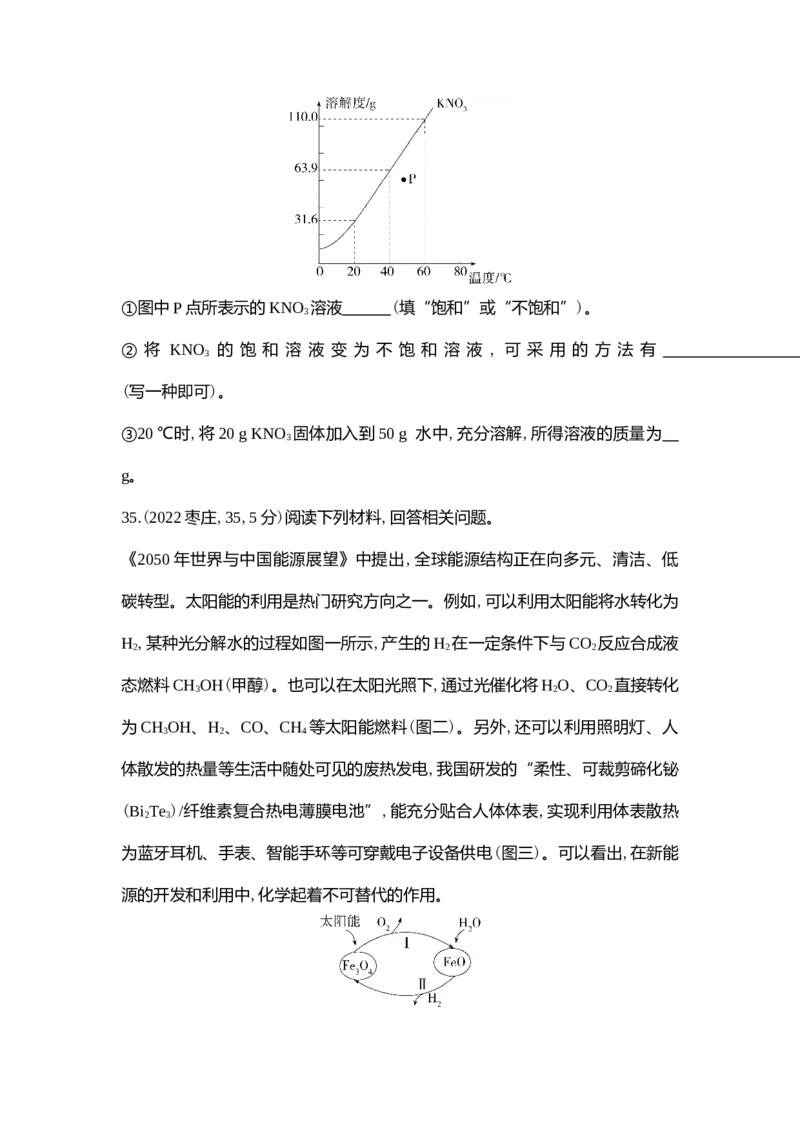
(3)硝酸钾的溶解度曲线如图所示,回答下列问题:①图中P点所表示的KNO 溶液 (填“饱和”或“不饱和”)。
3
② 将 KNO 的 饱 和 溶 液 变 为 不 饱 和 溶 液 , 可 采 用 的 方 法 有
3
(写一种即可)。
③20 ℃时,将20 g KNO 固体加入到50 g 水中,充分溶解,所得溶液的质量为
3
g。
35.(2022枣庄,35,5分)阅读下列材料,回答相关问题。
《2050年世界与中国能源展望》中提出,全球能源结构正在向多元、清洁、低
碳转型。太阳能的利用是热门研究方向之一。例如,可以利用太阳能将水转化为
H ,某种光分解水的过程如图一所示,产生的H 在一定条件下与CO 反应合成液
2 2 2
态燃料CH OH(甲醇)。也可以在太阳光照下,通过光催化将H O、CO 直接转化
3 2 2
为CH OH、H 、CO、CH 等太阳能燃料(图二)。另外,还可以利用照明灯、人
3 2 4
体散发的热量等生活中随处可见的废热发电,我国研发的“柔性、可裁剪碲化铋
(Bi Te )/纤维素复合热电薄膜电池”,能充分贴合人体体表,实现利用体表散热
2 3
为蓝牙耳机、手表、智能手环等可穿戴电子设备供电(图三)。可以看出,在新能
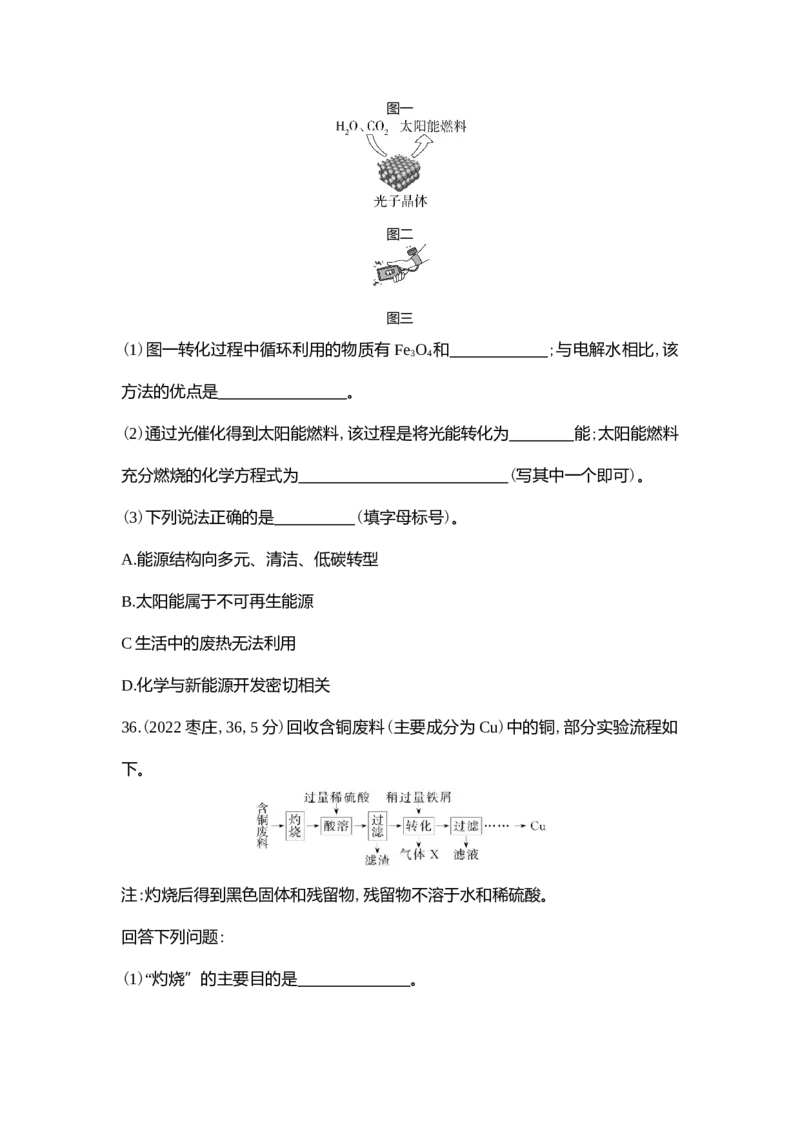
源的开发和利用中,化学起着不可替代的作用。图一
图二
图三
(1)图一转化过程中循环利用的物质有 Fe O 和 ;与电解水相比,该
3 4
方法的优点是 。
(2)通过光催化得到太阳能燃料,该过程是将光能转化为 能;太阳能燃料
充分燃烧的化学方程式为 (写其中一个即可)。
(3)下列说法正确的是 (填字母标号)。
A.能源结构向多元、清洁、低碳转型
B.太阳能属于不可再生能源
C生活中的废热无法利用
D.化学与新能源开发密切相关
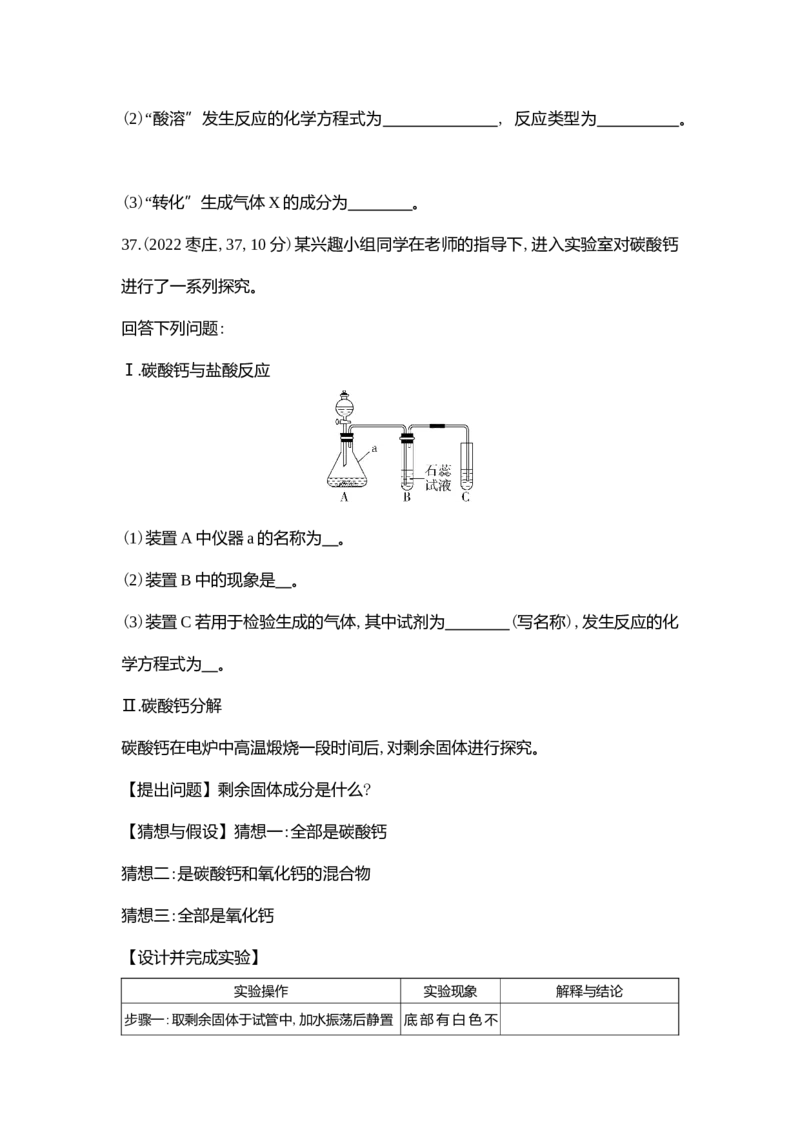
36.(2022枣庄,36,5分)回收含铜废料(主要成分为Cu)中的铜,部分实验流程如
下。
注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。
回答下列问题:
(1)“灼烧”的主要目的是 。(2)“酸溶”发生反应的化学方程式为 , 反应类型为 。
(3)“转化”生成气体X的成分为 。
37.(2022枣庄,37,10分)某兴趣小组同学在老师的指导下,进入实验室对碳酸钙
进行了一系列探究。
回答下列问题:
Ⅰ.碳酸钙与盐酸反应
(1)装置A中仪器a的名称为 。
(2)装置B中的现象是 。
(3)装置C若用于检验生成的气体,其中试剂为 (写名称),发生反应的化
学方程式为 。
Ⅱ.碳酸钙分解
碳酸钙在电炉中高温煅烧一段时间后,对剩余固体进行探究。
【提出问题】剩余固体成分是什么?
【猜想与假设】猜想一:全部是碳酸钙
猜想二:是碳酸钙和氧化钙的混合物
猜想三:全部是氧化钙
【设计并完成实验】
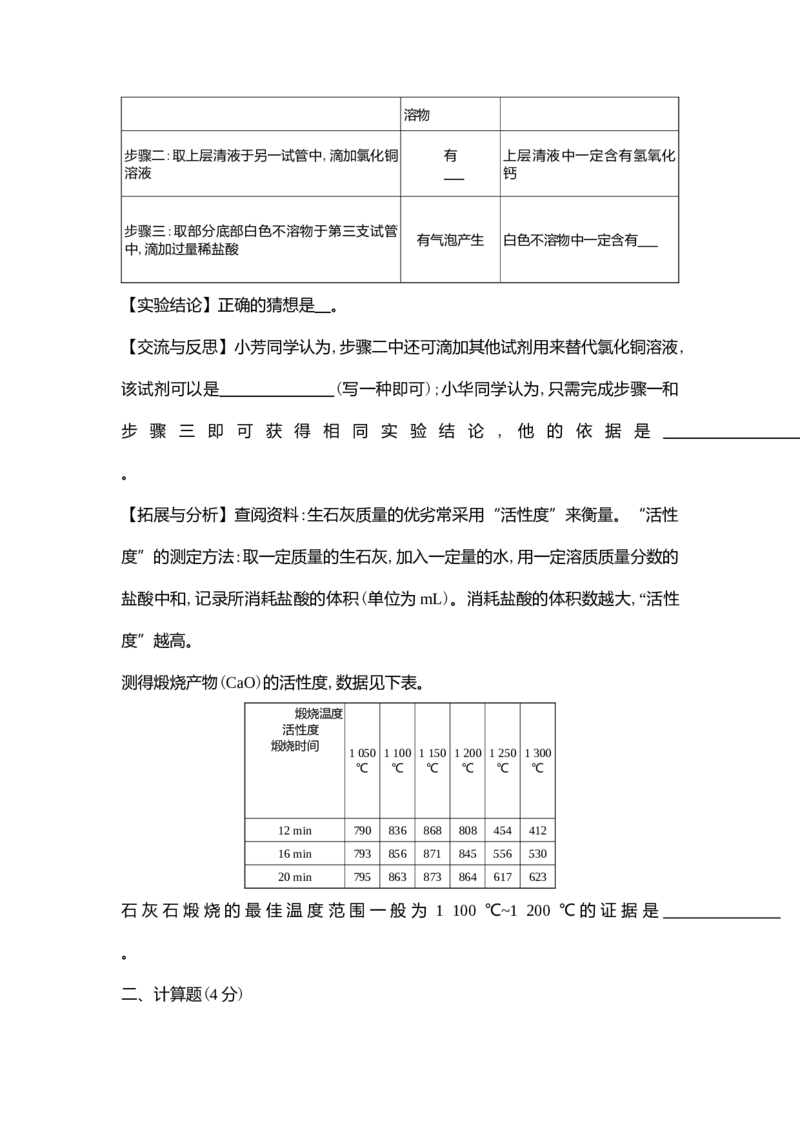
实验操作 实验现象 解释与结论
步骤一:取剩余固体于试管中,加水振荡后静置 底部有白色不溶物
步骤二:取上层清液于另一试管中,滴加氯化铜 有 上层清液中一定含有氢氧化
溶液 钙
步骤三:取部分底部白色不溶物于第三支试管
有气泡产生 白色不溶物中一定含有
中,滴加过量稀盐酸
【实验结论】正确的猜想是 。
【交流与反思】小芳同学认为,步骤二中还可滴加其他试剂用来替代氯化铜溶液,
该试剂可以是 (写一种即可);小华同学认为,只需完成步骤一和
步 骤 三 即 可 获 得 相 同 实 验 结 论 , 他 的 依 据 是
。
【拓展与分析】查阅资料:生石灰质量的优劣常采用“活性度”来衡量。“活性
度”的测定方法:取一定质量的生石灰,加入一定量的水,用一定溶质质量分数的
盐酸中和,记录所消耗盐酸的体积(单位为mL)。消耗盐酸的体积数越大,“活性
度”越高。
测得煅烧产物(CaO)的活性度,数据见下表。
煅烧温度
活性度
煅烧时间
1 050 1 100 1 150 1 200 1 250 1 300
℃ ℃ ℃ ℃ ℃ ℃
12 min 790 836 868 808 454 412
16 min 793 856 871 845 556 530
20 min 795 863 873 864 617 623
石 灰 石 煅 烧 的 最 佳 温 度 范 围 一 般 为 1 100 ℃~1 200 ℃ 的 证 据 是
。
二、计算题(4分)38.(2022枣庄,38,4分)碳酸氢钠是发酵粉的主要成分,常用作糕点、馒头的发
泡剂。为测定某碳酸氢钠样品中NaHCO 的质量分数,称取20.0 g样品,加热至恒
3
重(质量不再变化),称得固体质量为13.8 g。(已知:样品中杂质在加热过程中不
发生变化)
(1)计算样品中NaHCO 的质量分数。(写出计算过程)
3
(2)若上述测定过程中未加热至恒重,则测得NaHCO 的质量分数将 (填
3
“偏小”“偏大”或“无影响”)。
2022年山东省枣庄市初中学业水平考试
13.考点:金属材料。
C PET纤维属于有机合成材料,晶体硅、花岗岩属于无机非金属材料,钛合金属于金属材料,故
选C。
14.考点:化合价。
A 化合物中各元素正、负化合价的代数和为零。设氯元素的化合价为x,有+1+x+(-2)×3=0,解
得x=+5,故A正确;同理可得KClO、HClO、ClO 中氯元素的化合价分别为+7、+1、+4,故B、
4 2
C、D错误。
15.考点:实验基本技能。
C 为防止试剂腐蚀胶头或污染试剂,胶头滴管不能倒置,故A错误;给液体加热时,试管内的液
体不能超过其容积的三分之一,故B错误;稀释浓硫酸时,将浓硫酸慢慢倒入水中,并且用玻璃棒
不断搅拌,故C正确;过滤没有用玻璃棒引流,故D错误。
16.考点:物质的性质与用途。
B 用稀盐酸除铁锈是利用稀盐酸能和金属氧化物反应的化学性质,故A不符合题意;用石墨做
电极是利用石墨的导电性,属于物理性质,故B符合题意;用生石灰作干燥剂是利用生石灰能和
水反应的化学性质,故C不符合题意;用铁矿石炼铁是利用铁矿石能和一氧化碳反应的化学性质,
故D不符合题意。
17.考点:化学图表题。
D 电解水时生成氢气和氧气的体积比是2∶1,质量比是1∶8,故 A错误;向氢氧化钠溶液中不断加
入水,溶液碱性减弱,但溶液的pH不可能等于或小于7,故B错误;向氯化钙溶液中滴加碳酸钠溶
液,一开始就生成碳酸钙白色沉淀,故C错误;向等质量的镁粉和铁粉中分别逐渐加入同浓度的
稀硫酸,金属过量时,等质量稀硫酸反应生成的氢气质量相等,稀硫酸过量时,等质量的Mg和Fe
完全反应,Mg生成的氢气质量大,故D正确。
18.考点:物质的分类。
B 熟石灰是氢氧化钙的俗称,由三种元素组成,不属于氧化物,海水属于混合物;冰水混合物属
于氧化物,食盐水属于混合物;干冰是固态的二氧化碳,属于氧化物,硫酸钠属于纯净物;生铁属于
混合物,二氧化锰属于纯净物,故选B。
19.考点:燃烧与灭火。D 油锅着火不能用水浇灭,应用锅盖盖灭,故A错误;关闭阀门灭火的原理是移除可燃物,故B
错误;用高压水枪灭火,其原理是降低温度至可燃物的着火点以下,故C错误。
20.考点:物质的检验和鉴别。
D 固体粉末溶于水得到沉淀,说明原物质中一定有氢氧化钡。硫酸钾与氢氧化钡反应生成氢氧
化钾和硫酸钡,碳酸钠和氢氧化钡反应生成氢氧化钠和碳酸钡,溶液一定显碱性,故A正确;沉淀
全部溶解,说明沉淀是碳酸钡,原物质一定有氢氧化钡和碳酸钠,一定没有硫酸钾,故B正确;沉
淀部分溶解,说明沉淀是碳酸钡和硫酸钡,原物质一定有氢氧化钡、碳酸钠、硫酸钾,故C正确;
沉淀不溶解,说明沉淀是硫酸钡,原物质一定有氢氧化钡和硫酸钾,一定没有碳酸钠,故D错误。
33.考点:空气。
答案 (1)21% O (2) 得到 (3)分子间隔
2
解析 (1)空气中氧气的体积分数约为21% ,氧气是由O 构成的。
2
(2)氧原子的质子数是8,原子结构示意图为 ,最外层电子数是6,在化学反应中容易得到
电子。
(3)空气液化从微观视角分析是使分子间隔变小。
34.考点:溶液的配制。
答案 (1)B (2)②④①③ (3)①不饱和 ②加水(或升温) ③65.8
解析 (1)面粉不溶于水得到悬浊液;白糖溶于水得到溶液;豆油不溶于水得到乳浊液。
(2)配制一定溶质质量分数的溶液的步骤是计算、称量(量取)、溶解、装瓶并贴标签,故答案是
②④①③。(3)①P点在溶解度曲线下面,表示该温度下硝酸钾的不饱和溶液;②硝酸钾的饱和溶
液变为不饱和溶液的方法有加水或升温; ③20 ℃时,硝酸钾的溶解度是31.6 g,50 g水中只能溶
解15.8 g硝酸钾,故得到溶液的质量是65.8 g。
35.考点:化学与能源。
答案 (1)FeO 节约能源 (2)化学 2H+O 2HO(2CO+O 2CO 、CH+2O
2 2 2 2 2 4 2
CO+2HO、2CHOH+3O 2CO+4HO) (3)AD
2 2 3 2 2 2
解析 (1)从图一看出可以循环利用的物质有FeO 和FeO;该方法的优点是节约能源。
3 4
(2)该过程是将光能转化为化学能;太阳能燃料充分燃烧的化学方程式有2H+O 2HO、
2 2 2
2CO+O 2CO、CH+2O CO+2HO、2CHOH+3O 2CO+4HO 。
2 2 4 2 2 2 3 2 2 2
(3)太阳能属于可再生能源,故B错误;生活中的废热可以利用,故C错误;新能源的开发和利用
中,化学起着不可替代的作用,故D正确。
36.题型:工艺流程题。
答案 (1)将铜变为氧化铜 (2)CuO+HSO CuSO+HO 复分解反应 (3)H
2 4 4 2 2
解析 (1)“灼烧”的目的是将铜变为氧化铜。
(2)“酸溶”时,氧化铜和稀硫酸反应生成硫酸铜和水;该反应是两种化合物相互交换成分生成另
外两种化合物的反应,属于复分解反应。
(3)“转化”时,铁和过量的稀硫酸反应生成硫酸亚铁和氢气。37.题型:科学探究题。
答案 (1)锥形瓶 (2)石蕊试液变红 (3)澄清石灰水 Ca(OH)+CO HO+CaCO↓
2 2 2 3
【设计并完成实验】蓝色沉淀生成 碳酸钙 【实验结论】猜想二 【交流与反思】酚酞试液
(合理即可) 碳酸钙煅烧一定生成氧化钙,只要证明剩余固体中有碳酸钙即可 【拓展与分析】
该温度区间活性度最大
解析 (1)仪器a是锥形瓶。
(2)二氧化碳通入紫色石蕊试液中,二氧化碳和水反应生成碳酸,碳酸使石蕊试液变红。
(3)检验二氧化碳用澄清石灰水,反应的化学方程式为Ca(OH)+CO HO+CaCO↓。
2 2 2 3
【设计并完成实验】上层清液滴加氯化铜溶液,如果有氢氧化钙,则和氯化铜反应生成蓝色沉淀
氢氧化铜;不溶物滴加过量稀盐酸,碳酸钙能和稀盐酸反应生成二氧化碳气体,故有气泡产生。
【实验结论】通过实验证明固体中含有碳酸钙和氧化钙,所以猜想二正确。
【交流与反思】上层清液滴加酚酞试液,如果有氢氧化钙,则试液变为红色;其他能和氢氧化钙反
应有明显现象的也可以(合理即可)。
38.题型:化学计算题。
答案 (1)解:设样品中碳酸氢钠的质量为x。
2NaHCO NaCO+CO↑+HO↑
3 2 3 2 2
168 44+18
x (20.0 g-13.8 g)
168 x
=
44+18 20.0 g-13.8 g
x=16.8 g
16.8 g
样品中碳酸氢钠的质量分数= ×100%=84%
20.0 g
答:样品中碳酸氢钠的质量分数为84%。
(2)偏小
解析 (1)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,固体减少的质量是水和二氧化碳的质
量和。
(2)如果没有加热到恒重,固体减少的质量偏小,计算得出碳酸氢钠的质量偏小,样品中碳酸氢钠
的质量分数也会偏小。