文档内容
2022年山东日照初中学业水平考试
第Ⅰ卷(选择题 共36分)
一、选择题(本题共12小题,每小题3分,共36分。每小题只有一个选项符合题
目要求)
1.(2022日照,1,3分)我国提出争取在 2030年前实现碳达峰、2060年前实现碳
中和。碳中和是指CO 的排放总量和减少总量相当。下列措施中能促进碳中和
2
最直接有效的是 ( )
A.大力推广使用脱硫煤
B.加快煤的开采与使用,大力发展经济
C.大规模开采可燃冰作为新能源
D.用氨水捕集废气中的CO ,将其转化为氮肥
2
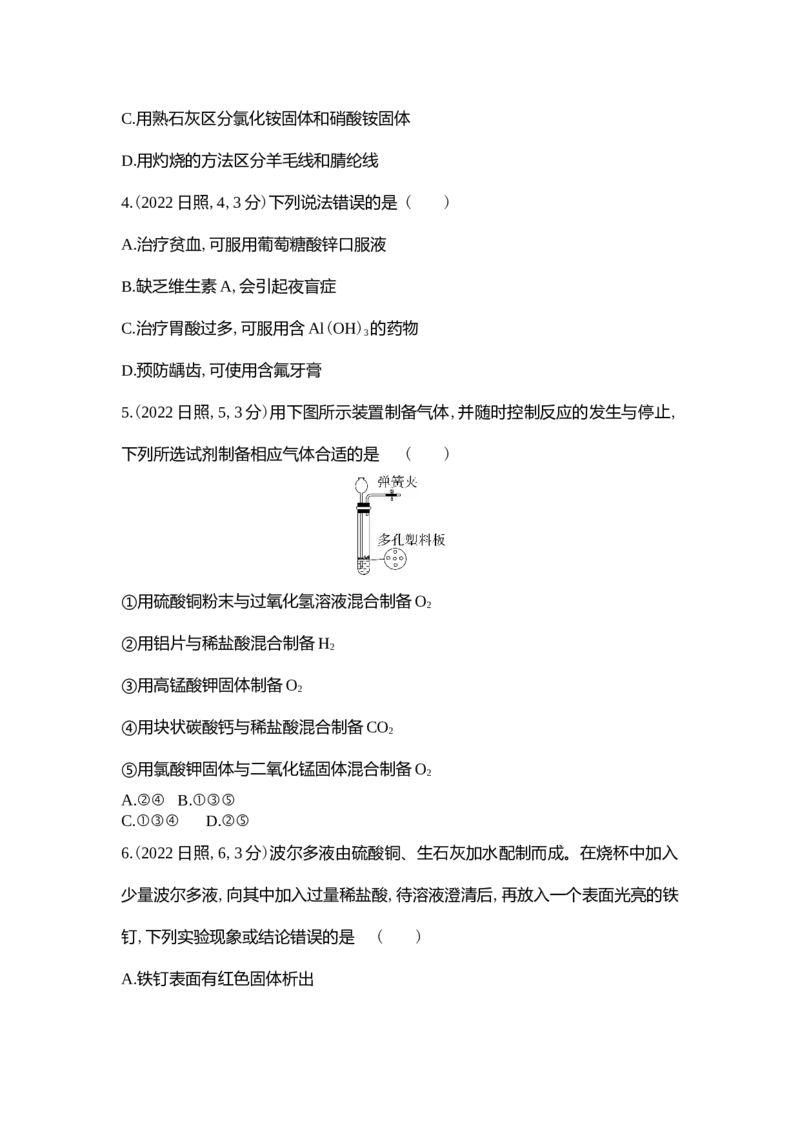
2.(2022日照,2,3分)下列图示的实验操作正确的是 ( )
3.(2022日照,3,3分)区分下列物质的试剂或方法错误的是 ( )
A.用水区分硝酸铵固体和氢氧化钠固体
B.用肥皂水区分硬水和软水C.用熟石灰区分氯化铵固体和硝酸铵固体
D.用灼烧的方法区分羊毛线和腈纶线
4.(2022日照,4,3分)下列说法错误的是 ( )
A.治疗贫血,可服用葡萄糖酸锌口服液
B.缺乏维生素A,会引起夜盲症
C.治疗胃酸过多,可服用含Al(OH) 的药物
3
D.预防龋齿,可使用含氟牙膏
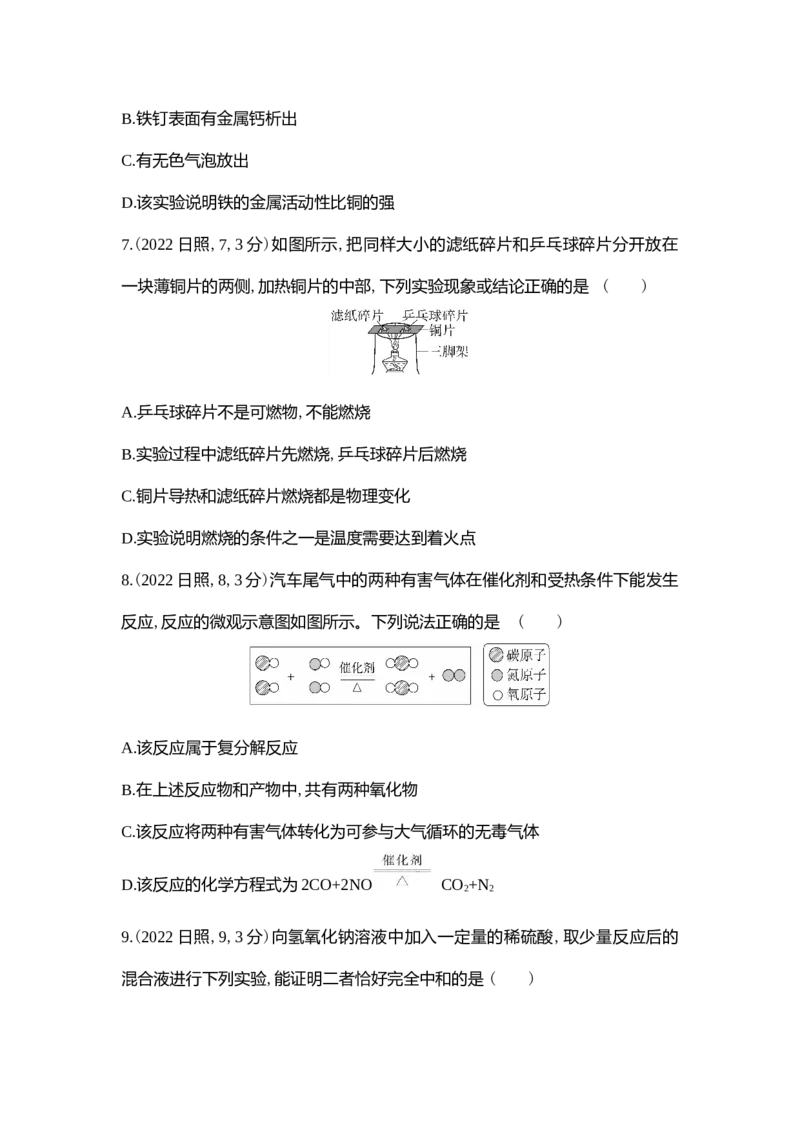
5.(2022日照,5,3分)用下图所示装置制备气体,并随时控制反应的发生与停止,
下列所选试剂制备相应气体合适的是 ( )
①用硫酸铜粉末与过氧化氢溶液混合制备O
2
②用铝片与稀盐酸混合制备H
2
③用高锰酸钾固体制备O
2
④用块状碳酸钙与稀盐酸混合制备CO
2
⑤用氯酸钾固体与二氧化锰固体混合制备O
2
A.②④ B.①③⑤
C.①③④ D.②⑤
6.(2022日照,6,3分)波尔多液由硫酸铜、生石灰加水配制而成。在烧杯中加入
少量波尔多液,向其中加入过量稀盐酸,待溶液澄清后,再放入一个表面光亮的铁
钉,下列实验现象或结论错误的是 ( )
A.铁钉表面有红色固体析出B.铁钉表面有金属钙析出
C.有无色气泡放出
D.该实验说明铁的金属活动性比铜的强
7.(2022日照,7,3分)如图所示,把同样大小的滤纸碎片和乒乓球碎片分开放在
一块薄铜片的两侧,加热铜片的中部,下列实验现象或结论正确的是 ( )
A.乒乓球碎片不是可燃物,不能燃烧
B.实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧
C.铜片导热和滤纸碎片燃烧都是物理变化
D.实验说明燃烧的条件之一是温度需要达到着火点
8.(2022日照,8,3分)汽车尾气中的两种有害气体在催化剂和受热条件下能发生
反应,反应的微观示意图如图所示。下列说法正确的是 ( )
A.该反应属于复分解反应
B.在上述反应物和产物中,共有两种氧化物
C.该反应将两种有害气体转化为可参与大气循环的无毒气体
D.该反应的化学方程式为2CO+2NO CO +N
2 2
9.(2022日照,9,3分)向氢氧化钠溶液中加入一定量的稀硫酸,取少量反应后的
混合液进行下列实验,能证明二者恰好完全中和的是( )A.滴入几滴酚酞溶液,溶液变红色
B.滴入适量CuCl 溶液,无沉淀生成
2
C.滴入适量BaCl 溶液和稀硝酸,观察到有白色沉淀
2
D.测得混合液中Na+与S 的个数比为2∶1
O2-
4
10.(2022日照,10,3分)用如图所示装置电解水,下列说法错误的是 ( )
A.M、N两导管口处收集的气体质量之比是1∶8
B.水中可加入少量硫酸钠或氢氧化钠以增强导电性
C.将带火星的木条放在M导管口处,木条会复燃
D.N处收集的气体,靠近火焰,若发出尖锐的爆鸣声,说明不纯
11.(2022日照,11,3分)白藜芦醇(C H O )广泛存在于葡萄、桑椹等植物果实
14 12 3
中,它具有抗肿瘤、抗氧化、延缓衰老等功效。下列说法正确的是 ( )
A.1个白藜芦醇分子中含有6个H 分子和1个O 分子
2 3
B.1个白藜芦醇分子是由14个碳元素、12个氢元素和3个氧元素组成的
C.白藜芦醇中C、H、O三种元素的质量比为14∶1∶4
D.白藜芦醇中氧元素的质量分数为48%
12.(2022日照,12,3分)某无色气体含有CH 、CO、H 中的一种或几种,在足量
4 2
O 中充分燃烧,生成的CO 与H O的质量比为11∶9,该无色气体不可能是 ( )
2 2 2
A.CH
4
B.CH 、H 分子数比为1∶2的混合气体
4 2C.CO、H 分子数比为1∶2的混合气体
2
D.CH 、CO、H 分子数比为1∶1∶2的混合气体
4 2
第Ⅱ卷(非选择题 共54分)
二、填空题(本题共4小题,共28分)
13.(2022日照,13,7分)近年来,我国航空航天事业成果显著,“北斗三号”导航卫
星搭载了精密计时的铷(Rb)原子钟。下图为铷元素在元素周期表中的信息和铷
的原子结构示意图。
回答下列问题:
(1)下列说法错误的是 (填标号)。
A.m=37,n=18
B.铷是金属元素
C.铷的相对原子质量是85.47
D.铷原子有5个电子层,最外层有1个电子
(2)Rb原子第一电子层上电子的能量比最外层上电子的能量 (填“低”或
“高”)。
(3)下图A~D所示粒子共表示 种元素,铷元素原子的化学性质与下图中
(填标号)的化学性质相似;Rb的硫酸盐的化学式为 。14.(2022日照,14,7分)新型冠状病毒肺炎疫情防控期间,应合理使用消毒剂进
行杀菌消毒。回答下列问题:
(1)用作消毒剂的医用酒精中乙醇的 (填“ 质量分数”或“体积分
数”)为 75%,因其易燃,使用时应远离火源,乙醇燃烧的化学方程式为
。
(2)“84消毒液”的有效成分是次氯酸钠,可由氯气与氢氧化钠溶液反应制得,反
应的化学方程式为Cl +2NaOH NaCl+R+H O(已配平) ,其中R代表次氯酸
2 2
钠,则其化学式为 。
(3)二氧化氯(ClO )常温下为黄色气体,易溶于水,其水溶液是一种广谱消毒剂。
2
ClO 中氯元素的化合价是 。
2
(4) 过 氧 化 氢 溶 液 是 一 种 绿 色 消 毒 剂 , 这 种 消 毒 剂 的 优 点 是
。
(5)过氧乙酸(CH COOOH)是一种高效消毒剂,它对热不稳定,易发生分解反应,
3
生成乙酸(CH COOH)和一种气态单质,这种气态单质为双原子分子,推测其化学
3
式为 。
15.(2022日照,15,7分)下表是KNO 和NH Cl分别在不同温度时的溶解度。
3 4
温度/℃ 0 10 20 30 40 50 60
KNO 13.3 20.9 31.6 45.8 63.9 85.5 110
3
溶解
度/g NHCl 29.4 33.3 37.2 41.4 45.8 50.4 55.2
4
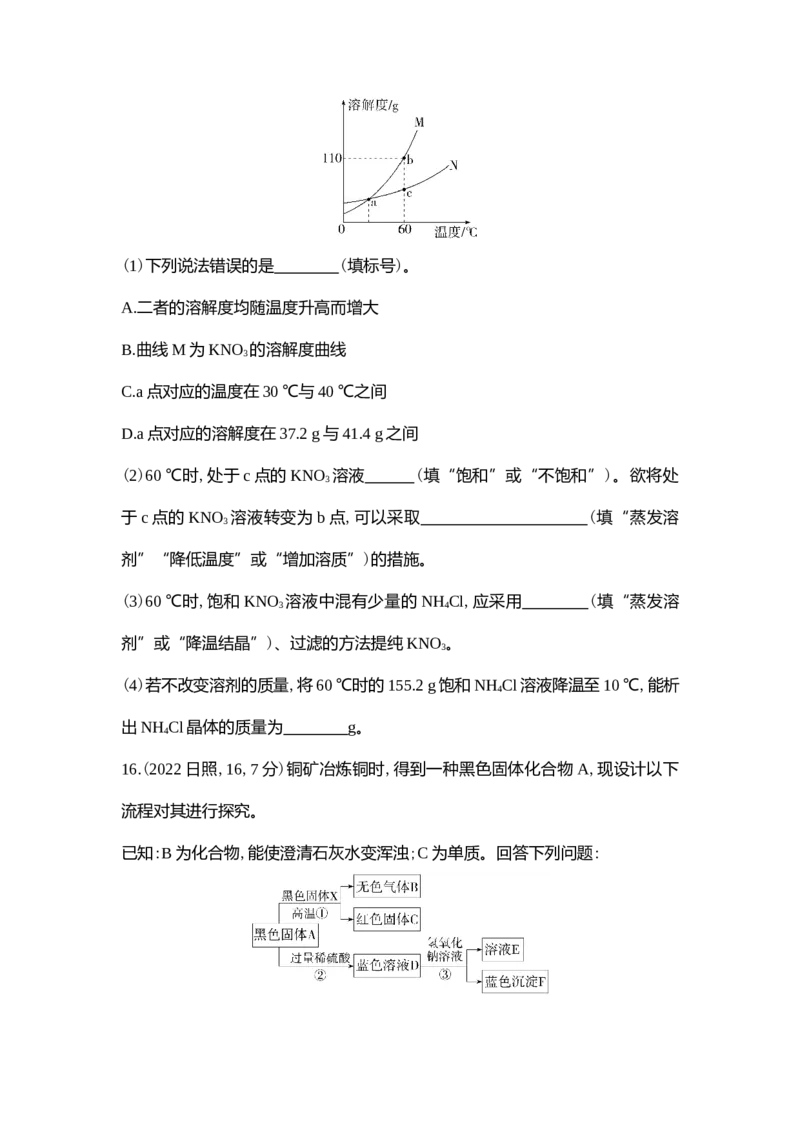
根据数据,绘制二者的溶解度曲线如图所示,a点为曲线的交点。回答下列问题:(1)下列说法错误的是 (填标号)。
A.二者的溶解度均随温度升高而增大
B.曲线M为KNO 的溶解度曲线
3
C.a点对应的温度在30 ℃与40 ℃之间
D.a点对应的溶解度在37.2 g与41.4 g之间
(2)60 ℃时,处于c点的KNO 溶液 (填“饱和”或“不饱和”)。欲将处
3
于c点的KNO 溶液转变为b点,可以采取 (填“蒸发溶
3
剂”“降低温度”或“增加溶质”)的措施。
(3)60 ℃时,饱和KNO 溶液中混有少量的NH Cl,应采用 (填“蒸发溶
3 4
剂”或“降温结晶”)、过滤的方法提纯KNO 。
3
(4)若不改变溶剂的质量,将60 ℃时的155.2 g饱和NH Cl溶液降温至10 ℃,能析
4
出NH Cl晶体的质量为 g。
4
16.(2022日照,16,7分)铜矿冶炼铜时,得到一种黑色固体化合物A,现设计以下
流程对其进行探究。
已知:B为化合物,能使澄清石灰水变浑浊;C为单质。回答下列问题:(1)反应①的化学方程式为 ,反应类型为 。
(2)用一种无色气体Y代替黑色固体X,也能在加热条件下与A反应生成B和C,
则Y的化学式为 。
(3)若③中逐滴加入NaOH溶液,则蓝色溶液D中首先与NaOH发生反应的物质
的化学式为 ;反应③中生成蓝色沉淀 F 的化学方程式为
。
三、实验题(本题共2小题,共16分)
17.(2022日照,17,8分)实验室欲用H O 溶液制备氧气,并进行铁丝在氧气里燃
2 2
烧的实验。
回答下列问题:
(1)若用溶质质量分数为30%的H O 溶液和MnO 制备氧气,反应速率太快。为
2 2 2
获得平稳的气流,下列发生装置最合适的是 (填标号);发生反应的化
学方程式为 。
A B
C D
(2)已知:用H O 制取氧气时,也可用铂丝代替MnO 作催化剂。下图甲装置可通
2 2 2
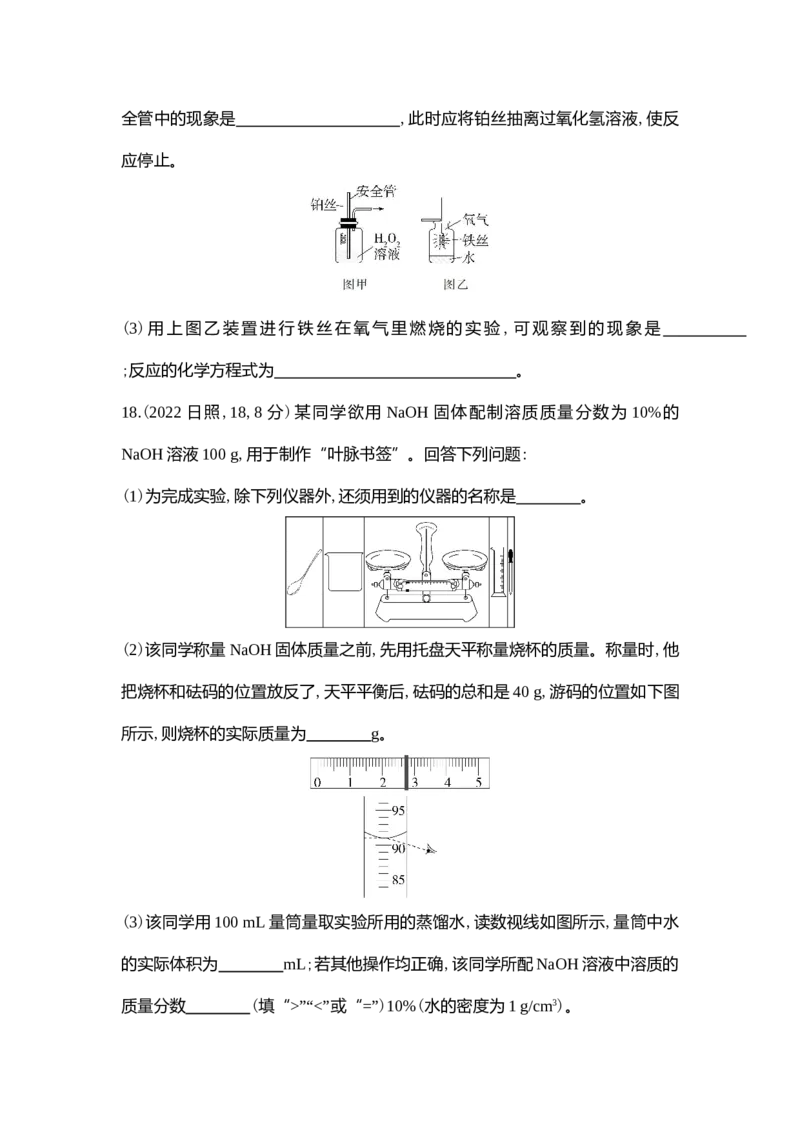
过铂丝的上下移动控制反应的发生与停止,若制备过程中体系内压强过大,则安全管中的现象是 ,此时应将铂丝抽离过氧化氢溶液,使反
应停止。
(3)用上图乙装置进行铁丝在氧气里燃烧的实验,可观察到的现象是
;反应的化学方程式为 。
18.(2022 日照,18,8 分)某同学欲用 NaOH 固体配制溶质质量分数为 10%的
NaOH溶液100 g,用于制作“叶脉书签”。回答下列问题:
(1)为完成实验,除下列仪器外,还须用到的仪器的名称是 。
(2)该同学称量NaOH固体质量之前,先用托盘天平称量烧杯的质量。称量时,他
把烧杯和砝码的位置放反了,天平平衡后,砝码的总和是40 g,游码的位置如下图
所示,则烧杯的实际质量为 g。
(3)该同学用100 mL量筒量取实验所用的蒸馏水,读数视线如图所示,量筒中水
的实际体积为 mL;若其他操作均正确,该同学所配NaOH溶液中溶质的
质量分数 (填“>”“<”或“=”)10%(水的密度为1 g/cm3)。(4)NaOH溶液长时间露置于空气中会变质生成Na CO ,发生反应的化学方程式
2 3
为 ;实验室里用于盛装NaOH溶液的试
剂瓶是 (填“带磨口玻璃塞的广口瓶”或“带橡胶塞的
细口瓶”)。
(5)氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要先用大量的水冲洗,再涂
上 溶液。
四、计算题(本题共1小题,共10分)
19.(2022日照,19,10分)已知某种钾肥是K CO 和KCl的混合物,为测定二者的
2 3
质量比,在烧杯里放入一定质量的该钾肥样品,加入适量水,完全溶解后,再向其
中加入CaCl 溶液至恰好完全反应,得到200 g溶质质量分数为14.9%的KCl溶
2
液,并生成10 g白色沉淀。
请计算:
(1)该钾肥样品中钾元素的质量。
(2)该钾肥样品中K CO 与KCl的质量比(用最简整数比表示)。
2 3
2022年山东日照初中学业水平考试
1.考点:化学与环境
D 使用脱硫煤主要减少二氧化硫的排放,故A不符合题意;加快煤的开采与使用,会增加二氧化
碳的排放量,故B不符合题意;可燃冰的主要成分为甲烷的水合物,燃烧会增加二氧化碳的排放
量,故C不符合题意;用氨水将二氧化碳转化为氮肥,能够有效减少二氧化碳的排放,故D符合题
意。
2.考点:实验基本操作
B 收集氢气应该用向下排空气法,故A错误;没有用玻璃棒引流,漏斗下端管口没有紧贴烧杯内
壁,故C错误;测定溶液的pH时,不能把pH试纸伸到溶液中,会污染溶液,故D错误。
3.考点:物质的检验和鉴别
C 硝酸铵溶于水吸热,溶液温度降低,氢氧化钠溶于水放热,溶液温度升高,故A正确。加入肥
皂水,硬水中泡沫少、浮渣多,软水中泡沫多、浮渣少,故B正确。氯化铵和硝酸铵都能与熟石
灰反应生成有刺激性气味的氨气,故C错误。灼烧时有烧焦羽毛的气味,不易结球的为羊毛线;
有特殊气味,易结球的为腈纶线,故D正确。
4.考点:化学与人体健康A 治疗贫血应该服用含有铁元素的药物,故A错误。
5.考点:常见气体的制备
A 题中装置适用于块状固体与液体在常温下制备气体的反应。①粉末状的硫酸铜溶于过氧化
氢溶液,无法控制反应停止。③⑤均为加热固体的反应,不满足题意。故选A。
6.考点:常见盐的性质 金属活动性
B 氧化钙和水反应生成氢氧化钙,氢氧化钙和硫酸铜反应生成氢氧化铜和硫酸钙,加入过量稀
盐酸和氢氧化铜反应生成氯化铜和水。铁和氯化铜反应生成红色的铜,证明铁的活动性比铜强,
故A、D正确;铁的活动性比钙弱,不能置换出钙,故B错误;过量的稀盐酸和铁反应生成氢气,故
C正确。
7.考点:燃烧与灭火
D 乒乓球碎片具有可燃性,属于可燃物,故A错误;乒乓球碎片的着火点比滤纸碎片的低,先燃
烧,故B错误;铜片导热属于物理变化,滤纸碎片燃烧属于化学变化,故C错误;题中实验说明燃
烧的条件之一是温度需要达到可燃物的着火点,故D正确。
8.考点:质量守恒定律,基本反应类型,物质的分类
C 题中反应的化学方程式为2CO+2NO 2CO+N,生成物中有单质,不属于复分解反应,
2 2
故A、D错误;该反应中有CO、NO、CO 三种氧化物,故B错误。
2
9.考点:中和反应,物质的检验与鉴别
D NaOH与HSO 反应后溶液中溶质情况有三种:NaSO;NaSO 、HSO;NaSO 、NaOH。滴
2 4 2 4 2 4 2 4 2 4
入酚酞溶液,溶液变红,证明氢氧化钠有剩余,故A错误;滴入氯化铜溶液,没有沉淀生成,证明无
OH-,但无法证明稀硫酸是否过量,故B错误;若稀硫酸过量也会与氯化钡反应生成白色沉淀,故
C错误;恰好完全反应时,Na+和S O2-全部来自Na
2
SO
4
,其个数比为2∶1,故D正确。
4
10.考点:自然界的水
A 电解水时,正极产生的是氧气,负极产生的是氢气,故M处产生的是氧气,N处产生的是氢气,
二者质量之比为8∶1,故A错误;电解水时加入少量硫酸钠或氢氧化钠,可增加自由移动离子的数
目,从而增强溶液的导电性,故B正确;M处产生的是氧气,能使带火星的木条复燃,故C正确;N
处产生的是氢气,靠近火焰,如果发出尖锐的爆鸣声,说明氢气不纯,故D正确。
11.考点:化学式及计算
C 1个白藜芦醇分子中含有12个H原子和3个O原子,故A错误;元素不能计个数,故B错误;
白藜芦醇中C、H、O元素的质量比为(12×14)∶(1×12)∶(16×3)=14∶1∶4,故C正确;白藜芦醇的相
48
对分子质量为12×14+1×12+16×3=228,其中氧元素的质量分数为 ×100%≈21%,故D错误。
228
12.考点:质量守恒定律
B 结 合 题 干 分 析 ,CO 2 、 H 2 O 的 分 子 个 数 比 为 CO 2 的质量 ∶
CO 的相对分子质量
2
H 2 O的质量 =11∶ 9 =1∶2,故C、H原子的个数比为1∶4。CH 4 中碳原子和氢原子
H O的相对分子质量 44 18
2
的个数比为1∶4,故A可能为题中气体;B所示混合气体中碳原子和氢原子的个数比为1∶8,故B不
可能为题中气体;C所示混合气体中碳原子和氢原子的个数比为1∶4,故C可能为题中气体;D所
示混合气体中碳原子和氢原子的个数比为2∶8=1∶4,故D可能为题中气体。
13.考点:元素与元素周期表 构成物质的微粒答案 (1)A (2)低 (3)3 D RbSO
2 4
解析 (1)元素周期表一格的左上角数字为原子序数,原子中,原子序数=质子数=核外电子数=核
电荷数=37,原子结构示意图中圆圈内数字为核电荷数,故m=37;2+8+18+n+1=37,n=8,A错误。
(3)质子数决定元素种类,四种粒子结构示意图中的质子数有3种,表示3种元素;最外层电子数
决定元素化学性质,铷的最外层电子数是1,D项所示原子的最外层电子数也是1,它们的化学性
质相似;铷在反应中容易失去1个电子,在化合物中显+1价,S O2-显-2价,故铷的硫酸盐的化学式
4
为RbSO。
2 4
14.考点:质量守恒定律 化合价
答案 (1)体积分数 CHOH+3O 3HO+2CO (2)NaClO (3)+4 (4)无污染 (5)O
2 5 2 2 2 2
解析 (4)过氧化氢溶液消毒时生成水和氧气,无污染。(5)过氧乙酸分子中H、O原子个数比为
4∶3,乙酸分子中H、O原子个数比为4∶2,根据化学反应前后原子个数和种类不变,该双原子分子
应为O。
2
15.考点:溶解度及溶解度曲线
答案 (1)C (2)不饱和 蒸发溶剂或增加溶质 (3)降温结晶 (4)21.9
解析 (1)从题中溶解度曲线可知,二者的溶解度都随温度升高而增大,故A正确。60 ℃时硝酸
钾的溶解度为110 g,则题图中曲线M代表KNO,曲线N代表NHCl,故B正确。a点对应的温度
3 4
范围在20 ℃~30 ℃,a点对应的溶解度在37.2 g至41.4 g之间,故C错误、D正确。(2)60 ℃时,c
点在硝酸钾溶解度曲线的下方,c点溶液为硝酸钾的不饱和溶液,b点溶液为饱和溶液;从c点变
为b点,可采用增加溶质或蒸发溶剂的措施。(4)60 ℃时,氯化铵的溶解度是55.2 g,155.2 g饱和
氯化铵溶液中含有溶质55.2 g、溶剂100 g;10 ℃时,氯化铵的溶解度是33.3 g,析出晶体的质量
为55.2 g-33.3 g=21.9 g。
16.题型:工艺流程题
答案 (1)C+2CuO 2Cu+CO↑ 置换反应
2
(2)CO (3)HSO CuSO+2NaOH Cu(OH)↓+NaSO
2 4 4 2 2 4
解析 (1)冶炼铜时得到的黑色固体A和稀硫酸反应得到蓝色溶液,和黑色固体X反应生成红色
固体C和无色气体B,化合物B能使澄清石灰水变浑浊,则B是二氧化碳,推测C是铜,则A是氧
化铜,X 是碳。反应①是氧化铜和碳反应生成铜和二氧化碳,化学方程式为 C+2CuO
2Cu+CO↑,属于置换反应。(2)一氧化碳也能和氧化铜反应生成铜和二氧化碳,CuO+CO
2
Cu+CO↑,故Y是CO。
2
17.题型:常见气体的制备
答案 (1)B 2HO 2HO+O↑ (2)液面上升 (3)剧烈燃烧,火星四射,生成黑色固体
2 2 2 2
3Fe+2O FeO
2 3 4
解析 (1)装置A、D中过氧化氢溶液和二氧化锰直接接触,无法控制反应速率,装置C无法控制
HO 溶液的滴加速率,无法控制反应速率,故选B。(2)题图甲装置内压强过大,会把过氧化氢溶
2 2
液压到安全管内,导致安全管内液面上升。
18.考点:配制溶液答案 (1)玻璃棒 (2)37.3 (3)91 <
(4)2NaOH+CO NaCO+HO 带橡胶塞的细口瓶 (5)硼酸
2 2 3 2
解析 (2)托盘天平称量质量的原理为左盘质量=右盘质量+游码示数。从题图中可知,游码的质
量是2.7 g,则烧杯的实际质量为40 g-2.7 g=37.3 g。(3)题图读数为90 mL,实际水的体积是91
mL,实际量取的水多了,配制的氢氧化钠溶液中溶质的质量分数小于10%。(4)因为氢氧化钠易
腐蚀表面粗糙的玻璃,故选用带橡胶塞的细口瓶。
19.题型:化学计算题
39
答案 (1)200 g×14.9%× =15.6 g。
74.5
(2)解:设碳酸钾的质量为x,反应生成的氯化钾的质量为y。
KCO +CaCl CaCO↓+2KCl
2 3 2 3
138 100 149
x 10 g y
138 x
= x=13.8 g
100 10 g
100 10 g
= y=14.9 g
149 y
原样品中氯化钾的质量为200 g×14.9%-14.9 g=14.9 g。
样品中碳酸钾和氯化钾的质量比为13.8 g∶14.9 g=138∶149。
答:该钾肥样品中KCO 与KCl的质量比为138∶149。
2 3
解析 (1)反应后得到的KCl溶液中KCl的来源包括:①原样品中的KCl,②样品中KCO 与氯
2 3
化钙反应生成的KCl。根据化学反应前后元素质量不变,得到的溶液中钾元素的质量与原钾肥样
品中K元素的质量相同。反应后溶液中KCl的质量为200 g×14.9%=29.8 g,K元素的质量为29.8
39
g× =15.6 g。
74.5