文档内容
第二讲 溶液和溶解度
知识讲解
(考什么,学什么,轻松提成绩!)
知识点一 溶液的形成
1.溶液
溶液是指一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
均一性:溶液中任意部分组成和性质完全相同。(如密度,糖水的任一部分同等甜)
稳定性:外界条件不变时,溶质不会从溶剂中分离出来。(如糖水不会无故析出蔗糖)
易错提醒
1.溶液一般是透明的,但透明不一定无色。如硫酸铜溶液是蓝色的。
练1 下列液体不属于溶液的是( )
A.氯化钠投入水中 B.冰投入水中
C.碘酒 D.二氧化碳通入水中
【答案】B
【解答】A、氯化钠投入水中形成的是均一、稳定的混合物,属于溶液,故A错;
B、冰投入水中是由水一种物质组成,属于纯净物,不属于溶液,故B正确;
C、碘酒是均一、稳定的混合物,属于溶液,故C错;
D、二氧化碳通入水中形成均一、稳定的混合物,属于溶液,故D错。故选:B。
练2 下列关于溶液的说法正确的是( )
A.混合物体一定是溶液
B.均一、稳定、透明的液体一定是溶液
C.溶液一定是混合物
D.一杯溶液中各部分的性质是不同的
【答案】C
【解答】A、溶液是均一的、稳定的混合物,但混合物不一定是溶液,故A错误;
B、溶液是均一的、稳定的混合物,均一、稳定、透明的液体不一定是溶液,如水,故B错误;C、溶液是均一的、稳定的混合物,故C正确;
D、溶液具有均一性,故溶液中各部分的性质是相同的,故D正确。故选:C。
2.溶液的组成
(1)溶液由溶质和溶剂组成。
习惯上把量多的看作溶剂;如NaCl溶液的溶剂是水,碘酒的溶剂是酒精。
(2)溶液质量=溶质质量 + 溶剂质量 溶液体积 ≠ 溶质体积 + 溶剂体积
(3)
归纳总结
1.溶液一定是混合物。因为它是至少由两种物质组成,如硫酸铜溶液由 CuSO 与水组成,海水由NaCl、
4
MgCl 等于水组成。
2
2.溶质可能有几种,但溶剂只有一种;溶液体积不等于溶质和溶剂的体积之和,因为分子间有间隙。
3.物质溶解时的热效应
(1)溶解放热:如NaOH固体溶解、浓HSO 溶解、CaO固体溶解;
2 4
(2)溶解吸热:如NH NO 溶解;
4 3
(3)溶解温度基本不变:如NaCl。
练1 下列物质加入水中,吸收热量的是( )
A.硝酸铵 B.氢氧化钠 C.浓硫酸 D.生石灰
【答案】A
【解答】A、NH NO 溶于水吸收热量。B、氢氧化钠溶于水放出热量;C、浓硫酸溶于水放出热量;
4 3
D、生石灰与水反应放出热量;故选:A。
4.乳化现象
溶液 悬浊液 乳浊液举例 盐水 浑浊的石灰水、泥沙河流 牛奶、原油
久置现象 不变 沉淀 分上下两层
(1)乳化是使用乳化剂将植物油分散成无数细小的液滴存在于水中而不能聚集。
(2)乳化作用在生活的应用:①洗涤:用洗涤剂可以将餐具上的油污洗干净。
练1 下列清洗方法中,利用乳化原理的是( )
A.用自来水洗手 B.用汽油清洗油污
C.用洗涤剂清洗餐具 D.用盐酸清除铁锈
【答案】C
【解答】A、用自来水洗手,使附着在手上的泥土等污物与水形成溶液或浊液而被冲洗掉,不属于乳化
作用,故选项错误。
B、用汽油洗去油污是利用汽油能溶解油污来达到目的,利用的是溶解原理,故选项不是利用乳化作用。
C、洗涤剂具有乳化作用,能将大的油滴分散成细小的油滴随水冲走,故选项是利用乳化作用。
D、用盐酸除去铁锈是因为铁锈的主要成分氧化铁能和盐酸反应,从而把铁锈除去,故选项不是利用乳
化作用。故选:C。
知识点二 饱和溶液
1.饱和溶液与不饱和溶液
饱和溶液:在一定温度下,在一定溶剂里,不能再溶解该溶质的溶液。
判断方法:继续加入该溶质,看能否溶解。
2.饱和溶液与不饱和溶液的转化
最保险的方法:加溶质、蒸发溶剂
3.浓、稀溶液与饱和、不饱和溶液的关系
(1)饱和溶液不一定是浓溶液。如饱和石灰水溶液就是稀溶液。
(2)不饱和溶液不一定是稀溶液。如不饱和的KNO 溶液,它的溶解度很大,可能是浓溶液。
3(3)看溶液浓稀,关注溶液中溶质的质量即可。
练1 20℃时,取甲、乙、丙、丁四种纯净物各20 g,分别加入到四只各盛有50g水的烧杯中,充分溶解
后的情况如表:
物质 甲 乙 丙 丁
未溶解固体的质量/g 4.2 2 0 9.2
下列说法正确的是( )
A.所得溶液一定都是饱和溶液
B.丁溶液中溶质质量分数一定最大
C.20℃时物质溶解度的关系为:丁>甲>乙>丙
D.所得溶液的质量关系为:丙>乙>甲>丁
【答案】D
【解答】A、丙中无固体剩余,故丙不一定是饱和溶液,故A错误;
B、丁溶液中未溶解的固体最多,溶质质量分数最小,故B错误;
C、20℃时物质溶解度的关系为:丙>乙>甲>丁,故C错误;
D、溶解的丙最多,故溶液质量最大,溶解的乙其次多,故乙的溶液质量小于丙,溶解的甲的质量第三
多,故甲溶液质量小于乙,溶解的丁最少,故丁溶液的质量最小,故D正确;
故选:D。
练2 欲使任何一种不饱和溶液转变为饱和溶液,下列措施肯定不可行的是( )
A.改变温度 B.蒸发溶剂 C.加入溶质 D.倒出溶液
【答案】D
【解答】不饱和溶液转变为饱和溶液的方法有:改变温度,蒸发溶剂,加溶质。
A 改变温度可以 B 蒸发溶剂可以 C 加入溶质可以 D 倒出溶液,溶剂溶质都没变,溶液性质不
变,不可以;综上,故答案为:D。
知识点三 溶解度
1.溶解度的定义
在一定温度下,某固态物质在100g溶剂中达到饱和状态时,所溶解的溶质质量。(1)含义:如“20℃时NaCl溶液的溶解度为36g”的含义:在20℃时,100g水最多能溶解36g NaCl。
(2)四要素:
①条件:在一定温度下。因为物质的溶解度会随温度的变化而变,故不指明温度,溶解度没有意义。
②标准:100g溶剂中。物质的溶解质量与溶剂量成正比,若要比较两种物质的溶解度大小,必须要等量溶
剂,注意是溶剂是100g,而非溶液是100g。
③状态:达到饱和时。溶质能在溶剂中持续溶解,只有达到饱和状态时,溶解度才是一个确定的值。
④单位:克。因为溶解度即溶质的质量,单位为g。
练1 判断下列说法是否正确
(1)把20g某物质溶解在100g水里恰好制成饱和溶液,这种物质的溶解度就是20g。( )
(2)20℃时 10g氯化钠可溶解在100g水里,故20℃时氯化钠的溶解度是10g。( )
【答案】×√
练2 “20 ℃时,氯化钠的溶解度是36g”。则 20 ℃时
①在100g水中,最多能溶解氯化钠的质量是 g,所得饱和溶液的质量 g。
②在50g水中,最多能溶解氯化钠的质量是 g,所得饱和溶液的质量 g。
③完全溶解72g氯化钠,至少需要 g水,所得饱和溶液的质量 g。
[来源:学科网ZXXK][来源:学#科#网]
【答案】36,136;18,68;200,272.
2.溶解性与溶解度
溶 解 度 /g <0.01 0.01~1 1~10 >10
(20℃)
溶解性分类 难溶 微溶 可溶 易溶
举例 CaCO 、BaSO Ca(OH) KClO NaCl、KNO
3 4 2 3 3
练1 (1)20℃时碳酸钙的溶解度是0.0013克,所以碳酸钙是 溶物质。
(2)20℃时食盐的溶解度是36克,所以食盐属于 溶物质。
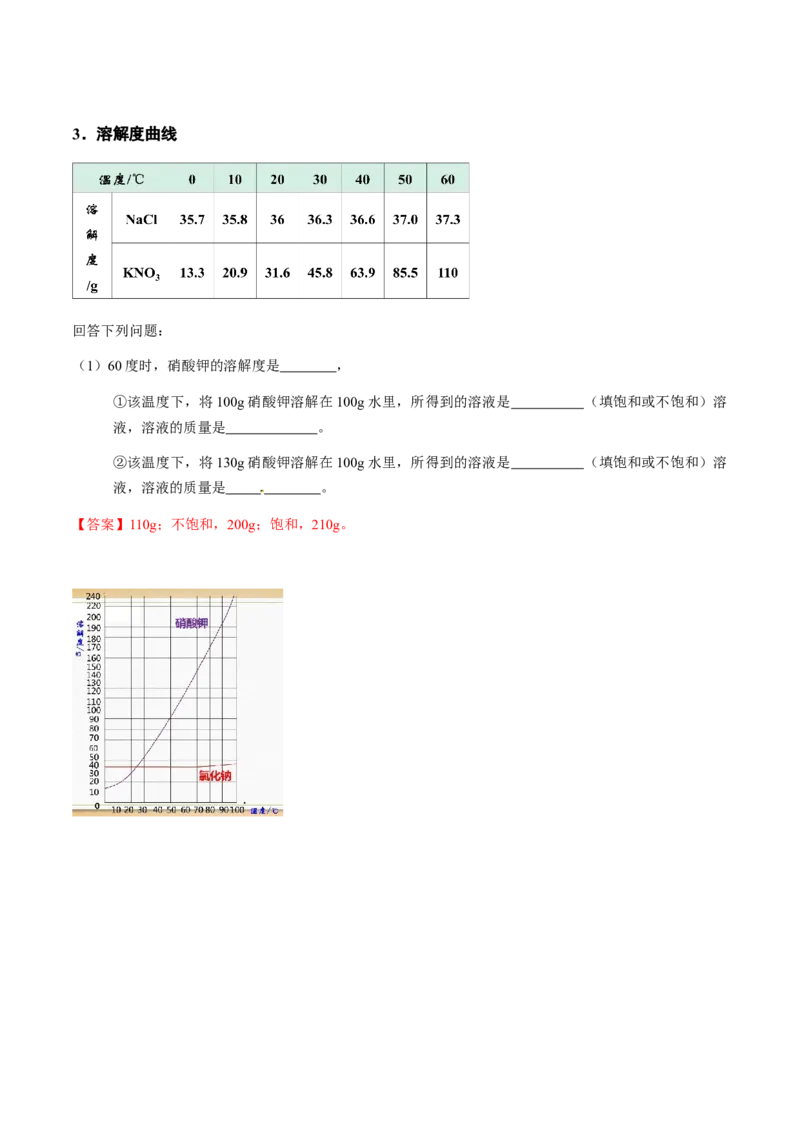
【答案】难溶;易溶。3.溶解度曲线
回答下列问题:
(1)60度时,硝酸钾的溶解度是 ,
①该温度下,将100g硝酸钾溶解在100g水里,所得到的溶液是 (填饱和或不饱和)溶
液,溶液的质量是 。
②该温度下,将130g硝酸钾溶解在100g水里,所得到的溶液是 (填饱和或不饱和)溶
液,溶液的质量是 。
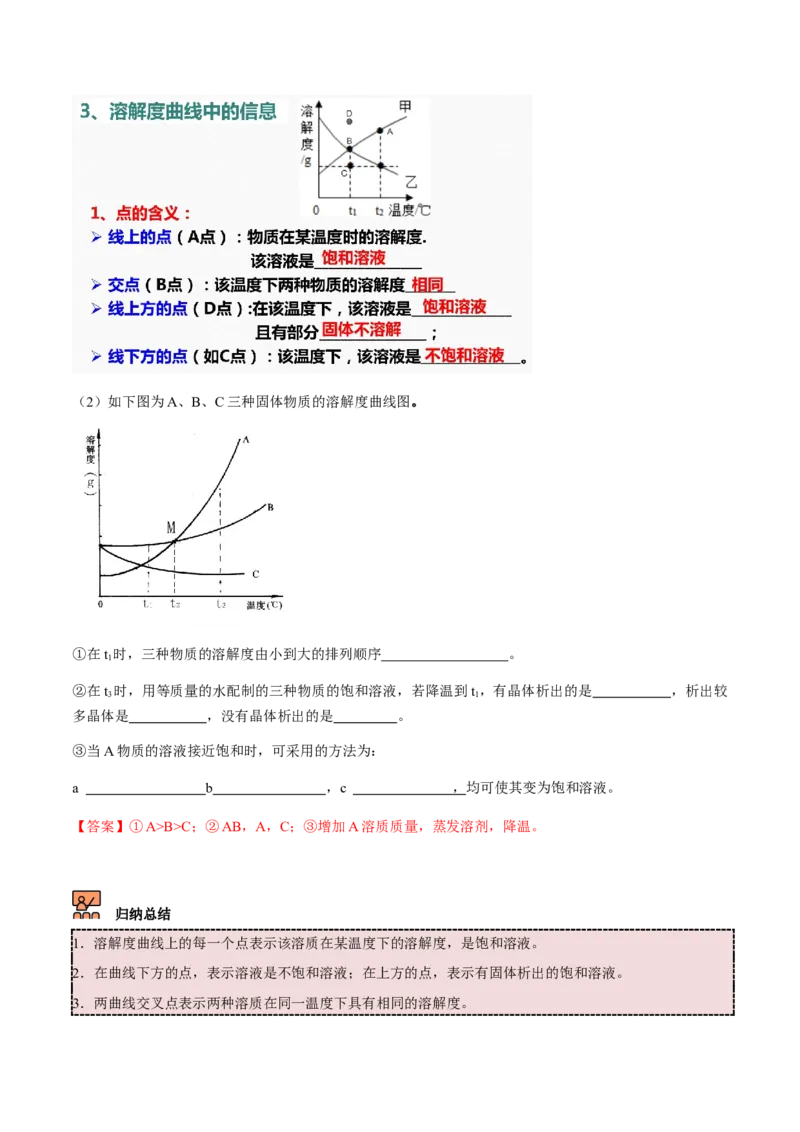
【答案】110g;不饱和,200g;饱和,210g。(2)如下图为A、B、C三种固体物质的溶解度曲线图。
①在t 时,三种物质的溶解度由小到大的排列顺序 。
1
②在t 时,用等质量的水配制的三种物质的饱和溶液,若降温到t ,有晶体析出的是 ,析出较
3 1
多晶体是 ,没有晶体析出的是 。
③当A物质的溶液接近饱和时,可采用的方法为:
a b ,c , 均可使其变为饱和溶液。
【答案】①A>B>C;②AB,A,C;③增加A溶质质量,蒸发溶剂,降温。
归纳总结
1.溶解度曲线上的每一个点表示该溶质在某温度下的溶解度,是饱和溶液。
2.在曲线下方的点,表示溶液是不饱和溶液;在上方的点,表示有固体析出的饱和溶液。
3.两曲线交叉点表示两种溶质在同一温度下具有相同的溶解度。4.任一溶液中, ;
饱和溶液中,数值上,溶质质量=溶解度,溶剂质量=100g水,
(2)曲线变化规律
①‘陡’:大多数固体物质的溶解度随温度升高而增大,如KNO、NH Cl;
3 4
②‘平’:少数固体物质的溶解度受温度的影响很小,如NaCl;
③‘降’:极少数固体的溶解度随温度的升高而减小,如Ca(OH) ;
2
所以民间有“冬天捞碱,夏天晒盐”的说法。
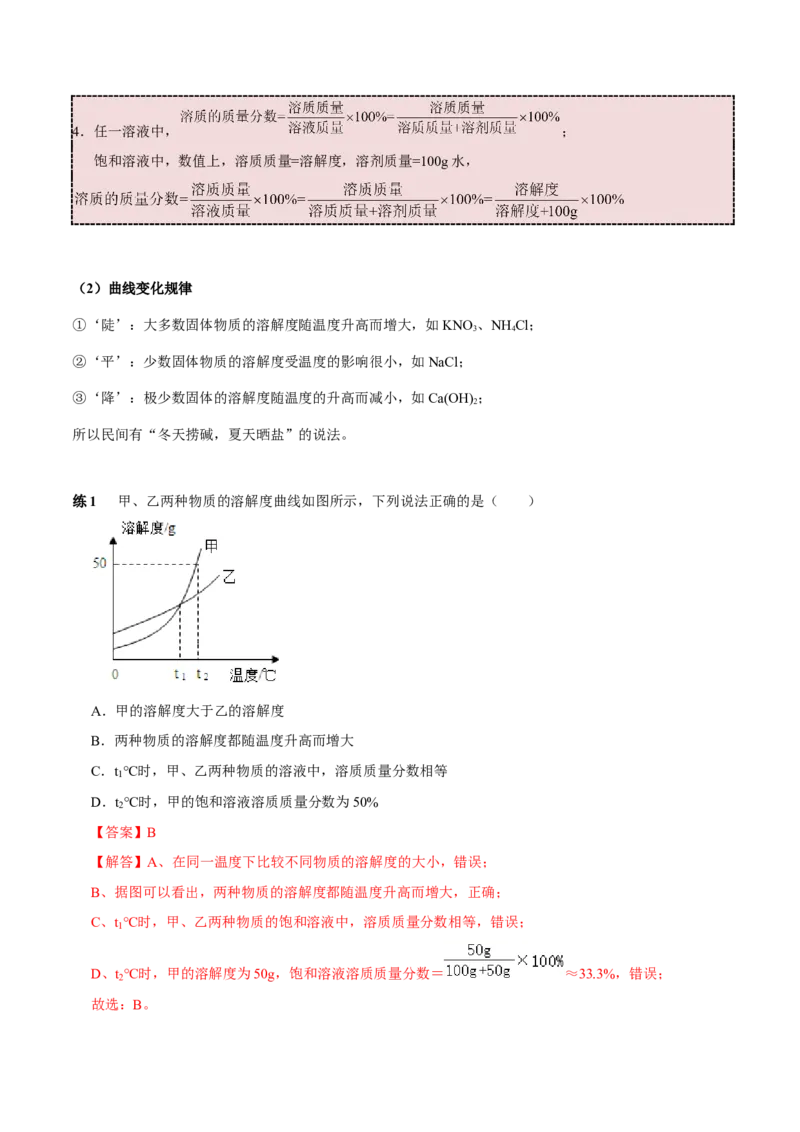
练1 甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.两种物质的溶解度都随温度升高而增大
C.t ℃时,甲、乙两种物质的溶液中,溶质质量分数相等
1
D.t ℃时,甲的饱和溶液溶质质量分数为50%
2
【答案】B
【解答】A、在同一温度下比较不同物质的溶解度的大小,错误;
B、据图可以看出,两种物质的溶解度都随温度升高而增大,正确;
C、t ℃时,甲、乙两种物质的饱和溶液中,溶质质量分数相等,错误;
1
D、t ℃时,甲的溶解度为50g,饱和溶液溶质质量分数= ≈33.3%,错误;
2
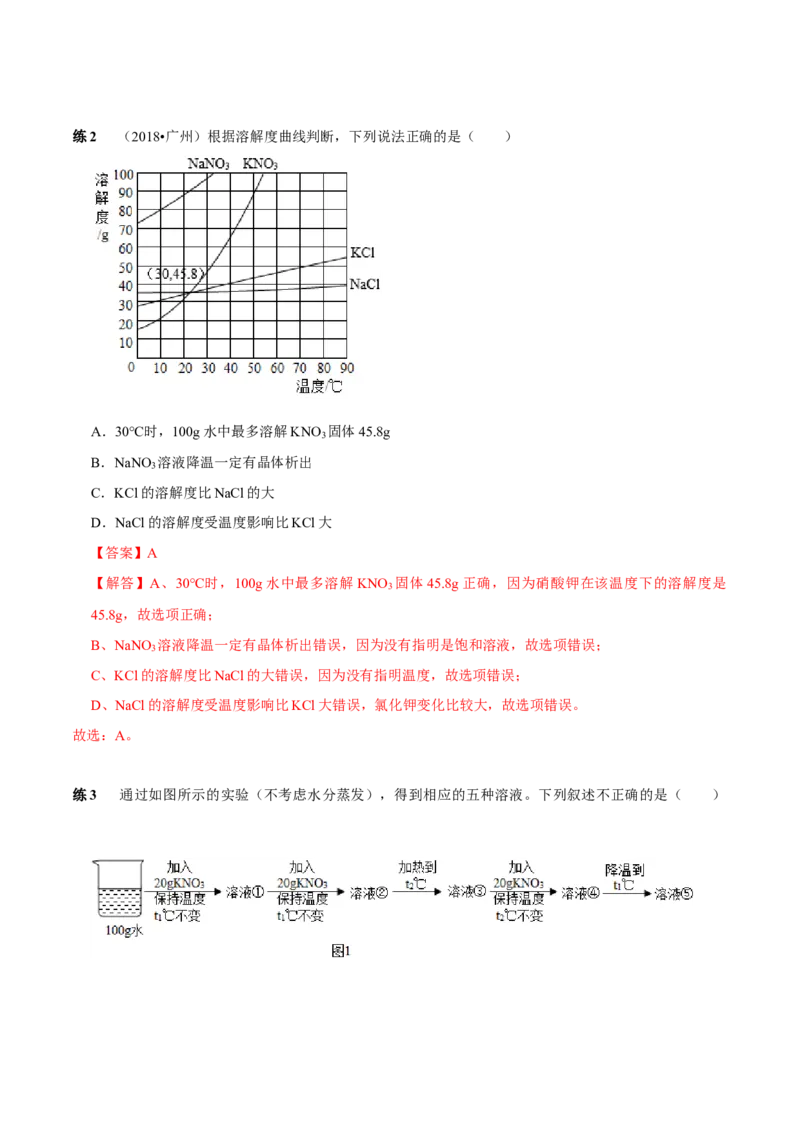
故选:B。练2 (2018•广州)根据溶解度曲线判断,下列说法正确的是( )
A.30℃时,100g水中最多溶解KNO 固体45.8g
3
B.NaNO 溶液降温一定有晶体析出
3
C.KCl的溶解度比NaCl的大
D.NaCl的溶解度受温度影响比KCl大
【答案】A
【解答】A、30℃时,100g水中最多溶解KNO 固体45.8g正确,因为硝酸钾在该温度下的溶解度是
3
45.8g,故选项正确;
B、NaNO 溶液降温一定有晶体析出错误,因为没有指明是饱和溶液,故选项错误;
3
C、KCl的溶解度比NaCl的大错误,因为没有指明温度,故选项错误;
D、NaCl的溶解度受温度影响比KCl大错误,氯化钾变化比较大,故选项错误。
故选:A。
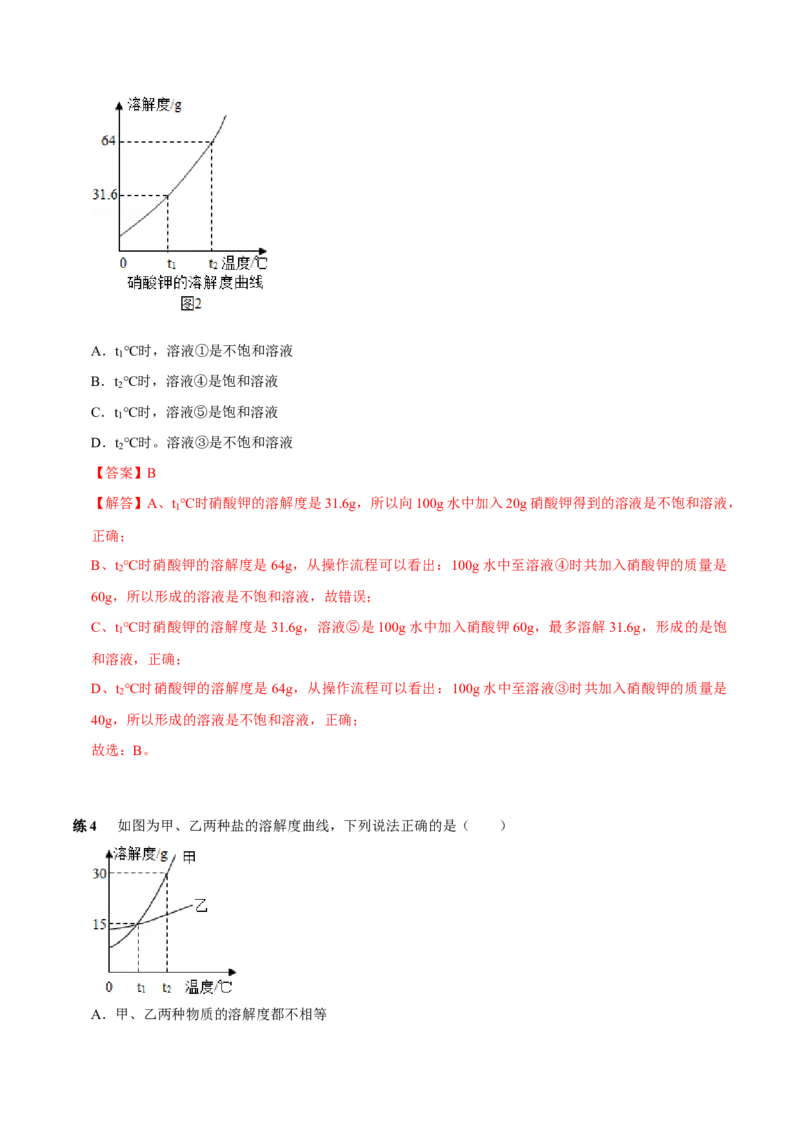
练3 通过如图所示的实验(不考虑水分蒸发),得到相应的五种溶液。下列叙述不正确的是( )A.t ℃时,溶液①是不饱和溶液
1
B.t ℃时,溶液④是饱和溶液
2
C.t ℃时,溶液⑤是饱和溶液
1
D.t ℃时。溶液③是不饱和溶液
2
【答案】B
【解答】A、t ℃时硝酸钾的溶解度是31.6g,所以向100g水中加入20g硝酸钾得到的溶液是不饱和溶液,
1
正确;
B、t ℃时硝酸钾的溶解度是64g,从操作流程可以看出:100g水中至溶液④时共加入硝酸钾的质量是
2
60g,所以形成的溶液是不饱和溶液,故错误;
C、t ℃时硝酸钾的溶解度是31.6g,溶液⑤是100g水中加入硝酸钾60g,最多溶解31.6g,形成的是饱
1
和溶液,正确;
D、t ℃时硝酸钾的溶解度是64g,从操作流程可以看出:100g水中至溶液③时共加入硝酸钾的质量是
2
40g,所以形成的溶液是不饱和溶液,正确;
故选:B。
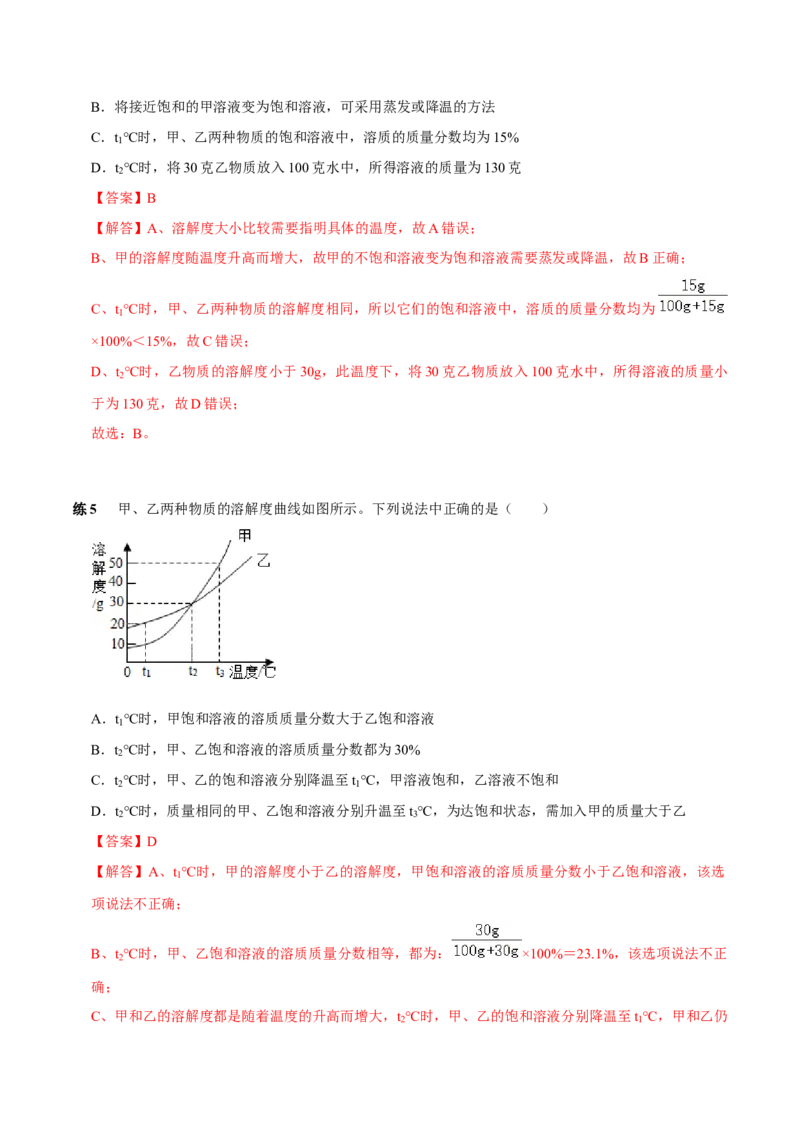
练4 如图为甲、乙两种盐的溶解度曲线,下列说法正确的是( )
A.甲、乙两种物质的溶解度都不相等B.将接近饱和的甲溶液变为饱和溶液,可采用蒸发或降温的方法
C.t ℃时,甲、乙两种物质的饱和溶液中,溶质的质量分数均为15%
1
D.t ℃时,将30克乙物质放入100克水中,所得溶液的质量为130克
2
【答案】B
【解答】A、溶解度大小比较需要指明具体的温度,故A错误;
B、甲的溶解度随温度升高而增大,故甲的不饱和溶液变为饱和溶液需要蒸发或降温,故B正确;
C、t ℃时,甲、乙两种物质的溶解度相同,所以它们的饱和溶液中,溶质的质量分数均为
1
×100%<15%,故C错误;
D、t ℃时,乙物质的溶解度小于30g,此温度下,将30克乙物质放入100克水中,所得溶液的质量小
2
于为130克,故D错误;
故选:B。
练5 甲、乙两种物质的溶解度曲线如图所示。下列说法中正确的是( )
A.t ℃时,甲饱和溶液的溶质质量分数大于乙饱和溶液
1
B.t ℃时,甲、乙饱和溶液的溶质质量分数都为30%
2
C.t ℃时,甲、乙的饱和溶液分别降温至t ℃,甲溶液饱和,乙溶液不饱和
2 1
D.t ℃时,质量相同的甲、乙饱和溶液分别升温至t ℃,为达饱和状态,需加入甲的质量大于乙
2 3
【答案】D
【解答】A、t ℃时,甲的溶解度小于乙的溶解度,甲饱和溶液的溶质质量分数小于乙饱和溶液,该选
1
项说法不正确;
B、t ℃时,甲、乙饱和溶液的溶质质量分数相等,都为: ×100%=23.1%,该选项说法不正
2
确;
C、甲和乙的溶解度都是随着温度的升高而增大,t ℃时,甲、乙的饱和溶液分别降温至t ℃,甲和乙仍
2 1然都是饱和溶液,该选项说法不正确;
D、因为t ℃时甲的溶解度大于乙的溶解度,因此 t ℃时,质量相同的甲、乙饱和溶液分别升温至
3 2
t ℃,为达饱和状态,需加入甲的质量大于乙,该选项说法正确。
3
故选:D。
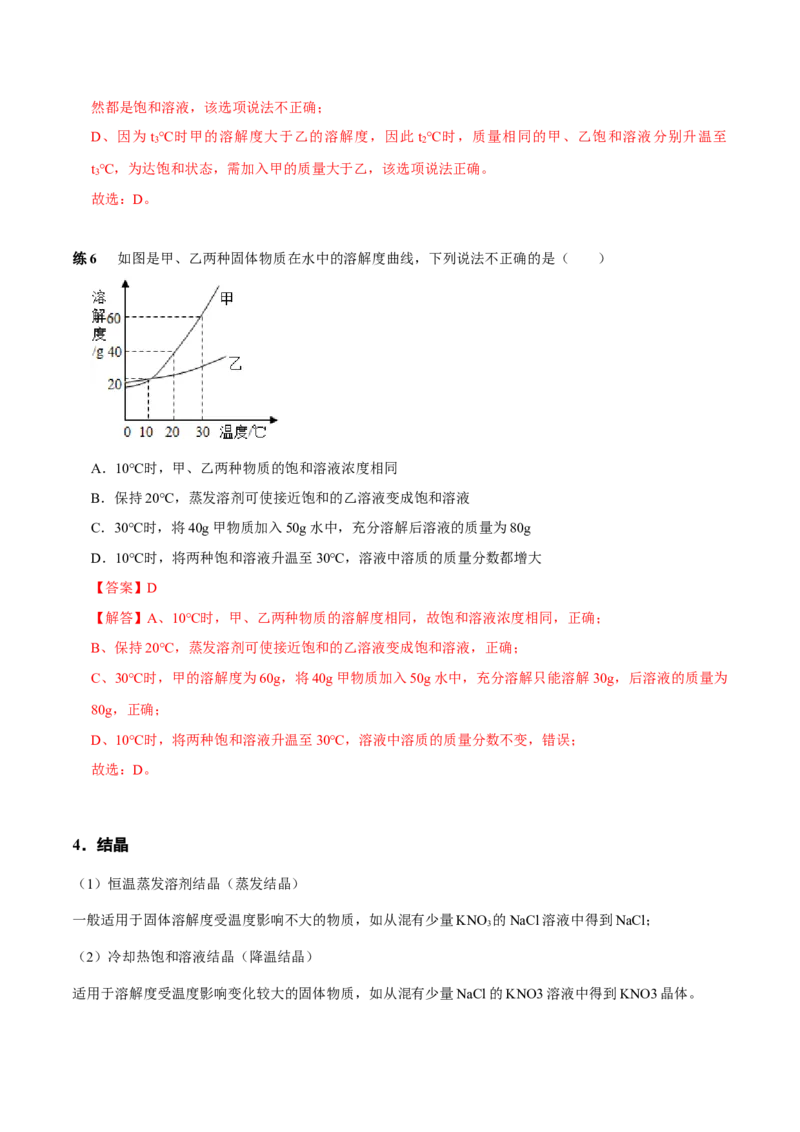
练6 如图是甲、乙两种固体物质在水中的溶解度曲线,下列说法不正确的是( )
A.10℃时,甲、乙两种物质的饱和溶液浓度相同
B.保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液
C.30℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为80g
D.10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数都增大
【答案】D
【解答】A、10℃时,甲、乙两种物质的溶解度相同,故饱和溶液浓度相同,正确;
B、保持20℃,蒸发溶剂可使接近饱和的乙溶液变成饱和溶液,正确;
C、30℃时,甲的溶解度为60g,将40g甲物质加入50g水中,充分溶解只能溶解30g,后溶液的质量为
80g,正确;
D、10℃时,将两种饱和溶液升温至30℃,溶液中溶质的质量分数不变,错误;
故选:D。
4.结晶
(1)恒温蒸发溶剂结晶(蒸发结晶)
一般适用于固体溶解度受温度影响不大的物质,如从混有少量KNO 的NaCl溶液中得到NaCl;
3
(2)冷却热饱和溶液结晶(降温结晶)
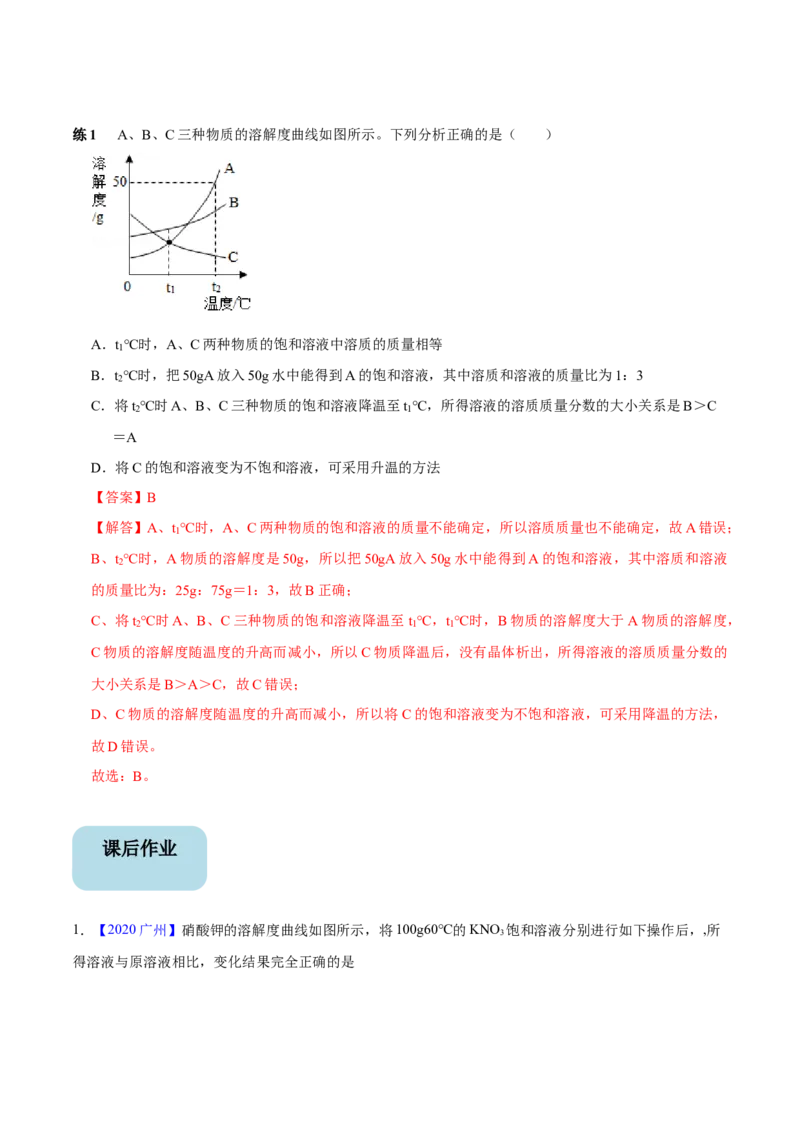
适用于溶解度受温度影响变化较大的固体物质,如从混有少量NaCl的KNO3溶液中得到KNO3晶体。练1 A、B、C三种物质的溶解度曲线如图所示。下列分析正确的是( )
A.t ℃时,A、C两种物质的饱和溶液中溶质的质量相等
1
B.t ℃时,把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3
2
C.将t ℃时A、B、C三种物质的饱和溶液降温至t ℃,所得溶液的溶质质量分数的大小关系是B>C
2 1
=A
D.将C的饱和溶液变为不饱和溶液,可采用升温的方法
【答案】B
【解答】A、t ℃时,A、C两种物质的饱和溶液的质量不能确定,所以溶质质量也不能确定,故A错误;
1
B、t ℃时,A物质的溶解度是50g,所以把50gA放入50g水中能得到A的饱和溶液,其中溶质和溶液
2
的质量比为:25g:75g=1:3,故B正确;
C、将t ℃时A、B、C三种物质的饱和溶液降温至t ℃,t ℃时,B物质的溶解度大于A物质的溶解度,
2 1 1
C物质的溶解度随温度的升高而减小,所以C物质降温后,没有晶体析出,所得溶液的溶质质量分数的
大小关系是B>A>C,故C错误;
D、C物质的溶解度随温度的升高而减小,所以将C的饱和溶液变为不饱和溶液,可采用降温的方法,
故D错误。
故选:B。
课后作业
1.【2020广州】硝酸钾的溶解度曲线如图所示,将100g60℃的KNO 饱和溶液分别进行如下操作后,,所
3
得溶液与原溶液相比,变化结果完全正确的是选项 操作 溶质质量 溶液质量 溶质的质量分数 KNO 的溶解度
3
A 升温 变大 变大 不变 变大
B 降温 变小 变小 不变 变小
C 加入KNO 固体 不变 变大 变大 变大
3
D 恒温蒸发部分水 变小 变小 不变 不变
【答案】D
【解析】
A、根据硝酸钾的溶解度曲线可知,升温后硝酸钾的溶解度变大,溶质质量、溶液质量、溶质的质量分数
都不变,故错误;
B、根据硝酸钾的溶解度曲线可知,降温后硝酸钾的溶解度变小,硝酸钾会结晶析出,溶质质量、溶液质
量、溶质的质量分数都变小,故错误;
C、加入KNO 固体后,不会继续溶解,溶质质量、溶液质量、溶质的质量分数、溶解度都不变,故错误;
3
D、恒温蒸发部分水,硝酸钾会结晶析出,溶质质量、溶液质量都变小,溶质的质量分数、解度都不变,
故正确。
故选D。
2.【2019广州】25℃时,探究某固体物质的溶解性,实验记录如下表。下列实验结论正确的是
编号 ① ② ③ ④
水的质量/g 50 50 50 50
加入固体质量/g 5 10 15 20
现象 固体完全溶解 固体完全溶解 剩余少量固体 剩余较多固体A.实验①所得溶液质量分数为10%
B.实验②说明25℃时该物质的溶解度是20g
C.实验③④所得溶液质量分数相同
D.实验④所得溶液中含溶质20g
【答案】C
【解析】A、实验①所得溶液质量分数为: ×100%=9.1%,该选项说法不正确;
B、固体完全溶解,形成的溶液可能是饱和溶液,也可能是不饱和溶液,如果是饱和溶液,则25℃时该
物质的溶解度是20g,如果是不饱和溶液,则25℃时该物质的溶解度大于20g,该选项说法不正确;
C、实验③④所得溶液都是饱和溶液,因此质量分数相同,该选项说法正确;
D、实验④所得溶液中溶质质量小于20g,该选项说法不正确。
故选:C。
3.【2017深圳】如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
A.甲的溶解度大于乙的溶解度
B.a ℃时,甲、乙的饱和溶液升温至a ℃时,均有固体析出
1 2
C.a ℃时,M点对应的甲溶液不饱和
2
D.a ℃时,乙饱和溶液的质量分数为20%
2
【答案】C
【解析】A、在比较物质的溶解度时,需要指明温度,故A错误;
B、乙物质的溶解度随温度的升高而减小,所以a ℃时,甲、乙的饱和溶液升温至a ℃时,乙物质有固
1 2
体析出,甲物质没有共同析出,故B错误;
C、a ℃时,M点在甲物质溶解度曲线的下方,所以M点对应的甲溶液不饱和,故C正确;
2
D、a ℃时,乙物质的溶解度是20g,所以乙饱和溶液的质量分数为: ×100%=16.7%,故D错误。
2
故选:C。
4.【2017广州】如图为KNO 的溶解度曲线,a、b在溶解度曲线上。
3(1)a点对应的溶液是 溶液。(填“饱和”或者“不饱和”)。
(2)a点对应的溶液的质量分数是 。(只列计算式)
(3)将a点对应的溶液升温到70℃,其质量分数 。(填写“变大”、“变小”或“不变”)
(4)欲使KNO 溶液的状态从b点转化为c点,可采取的措施是 。
3
【答案】(1)饱和;
(2) ;
(3)不变;
(4)加溶剂;
【解析】(1)a点对应的溶液是饱和溶液,因为a点在溶解度曲线上;故答案为:饱和;
(2)a点对应的溶液的质量分数= ;故答案为: ;
(3)将a点对应的溶液升温到70℃,其质量分数不变,因为硝酸钾固体物质的溶解度,是随温度升高
而增大的;故答案为:不变;
(4)欲使KNO 溶液的状态从b点转化为c点,可采取的措施是:加溶剂;故答案为:加溶剂;
3
5.【2016广州】某温度下,在100g质量分数为20%的KNO 不饱和溶液甲中加入10gKNO 固体,恰好得
3 3
到饱和溶液乙,下列说法正确的是( )
A.该温度下,KNO 的溶解度为30g
3
B.乙溶液的质量分数为30%
C.降低温度,可以使甲溶液变成饱和溶液
D.升高温度,甲、乙两溶液的质量分数都增大
【答案】C
【解答】某温度下,在100g质量分数为20%的KNO 不饱和溶液甲中加入10gKNO 固体,恰好得到饱
3 3
和溶液乙,即100g×20%+10g=30g硝酸钾,溶于水,形成100g+10g=110g溶液,即某温度下,30g硝
酸钾溶于110g﹣30g=80g水,形成110g饱和溶液。A、溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量某温度下,30g
硝酸钾溶于80g水,形成110g饱和溶液,则该温度下,KNO 的溶解度大于30g,故选项说法错误。
3
B、乙溶液的质量分数为 ×100%<30%,故选项说法错误。
C、硝酸钾的溶解度随着温度的降低而减小,降低温度,可以使甲溶液变成饱和溶液,故选项说法正确。
D、升高温度,硝酸钾的溶解度增大,但甲、乙溶液的组成没有发生改变,甲、乙两溶液的质量分数都
不变,故选项说法错误。
故选:C。
6.溶解度曲线如图所示。下列说法不正确的是( )
A.0℃时,NaCl的饱和溶液中溶质和溶剂的质量之为37:100
B.t℃时,NaCl和KNO 两种饱和溶液中溶质的质量分数相等
3
C.30℃时,将接近饱和的KNO 溶液变成饱和溶液,可采用降温或添加溶质的方法
3
D.将恒温下的饱和NaCl溶液敞口放置几天,有晶体析出,说明NaCl的溶解度降低
【答案】D
【解析】A、据图可以看出,在0℃时,氯化钠的溶解度是37g,所以NaCl的饱和溶液中溶质和溶剂的
质量之为37:100,正确;
B、由溶解度曲线可知,t℃时,NaCl和KNO 两条溶解度曲线交于一点,所以此温度时溶解度相同,
3
NaCl和KNO 两种饱和溶液中溶质的质量分数相等,正确;
3
C、由溶解度曲线可知,硝酸钾的溶解度随温度的圣盖而增大,30℃时,将接近饱和的KNO 溶液变成
3
饱和溶液,可采用降温或添加溶质的方法,正确;
D、将恒温下的饱和NaCl溶液敞口放置几天,有晶体析出,是由于溶解减少析出晶体,不能说明NaCl
的溶解度降低,错误。
故选:D。
7. MgSO 饱和溶液的溶质质量分数随温度变化的曲线如图所示。下列说法正确的是( )
4A.N点对应的MgSO 溶液升温或降温均都可能析出晶体
4
B.M点对应的MgSO 溶液是不饱和溶液
4
C.MgSO 饱和溶液的溶质质量分数随温度升高而增大
4
D.40℃时,MgSO 的溶解度为41g
4
【答案】A
【解析】A、通过分析溶解度曲线可知,N点对应的MgSO 溶液升温或降温均都可能析出晶体,故A正
4
确;
B、M点在溶解度曲线上,对应的MgSO 溶液是饱和溶液,故B错误;
4
C、通过分析溶解度曲线可知,0℃﹣70℃,溶解度逐渐增大,大于70℃,溶解度逐渐减小,故C错误;
D、40℃时,MgSO 的溶质质量分数为41%,所以溶解度应该是大于41g,大约是69.5g,故D错误。
4
故选:A。
8.硝酸钾和氯化钾的溶解度曲线如图所示:
(1)t ℃时,硝酸钾的溶解度为 。
1
(2)t ℃时,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的质量分数为 。
1
(3)t ℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯氯化钾的方法是 。
2
(4)将t ℃时硝酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t ℃过滤,得到溶液a
3 2
和溶液b。对于溶液a和溶液b,下列说法正确的是
A.都是饱和溶液
B.溶液质量a<b
C.溶质质量a=b
D.溶剂质量a<b
E.溶质的质量分数a=b【答案】(1)25g;
(2)20%;
(3)蒸发结晶;
(4)ABDE。
【解析】(1)通过分析溶解度曲线可知,t ℃时,硝酸钾的溶解度为25g;
1
(2)t ℃时,硝酸钾的溶解度为25g,将50g硝酸钾加入到50g水中,充分溶解后,所得溶液中溶质的
1
质量分数为 ×100%=20%;
(3)氯化钾的溶解度受温度变化影响较大,所以 t ℃时,氯化钾的饱和溶液中含有少量硝酸钾,提纯
2
氯化钾的方法是蒸发结晶;
(4)硝酸钾、氯化钾的溶解度随温度降低而减小,t ℃时,硝酸钾、氯化钾的溶解度相等,将t ℃时硝
2 3
酸钾和氯化钾的饱和溶液各100g分别蒸发10g水,然后降温至t ℃过滤,得到溶液a和溶液b。对于溶
2
液a和溶液b,所以
A、都是饱和溶液,故正确;
B、t ℃时,氯化钾的溶解度小于硝酸钾的溶解度,蒸发 10g水,氯化钾析出的晶体少,此时氯化钾饱
3
和溶液的质量大于硝酸钾饱和溶液的质量,虽然降低相同的温度,但氯化钾溶解度减小的幅度小于硝酸
钾,所以硝酸钾析出晶体质量较大,所以溶液质量a<b,故正确;
C、t ℃时,氯化钾的溶解度小于硝酸钾的溶解度,蒸发 10g水,氯化钾析出的晶体少,溶质质量不相
3
等,故错误;
D、t ℃时,氯化钾的溶解度小于硝酸钾的溶解度,硝酸钾和氯化钾的饱和溶液各 100g,b溶液中的溶
3
剂多,蒸发10g,水,还是b中的溶剂多,所以溶剂质量a<b,故正确;
E、a、b都是t ℃时的饱和溶液,所以溶质的质量分数a=b,故正确。
2
故选:ABDE。