文档内容
第七讲 常见的碱
模块一 碱的含义
知识点一 碱的含义
碱:在水溶液中,解离出的阴离子全部是OH-的化合物。通式:碱 = 金属离子 + OH-。
(1)命名:由金属离子和氢氧根构成的碱,称为‘氢氧化某’,如NaOH称为氢氧化钠。
资料卡片——初中阶段需掌握的几种碱
根据碱的溶解性,将碱分为:
(1)可溶性碱:氢氧化钠 、氢氧化钾 、氢氧化钡 ;
(2)微溶性碱:氢氧化钙 ;
(3)难溶性碱:氢氧化铜 (蓝色)、氢氧化镁 (白色)、
氢氧化亚铁 (灰绿色)氢氧化铁 (红褐色)。
有个特殊的碱:氨水(NH •HO),它可看作NH OH,NH OH = NH +(铵根) + OH- (氢氧根)。
3 2 4 4 4
【答案】(1)NaOH、KOH、Ba(OH) ;(2)Ca(OH) ;(3)Cu(OH) 、Mg(OH) 、Fe(OH) 、Fe(OH) 。
2 2 2 2 2 3
(2)碱在水溶液的解离
如氢氧化钠:NaOH在水溶液中以Na+和OH-形式存在,发生解离:NaOH=Na++ OH-
思考与交流
(1)Cu(OH) CO 属于碱吗?
2 2 3
【答案】不属于。因为解离出的阴离子有OH-、CO2-,不只是一个阴离子。
3经典例题
碱的含义
【例1】下列物质属于碱的是( )
A.HO B.NaHCO C.Ca(OH) D.HBO
2 3 2 3 3
【答案】C
【例2】下列物质不属于碱的是( )
A.NaOH B.NH ·H O C.C HOH D.Zn(OH)
3 2 2 5 2
【答案】C
模块二 常见的碱
知识点二 常见的碱
1.氢氧化钠和氢氧化钙
氢氧化钠(NaOH) 氢氧化钙[Ca(OH) ]
2
俗名 火碱、烧碱、苛性钠 熟石灰、消石灰
颜色状态 白色固体 白色粉末
53g(20℃) 0.16g(20℃)
溶解性
易溶于水;且溶解时放出大量热 微溶于水;随温度升高,溶解度降低
腐蚀性 强烈的腐蚀性 较强的腐蚀性
生活 除油污、作炉具清洁剂;作干燥剂 石灰浆涂在树木上,防止害虫生卵
用途 应用于造纸、纺织、印染等工业; 配制农药波尔多液;
生产
制取肥皂, 改良酸性土壤
资料卡片——NaOH的用途(1)为什么NaOH能用于造纸?
造纸的原料主要是木材,木材中除含纤维素外,还含有相当多的非纤维素(木质素,树胶等),加入氢
氧化钠稀溶液蒸煮原料,利用稀碱不能跟纤维素反应,而能腐蚀溶解非纤维素成分的特点,可分离出
纤维素,可制出质量高,成本低的纸。
(2)为什么NaOH能除油污?
油污中含有大量的油脂,而油脂难溶于水,所以水很难冲掉油污;加入稀NaOH溶液后,它会与油脂
反应生成能溶于水的新物质,这时就可以用水冲洗掉。
2.氢氧化钠的特性
(1)腐蚀性
氢氧化钠固体有较强的腐蚀性,溶于水还能放出大量的热,
若不慎沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。
(2)潮解
氢氧化钠固体暴露在空气中,易吸收空气中的水分,表面逐渐溶解,这种现象叫潮解。
故可作某些气体的干燥剂,如氢气、氧气、一氧化碳等。
3.氢氧化钙的特性
(1)氢氧化钙的制备:CaO+HO= Ca(OH) (石灰乳或石灰浆);
2 2
(2)用澄清石灰水检验二氧化碳: 。
【答案】Ca(OH) +CO =CaCO↓+H O
2 2 3 2
归纳总结——物质放置在空气中的变化规律
CaO 浓盐酸 浓硫酸 NaOH Ca(OH)
2
特性 吸水性 挥发性 吸水性 吸水潮解 与CO 反应
2
变化 挥发HCl 吸收空气中 吸收空气中
CaO+HO=Ca(OH) Ca(OH) +CO =CaCO↓+H O
2 2 2 2 3 2
原因 气体, 水蒸气 水蒸气
溶液
增大 减小 增大 增大 增大
质量经典例题
氢氧化钠与氢氧化钙
【例1】氢氧化钙俗称( )
A.烧碱 B.纯碱 C.熟石灰 D.石灰石
【答案】C
【例2】如图所示,装置气密性良好,若想使∪形管中a端液面下降,b端液面上升,不能达到目的的选项
是( )
选项 A B C D
X 水 水 稀盐酸 水
Y 氢氧化钠固体 生石灰 镁 硝酸铵
【答案】D
各物质敞口放置变化
【例1】下列物质存放在烧杯中一段时间后,质量变大且变质的是( )
①浓盐酸 ②浓硫酸 ③烧碱 ④生石灰 ⑤澄清石灰水
A.③④⑤ B.②③④⑤ C.①②③④⑤ D.④⑤[来源
【答案】A
【解析】①浓盐酸会挥发出氯化氢气体使自身质量减小,错误;②浓硫酸会吸收空气中的水蒸气自身变稀
但不会发生化学变化,错误;③烧碱会潮解并与二氧化碳反应,自身质量变大,发生化学变化,正确;
④生石灰会吸收空气中的水蒸气生成氢氧化钙自身质量变大,正确;⑤石灰水吸收空气中的二氧化碳
生成碳酸钙,质量增大,正确。所以③④⑤符合题意,正确选项是A。
模块二 碱的化学性质
知识精讲
知识点三 碱的化学性质1.与酸碱指示剂作用
回顾用指示剂检验物质的酸碱性:
溶液类型 紫色石蕊溶液 无色酚酞溶液
碱性 NaOH溶液 蓝 红
Ca(OH) 溶液 蓝 红
2
根据上面实验,填写指示剂变化的颜色:
紫色石蕊溶液 无色酚酞溶液
碱
【答案】蓝色;红色。
思考与交流
(1)碱与指示剂作用是物理变化还是化学变化?
(2)所有的碱都能使无色酚酞变红吗?Cu(OH) 、Fe(OH) 等难溶性碱能使其变色吗?
2 3
【答案】(1)化学变化;(2)不是,难溶性碱的OH-浓度很小,不能使指示剂变色。
2.与某些非金属氧化物反应
回顾用澄清石灰水检验CO:
2
Ca(OH) +CO =CaCO↓+H O,
2 2 3 2
碱 + 非金属氧化物 = 盐 + 水
模仿其反应形式,书写化学方程式
化学方程式
石灰水+CO Ca(OH) +CO =CaCO↓+H O
2 2 2 3 2
NaOH溶液+CO 2NaOH+CO =Na CO+H O
2 2 2 3 2
NaOH溶液+SO 2NaOH+SO =Na CO+H O
2 2 2 3 2
NaOH溶液+SO 2NaOH+SO =Na SO +H O
3 3 2 4 2归纳总结——气体干燥剂
浓硫酸 固体NaOH 生石灰CaO
干燥 吸水性 吸水性 与水反应
原理 (物理性质) (物理性质) (化学性质)
不能干燥
NH CO、SO 、HCl
气体 3 2 2
装置
经典例题
碱的化学性质
【例1】下列关于氢氧化钠的描述中不正确的是( )
A.曝露在空气中易潮解 B.能吸收空气中的二氧化碳
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
【答案】C
【例2】1839年虎门销烟采用的方法是:在海边挖池,放入烟土,引入海水浸泡,投入石灰,石灰遇水沸
腾,烟土溶解。该过程发生的反应有CaO+H O=Ca(OH) 。下列说法不正确的是
2 2
A. 该反应属于化合反应
B. 该反应会放出热量
C. 由此反应推测氧化钙可干燥氯化氢气体
D. 此反应可制备氢氧化钙
【答案】C
【例3】(1)氢氧化钠必须密封保存原因是它既易潮解,又易与空气中二氧化碳反应而变质,反应化学方
程式为
;
氢氧化钠也能吸收尾气中的二氧化硫,反应化学方程式为 ;
(2)氢氧化钙在空气中易与二氧化碳反应生成坚固的碳酸钙,故在建筑上常用来砌砖抹墙,该反应的化
学方程式为 。
【答案】(1)2NaOH+SO ===Na SO +H O;2NaOH+CO===Na CO+H O。
2 2 3 2 2 2 3 2
(2)Ca(OH) +CO ===CaCO ↓+H O。
2 2 3 2
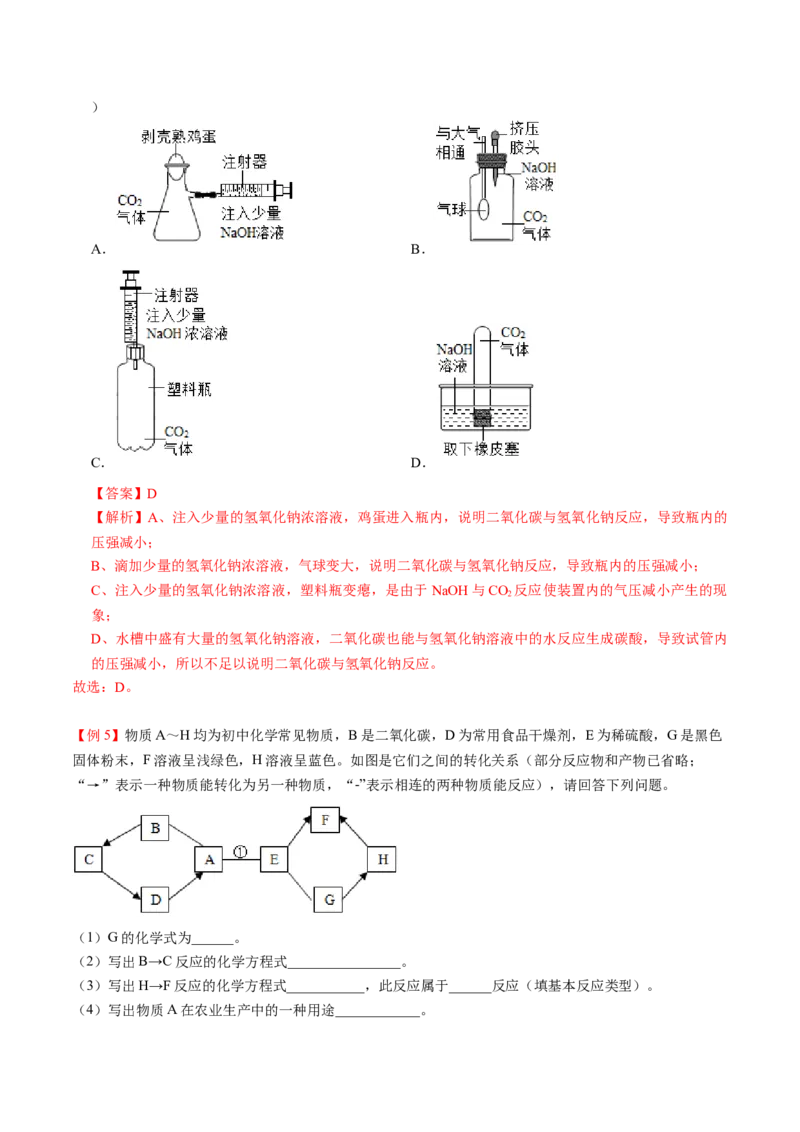
【例4】有下列四种实验设计及操作,实验过程中其现象不足以说明 CO 与NaOH溶液发生了反应的是(
2)
A. B.
C. D.
【答案】D
【解析】A、注入少量的氢氧化钠浓溶液,鸡蛋进入瓶内,说明二氧化碳与氢氧化钠反应,导致瓶内的
压强减小;
B、滴加少量的氢氧化钠浓溶液,气球变大,说明二氧化碳与氢氧化钠反应,导致瓶内的压强减小;
C、注入少量的氢氧化钠浓溶液,塑料瓶变瘪,是由于NaOH与CO 反应使装置内的气压减小产生的现
2
象;
D、水槽中盛有大量的氢氧化钠溶液,二氧化碳也能与氢氧化钠溶液中的水反应生成碳酸,导致试管内
的压强减小,所以不足以说明二氧化碳与氢氧化钠反应。
故选:D。
【例5】物质A~H均为初中化学常见物质,B是二氧化碳,D为常用食品干燥剂,E为稀硫酸,G是黑色
固体粉末,F溶液呈浅绿色,H溶液呈蓝色。如图是它们之间的转化关系(部分反应物和产物已省略;
“→”表示一种物质能转化为另一种物质,“-”表示相连的两种物质能反应),请回答下列问题。
(1)G的化学式为______。
(2)写出B→C反应的化学方程式________________。
(3)写出H→F反应的化学方程式___________,此反应属于______反应(填基本反应类型)。
(4)写出物质A在农业生产中的一种用途____________。【答案】CuO Ca(OH) +CO ===CaCO ↓+H O Fe+CuSO =FeSO+Cu 置换 改良酸性土壤
2 2 3 2 4 4
【分析】
D为常用食品干燥剂,则D是CaO,D→A,E为稀硫酸,A可与稀硫酸反应,结合氧化钙的性质,A应该
是Ca(OH) 。稀硫酸→F,F溶液呈浅绿色,则F是FeSO ,H溶液呈蓝色,H溶液中含有铜离子,G是黑
2 4
色固体粉末,G→H,则G是CuO,H是CuSO 。CO→C→CaO,则C是CaCO 。代入验证,推断正确。
4 2 3
气体干燥剂
【例1】如图所示装置有多种用途,其中不正确的是( )
选 广口瓶内盛放的药品 用途
项
A 浓硫酸 干燥氧气
B 水 收集氧气
C 氢氧化钠溶液 除去H 中混有的CO 气体
2 2
D 石灰水 检验CO 气体
2
【答案】B
【解析】B、用排水法收集氧气,瓶内盛满水,气体应该从短管进,利用气体的压力将水从长管压出,故
B错误;
模块三 NaOH 的变质问题
1.NaOH的变质
放置一些NaOH固体在空气中,发生以下变化:
白色片状固体 → 表面溶解 → 逐渐风干,生成白色粉末
思考与交流(1)NaOH固体的表面溶解,是为什么?
(2)最终的白色粉末是什么?用化学方程式表示该过程。
(3)NaOH固体最终的质量增加了还是减少了?
【答案】(1)NaOH的潮解;(2)NaCO,2NaOH+CO =Na CO+H O;(3)增加。
2 3 2 2 3 2
2.CaO的变质
放置一些CaO固体在空气中,发生以下变化:
CO2
CaO Ca(OH)
②
CaCO
2 3
如果CaO发生变质,即有CaCO 的存在,那如何证明碳酸钙的呢?
3
思考与交流
(1)实验室用CaCO 制备CO 时,采用的是什么酸?有什么现象?反应方程式是?
3 2
(2)若NaOH发生变质,会产生NaCO,那也可以用稀盐酸来检验碳酸钠的存在,反应也会产生大
2 3
量气泡。模仿碳酸钙与稀盐酸的反应,书写NaCO 和稀HCl的反应方程式。
2 3
【答案】(1)稀盐酸,产生大量气泡,CaCO +2HCl=CaCl +H O+CO↑;
3 2 2 2
(2)NaCO+2HCl=2NaCl+H O+CO↑。
2 3 2 2
经典例题
NaOH的变质问题
【例1】下列溶液在空气中敞口放置后,溶质质量因发生化学反应而减小的是( )
A.石灰水 B.浓硫酸 C.浓盐酸 D.烧碱溶液
【答案】A
【例2】实验室中的试剂一般要密封保存,否则可能会与空气接触而变质。某研究性学习小组发现一瓶未
密闭的KOH固体,对其成分提出以下假设,并完成了实验探究。
假设1:只含KOH; 假设2:含KOH和KCO; 假设3:只含KCO
2 3 2 3
(1)成分中可能含有KCO 的原因是(用化学方程式回答)________________________。
2 3(2)取少量样品于试管中,加入足量稀盐酸,观察到_____________________,说明假设2或假设3成立。
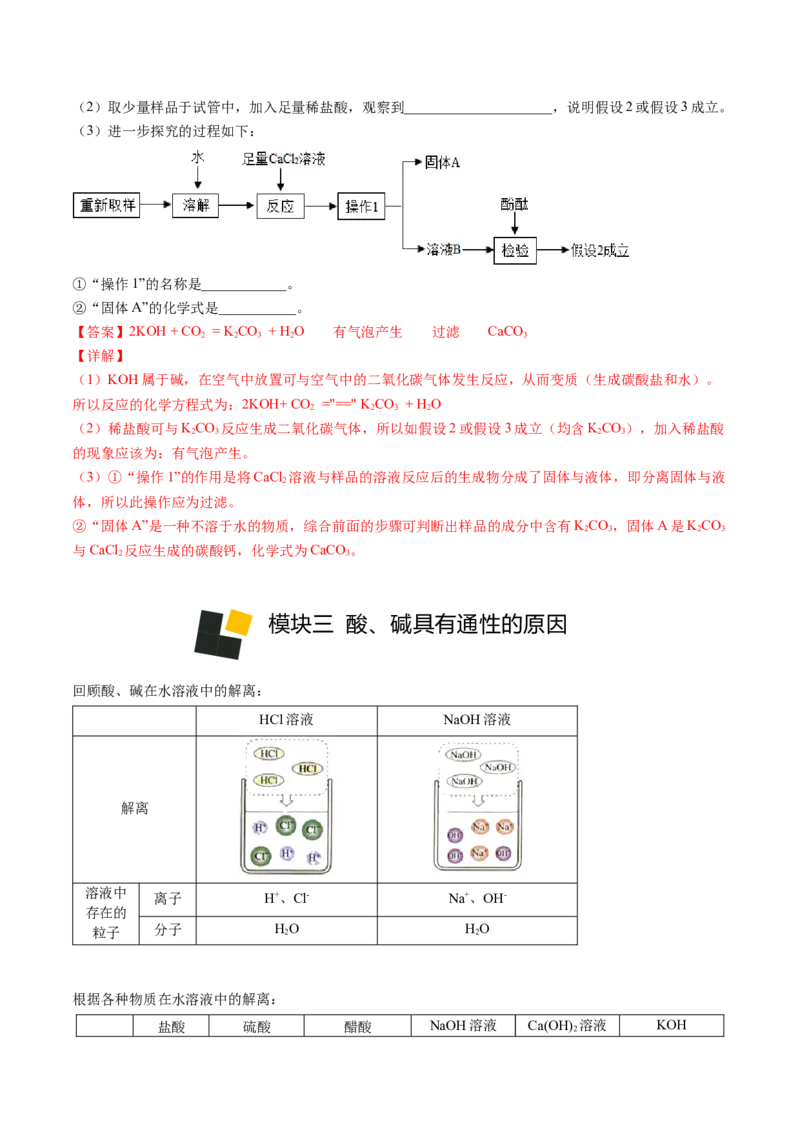
(3)进一步探究的过程如下:
①“操作1”的名称是____________。
②“固体A”的化学式是___________。
【答案】2KOH + CO = K CO + H O 有气泡产生 过滤 CaCO
2 2 3 2 3
【详解】
(1)KOH属于碱,在空气中放置可与空气中的二氧化碳气体发生反应,从而变质(生成碳酸盐和水)。
所以反应的化学方程式为:2KOH+ CO ="==" K CO + H O
2 2 3 2
(2)稀盐酸可与KCO 反应生成二氧化碳气体,所以如假设2或假设3成立(均含KCO),加入稀盐酸
2 3 2 3
的现象应该为:有气泡产生。
(3)①“操作1”的作用是将CaCl 溶液与样品的溶液反应后的生成物分成了固体与液体,即分离固体与液
2
体,所以此操作应为过滤。
②“固体A”是一种不溶于水的物质,综合前面的步骤可判断出样品的成分中含有KCO,固体A是KCO
2 3 2 3
与CaCl 反应生成的碳酸钙,化学式为CaCO 。
2 3
模块三 酸、碱具有通性的原因
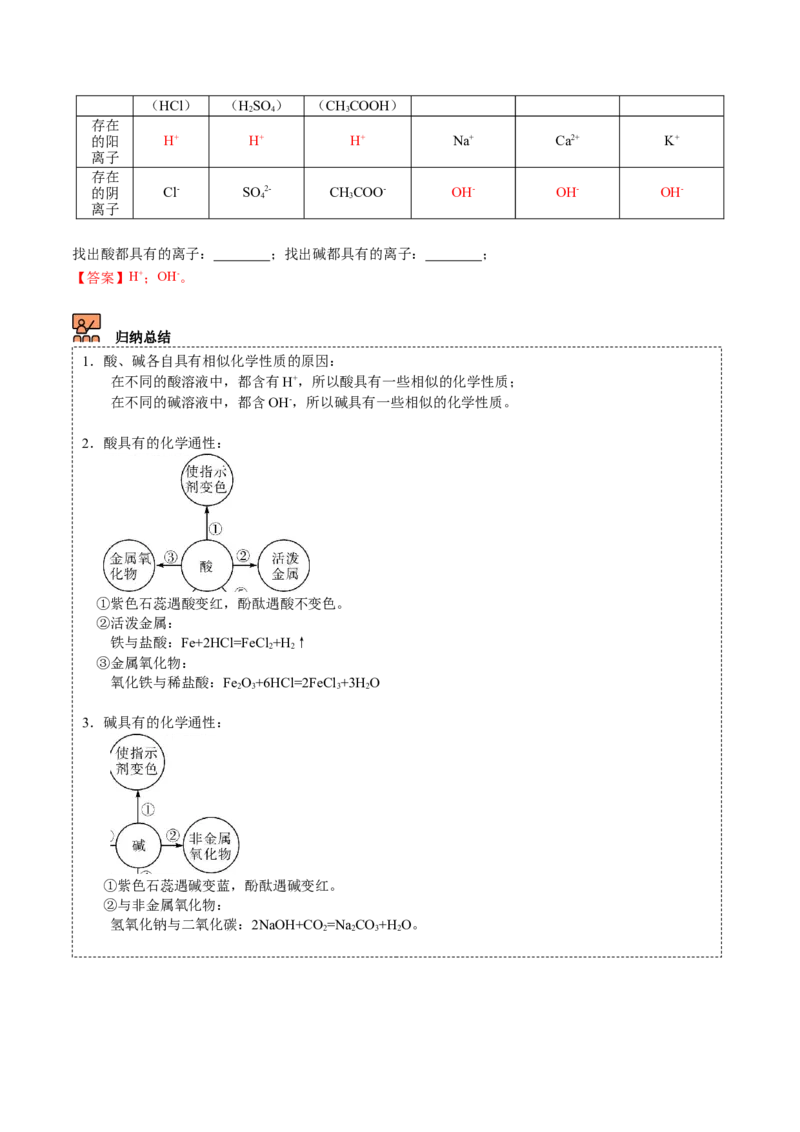
回顾酸、碱在水溶液中的解离:
HCl溶液 NaOH溶液
解离
溶液中
离子 H+、Cl- Na+、OH-
存在的
粒子 分子 H 2 O H 2 O
根据各种物质在水溶液中的解离:
盐酸 硫酸 醋酸 NaOH溶液 Ca(OH) 溶液 KOH
2(HCl) (HSO ) (CHCOOH)
2 4 3
存在
的阳 H+ H+ H+ Na+ Ca2+ K+
离子
存在
的阴 Cl- SO 2- CHCOO- OH- OH- OH-
4 3
离子
找出酸都具有的离子: ;找出碱都具有的离子: ;
【答案】H+;OH-。
归纳总结
1.酸、碱各自具有相似化学性质的原因:
在不同的酸溶液中,都含有H+,所以酸具有一些相似的化学性质;
在不同的碱溶液中,都含OH-,所以碱具有一些相似的化学性质。
2.酸具有的化学通性:
①紫色石蕊遇酸变红,酚酞遇酸不变色。
②活泼金属:
铁与盐酸:Fe+2HCl=FeCl +H ↑
2 2
③金属氧化物:
氧化铁与稀盐酸:FeO+6HCl=2FeCl +3H O
2 3 3 2
3.碱具有的化学通性:
①紫色石蕊遇碱变蓝,酚酞遇碱变红。
②与非金属氧化物:
氢氧化钠与二氧化碳:2NaOH+CO=Na CO+H O。
2 2 3 2经典例题
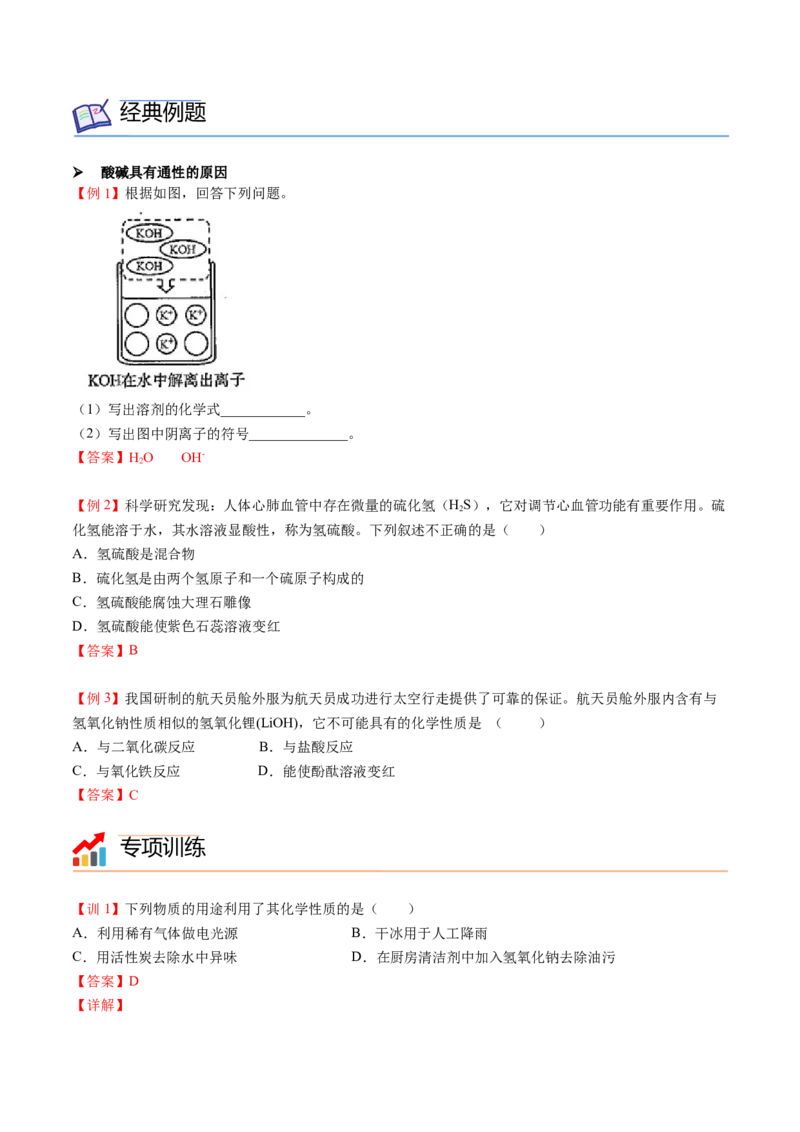
酸碱具有通性的原因
【例1】根据如图,回答下列问题。
(1)写出溶剂的化学式____________。
(2)写出图中阴离子的符号______________。
【答案】HO OH-
2
【例2】科学研究发现:人体心肺血管中存在微量的硫化氢(HS),它对调节心血管功能有重要作用。硫
2
化氢能溶于水,其水溶液显酸性,称为氢硫酸。下列叙述不正确的是( )
A.氢硫酸是混合物
B.硫化氢是由两个氢原子和一个硫原子构成的
C.氢硫酸能腐蚀大理石雕像
D.氢硫酸能使紫色石蕊溶液变红
【答案】B
【例3】我国研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证。航天员舱外服内含有与
氢氧化钠性质相似的氢氧化锂(LiOH),它不可能具有的化学性质是 ( )
A.与二氧化碳反应 B.与盐酸反应
C.与氧化铁反应 D.能使酚酞溶液变红
【答案】C
专项训练
【训1】下列物质的用途利用了其化学性质的是( )
A.利用稀有气体做电光源 B.干冰用于人工降雨
C.用活性炭去除水中异味 D.在厨房清洁剂中加入氢氧化钠去除油污
【答案】D
【详解】A、稀有气体做电光源,是因为稀有气体通电时能发出不同颜色的光,不需要通过化学变化便能表现出来,
利用的是其物理性质,不符合题意;
B、干冰用于人工降雨,是因为干冰升华吸热,不需要通过化学变化便能表现出来,利用的是其物理性质,
不符合题意;
C、用活性炭去除水中异味,是因为活性炭具有吸附性,不需要通过化学变化便能表现出来,利用的是其
物理性质,不符合题意;
D、氢氧化钠去除油污,是因为氢氧化钠能与油污反应,需要通过化学变化才能表现出来,利用的是其化
学性质,符合题意。
故选D。
【训2】某些食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”。
下列物质属于“双吸剂”的是( )
A.炭粉 B.铁粉
C.氯化钙 D.生石灰
【答案】B
【解析】
在通常情况下铁能和空气中的氧气和水反应生成铁锈,从而除去氧气和水蒸气.可以用作双吸剂.观察选
项,故选B.
【训3】如图所示,滴管中吸入某种液体,平底烧瓶中盛有另一种物质,挤压滴管滴入液体,一段时间后
气球明显鼓起。下列选项符合题意的是
【答案】C
【训4】下列关于酸和碱的说法中错误的是( )
A.酸的溶液中都存在氢离子
B.碱中一定含有氢元素和氧元素
C.酸一定能使无色酚酞溶液变红
D.碱中不一定含有金属元素
【答案】C
【训5】下列转化中,加酸不能一步实现的是( )A.Zn→ZnSO B.CaCO →CO
4 3 2
C.MgO→MgCl D.Cu→CuCl
2 2
【答案】D
【训6】氢氧化钴[Co(OH) ]受热易分解,能与酸性溶液反应,可作涂料的干燥剂,制备方法是①Co+
2
2HCl==CoCl +H↑,②CoCl +2NaOH==Co(OH) ↓+2NaCl。下列说法中正确的是( )
2 2 2 2
A.氢氧化钴的化学性质稳定
B.氢氧化钴可以干燥CO 气体
2
C.可以用适量NaOH溶液除去NaCl中混有的少量CoCl
2
D.Co(OH) 中Co元素的化合价为+4
2
【答案】C
【训7】某兴趣小组进行了化学探究活动。
实验一:相同条件下,将10.00g下列物质分别置于相同规格的烧杯中,敞口放置在空气中,烧杯中物质质
量随时间变化如下表。
时间 水 饱和石灰水 稀盐酸 浓硫酸 氢氧化钠溶液
n小时 8.14g 8.32g 8.62g 11.16g 9.36g
2n小时 5.74g 5.93g 6.67g 12.53g 8.45g
实验二:
下列说法不正确的是( )
A. 浓硫酸敞口久置后浓度会变小
B. 实验二的溶液①中溶质只有NaCO
2 3
C. 稀盐酸敞口久置后浓度可能会变大
D. 饱和石灰水的质量变化小于水的质量变化,原因之一是饱和石灰水吸收了空气中的CO
2
【答案】B
【训8】(1)氢氧化钠溶液因与空气中的______________(填物质化学式)发生反应易变质,所以必须密
封保存。
(2)Ba(OH) 是一种易溶于水的碱,向Ba(OH) 溶液中加入少量液态三氧化硫,反应的化学方程式是
2 2
_______________。
【答案】(1)二氧化碳(或CO);(2)Ba(OH) + SO = BaSO↓+ HO.
2 2 3 4 2
【训9】某化学学习小组的同学对一瓶敞口放置氢氧化钙固体的化学成分产生了兴趣,他们根据自己所学
知识进行如下探究:
【提出问题】该瓶药品的化学成分是什么?
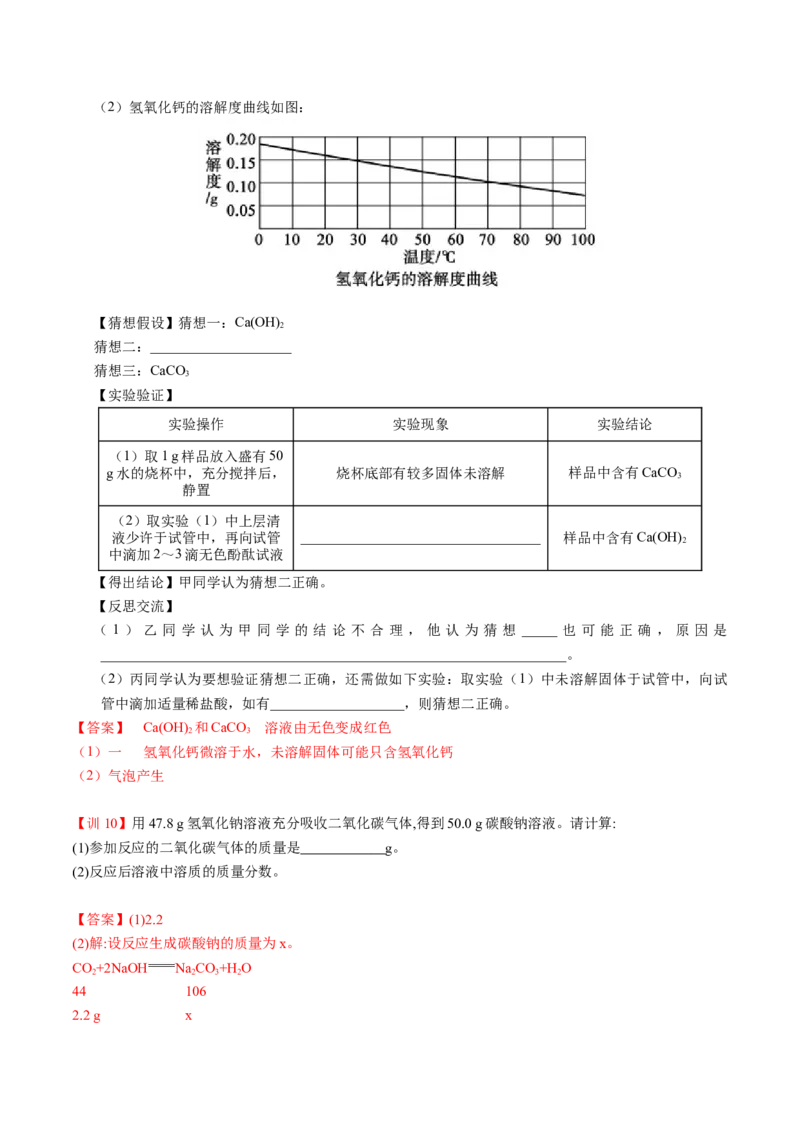
【查阅资料】(1)氢氧化钙能与空气中的二氧化碳反应而变质。(2)氢氧化钙的溶解度曲线如图:
【猜想假设】猜想一:Ca(OH)
2
猜想二:____________________
猜想三:CaCO
3
【实验验证】
实验操作 实验现象 实验结论
(1)取1 g样品放入盛有50
g水的烧杯中,充分搅拌后, 烧杯底部有较多固体未溶解 样品中含有CaCO
3
静置
(2)取实验(1)中上层清
液少许于试管中,再向试管 __________________________________ 样品中含有Ca(OH)
2
中滴加2~3滴无色酚酞试液
【得出结论】甲同学认为猜想二正确。
【反思交流】
( 1 ) 乙 同 学 认 为 甲 同 学 的 结 论 不 合 理 , 他 认 为 猜 想 _____ 也 可 能 正 确 , 原 因 是
__________________________________________________________________。
(2)丙同学认为要想验证猜想二正确,还需做如下实验:取实验(1)中未溶解固体于试管中,向试
管中滴加适量稀盐酸,如有___________________,则猜想二正确。
【答案】 Ca(OH) 和CaCO 溶液由无色变成红色
2 3
(1)一 氢氧化钙微溶于水,未溶解固体可能只含氢氧化钙
(2)气泡产生
【训10】用47.8 g氢氧化钠溶液充分吸收二氧化碳气体,得到50.0 g碳酸钠溶液。请计算:
(1)参加反应的二氧化碳气体的质量是 g。
(2)反应后溶液中溶质的质量分数。
【答案】(1)2.2
(2)解:设反应生成碳酸钠的质量为x。
CO+2NaOH NaCO+H O
2 2 3 2
44 106
2.2 g x44 2.2 g
= x=5.3 g
106 x
反应后溶液中溶质的质量分数为
5.3 g
×100%=10.6%。
50.0 g
答:反应后溶液中溶质的质量分数是10.6%。
提分作业
1.下列选项中物质的名称、俗名、化学式、类别完全一致的是( )
A.氧化钙 消石灰 CaO 氧化物 B.氢氧化钠 烧碱 NaOH 碱
C.乙醇 酒精 C HOH 氧化物 D.氢氧化钙 石灰石 Ca(OH) 碱
2 5 2
【答案】B
【详解】
A、氧化钙俗称生石灰,化学式为:CaO,氧化钙是由两种元素组成,其中一种元素为氧元素的化合物,
属于氧化物,不符合题意;
B、氢氧化钠俗称烧碱,化学式为:NaOH,属于碱,符合题意;
C、乙醇俗称酒精,化学式为:C HOH,乙醇含三种元素,不属于氧化物,不符合题意;
2 5
D、氢氧化钙俗称熟石灰或消石灰,化学式为:Ca(OH) ,属于碱,不符合题意;
2
故选B。
2.下列过程涉及化学变化的是( )
A.氢氧化钠的潮解 B.浓硫酸腐蚀纸张
C.刻画比较金属和合金的硬度 D.蔗糖的溶解
【答案】B
3.下列药品需要密封保存的原因,解释错误的是( )
A.浓盐酸—— 防止挥发 B.氢氧化钠溶液 ——防止与二氧化碳反应
C.浓硫酸 ——防止吸水 D.生石灰 —— 防止与氧气反应
【答案】D
【详解】
A、浓盐酸具有挥发性,要密封保存,防止挥发,故A正确;
B、氢氧化钠溶液和二氧化碳反应生成碳酸钠和水,要密封保存,防止与二氧化碳反应,故B正确;
C、浓硫酸具有吸水性,要密封保存,防止吸水,故C正确;
D、生石灰能和水反应生成氢氧化钙,不和氧气反应,故D不正确。故选D。
4.氢氧化钠固体长时间露置在空气中,表面已经潮湿,经充分干燥后,该固体的质量( )
A.增大 B.减少 C.不变 D.无法确定【答案】A
【详解】
氢氧化钠固体露置在空气中易吸水潮解,易和二氧化碳反应生成碳酸钠,经充分干燥后,剩余的固体中含
有了碳酸钠,使固体质量增加。故选A。
5.现有如下物质:浓硫酸、烧碱、氯化钠、稀盐酸、熟石灰、干冰等物质。请用它们的化学式填写:
(1)能用来改良酸性土壤的是_____________;(2)能用来人工降雨的是__________;
(3)可干燥二氧化碳气体的是_____________;(4)在空气中易潮解的是__________;
(5)能除去铁制品表面铁锈的是___________;(6)可用于调味和腌渍食品的是________.
【答案】 Ca(OH) CO H SO NaOH HCl NaCl
2 2 2 4
【解析】(1)熟石灰是氢氧化钙的俗称,具有碱性,属于碱,可用于改良酸性土壤,其化学式为:
Ca(OH) ;(2)干冰(固体的二氧化碳)升华时吸收大量的热,可用于人工降雨,其化学式为:CO;(3)浓
2 2
硫酸具有吸水性,且不与二氧化碳反应,可干燥二氧化碳气体,其化学式为:HSO ;(4)烧碱是氢氧化钠
2 4
的俗称,在空气中易潮解,其化学式为:NaOH;(5)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和
水,则盐酸能除去铁制品表面铁锈,其化学式为:HCl;(6)氯化钠可用于调味和腌渍食品,其化学式为:
NaCl。
6.小明利用如图装置探究了CO 与NaOH能否发生反应的实验后,对塑料瓶内溶液溶质成分产生了兴趣。
2
(提出问题)塑料瓶内的溶液溶质的成分是什么?
(查阅资料)向NaOH溶液不断通入CO,此时发生的反应为CO+2NaOH=Na CO+H O;当NaOH全部转
2 2 2 3 2
化为NaCO 后,再通入CO,发生的反应为CO+Na CO+H O=2NaHCO 。
2 3 2 2 2 3 2 3
(作出猜想)猜想1:NaOH、NaCO
2 3
猜想2:_________
猜想3:NaCO、NaHCO
2 3 3
猜想4:NaHCO
3
(实验探究)小明设计了如下实验来验证。请你帮助完成实验,填写以下表格:
实验步骤 实验现象 实验结论
步骤Ⅰ:取少量塑料瓶中的
溶液于试管中,加入 有白色沉淀产生 猜想_____错误
_________。
步骤Ⅱ:取少量步骤1所得
上层清液于试管中,加入适 _________ 猜想3正确
量稀盐酸。【答案】NaCO 足量BaCl 溶液 4 有气泡产生
2 3 2
【详解】
[作出猜想]向NaOH溶液不断通入CO,此时发生的反应为CO+2NaOH=Na CO+H O;当NaOH全部转化
2 2 2 3 2
为NaCO 后,再通入CO,发生的反应为CO+Na CO+H O=2NaHCO 。结合其他猜想,可知猜想2为只
2 3 2 2 2 3 2 3
有碳酸钠;
[实验探究] 步骤Ⅰ:由于碳酸钠能与氯化钡反应生成沉淀,而碳酸氢钠、氢氧化钠和氯化钡均不反应,取
少量塑料瓶中的溶液于试管中,加入足量BaCl 溶液(验证并除尽碳酸钠)。有白色沉淀产生,证明有碳
2
酸钠,猜想 4错误;
步骤Ⅱ:取少量步骤1所得上层清液于试管中,加入适量稀盐酸。有气泡产生,说明有碳酸氢钠,猜想3
正确;
[拓展延伸]本探究实验说明反应物的用量不同,产物也不同。如碳与氧气的反应,氧气不足时生成CO,氧
气充足时生成CO。
2