文档内容
成都七中 2028 届高一阶段测试卷
考试时间:75 分钟 总分:100 分
可能用到的相对原子质量:H:1;C:12;O:16;Na:23;Cl:35.5;K:39;Ag:108
一、选择题:本题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.化学源自生活和生产实践,并随着社会的进步而不断发展,下列说法不正确的是( )
A.我国是世界上发明陶瓷、冶金、火药、塑料最早的国家
B.李时珍著作的《本草纲目》中,蕴含着丰富的化学知识
C.化学与其它学科交叉渗透,成为自然科学领域中一门中心基础科学
D.材料的研制和开发以研究和优化物质的组成、结构和性能为基础
2.17世纪中叶后的200多年里,化学逐渐形成了独立的学科体系,下列说法错误的是( )
A.法国化学家拉瓦锡提出了燃烧学说,使近代化学取得革命性进展
B.英国科学家道尔顿提出了原子学说,为近代化学的发展奠定了基础
C.英国化学家波义尔提出了分子学说,标志着近代化学的诞生
D.俄国化学家门捷列夫发现了元素周期律,使化学研究变得有规律可循
3.近日,大连化学专家通过多种原位表征手段揭示了氧化锌在二氧化碳与氢气制甲醇反应体系下的结构
敏感性,有效提高了甲醇选择性和收率。该反应的微观示意图如下。下列说法正确的是( )
A.该反应体系中共有2种化合物
B.该反应属于置换反应
C.此反应的方程式可以表示为H +CO =CH OH+H O
2 2 3 2
D.该反应体现了无机物在一定条件下可以转化为有机化合物的思想
4.已知亚磷酸(H PO )与足量NaOH溶液反应生成Na HPO ,下列关于物质分类的组合正确的是( )
3 3 2 3
选项 碱 电解质 酸式盐 碱性氧化物 酸性氧化物
A 烧碱 蔗糖 NaHS Na O SO
2 2 2
B Ba(OH) CH COONH Na HPO Na O CO
2 3 4 2 3 2
C KOH BaSO NaHSO CaO SO
4 4 3
D 纯碱 H SO NaHCO K O CO
2 4 3 2 2
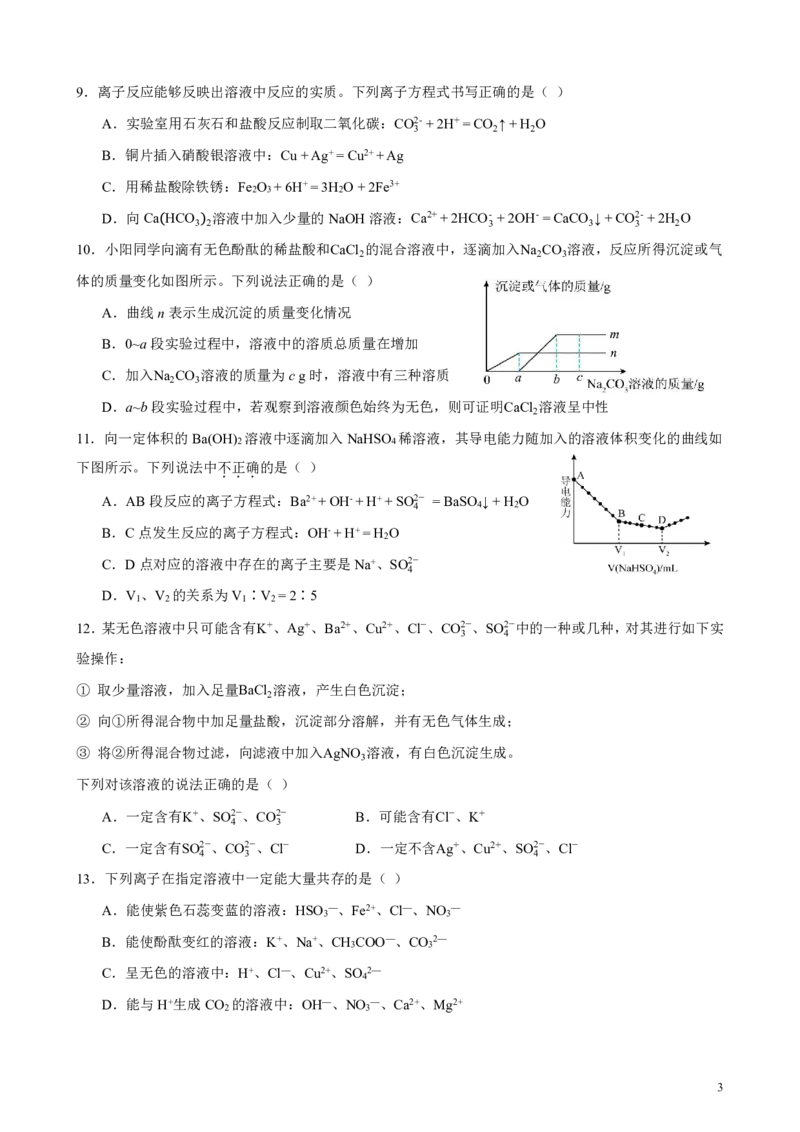
19.离子反应能够反映出溶液中反应的实质。下列离子方程式书写正确的是( )
A.实验室用石灰石和盐酸反应制取二氧化碳:CO2-+2H+=CO ↑+H O
3 2 2
B.铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag
C.用稀盐酸除铁锈:Fe O +6H+=3H O+2Fe3+
2 3 2
D.向Ca HCO 溶液中加入少量的NaOH溶液:Ca2++2HCO- +2OH-=CaCO ↓+CO2-+2H O
3 2 3 3 3 2
10.小阳同学向滴有无色酚酞的稀盐酸和CaCl 的混合溶液中,逐滴加入Na CO 溶液,反应所得沉淀或气
2 2 3
体的质量变化如图所示。下列说法正确的是( )
A.曲线n表示生成沉淀的质量变化情况
B.0~a段实验过程中,溶液中的溶质总质量在增加
C.加入Na CO 溶液的质量为cg时,溶液中有三种溶质
2 3
D.a~b段实验过程中,若观察到溶液颜色始终为无色,则可证明CaCl 溶液呈中性
2
11.向一定体积的Ba(OH) 溶液中逐滴加入NaHSO 稀溶液,其导电能力随加入的溶液体积变化的曲线如
2 4
下图所示。下列说法中不正确的是( )
...
A.AB段反应的离子方程式:Ba2++OH-+H++SO2− =BaSO ↓+H O
4 4 2
B.C点发生反应的离子方程式:OH-+H+=H O
2
C.D点对应的溶液中存在的离子主要是Na+、SO2−
4
D.V 、V 的关系为V ∶V =2∶5
1 2 1 2
12.某无色溶液中只可能含有K+、Ag+、Ba2+、Cu2+、Cl−、CO2−、SO2−中的一种或几种,对其进行如下实
3 4
验操作:
① 取少量溶液,加入足量BaCl 溶液,产生白色沉淀;
2
② 向①所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
③ 将②所得混合物过滤,向滤液中加入AgNO 溶液,有白色沉淀生成。
3
下列对该溶液的说法正确的是( )
A.一定含有K+、SO2−、CO2− B.可能含有Cl−、K+
4 3
C.一定含有SO2−、CO2−、Cl− D.一定不含Ag+、Cu2+、SO2−、Cl−
4 3 4
13.下列离子在指定溶液中一定能大量共存的是( )
A.能使紫色石蕊变蓝的溶液:HSO —、Fe2+、Cl—、NO —
3 3
B.能使酚酞变红的溶液:K+、Na+、CH COO—、CO 2—
3 3
C.呈无色的溶液中:H+、Cl—、Cu2+、SO 2—
4
D.能与H+生成CO 的溶液中:OH—、NO —、Ca2+、Mg2+
2 3
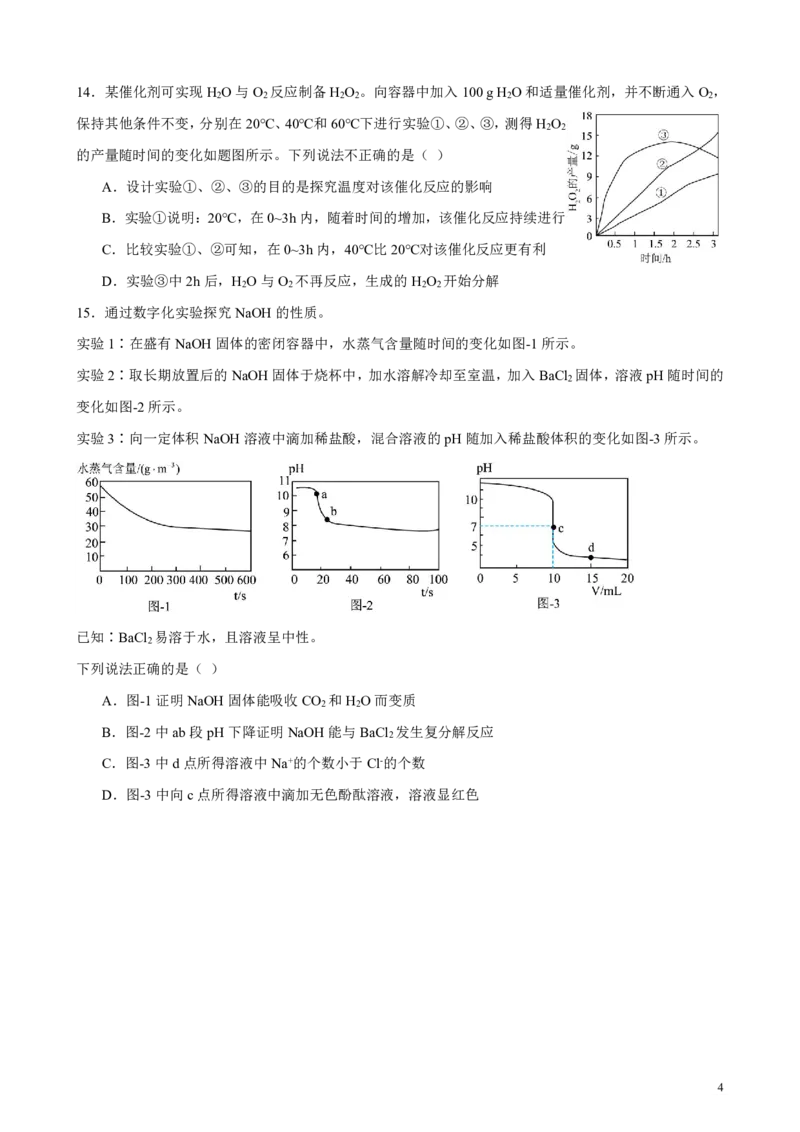
314.某催化剂可实现H O与O 反应制备H O 。向容器中加入100gH O和适量催化剂,并不断通入O ,
2 2 2 2 2 2
保持其他条件不变,分别在20℃、40℃和60℃下进行实验①、②、③,测得H O
2 2
的产量随时间的变化如题图所示。下列说法不正确的是( )
A.设计实验①、②、③的目的是探究温度对该催化反应的影响
B.实验①说明:20℃,在0~3h内,随着时间的增加,该催化反应持续进行
C.比较实验①、②可知,在0~3h内,40℃比20℃对该催化反应更有利
D.实验③中2h后,H O与O 不再反应,生成的H O 开始分解
2 2 2 2
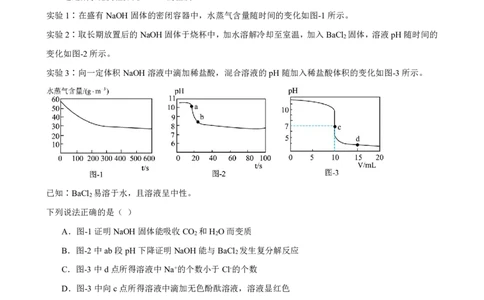
15.通过数字化实验探究NaOH的性质。
实验1∶在盛有NaOH固体的密闭容器中,水蒸气含量随时间的变化如图-1所示。
实验2∶取长期放置后的NaOH固体于烧杯中,加水溶解冷却至室温,加入BaCl 固体,溶液pH随时间的
2
变化如图-2所示。
实验3∶向一定体积NaOH溶液中滴加稀盐酸,混合溶液的pH随加入稀盐酸体积的变化如图-3所示。
已知∶BaCl 易溶于水,且溶液呈中性。
2
下列说法正确的是( )
A.图-1证明NaOH固体能吸收CO 和H O而变质
2 2
B.图-2中ab段pH下降证明NaOH能与BaCl 发生复分解反应
2
C.图-3中d点所得溶液中Na+的个数小于Cl-的个数
D.图-3中向c点所得溶液中滴加无色酚酞溶液,溶液显红色
4二、非选择题:本题共 4小题,共 55分。
16.(12分)实验室中盛有三种物质的试剂瓶上的标签已损坏,某同学想了解这三种物质(甲为液态,乙、
丙为固态,且乙、丙均为盐)的成分,他将三种物质一起溶于水得到一种无色透明溶液且无气泡产生,该溶
液中可能含有下列离子:MnO−、H+、K+、Mg2+、Ba2+、CO2−和Cl-,取该溶液进行如下实验:
4 3
I.用玻璃棒蘸取少量溶液于pH试纸上,与标准比色卡对比,pH约为3。
Ⅱ.取少许原溶液滴入硫酸溶液,产生白色沉淀。
Ⅲ.另取少许原溶液,滴加少量AgNO 溶液,产生白色沉淀。
3
Ⅳ.取Ⅲ中过滤后的滤液少许,滴加过量NaOH溶液,未产生白色沉淀。
(1)①由题意和Ⅰ中操作判断,原溶液中肯定不存在的离子是 (填离子符号,下同),肯定存在
的阳离子是 。
②根据Ⅱ、Ⅲ中实验现象判断,原溶液中存在的离子是 。
(2)依次写出实验Ⅲ、Ⅳ中发生反应的离子方程式: 、 。
(3)取7.45g的固体乙溶于水,向其中加入过量硝酸银溶液,产生14.35g沉淀。写出乙与硝酸银反应的
化学方程式: 。
(4)由分析可知甲、丙的标签依次为 、 。
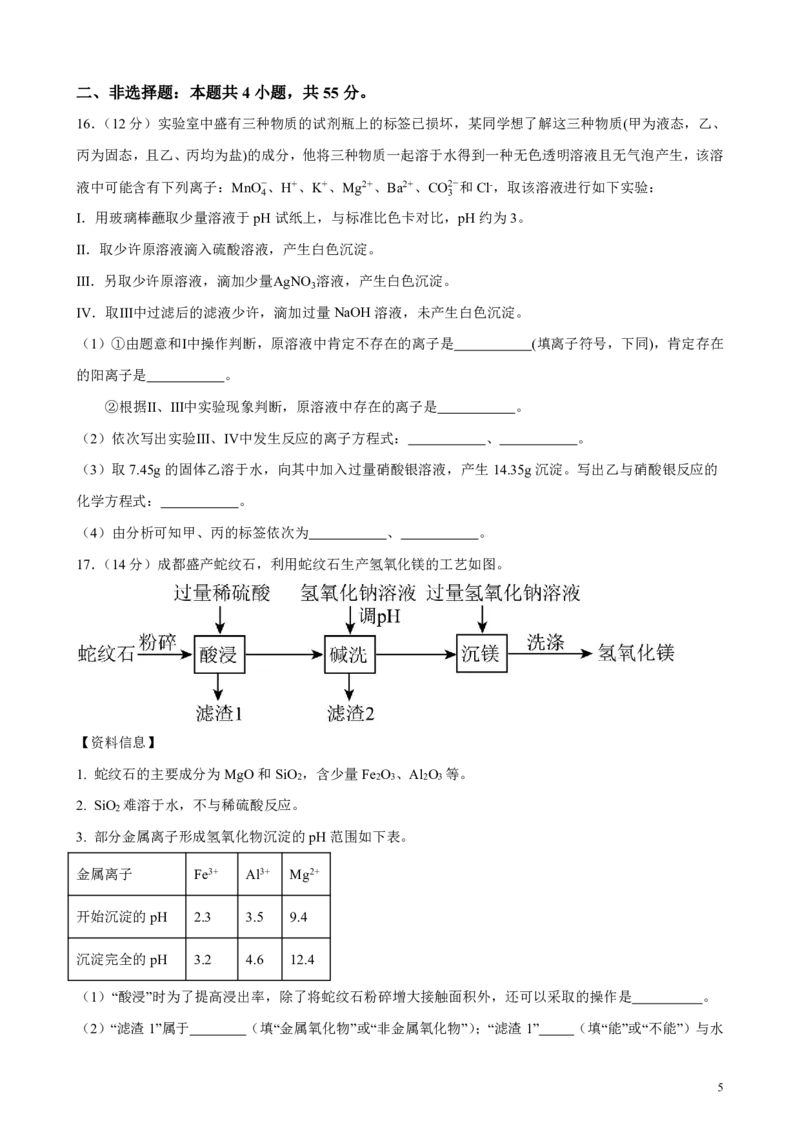
17.(14分)成都盛产蛇纹石,利用蛇纹石生产氢氧化镁的工艺如图。
【资料信息】
1. 蛇纹石的主要成分为MgO和SiO ,含少量Fe O 、Al O 等。
2 2 3 2 3
2. SiO 难溶于水,不与稀硫酸反应。
2
3. 部分金属离子形成氢氧化物沉淀的pH范围如下表。
金属离子 Fe3+ Al3+ Mg2+
开始沉淀的pH 2.3 3.5 9.4
沉淀完全的pH 3.2 4.6 12.4
(1)“酸浸”时为了提高浸出率,除了将蛇纹石粉碎增大接触面积外,还可以采取的操作是 。
(2)“滤渣1”属于 (填“金属氧化物”或“非金属氧化物”);“滤渣1” (填“能”或“不能”)与水
5反应生成硅酸。
(3)酸浸时,主要成分MgO发生反应的离子方程式为 。
(4)“碱洗”,适宜的pH范围为 。
(5)“沉镁”对应反应的化学方程式为 。
(6)“沉镁”时,证明氢氧化镁已沉淀完全的方法是 。
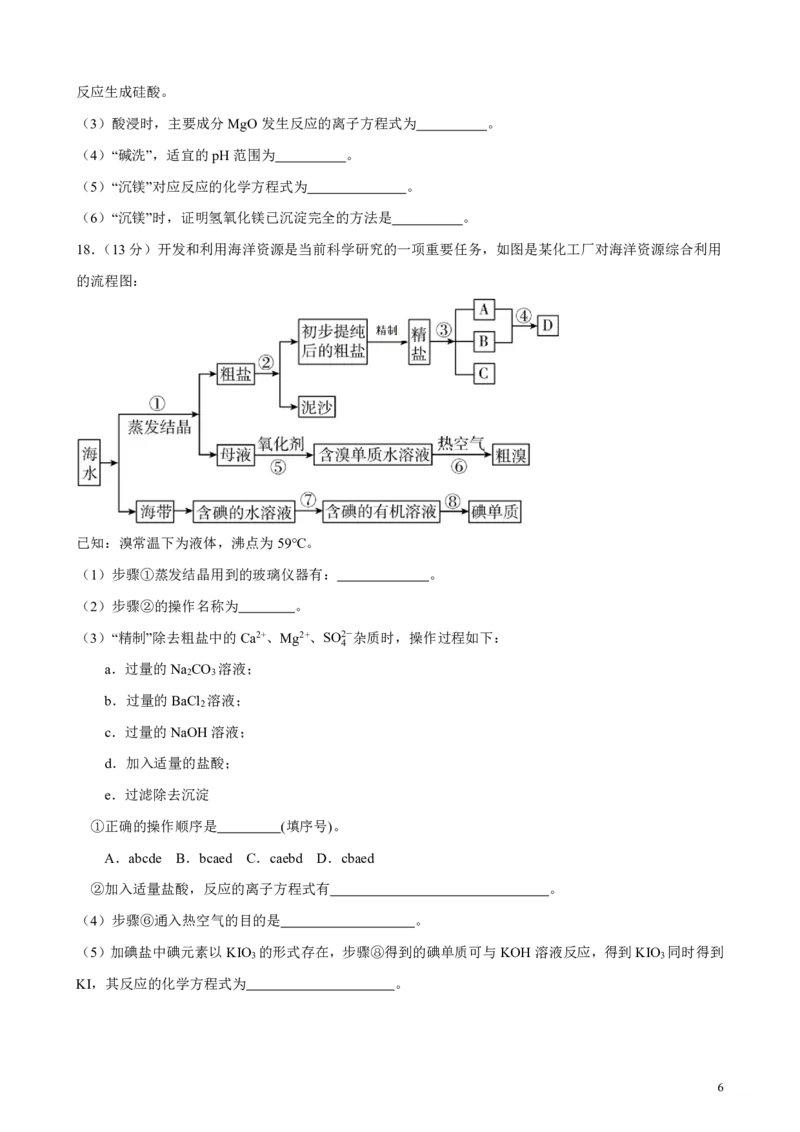
18.(13分)开发和利用海洋资源是当前科学研究的一项重要任务,如图是某化工厂对海洋资源综合利用
的流程图:
已知:溴常温下为液体,沸点为59℃。
(1)步骤①蒸发结晶用到的玻璃仪器有: 。
(2)步骤②的操作名称为 。
(3)“精制”除去粗盐中的Ca2+、Mg2+、SO2−杂质时,操作过程如下:
4
a.过量的Na CO 溶液;
2 3
b.过量的BaCl 溶液;
2
c.过量的NaOH溶液;
d.加入适量的盐酸;
e.过滤除去沉淀
①正确的操作顺序是 (填序号)。
A.abcde B.bcaed C.caebd D.cbaed
②加入适量盐酸,反应的离子方程式有 。
(4)步骤⑥通入热空气的目的是 。
(5)加碘盐中碘元素以KIO 的形式存在,步骤⑧得到的碘单质可与KOH溶液反应,得到KIO 同时得到
3 3
KI,其反应的化学方程式为 。
619.(16分)过碳酸钠(xNa CO ·yH O )俗称“固体双氧水”,常用于特定环境供氧。它遇水能分解为碳酸
2 3 2 2
钠和过氧化氢。兴趣小组对过碳酸钠的组成和性质进行以下探究。
活动一:验证过碳酸钠部分化学性质
【设计并实施实验】小组设计并实施实验如下表,完成相关内容。
实验操作 实验现象 实验结论
步骤I.取少量过碳酸钠样品和MnO
2
粉末于试管中,加足量水,将带火星 。 过碳酸钠溶于水能产生氧气。
的木条放在试管口。
步骤Ⅱ.取步骤Ⅰ反应后的上层清液, 上层清液与稀盐酸反应能产生二氧
。
滴加过量的稀盐酸, 。 化碳。
活动二:测定过碳酸钠的组成
【设计并实施实验】
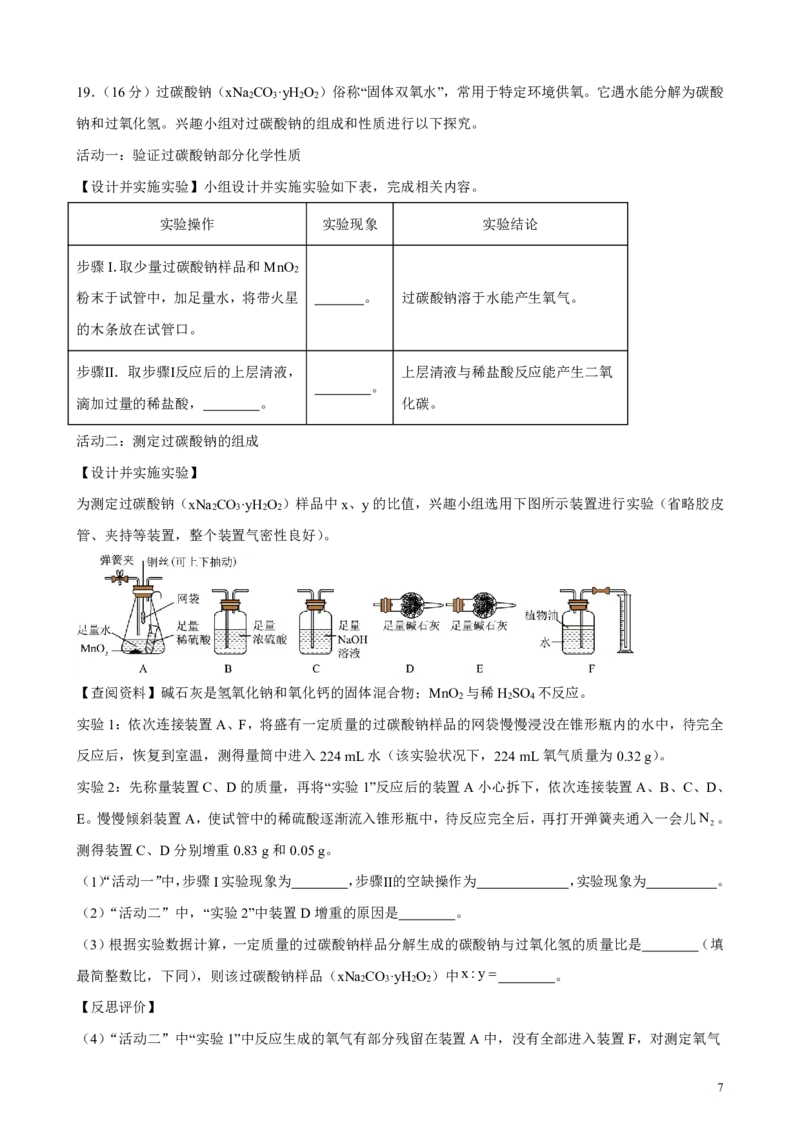
为测定过碳酸钠(xNa CO ·yH O )样品中x、y的比值,兴趣小组选用下图所示装置进行实验(省略胶皮
2 3 2 2
管、夹持等装置,整个装置气密性良好)。
【查阅资料】碱石灰是氢氧化钠和氧化钙的固体混合物;MnO 与稀H SO 不反应。
2 2 4
实验1:依次连接装置A、F,将盛有一定质量的过碳酸钠样品的网袋慢慢浸没在锥形瓶内的水中,待完全
反应后,恢复到室温,测得量筒中进入224mL水(该实验状况下,224mL氧气质量为0.32g)。
实验2:先称量装置C、D的质量,再将“实验1”反应后的装置A小心拆下,依次连接装置A、B、C、D、
E。慢慢倾斜装置A,使试管中的稀硫酸逐渐流入锥形瓶中,待反应完全后,再打开弹簧夹通入一会儿N 。
2
测得装置C、D分别增重0.83g和0.05g。
(1)“活动一”中,步骤I实验现象为 ,步骤Ⅱ的空缺操作为 ,实验现象为 。
(2)“活动二”中,“实验2”中装置D增重的原因是 。
(3)根据实验数据计算,一定质量的过碳酸钠样品分解生成的碳酸钠与过氧化氢的质量比是 (填
最简整数比,下同),则该过碳酸钠样品(xNa CO ·yH O )中x:y 。
2 3 2 2
【反思评价】
(4)“活动二”中“实验1”中反应生成的氧气有部分残留在装置A中,没有全部进入装置F,对测定氧气
7体积的影响是 (填“偏大”“偏小”或“无影响”)。
(5)过碳酸钠的实际组成是2Na CO ·3H O 。如果你计算的过碳酸钠组成中Na CO 的量偏大,试分析造
2 3 2 2 2 3
成实验误差的原因可能是 (写1条)。
8