文档内容
松江区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2020.1
相对原子质量:H-1 C-12 O-16 N-14 K-39 Cl-35.5 Ca-40
Mg-24 Cu-64
六、选择题(共 20 分)
1.供人类呼吸的气体是
A. 二氧化碳 B. 水蒸气 C. 氧气 D. 氮气
2.化学变化的判断依据是
A. 放热 B. 发光 C. 生成新物质 D. 生成沉淀
3.Fe O 中Fe的化合价是
2 3
A. -3 B. -2 C. +2 D. +3
4.放入一定量水中,充分搅拌后形成溶液的是
A. 泥土 B. 麻油 C. 食盐 D. 牛奶
5.属于纯净物的是
A. 石灰石 B. 二氧化碳 C. 空气 D. 天然气
6.上海市垃圾分类实行的“四分类”标准,蛋壳属于
A. 可回收垃圾 B. 有害垃圾 C. 湿垃圾 D. 干垃圾
7.常温下测得一些食物的近似 pH,酸性最强的是
A. 苹果汁~3.1 B. 番茄汁~4.2 C. 牛奶~6.5 D. 玉米粥~7.5
8.属于氧化物的是
.
A KClO B. O C. HO D. O
3 2 2 3
9.下列物质的用途中,利用其物理性质的是
A. 氧气用于气焊 B. 焦炭用于冶炼金属
C. 氮气用作保护气 D. 干冰用于人工降雨
10.物质在氧气中燃烧,现象正确的是
A. 红磷:大量白雾 B. 木炭:白色浑浊
C. 铁丝:火星四射 D. 硫粉:淡蓝色火焰
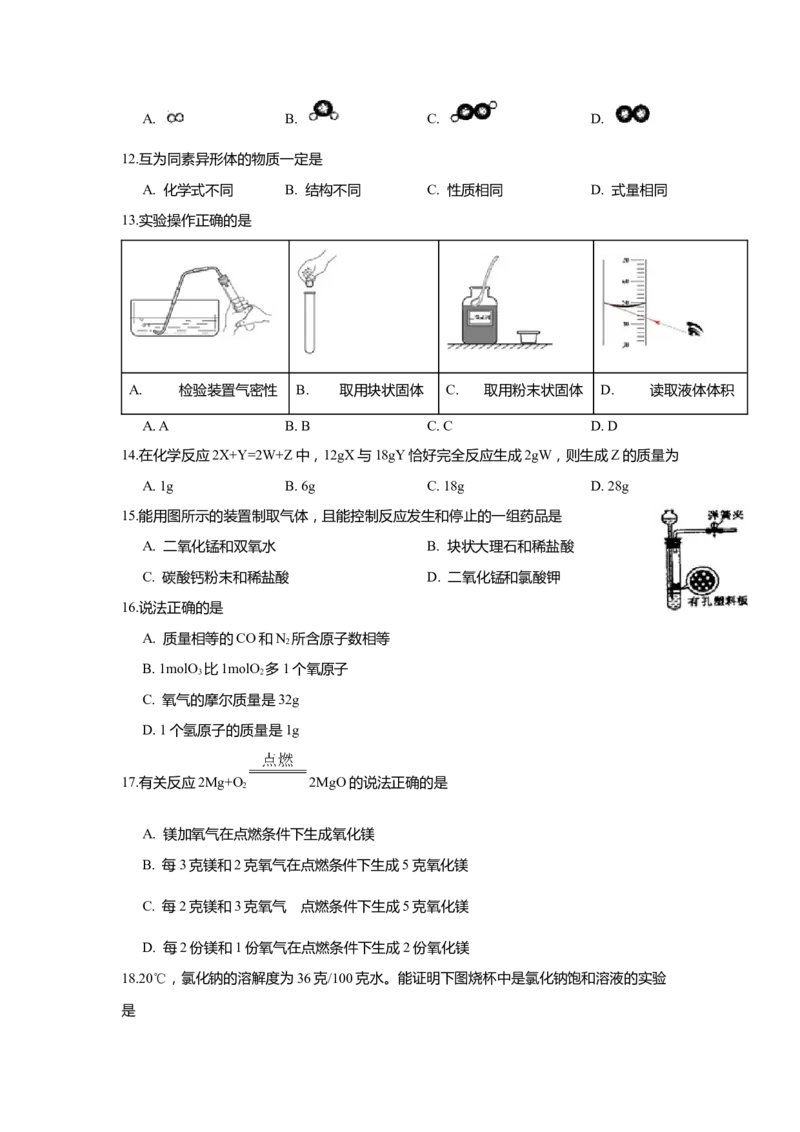
11.用“ ”表示氢原子“ ”表示氧原子,表示氢分子的是A. B. C. D.
12.互为同素异形体的物质一定是
A. 化学式不同 B. 结构不同 C. 性质相同 D. 式量相同
13.实验操作正确的是
A. 检验装置气密性 B. 取用块状固体 C. 取用粉末状固体 D. 读取液体体积
A. A B. B C. C D. D
14.在化学反应2X+Y=2W+Z中,12gX与18gY恰好完全反应生成2gW,则生成Z的质量为
A. 1g B. 6g C. 18g D. 28g
15.能用图所示的装置制取气体,且能控制反应发生和停止的一组药品是
A. 二氧化锰和双氧水 B. 块状大理石和稀盐酸
C. 碳酸钙粉末和稀盐酸 D. 二氧化锰和氯酸钾
16.说法正确的是
A. 质量相等的CO和N 所含原子数相等
2
B. 1molO 比1molO 多1个氧原子
3 2
C. 氧气的摩尔质量是32g
D. 1个氢原子的质量是1g
17.有关反应2Mg+O 2MgO的说法正确的是
2
A. 镁加氧气在点燃条件下生成氧化镁
B. 每3克镁和2克氧气在点燃条件下生成5克氧化镁
在
C. 每2克镁和3克氧气 点燃条件下生成5克氧化镁
D. 每2份镁和1份氧气在点燃条件下生成2份氧化镁
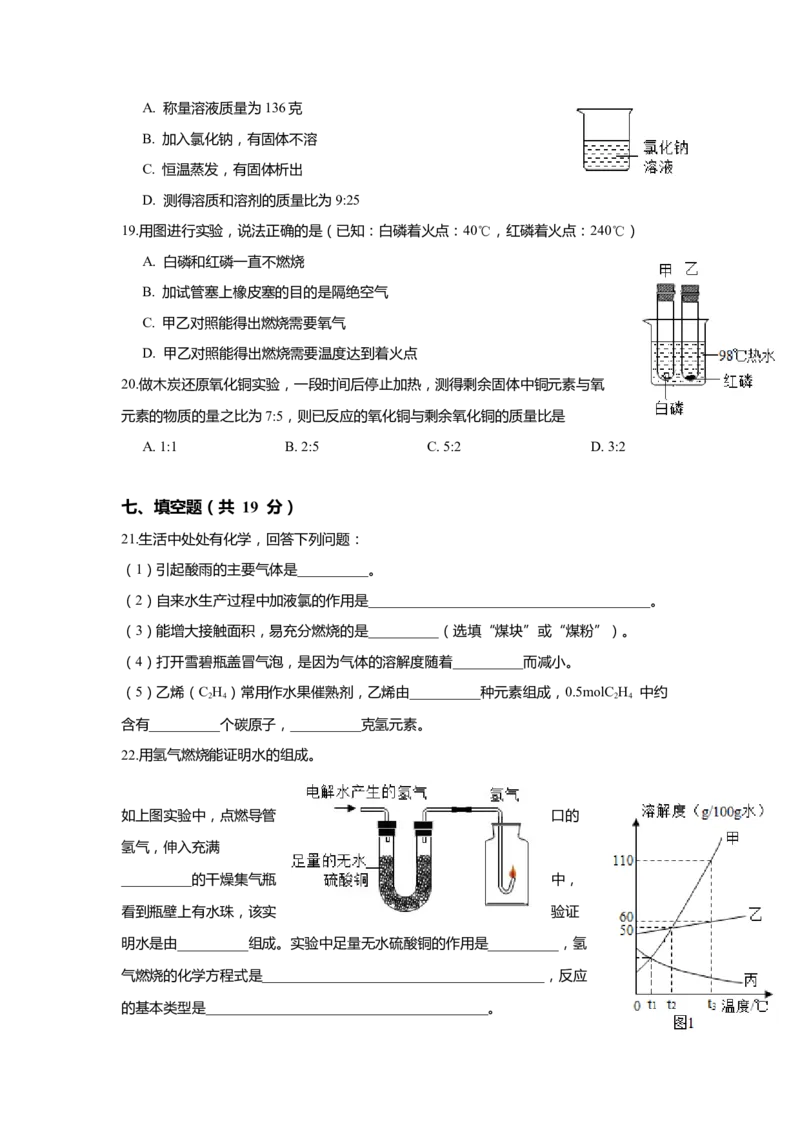
18.20℃,氯化钠的溶解度为36克/100克水。能证明下图烧杯中是氯化钠饱和溶液的实验
是A. 称量溶液质量为136克
B. 加入氯化钠,有固体不溶
C. 恒温蒸发,有固体析出
D. 测得溶质和溶剂的质量比为9:25
19.用图进行实验,说法正确的是(已知:白磷着火点:40℃,红磷着火点:240℃)
A. 白磷和红磷一直不燃烧
B. 加试管塞上橡皮塞的目的是隔绝空气
C. 甲乙对照能得出燃烧需要氧气
D. 甲乙对照能得出燃烧需要温度达到着火点
20.做木炭还原氧化铜实验,一段时间后停止加热,测得剩余固体中铜元素与氧
元素的物质的量之比为7:5,则已反应的氧化铜与剩余氧化铜的质量比是
A. 1:1 B. 2:5 C. 5:2 D. 3:2
七、填空题(共 19 分)
21.生活中处处有化学,回答下列问题:
(1)引起酸雨的主要气体是__________。
(2)自来水生产过程中加液氯的作用是________________________________________。
(3)能增大接触面积,易充分燃烧的是__________(选填“煤块”或“煤粉”)。
(4)打开雪碧瓶盖冒气泡,是因为气体的溶解度随着__________而减小。
(5)乙烯(C H)常用作水果催熟剂,乙烯由__________种元素组成,0.5molC H 中约
2 4 2 4
含有__________个碳原子,__________克氢元素。
22.用氢气燃烧能证明水的组成。
如上图实验中,点燃导管 口的
氢气,伸入充满
__________的干燥集气瓶 中,
看到瓶壁上有水珠,该实 验证
明水是由__________组成。实验中足量无水硫酸铜的作用是__________,氢
气燃烧的化学方程式是________________________________________,反应
的基本类型是________________________________________。23.研究物质的溶解对于生产、生活有重要意义。
(1)图 1 为甲、乙、丙(均不含结晶水)三种固体物质的溶解度曲线。t℃,甲物质的
3
溶解度是__________克/100g 水,把丙的饱和溶液转化为不饱和溶液的一种方法是
________________________________________。
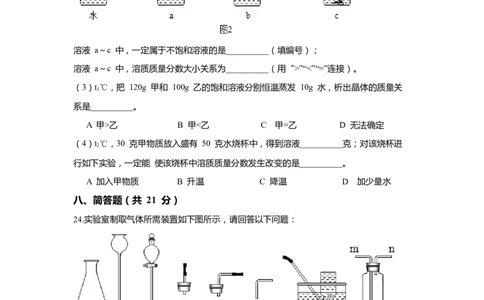
(2)t℃,在一定量水中依次进行如图2实验,得到相应的溶液 a~c。
1
溶液 a~c 中,一定属于不饱和溶液的是__________(填编号);
溶液 a~c 中,溶质质量分数大小关系为__________(用“>”“<”“=”连接)。
(3)t℃,把 120g 甲和 100g 乙的饱和溶液分别恒温蒸发 10g 水,析出晶体的质量关
1
系是__________。
A 甲>乙 B 甲<乙 C 甲=乙 D 无法确定
(4)t℃,30 克甲物质放入盛有 50 克水烧杯中,得到溶液__________克;对该烧杯进
2
行如下实验,一定能 使该烧杯中溶质质量分数发生改变的是__________。
A 加入甲物质 B 升温 C 降温 D 加少量水
八、简答题(共 21 分)
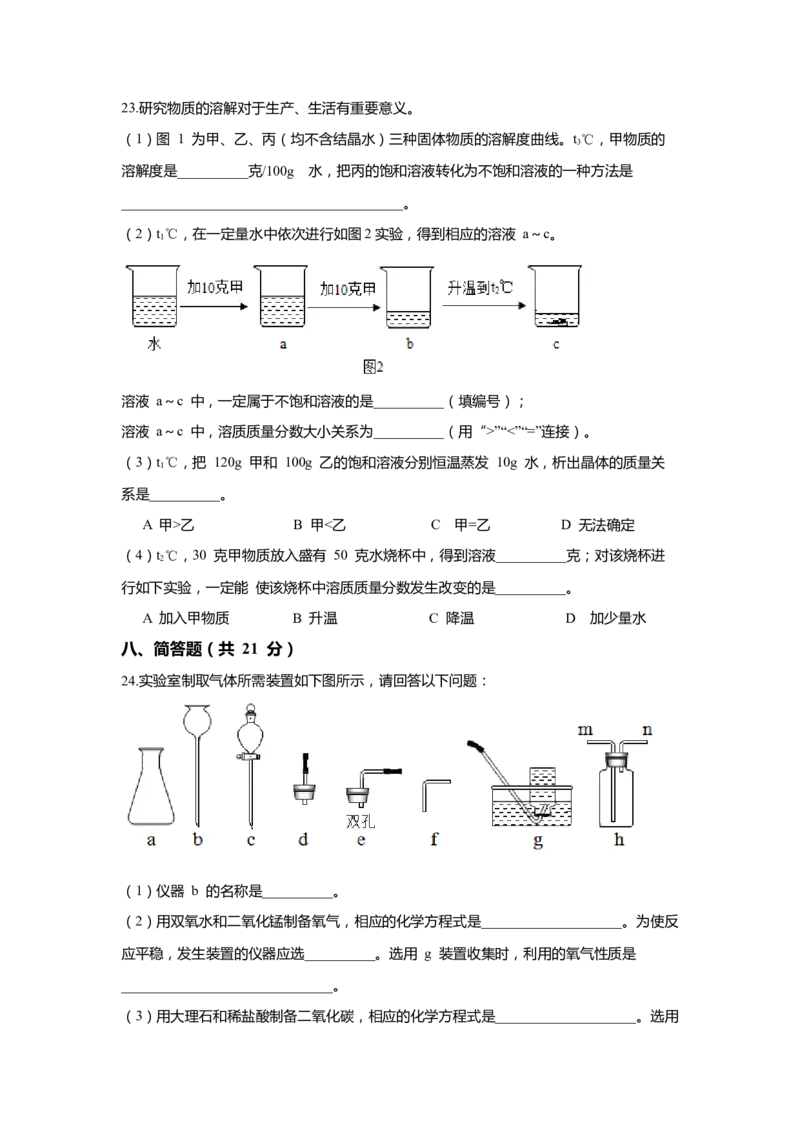
24.实验室制取气体所需装置如下图所示,请回答以下问题:
(1)仪器 b 的名称是__________。
(2)用双氧水和二氧化锰制备氧气,相应的化学方程式是____________________。为使反
应平稳,发生装置的仪器应选__________。选用 g 装置收集时,利用的氧气性质是
______________________________。
(3)用大理石和稀盐酸制备二氧化碳,相应的化学方程式是____________________。选用h 装置收集二氧化碳,验满的方法是______________________________。若用块状大理石
和稀硫酸反应,现象是______________________________。
(4)加热氯酸钾与二氧化锰的混合物制得氧气 9.6 克,计算生成氯化钾的物质的量(根
据化学方程式计算)__________________________________________________。
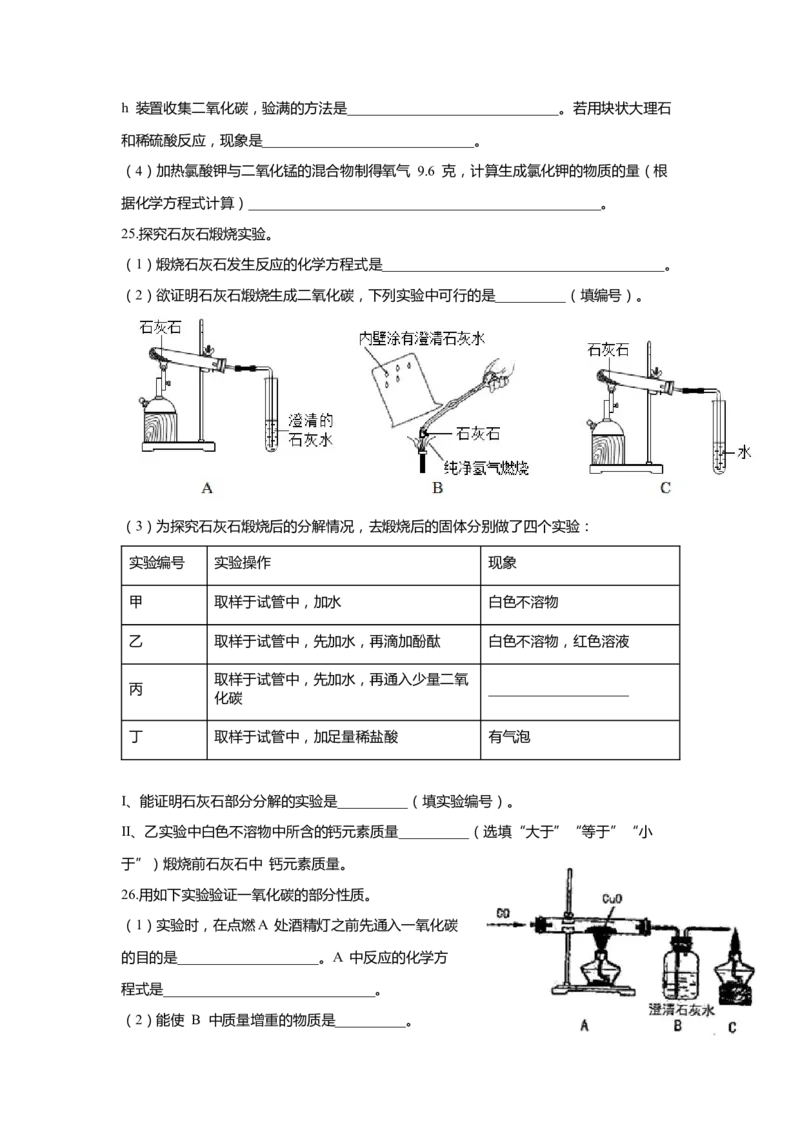
25.探究石灰石煅烧实验。
(1)煅烧石灰石发生反应的化学方程式是________________________________________。
(2)欲证明石灰石煅烧生成二氧化碳,下列实验中可行的是__________(填编号)。
(3)为探究石灰石煅烧后的分解情况,去煅烧后的固体分别做了四个实验:
实验编号 实验操作 现象
甲 取样于试管中,加水 白色不溶物
乙 取样于试管中,先加水,再滴加酚酞 白色不溶物,红色溶液
取样于试管中,先加水,再通入少量二氧
丙 ____________________
化碳
丁 取样于试管中,加足量稀盐酸 有气泡
I、能证明石灰石部分分解的实验是__________(填实验编号)。
II、乙实验中白色不溶物中所含的钙元素质量__________(选填“大于”“等于”“小
于”)煅烧前石灰石中 钙元素质量。
26.用如下实验验证一氧化碳的部分性质。
(1)实验时,在点燃A 处酒精灯之前先通入一氧化碳
的目的是____________________。A 中反应的化学方
程式是______________________________。
(2)能使 B 中质量增重的物质是__________。(3)实验过程中不会出现的现象是__________。
I、A 中固体部分变红,B 处右导管口无蓝色火焰
II、B 中溶液澄清,右导管口有蓝色火焰
III、B 中溶液浑浊,右导管口有蓝色火焰
IV、A 中固体红色,B 中溶液浑浊
(4)反应前A 中氧化铜 8 克,反应结束,冷却至室温,称量 A 中固体为 7 克,则固体
的成分是__________。