文档内容
专题 06 简答题第 1 题、气体制取题
一、填空题
1.(2023·上海崇明·统考一模)化学与生活、科技、科学实验息息相关。
(1)自来水厂在净化水的过程中加入明矾的作用是______(填“杀菌消毒”或“使悬浮物沉淀”)。
(2)2022年12月4日,航天员陈冬、刘洋、蔡旭哲结束了为期6个月的太空之旅,安全返回地球。
Ⅰ.航天员呼吸所需的O 来自水的电解,其反应的化学方程式是____,该反应属于____(选填“化合”或
2
“分解”)反应。
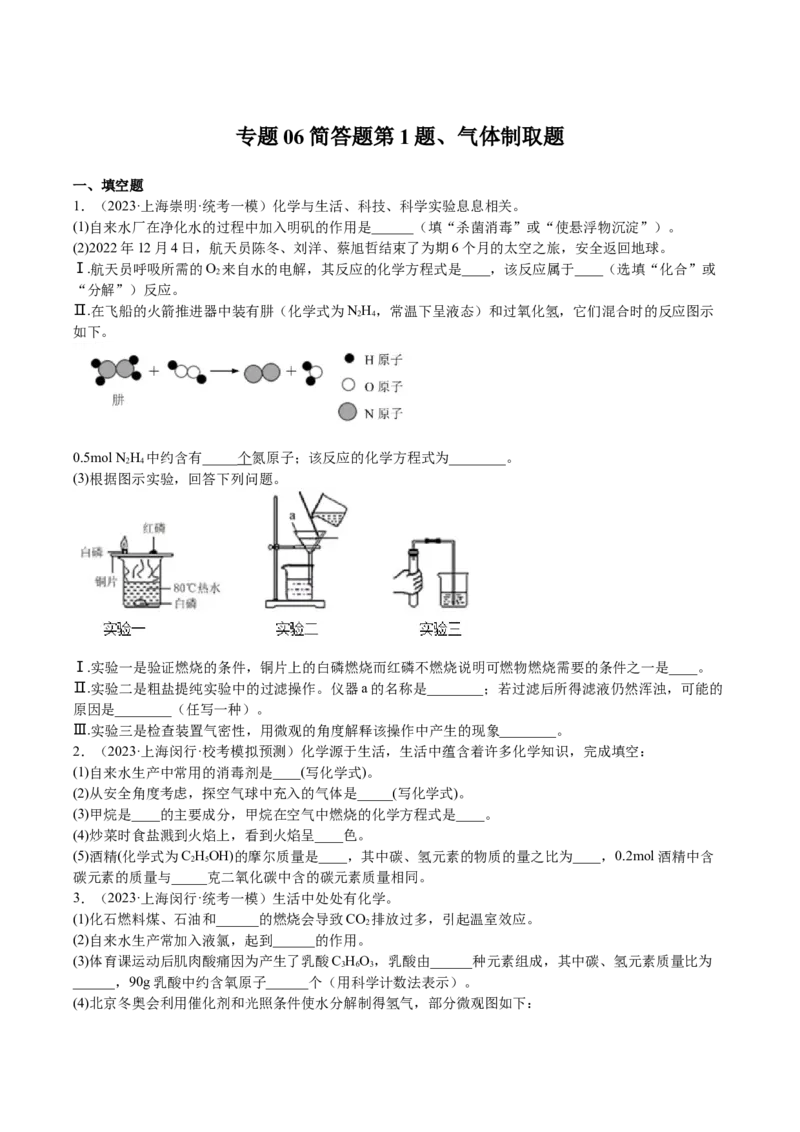
Ⅱ.在飞船的火箭推进器中装有肼(化学式为NH,常温下呈液态)和过氧化氢,它们混合时的反应图示
2 4
如下。
0.5mol N H 中约含有_____个氮原子;该反应的化学方程式为________。
2 4
(3)根据图示实验,回答下列问题。
Ⅰ.实验一是验证燃烧的条件,铜片上的白磷燃烧而红磷不燃烧说明可燃物燃烧需要的条件之一是____。
Ⅱ.实验二是粗盐提纯实验中的过滤操作。仪器a的名称是________;若过滤后所得滤液仍然浑浊,可能的
原因是________(任写一种)。
Ⅲ.实验三是检查装置气密性,用微观的角度解释该操作中产生的现象________。
2.(2023·上海闵行·校考模拟预测)化学源于生活,生活中蕴含着许多化学知识,完成填空:
(1)自来水生产中常用的消毒剂是____(写化学式)。
(2)从安全角度考虑,探空气球中充入的气体是_____(写化学式)。
(3)甲烷是____的主要成分,甲烷在空气中燃烧的化学方程式是____。
(4)炒菜时食盐溅到火焰上,看到火焰呈____色。
(5)酒精(化学式为C HOH)的摩尔质量是____,其中碳、氢元素的物质的量之比为____,0.2mol酒精中含
2 5
碳元素的质量与_____克二氧化碳中含的碳元素质量相同。
3.(2023·上海闵行·统考一模)生活中处处有化学。
(1)化石燃料煤、石油和______的燃烧会导致CO 排放过多,引起温室效应。
2
(2)自来水生产常加入液氯,起到______的作用。
(3)体育课运动后肌肉酸痛因为产生了乳酸C HO,乳酸由______种元素组成,其中碳、氢元素质量比为
3 6 3
______,90g乳酸中约含氧原子______个(用科学计数法表示)。
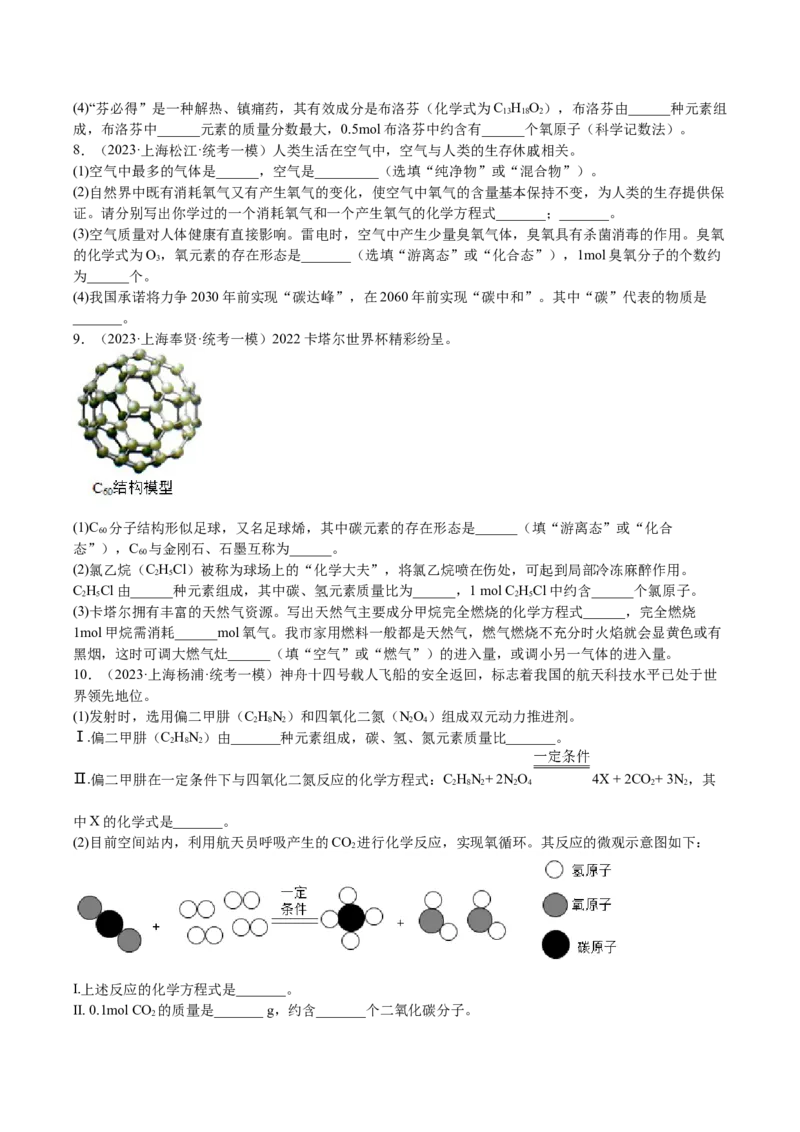
(4)北京冬奥会利用催化剂和光照条件使水分解制得氢气,部分微观图如下:反应I的化学方程式______,反应II属于______反应(填基本反应类型)。
4.(2023·上海青浦·统考一模)中国是茶的故乡,中国人的饮茶史,从有历史记载起,至今已经有四千多
年。
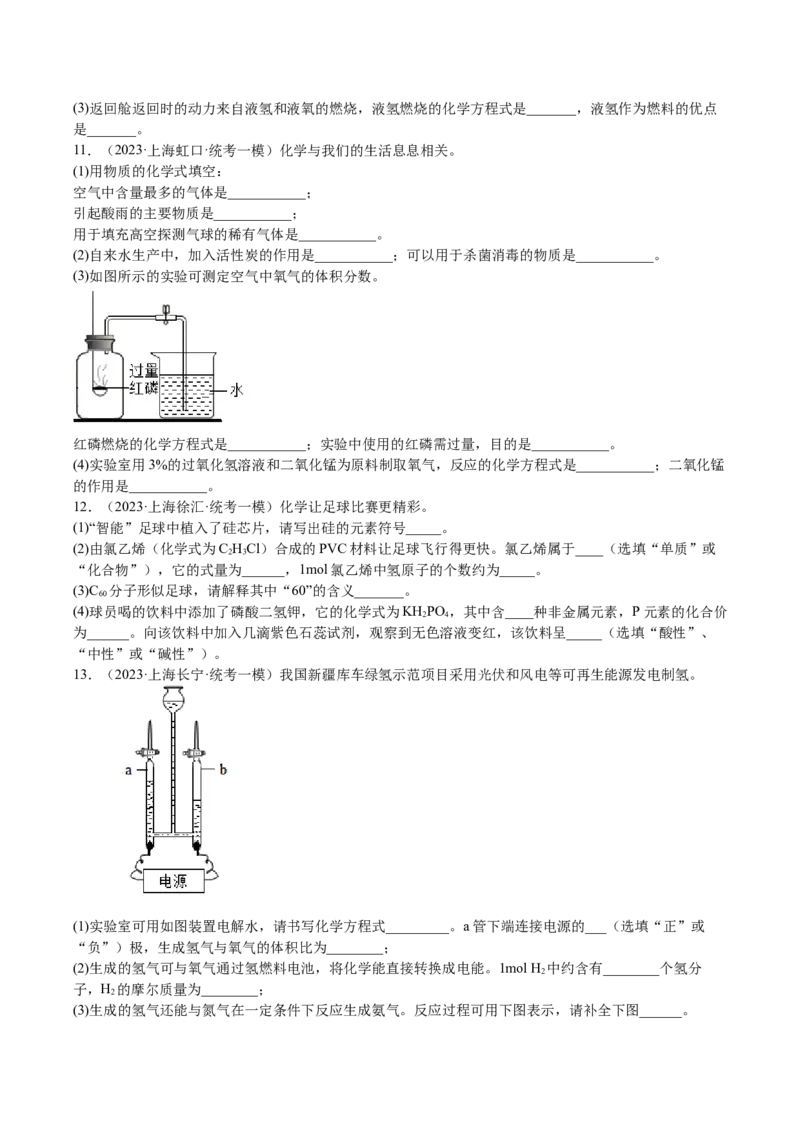
(1)下列泡茶的主要步骤中,与实验室过滤操作原理相同的是______。
(2)茶叶中含有茶氨酸(化学式为C H NO)。茶氨酸由______种元素组成,茶氨酸中碳、氢元素的物质
7 14 2 3
的量之比为______,1mol茶氨酸中约含______个氮原子。茶氨酸______(填“属于”或“不属于”)氧化
物,你的理由是______。
5.(2023·上海杨浦·校考二模)我国航天工作者自立自强,创新超越,将航天事业推向了新的高度。
(1)今年4月,“天和”核心舱由“长征五号B”火箭发射并进入预定轨道。
①火箭外壳中含有铝,它会在空气中会形成致密的保护层,方程式为_______。
②火箭推进剂采用液氧、液氢,两者反应生成水,反应的基本类型是_______。
(2)今年5月,“天问一号”探测器在火星着落。
火星大气含微量甲烷(CH),CH 属于______(选填“有机物”或“无机物”),0.5 mol CH 中约含
4 4 4
_______个碳原子,其质量为_______克。
(3)预计明年,“天宫”空间站在轨道上完成组装。
空间站供氧的方式有多种:
①携带加压氧气罐。液氧气化的过程微观上发生改变的是_______。
②使用氧气发生器。发生器中装有NaClO 和催化剂,若其反应类似实验室制氧气,写出该反应方程式
3
_______。
6.(2023·上海宝山·一模)人类生存、生活、生产离不开化学。
(1)我们需要清洁的空气。空气中二氧化碳含量过多会引发________;工厂大量燃烧含硫的煤,生成_____
会造成酸雨,了解某地酸雨的酸碱度,可用________粗略测定。
(2)我们需要洁净的水。河水经沉降、过滤、吸附、加液氯等净化过程得到洁净的自来水,水净化过程中吸
附常用的物质是________(填名称),液氯的作用是_________,其实质是利用液氯与水反应生成的次氯
酸(化学式为HClO);HClO中Cl的化合价为_________,其摩尔质量是_______g/mol,1mol HClO含原
子数为________个。
7.(2023·上海嘉定·统考一模)化学对人体健康和人类生活有着十分重要的作用。请回答下列问题。
(1)活性炭口罩中的活性炭起______作用。
(2)75%的酒精可以有效灭活病毒,25mL酒精和75mL水混合,总体积______100mL。(填“>”“=”或
“<”)
(3)0.9%的生理盐水中溶质是______。(4)“芬必得”是一种解热、镇痛药,其有效成分是布洛芬(化学式为C H O),布洛芬由______种元素组
13 18 2
成,布洛芬中______元素的质量分数最大,0.5mol布洛芬中约含有______个氧原子(科学记数法)。
8.(2023·上海松江·统考一模)人类生活在空气中,空气与人类的生存休戚相关。
(1)空气中最多的气体是______,空气是_________(选填“纯净物”或“混合物”)。
(2)自然界中既有消耗氧气又有产生氧气的变化,使空气中氧气的含量基本保持不变,为人类的生存提供保
证。请分别写出你学过的一个消耗氧气和一个产生氧气的化学方程式_______;_______。
(3)空气质量对人体健康有直接影响。雷电时,空气中产生少量臭氧气体,臭氧具有杀菌消毒的作用。臭氧
的化学式为O,氧元素的存在形态是_______(选填“游离态”或“化合态”),1mol臭氧分子的个数约
3
为______个。
(4)我国承诺将力争2030年前实现“碳达峰”,在2060年前实现“碳中和”。其中“碳”代表的物质是
_______。
9.(2023·上海奉贤·统考一模)2022卡塔尔世界杯精彩纷呈。
(1)C 分子结构形似足球,又名足球烯,其中碳元素的存在形态是______(填“游离态”或“化合
60
态”),C 与金刚石、石墨互称为______。
60
(2)氯乙烷(C HCl)被称为球场上的“化学大夫”,将氯乙烷喷在伤处,可起到局部冷冻麻醉作用。
2 5
C HCl由______种元素组成,其中碳、氢元素质量比为______,1 mol C HCl中约含______个氯原子。
2 5 2 5
(3)卡塔尔拥有丰富的天然气资源。写出天然气主要成分甲烷完全燃烧的化学方程式______,完全燃烧
1mol甲烷需消耗______mol氧气。我市家用燃料一般都是天然气,燃气燃烧不充分时火焰就会显黄色或有
黑烟,这时可调大燃气灶______(填“空气”或“燃气”)的进入量,或调小另一气体的进入量。
10.(2023·上海杨浦·统考一模)神舟十四号载人飞船的安全返回,标志着我国的航天科技水平已处于世
界领先地位。
(1)发射时,选用偏二甲肼(C HN)和四氧化二氮(NO)组成双元动力推进剂。
2 8 2 2 4
Ⅰ.偏二甲肼(C HN)由_______种元素组成,碳、氢、氮元素质量比_______。
2 8 2
Ⅱ.偏二甲肼在一定条件下与四氧化二氮反应的化学方程式:C HN+ 2N O 4X + 2CO + 3N ,其
2 8 2 2 4 2 2
中X的化学式是_______。
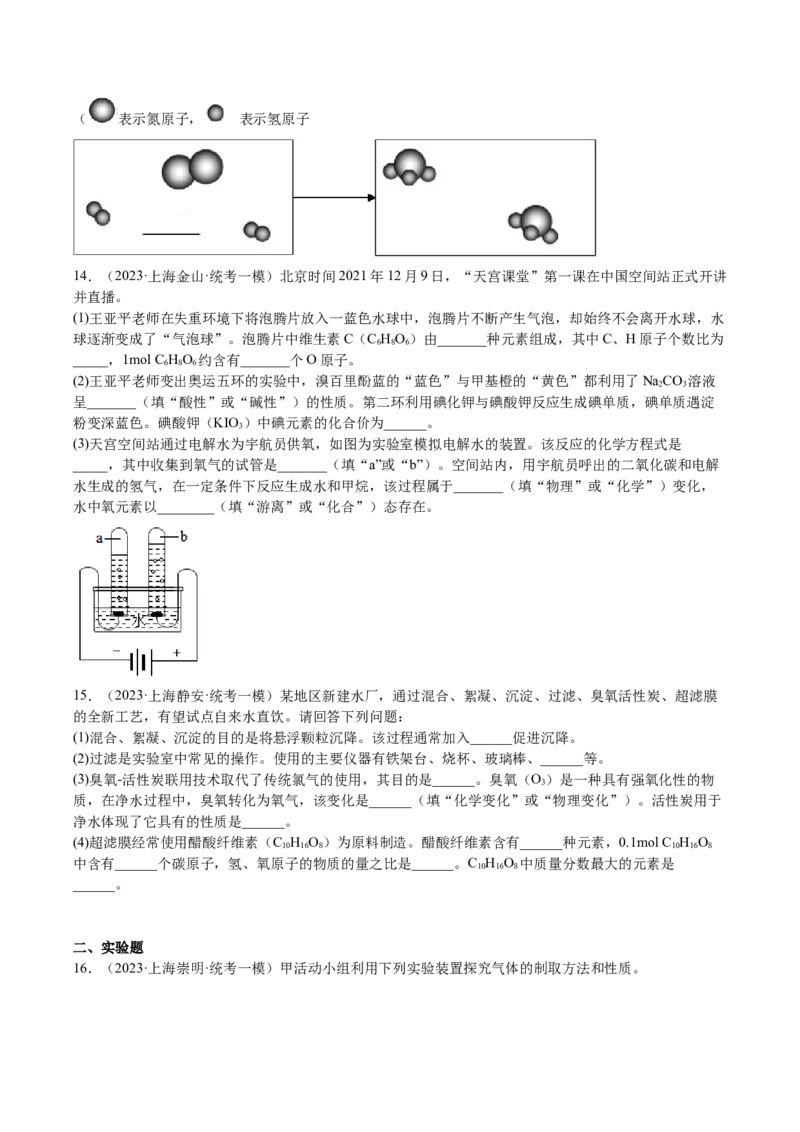
(2)目前空间站内,利用航天员呼吸产生的CO 进行化学反应,实现氧循环。其反应的微观示意图如下:
2
I.上述反应的化学方程式是_______。
II. 0.1mol CO 的质量是_______ g,约含_______个二氧化碳分子。
2(3)返回舱返回时的动力来自液氢和液氧的燃烧,液氢燃烧的化学方程式是_______,液氢作为燃料的优点
是_______。
11.(2023·上海虹口·统考一模)化学与我们的生活息息相关。
(1)用物质的化学式填空:
空气中含量最多的气体是___________;
引起酸雨的主要物质是___________;
用于填充高空探测气球的稀有气体是___________。
(2)自来水生产中,加入活性炭的作用是___________;可以用于杀菌消毒的物质是___________。
(3)如图所示的实验可测定空气中氧气的体积分数。
红磷燃烧的化学方程式是___________;实验中使用的红磷需过量,目的是___________。
(4)实验室用3%的过氧化氢溶液和二氧化锰为原料制取氧气,反应的化学方程式是___________;二氧化锰
的作用是___________。
12.(2023·上海徐汇·统考一模)化学让足球比赛更精彩。
(1)“智能”足球中植入了硅芯片,请写出硅的元素符号_____。
(2)由氯乙烯(化学式为C HCl)合成的PVC材料让足球飞行得更快。氯乙烯属于____(选填“单质”或
2 3
“化合物”),它的式量为______,1mol氯乙烯中氢原子的个数约为_____。
(3)C 分子形似足球,请解释其中“60”的含义_______。
60
(4)球员喝的饮料中添加了磷酸二氢钾,它的化学式为KH PO ,其中含____种非金属元素,P元素的化合价
2 4
为______。向该饮料中加入几滴紫色石蕊试剂,观察到无色溶液变红,该饮料呈_____(选填“酸性”、
“中性”或“碱性”)。
13.(2023·上海长宁·统考一模)我国新疆库车绿氢示范项目采用光伏和风电等可再生能源发电制氢。
(1)实验室可用如图装置电解水,请书写化学方程式_________。a管下端连接电源的___(选填“正”或
“负”)极,生成氢气与氧气的体积比为________;
(2)生成的氢气可与氧气通过氢燃料电池,将化学能直接转换成电能。1mol H 中约含有________个氢分
2
子,H 的摩尔质量为________;
2
(3)生成的氢气还能与氮气在一定条件下反应生成氨气。反应过程可用下图表示,请补全下图______。( 表示氮原子, 表示氢原子
14.(2023·上海金山·统考一模)北京时间2021年12月9日,“天宫课堂”第一课在中国空间站正式开讲
并直播。
(1)王亚平老师在失重环境下将泡腾片放入一蓝色水球中,泡腾片不断产生气泡,却始终不会离开水球,水
球逐渐变成了“气泡球”。泡腾片中维生素C(C HO)由_______种元素组成,其中C、H原子个数比为
6 8 6
_____,1mol C HO 约含有_______个O原子。
6 8 6
(2)王亚平老师变出奥运五环的实验中,溴百里酚蓝的“蓝色”与甲基橙的“黄色”都利用了NaCO 溶液
2 3
呈_______(填“酸性”或“碱性”)的性质。第二环利用碘化钾与碘酸钾反应生成碘单质,碘单质遇淀
粉变深蓝色。碘酸钾(KIO )中碘元素的化合价为______。
3
(3)天宫空间站通过电解水为宇航员供氧,如图为实验室模拟电解水的装置。该反应的化学方程式是
_____,其中收集到氧气的试管是_______(填“a”或“b”)。空间站内,用宇航员呼出的二氧化碳和电解
水生成的氢气,在一定条件下反应生成水和甲烷,该过程属于_______(填“物理”或“化学”)变化,
水中氧元素以________(填“游离”或“化合”)态存在。
15.(2023·上海静安·统考一模)某地区新建水厂,通过混合、絮凝、沉淀、过滤、臭氧活性炭、超滤膜
的全新工艺,有望试点自来水直饮。请回答下列问题:
(1)混合、絮凝、沉淀的目的是将悬浮颗粒沉降。该过程通常加入______促进沉降。
(2)过滤是实验室中常见的操作。使用的主要仪器有铁架台、烧杯、玻璃棒、______等。
(3)臭氧-活性炭联用技术取代了传统氯气的使用,其目的是______。臭氧(O)是一种具有强氧化性的物
3
质,在净水过程中,臭氧转化为氧气,该变化是______(填“化学变化”或“物理变化”)。活性炭用于
净水体现了它具有的性质是______。
(4)超滤膜经常使用醋酸纤维素(C H O)为原料制造。醋酸纤维素含有______种元素,0.1mol C H O
10 16 8 10 16 8
中含有______个碳原子,氢、氧原子的物质的量之比是______。C H O 中质量分数最大的元素是
10 16 8
______。
二、实验题
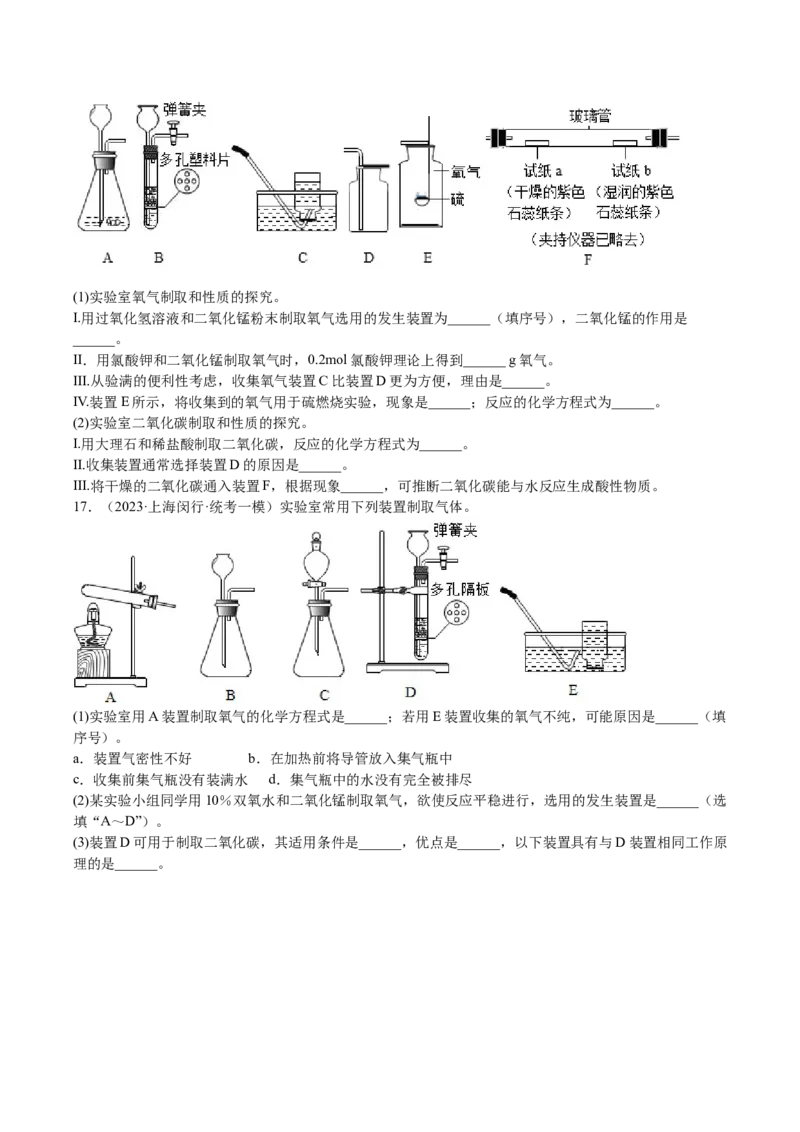
16.(2023·上海崇明·统考一模)甲活动小组利用下列实验装置探究气体的制取方法和性质。(1)实验室氧气制取和性质的探究。
I.用过氧化氢溶液和二氧化锰粉末制取氧气选用的发生装置为______(填序号),二氧化锰的作用是
______。
II.用氯酸钾和二氧化锰制取氧气时,0.2mol氯酸钾理论上得到______ g氧气。
III.从验满的便利性考虑,收集氧气装置C比装置D更为方便,理由是______。
IV.装置E所示,将收集到的氧气用于硫燃烧实验,现象是______;反应的化学方程式为______。
(2)实验室二氧化碳制取和性质的探究。
I.用大理石和稀盐酸制取二氧化碳,反应的化学方程式为______。
II.收集装置通常选择装置D的原因是______。
III.将干燥的二氧化碳通入装置F,根据现象______,可推断二氧化碳能与水反应生成酸性物质。
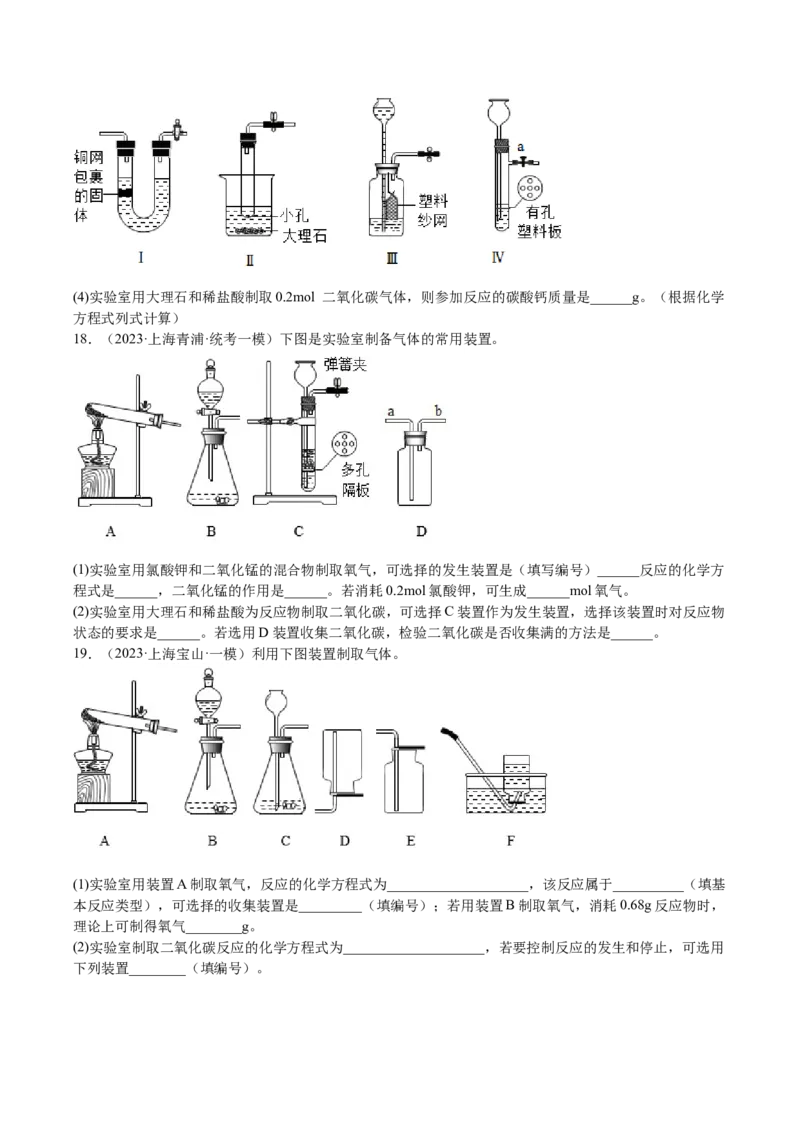
17.(2023·上海闵行·统考一模)实验室常用下列装置制取气体。
(1)实验室用A装置制取氧气的化学方程式是______;若用E装置收集的氧气不纯,可能原因是______(填
序号)。
a.装置气密性不好 b.在加热前将导管放入集气瓶中
c.收集前集气瓶没有装满水 d.集气瓶中的水没有完全被排尽
(2)某实验小组同学用10%双氧水和二氧化锰制取氧气,欲使反应平稳进行,选用的发生装置是______(选
填“A~D”)。
(3)装置D可用于制取二氧化碳,其适用条件是______,优点是______,以下装置具有与D装置相同工作原
理的是______。(4)实验室用大理石和稀盐酸制取0.2mol 二氧化碳气体,则参加反应的碳酸钙质量是______g。(根据化学
方程式列式计算)
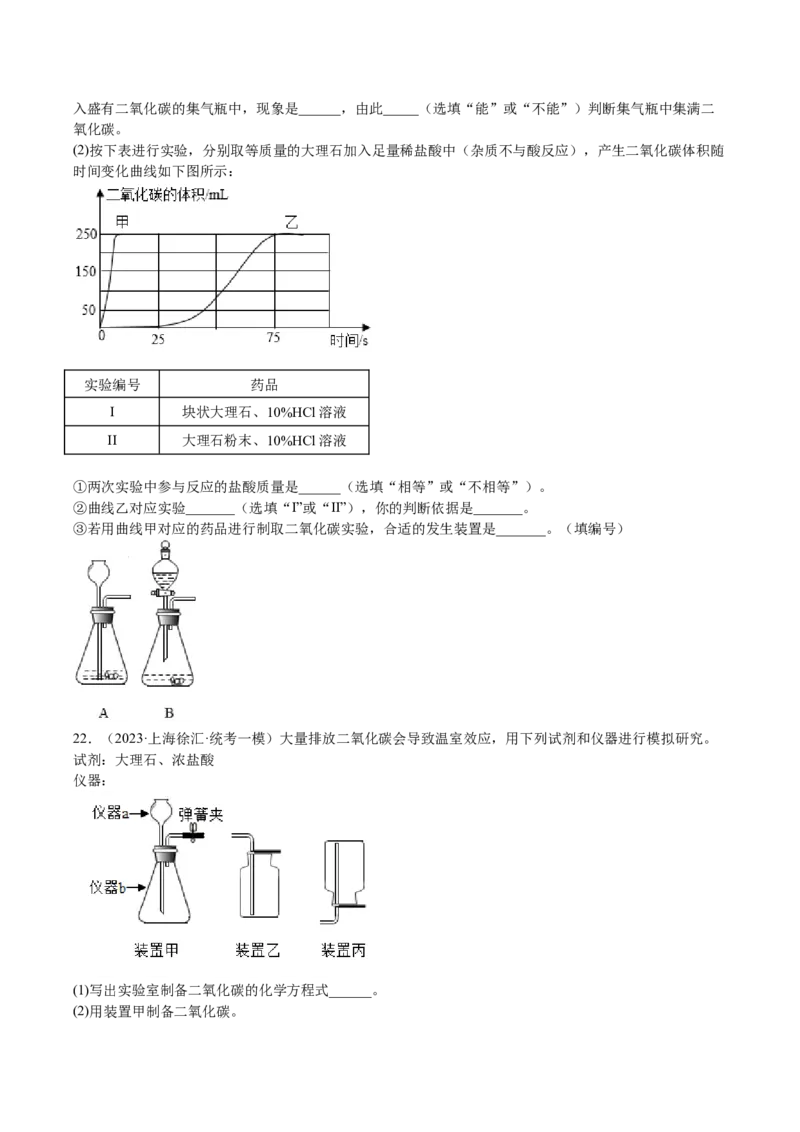
18.(2023·上海青浦·统考一模)下图是实验室制备气体的常用装置。
(1)实验室用氯酸钾和二氧化锰的混合物制取氧气,可选择的发生装置是(填写编号)______反应的化学方
程式是______,二氧化锰的作用是______。若消耗0.2mol氯酸钾,可生成______mol氧气。
(2)实验室用大理石和稀盐酸为反应物制取二氧化碳,可选择C装置作为发生装置,选择该装置时对反应物
状态的要求是______。若选用D装置收集二氧化碳,检验二氧化碳是否收集满的方法是______。
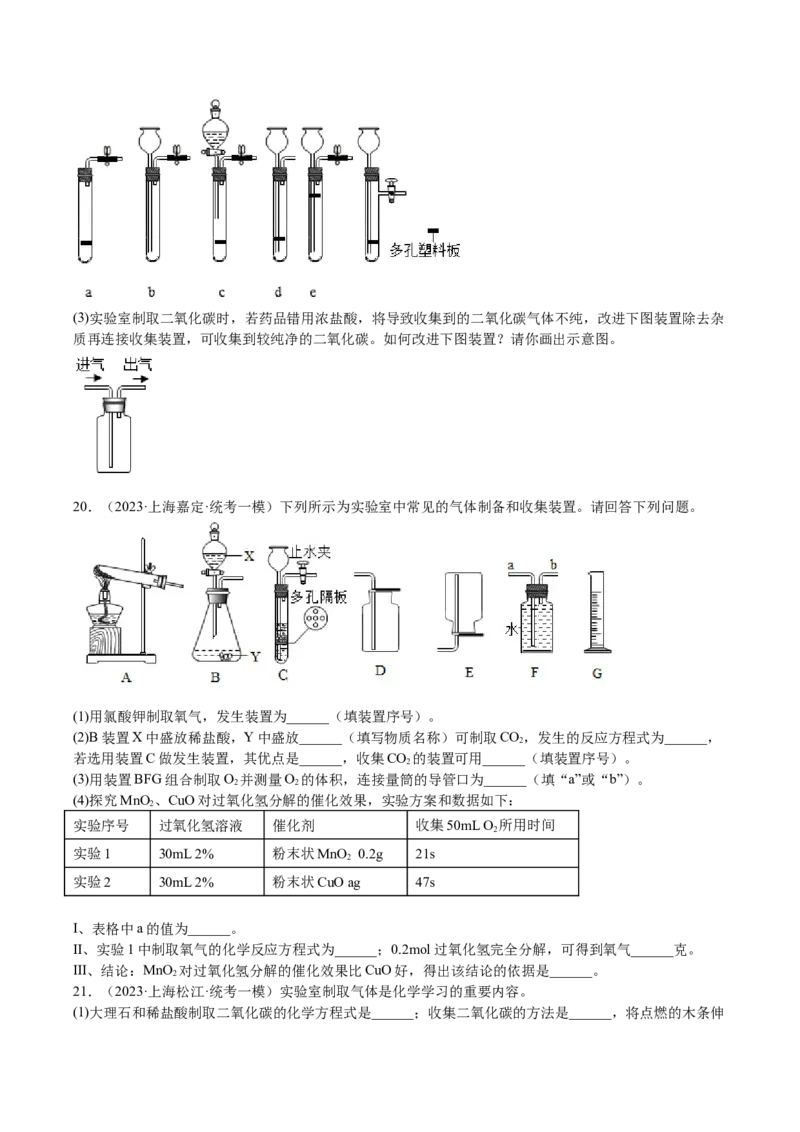
19.(2023·上海宝山·一模)利用下图装置制取气体。
(1)实验室用装置A制取氧气,反应的化学方程式为____________________,该反应属于__________(填基
本反应类型),可选择的收集装置是_________(填编号);若用装置B制取氧气,消耗0.68g反应物时,
理论上可制得氧气________g。
(2)实验室制取二氧化碳反应的化学方程式为____________________,若要控制反应的发生和停止,可选用
下列装置________(填编号)。(3)实验室制取二氧化碳时,若药品错用浓盐酸,将导致收集到的二氧化碳气体不纯,改进下图装置除去杂
质再连接收集装置,可收集到较纯净的二氧化碳。如何改进下图装置?请你画出示意图。
20.(2023·上海嘉定·统考一模)下列所示为实验室中常见的气体制备和收集装置。请回答下列问题。
(1)用氯酸钾制取氧气,发生装置为______(填装置序号)。
(2)B装置X中盛放稀盐酸,Y中盛放______(填写物质名称)可制取CO,发生的反应方程式为______,
2
若选用装置C做发生装置,其优点是______,收集CO 的装置可用______(填装置序号)。
2
(3)用装置BFG组合制取O 并测量O 的体积,连接量筒的导管口为______(填“a”或“b”)。
2 2
(4)探究MnO 、CuO对过氧化氢分解的催化效果,实验方案和数据如下:
2
实验序号 过氧化氢溶液 催化剂 收集50mL O 所用时间
2
实验1 30mL 2% 粉末状MnO 0.2g 21s
2
实验2 30mL 2% 粉末状CuO ag 47s
I、表格中a的值为______。
II、实验1中制取氧气的化学反应方程式为______;0.2mol过氧化氢完全分解,可得到氧气______克。
III、结论:MnO 对过氧化氢分解的催化效果比CuO好,得出该结论的依据是______。
2
21.(2023·上海松江·统考一模)实验室制取气体是化学学习的重要内容。
(1)大理石和稀盐酸制取二氧化碳的化学方程式是______;收集二氧化碳的方法是______,将点燃的木条伸入盛有二氧化碳的集气瓶中,现象是______,由此_____(选填“能”或“不能”)判断集气瓶中集满二
氧化碳。
(2)按下表进行实验,分别取等质量的大理石加入足量稀盐酸中(杂质不与酸反应),产生二氧化碳体积随
时间变化曲线如下图所示:
实验编号 药品
I 块状大理石、10%HCl溶液
II 大理石粉末、10%HCl溶液
①两次实验中参与反应的盐酸质量是______(选填“相等”或“不相等”)。
②曲线乙对应实验_______(选填“I”或“II”),你的判断依据是_______。
③若用曲线甲对应的药品进行制取二氧化碳实验,合适的发生装置是_______。(填编号)
22.(2023·上海徐汇·统考一模)大量排放二氧化碳会导致温室效应,用下列试剂和仪器进行模拟研究。
试剂:大理石、浓盐酸
仪器:
(1)写出实验室制备二氧化碳的化学方程式______。
(2)用装置甲制备二氧化碳。①写出仪器的名称:a________,b________。
②对装置甲检验气密性时,先用弹簧夹夹紧橡胶管,再向仪器a中加入适量水,观察到_______现象,说明
气密性良好。
③将提供的试剂加入甲装置,发现生成气体太快,请写出一条改进方法_______。
(3)在装置乙和丙之间选择装置乙收集二氧化碳的依据是________。请简述如何判断二氧化碳已经收集满
________。
(4)集满一瓶二氧化碳后,用弹簧夹夹紧橡胶管,能否使甲装置中的反应停止? 理由是________。
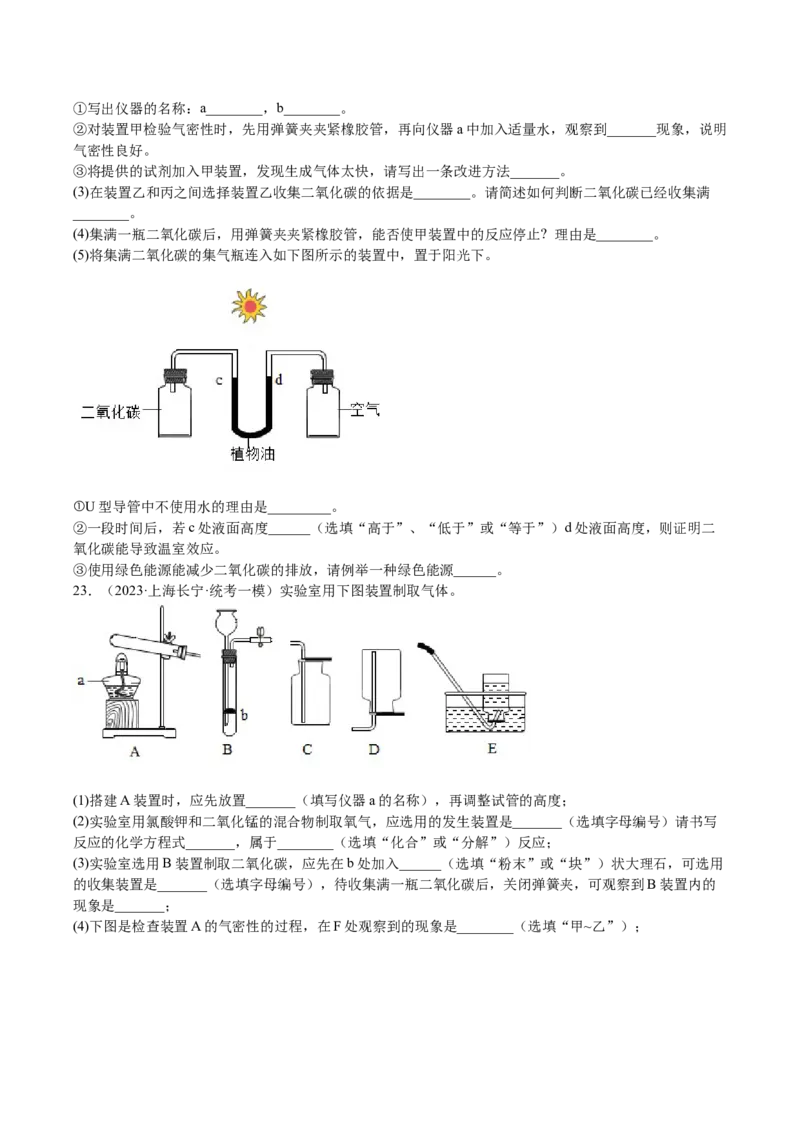
(5)将集满二氧化碳的集气瓶连入如下图所示的装置中,置于阳光下。
①U型导管中不使用水的理由是_________。
②一段时间后,若c处液面高度______(选填“高于”、“低于”或“等于”)d处液面高度,则证明二
氧化碳能导致温室效应。
③使用绿色能源能减少二氧化碳的排放,请例举一种绿色能源______。
23.(2023·上海长宁·统考一模)实验室用下图装置制取气体。
(1)搭建A装置时,应先放置_______(填写仪器a的名称),再调整试管的高度;
(2)实验室用氯酸钾和二氧化锰的混合物制取氧气,应选用的发生装置是_______(选填字母编号)请书写
反应的化学方程式_______,属于________(选填“化合”或“分解”)反应;
(3)实验室选用B装置制取二氧化碳,应先在b处加入______(选填“粉末”或“块”)状大理石,可选用
的收集装置是_______(选填字母编号),待收集满一瓶二氧化碳后,关闭弹簧夹,可观察到B装置内的
现象是_______;
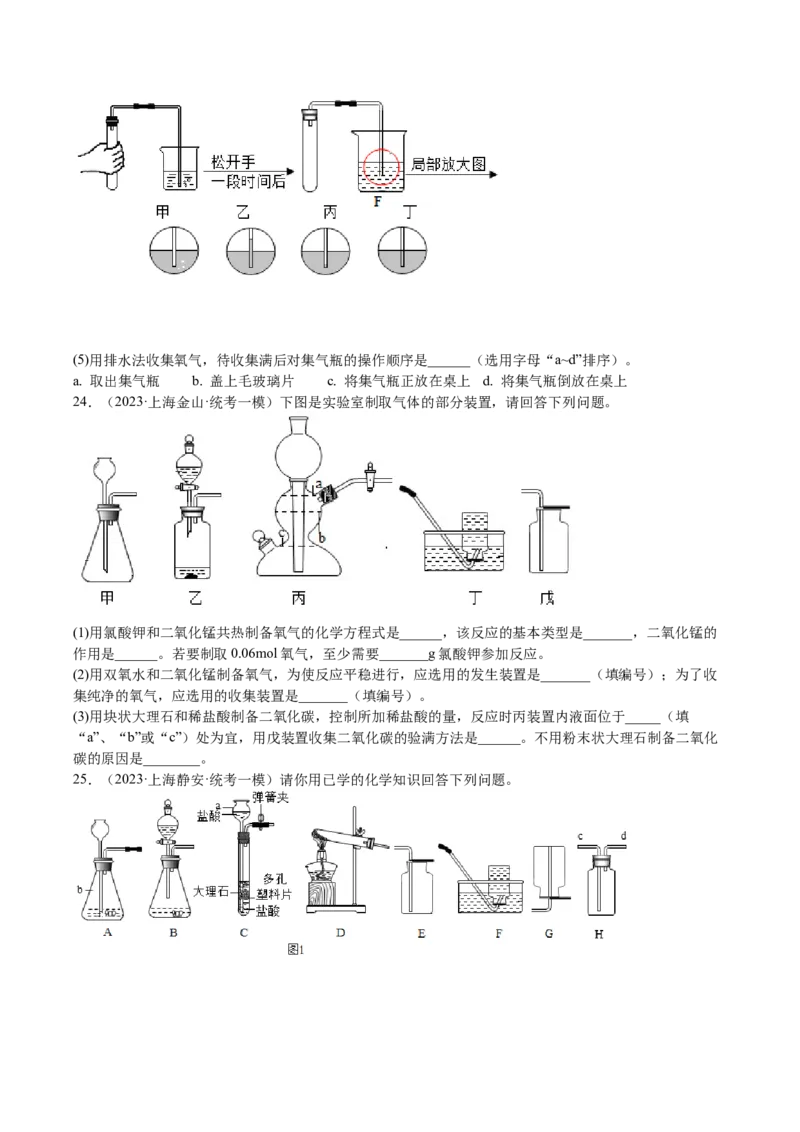
(4)下图是检查装置A的气密性的过程,在F处观察到的现象是________(选填“甲~乙”);(5)用排水法收集氧气,待收集满后对集气瓶的操作顺序是______(选用字母“a~d”排序)。
a. 取出集气瓶 b. 盖上毛玻璃片 c. 将集气瓶正放在桌上 d. 将集气瓶倒放在桌上
24.(2023·上海金山·统考一模)下图是实验室制取气体的部分装置,请回答下列问题。
(1)用氯酸钾和二氧化锰共热制备氧气的化学方程式是______,该反应的基本类型是_______,二氧化锰的
作用是______。若要制取0.06mol氧气,至少需要_______g氯酸钾参加反应。
(2)用双氧水和二氧化锰制备氧气,为使反应平稳进行,应选用的发生装置是_______(填编号);为了收
集纯净的氧气,应选用的收集装置是_______(填编号)。
(3)用块状大理石和稀盐酸制备二氧化碳,控制所加稀盐酸的量,反应时丙装置内液面位于_____(填
“a”、“b”或“c”)处为宜,用戊装置收集二氧化碳的验满方法是______。不用粉末状大理石制备二氧化
碳的原因是________。
25.(2023·上海静安·统考一模)请你用已学的化学知识回答下列问题。(1)图1中仪器名称a是______;b 是______。
(2)氯酸钾制取氧气,选用的发生装置是______。
(3)实验结束后,A、B、C装置中能实现固液分离的是______。
(4)若用装置B制取氧气,则该反应的化学方程式为______,如气流过快,则进行的操作是______,如果用
图F所示装置收集氧气,是因为氧气具有______且不与水反应的性质,如用H收集二氧化碳,气体应从
______端(填“c”或“d”)导入。将收集的氧气用作性质实验,如图2所示,水的作用是______,图2实
验发生反应的化学方程式是______。
(5)实验室常用稀盐酸和块状大理石在装置A中反应制取二氧化碳,如大理石中参与反应的碳酸钙的质量为
10克,计算产生二氧化碳的物质的量?______。(根据化学方程式列式计算)
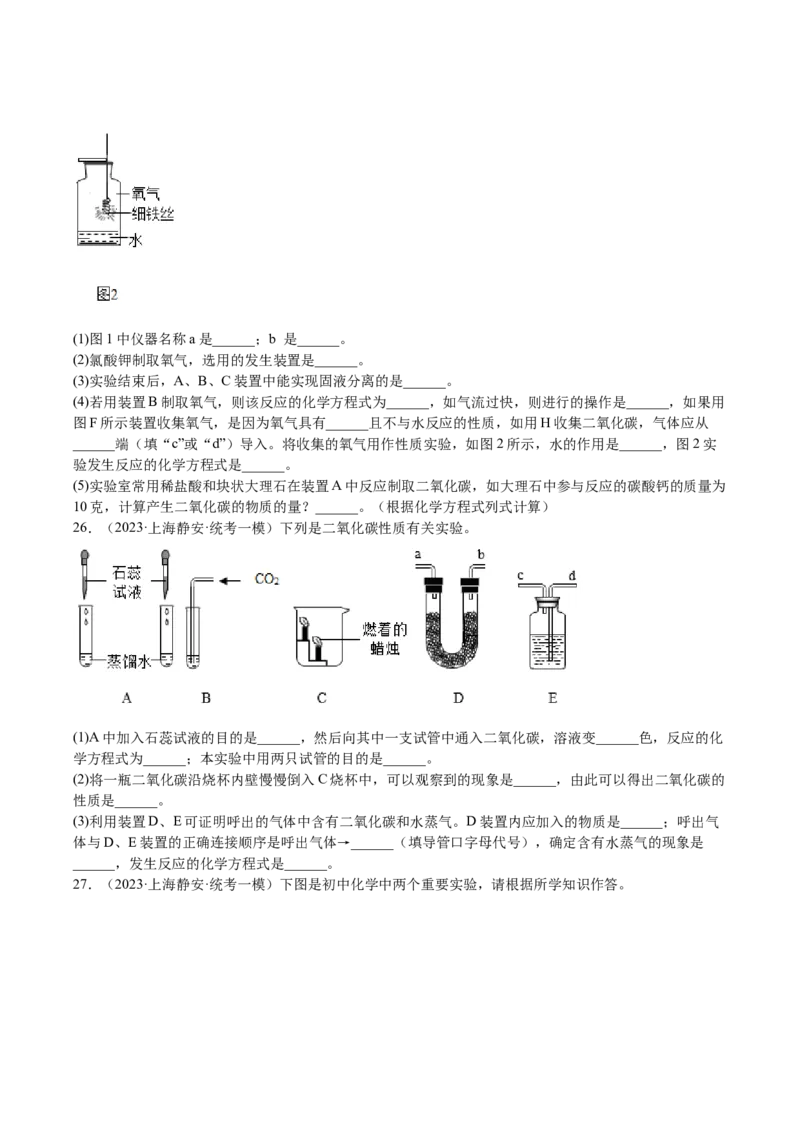
26.(2023·上海静安·统考一模)下列是二氧化碳性质有关实验。
(1)A中加入石蕊试液的目的是______,然后向其中一支试管中通入二氧化碳,溶液变______色,反应的化
学方程式为______;本实验中用两只试管的目的是______。
(2)将一瓶二氧化碳沿烧杯内壁慢慢倒入C烧杯中,可以观察到的现象是______,由此可以得出二氧化碳的
性质是______。
(3)利用装置D、E可证明呼出的气体中含有二氧化碳和水蒸气。D装置内应加入的物质是______;呼出气
体与D、E装置的正确连接顺序是呼出气体→______(填导管口字母代号),确定含有水蒸气的现象是
______,发生反应的化学方程式是______。
27.(2023·上海静安·统考一模)下图是初中化学中两个重要实验,请根据所学知识作答。(1)图1实验:加热前的是操作是______,目的是______,该装置设计的不足之处是______。
(2)图2实验:实验过程中观察到的现象是______,发生反应的化学方程是______。
(3)对图1、2实验的分析正确的是______(填编号)。
a.碳和一氧化碳都具有还原性
b.图2 C中试管口略向下倾斜是为了防止试管炸裂
c.防止液体倒流,都要先将导管移出石灰水,再熄灭酒精灯或喷灯
d.相同质量的氧化铜完全反应后,生成相同质量的二氧化碳
三、综合应用题
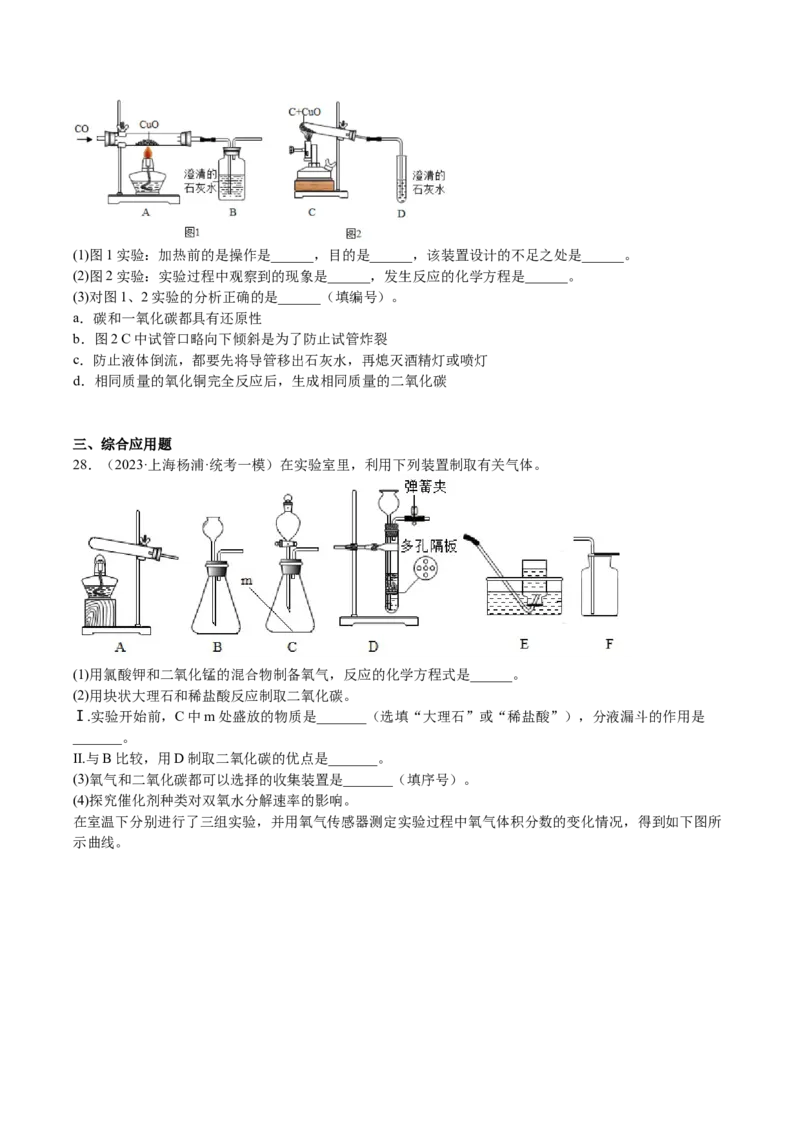
28.(2023·上海杨浦·统考一模)在实验室里,利用下列装置制取有关气体。
(1)用氯酸钾和二氧化锰的混合物制备氧气,反应的化学方程式是______。
(2)用块状大理石和稀盐酸反应制取二氧化碳。
Ⅰ.实验开始前,C中m处盛放的物质是_______(选填“大理石”或“稀盐酸”),分液漏斗的作用是
_______。
II.与B比较,用D制取二氧化碳的优点是_______。
(3)氧气和二氧化碳都可以选择的收集装置是_______(填序号)。
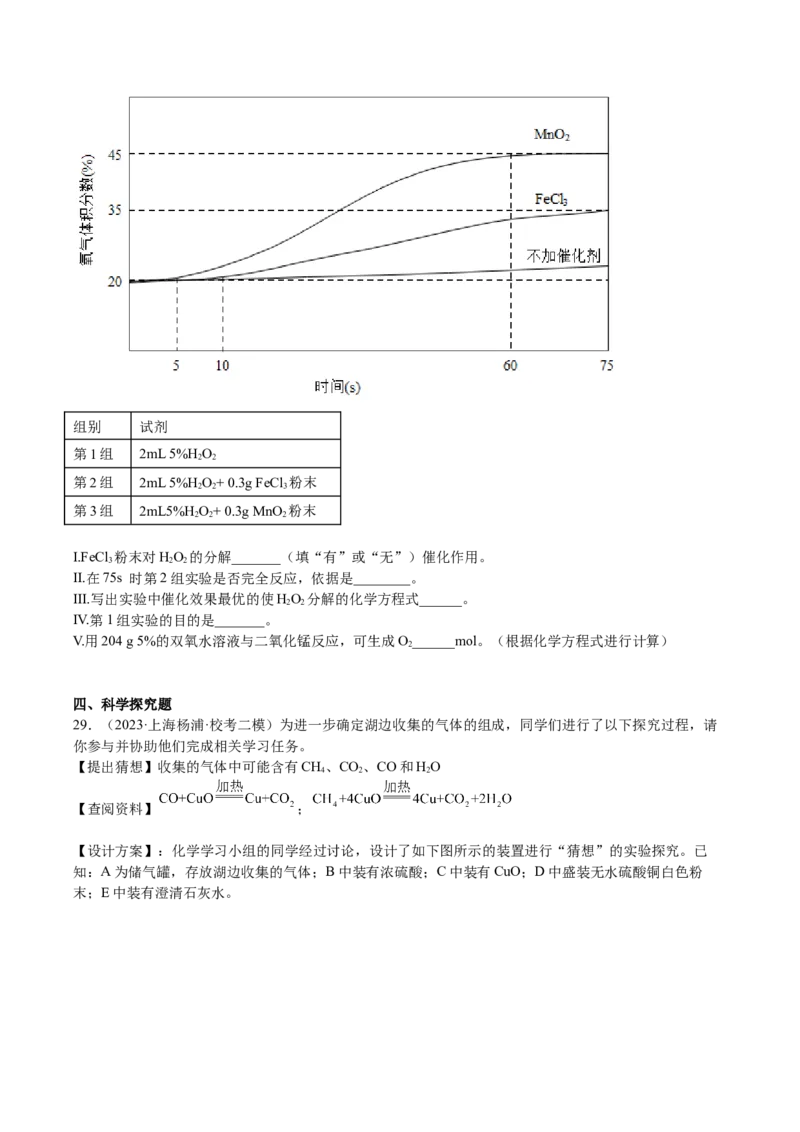
(4)探究催化剂种类对双氧水分解速率的影响。
在室温下分别进行了三组实验,并用氧气传感器测定实验过程中氧气体积分数的变化情况,得到如下图所
示曲线。组别 试剂
第1组 2mL 5%HO
2 2
第2组 2mL 5%HO+ 0.3g FeCl 粉末
2 2 3
第3组 2mL5%H O+ 0.3g MnO 粉末
2 2 2
I.FeCl 粉末对HO 的分解_______(填“有”或“无”)催化作用。
3 2 2
II.在75s 时第2组实验是否完全反应,依据是________。
III.写出实验中催化效果最优的使HO 分解的化学方程式______。
2 2
IV.第1组实验的目的是_______。
V.用204 g 5%的双氧水溶液与二氧化锰反应,可生成O______mol。(根据化学方程式进行计算)
2
四、科学探究题
29.(2023·上海杨浦·校考二模)为进一步确定湖边收集的气体的组成,同学们进行了以下探究过程,请
你参与并协助他们完成相关学习任务。
【提出猜想】收集的气体中可能含有CH、CO、CO和HO
4 2 2
【查阅资料】 ;
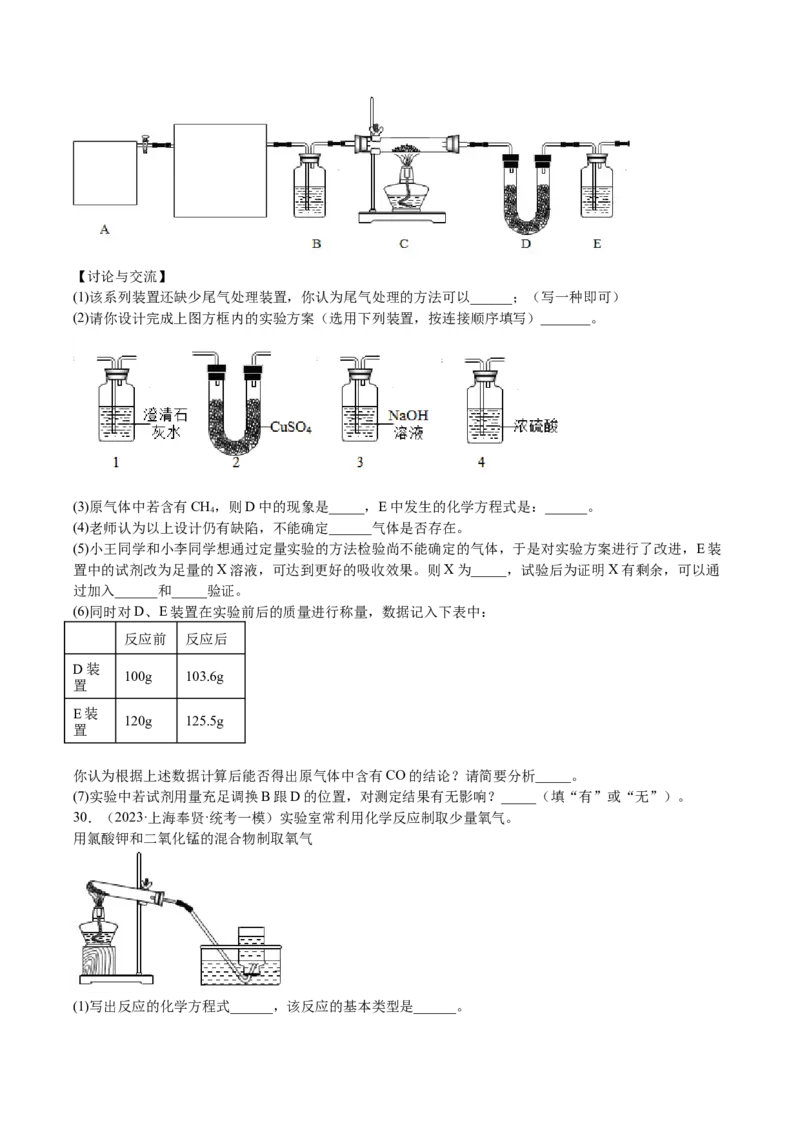
【设计方案】:化学学习小组的同学经过讨论,设计了如下图所示的装置进行“猜想”的实验探究。已
知:A为储气罐,存放湖边收集的气体;B中装有浓硫酸;C中装有CuO;D中盛装无水硫酸铜白色粉
末;E中装有澄清石灰水。【讨论与交流】
(1)该系列装置还缺少尾气处理装置,你认为尾气处理的方法可以______;(写一种即可)
(2)请你设计完成上图方框内的实验方案(选用下列装置,按连接顺序填写)_______。
(3)原气体中若含有CH,则D中的现象是_____,E中发生的化学方程式是:______。
4
(4)老师认为以上设计仍有缺陷,不能确定______气体是否存在。
(5)小王同学和小李同学想通过定量实验的方法检验尚不能确定的气体,于是对实验方案进行了改进,E装
置中的试剂改为足量的X溶液,可达到更好的吸收效果。则X为_____,试验后为证明X有剩余,可以通
过加入______和_____验证。
(6)同时对D、E装置在实验前后的质量进行称量,数据记入下表中:
反应前 反应后
D装
100g 103.6g
置
E装
120g 125.5g
置
你认为根据上述数据计算后能否得出原气体中含有CO的结论?请简要分析_____。
(7)实验中若试剂用量充足调换B跟D的位置,对测定结果有无影响?_____(填“有”或“无”)。
30.(2023·上海奉贤·统考一模)实验室常利用化学反应制取少量氧气。
用氯酸钾和二氧化锰的混合物制取氧气
(1)写出反应的化学方程式______,该反应的基本类型是______。(2)用如图所示方法收集氧气,集满的现象是______;若要收集一瓶体积分数为80%的氧气,应预先向容积
为400mL的集气瓶中装约______mL水。
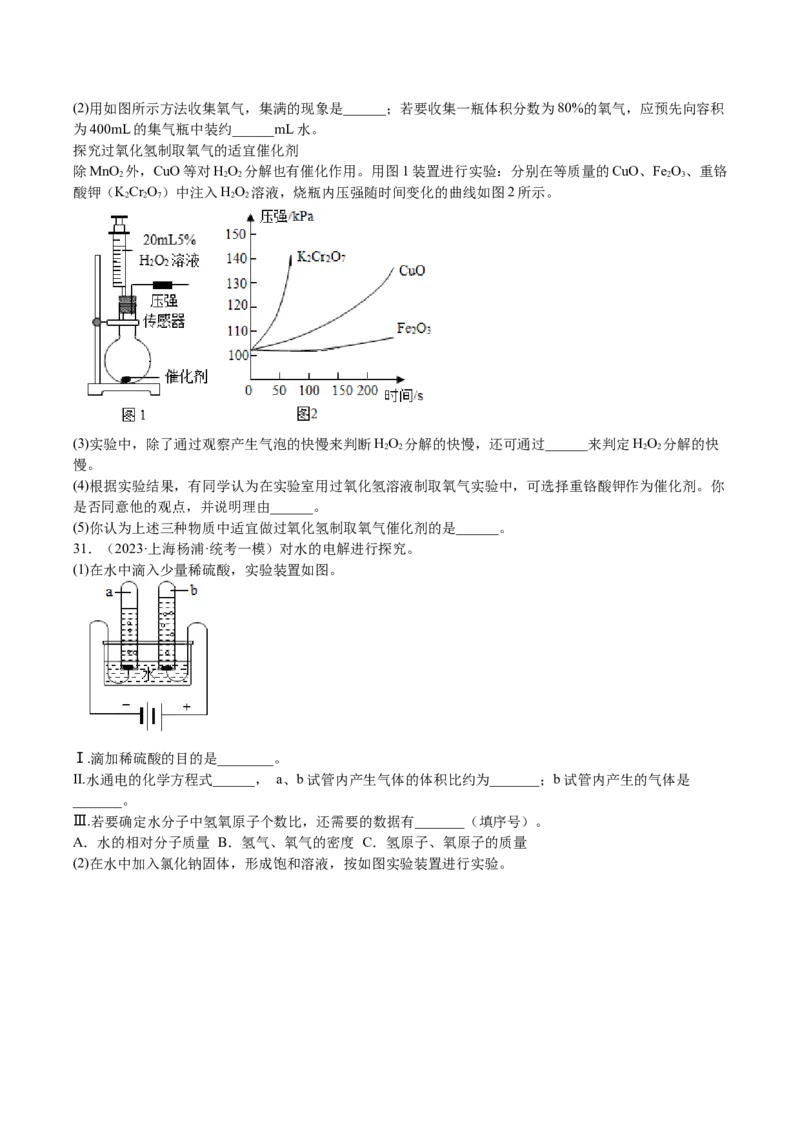
探究过氧化氢制取氧气的适宜催化剂
除MnO 外,CuO等对HO 分解也有催化作用。用图1装置进行实验:分别在等质量的CuO、Fe O、重铬
2 2 2 2 3
酸钾(KCr O)中注入HO 溶液,烧瓶内压强随时间变化的曲线如图2所示。
2 2 7 2 2
(3)实验中,除了通过观察产生气泡的快慢来判断HO 分解的快慢,还可通过______来判定HO 分解的快
2 2 2 2
慢。
(4)根据实验结果,有同学认为在实验室用过氧化氢溶液制取氧气实验中,可选择重铬酸钾作为催化剂。你
是否同意他的观点,并说明理由______。
(5)你认为上述三种物质中适宜做过氧化氢制取氧气催化剂的是______。
31.(2023·上海杨浦·统考一模)对水的电解进行探究。
(1)在水中滴入少量稀硫酸,实验装置如图。
Ⅰ.滴加稀硫酸的目的是________。
II.水通电的化学方程式______, a、b试管内产生气体的体积比约为_______;b试管内产生的气体是
_______。
Ⅲ.若要确定水分子中氢氧原子个数比,还需要的数据有_______(填序号)。
A.水的相对分子质量 B.氢气、氧气的密度 C.氢原子、氧原子的质量
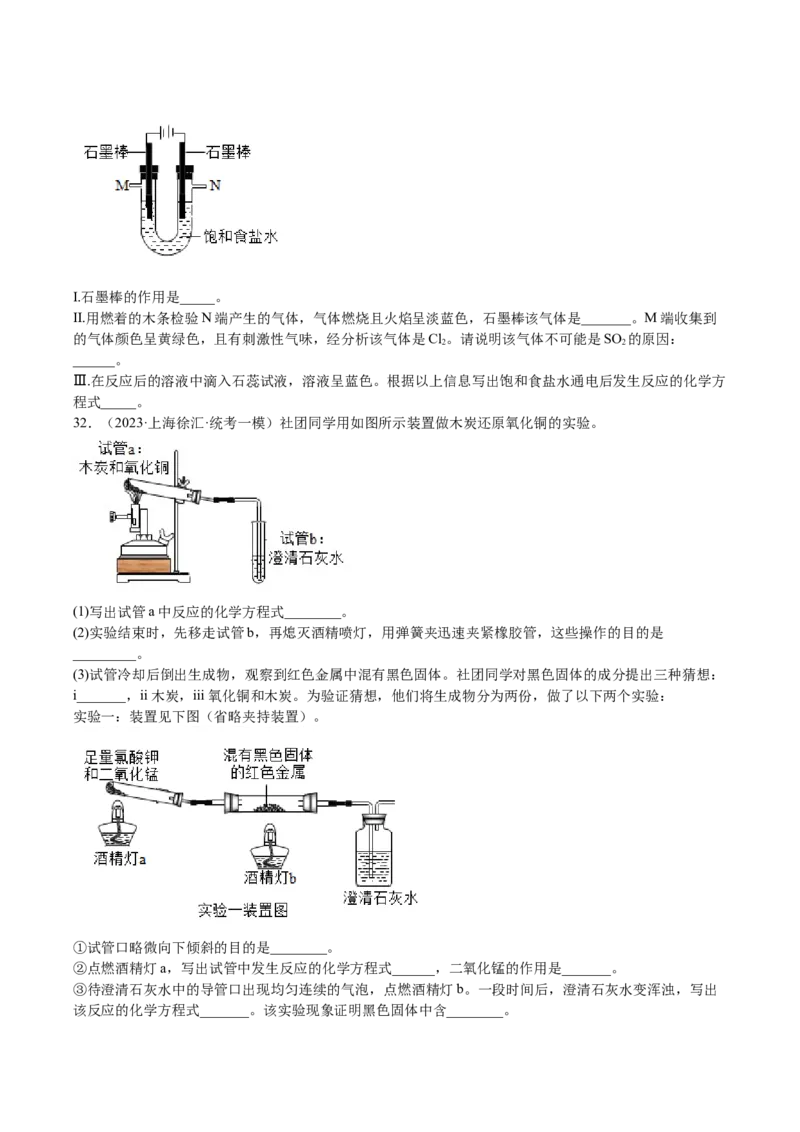
(2)在水中加入氯化钠固体,形成饱和溶液,按如图实验装置进行实验。I.石墨棒的作用是_____。
II.用燃着的木条检验N端产生的气体,气体燃烧且火焰呈淡蓝色,石墨棒该气体是_______。M端收集到
的气体颜色呈黄绿色,且有刺激性气味,经分析该气体是Cl。请说明该气体不可能是SO 的原因:
2 2
______。
Ⅲ.在反应后的溶液中滴入石蕊试液,溶液呈蓝色。根据以上信息写出饱和食盐水通电后发生反应的化学方
程式_____。
32.(2023·上海徐汇·统考一模)社团同学用如图所示装置做木炭还原氧化铜的实验。
(1)写出试管a中反应的化学方程式________。
(2)实验结束时,先移走试管b,再熄灭酒精喷灯,用弹簧夹迅速夹紧橡胶管,这些操作的目的是
_________。
(3)试管冷却后倒出生成物,观察到红色金属中混有黑色固体。社团同学对黑色固体的成分提出三种猜想:
i_______,ii木炭,iii氧化铜和木炭。为验证猜想,他们将生成物分为两份,做了以下两个实验:
实验一:装置见下图(省略夹持装置)。
①试管口略微向下倾斜的目的是________。
②点燃酒精灯a,写出试管中发生反应的化学方程式______,二氧化锰的作用是_______。
③待澄清石灰水中的导管口出现均匀连续的气泡,点燃酒精灯b。一段时间后,澄清石灰水变浑浊,写出
该反应的化学方程式_______。该实验现象证明黑色固体中含________。实验二:在5支试管中分别混合对应的试剂,记录实验现象。
试管编号 试剂组合 实验现象
1 稀硫酸+木炭 无明显现象
2 稀硫酸+铜 无明显现象
3 稀硫酸+氧化铜 无色溶液变为蓝色
4 稀硫酸+木炭+铜 无明显现象
5 稀硫酸+混有黑色固体的红色金属 无色溶液变为蓝色
①稀硫酸中溶质的化学式为________。
②根据实验现象,证明猜想_______正确。
五、计算题
33.(2023·上海闵行·校考模拟预测)实验室用98%的浓硫酸配制稀硫酸,并进行相关的性质实验。(夹持
仪器省略,装置气密性良好)
(1)配制100g19.6%的稀硫酸的步骤是
I.____,II.称量,III.溶解。读取水的体积时,视线应与量筒内液体____保持水平。
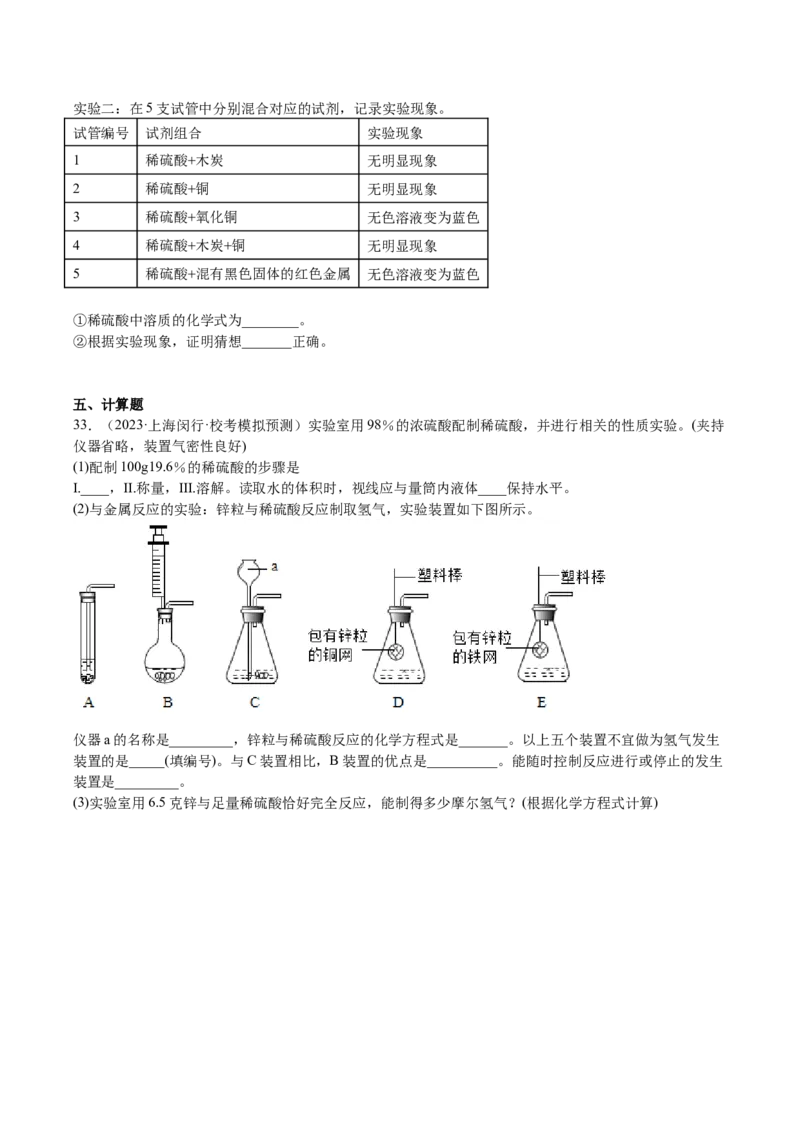
(2)与金属反应的实验:锌粒与稀硫酸反应制取氢气,实验装置如下图所示。
仪器a的名称是_________,锌粒与稀硫酸反应的化学方程式是_______。以上五个装置不宜做为氢气发生
装置的是_____(填编号)。与C装置相比,B装置的优点是__________。能随时控制反应进行或停止的发生
装置是_________。
(3)实验室用6.5克锌与足量稀硫酸恰好完全反应,能制得多少摩尔氢气?(根据化学方程式计算)